LES DIAGRAMMES DE PHASE Les systmes binaires Thermochimie

LES DIAGRAMMES DE PHASE Les systèmes binaires Thermochimie : chapitre 11 Guy COLLIN, 2014 -12 -29

Les systèmes binaires solides n n n u = C + 2 - On imagine aisément l’existence de systèmes solides totalement non miscibles ou insolubles. On connaît sans doute moins bien l’existence de systèmes binaires solides totalement miscibles. Qu’en est-il réellement de l’équilibre entre les phases solides de deux constituants purs A et B ? Comment peut-on décrire et caractériser les diagrammes représentant ces équilibres ? Quelles sont leurs propriétés ? Et en particulier, comment peut-on séparer les deux constituants d’un tel mélange ? 2014 -12 -29

La règle des phases Une phase est toute partie homogène d’un système physiquement distincte des autres parties dont elle est séparée par des surfaces de délimitation bien définies. n Le nombre de composants est ce nombre d’espèces diminué du nombre de relations chimiques qui les relient. n Lorsque le nombre de composants d’un système et les composants de chacune des phases sont précisés, la variance est le nombre de facteurs qu’il faut préciser pour que l’équilibre soit défini : u = C + 2 - n u = C + 2 - 2014 -12 -29
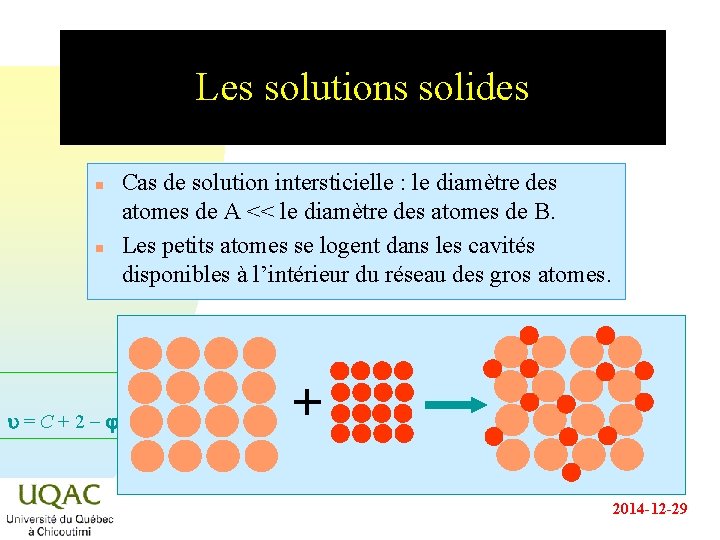
Les solutions solides n n Cas de solution intersticielle : le diamètre des atomes de A << le diamètre des atomes de B. Les petits atomes se logent dans les cavités disponibles à l’intérieur du réseau des gros atomes. u = C + 2 - 2014 -12 -29

Les solutions solides n n Cas de solution par substitution : le diamètre d des atomes de A est voisin du diamètre des atomes de B. Les atomes se substituent les uns les autres dans leur réseau : Les deux composés cristallisent dans le même système cristallin; u Les valences ou degré d’oxydation de A et de B sont les mêmes; F = (d. A - d. B )/ d. A u Le facteur de dimension, F, est < à 15 %. u d. A d. B u = C + 2 - 2014 -12 -29
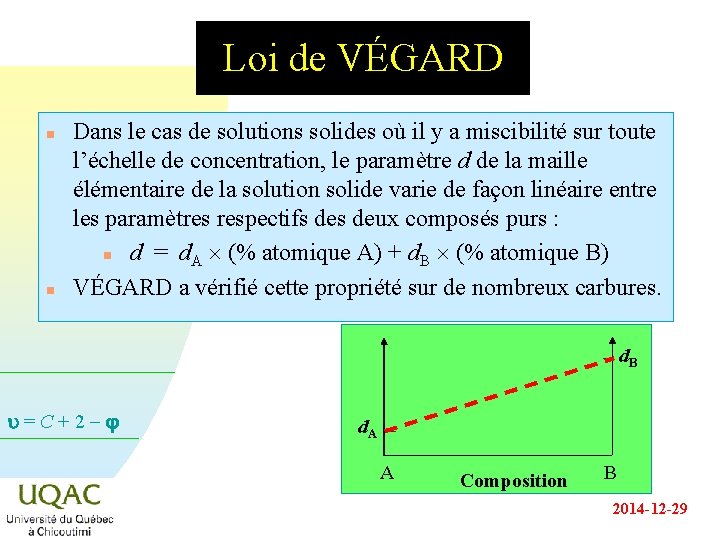
Loi de VÉGARD n n Dans le cas de solutions solides où il y a miscibilité sur toute l’échelle de concentration, le paramètre d de la maille élémentaire de la solution solide varie de façon linéaire entre les paramètres respectifs deux composés purs : n d = d. A ´ (% atomique A) + d. B ´ (% atomique B) VÉGARD a vérifié cette propriété sur de nombreux carbures. d. B u = C + 2 - d. A A Composition B 2014 -12 -29

Mailles élémentaires de certains carbures u = C + 2 - 2014 -12 -29
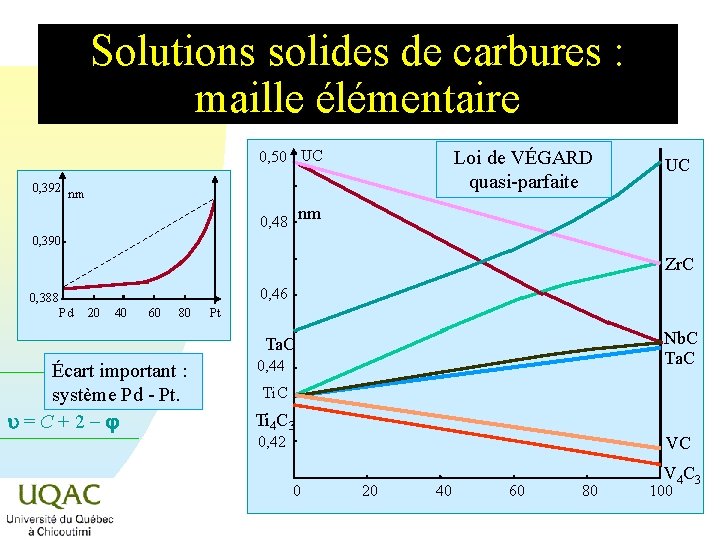
Solutions solides de carbures : maille élémentaire Loi de VÉGARD quasi-parfaite 0, 50 UC 0, 392 nm UC nm 0, 48 0, 390 Zr. C 0, 46 0, 388 Pd 20 40 60 80 Pt Nb. C Ta. C Écart important : système Pd - Pt. u = C + 2 - 0, 44 Ti. C Ti 4 C 3 0, 42 VC 0 20 40 60 80 V 4 C 3 100 2014 -12 -29
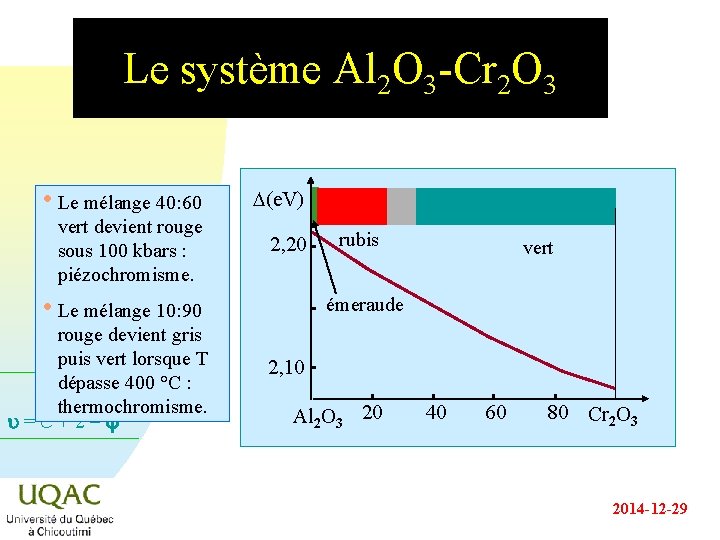
Le système Al 2 O 3 -Cr 2 O 3 • Le mélange 40: 60 vert devient rouge sous 100 kbars : piézochromisme. D(e. V) 2, 20 • Le mélange 10: 90 rouge devient gris puis vert lorsque T dépasse 400 °C : thermochromisme. u = C + 2 - rubis vert émeraude 2, 10 Al 2 O 3 20 40 60 80 Cr 2 O 3 2014 -12 -29
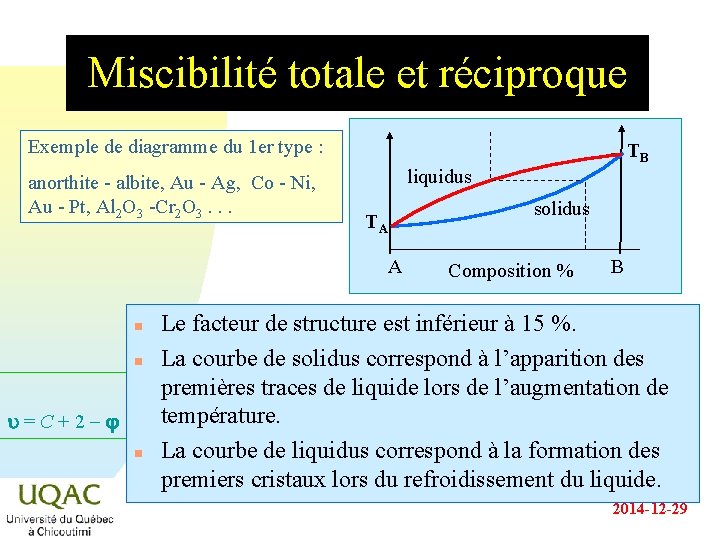
Miscibilité totale et réciproque Exemple de diagramme du 1 er type : anorthite - albite, Au - Ag, Co - Ni, Au - Pt, Al 2 O 3 -Cr 2 O 3. . . TB liquidus TA A n n u = C + 2 - n solidus Composition % B Le facteur de structure est inférieur à 15 %. La courbe de solidus correspond à l’apparition des premières traces de liquide lors de l’augmentation de température. La courbe de liquidus correspond à la formation des premiers cristaux lors du refroidissement du liquide. 2014 -12 -29
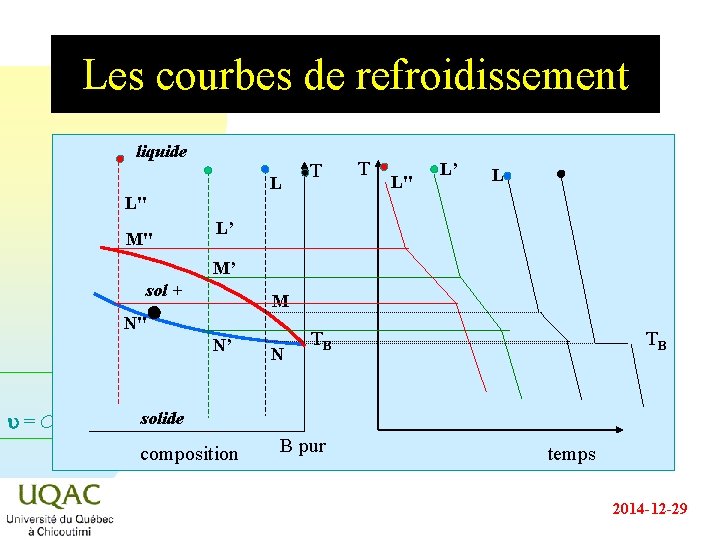
Les courbes de refroidissement liquide L L" M" T T L" L’ L L’ M’ sol + M l N" N’ u = C + 2 - N TB TB solide composition B pur temps 2014 -12 -29
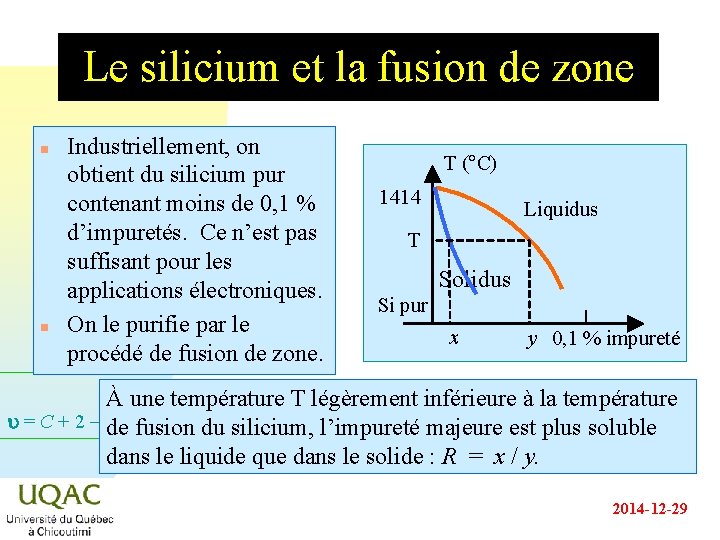
Le silicium et la fusion de zone n n Industriellement, on obtient du silicium pur contenant moins de 0, 1 % d’impuretés. Ce n’est pas suffisant pour les applications électroniques. On le purifie par le procédé de fusion de zone. T (°C) 1414 Liquidus T Solidus Si pur x y 0, 1 % impureté À une température T légèrement inférieure à la température u = C + 2 - de fusion du silicium, l’impureté majeure est plus soluble dans le liquide que dans le solide : R = x / y. 2014 -12 -29
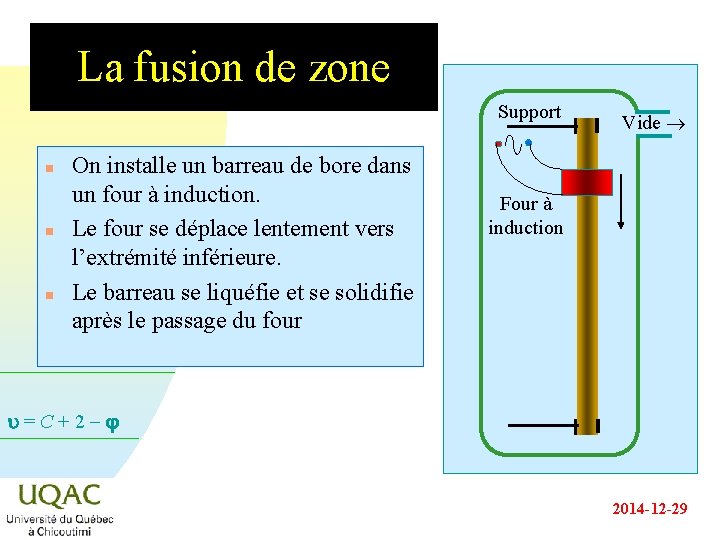
La fusion de zone Support n n n On installe un barreau de bore dans un four à induction. Le four se déplace lentement vers l’extrémité inférieure. Le barreau se liquéfie et se solidifie après le passage du four Vide Four à induction u = C + 2 - 2014 -12 -29
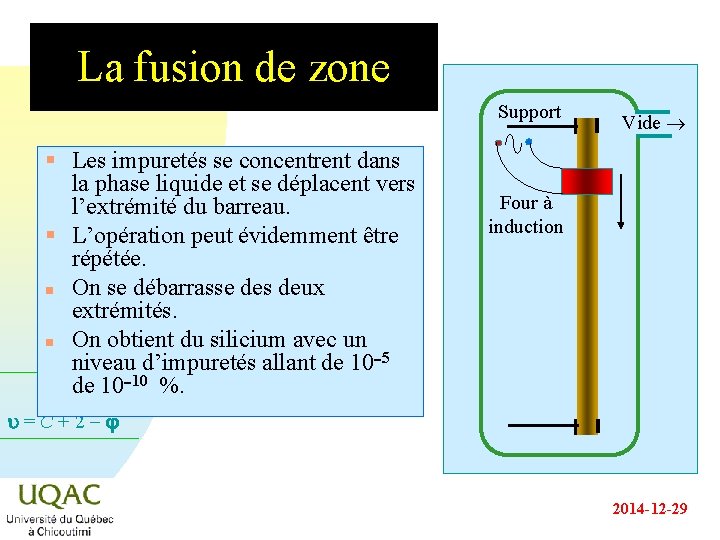
La fusion de zone Support § Les impuretés se concentrent dans la phase liquide et se déplacent vers l’extrémité du barreau. § L’opération peut évidemment être répétée. n On se débarrasse des deux extrémités. n On obtient du silicium avec un niveau d’impuretés allant de 10 -5 de 10 -10 %. Vide Four à induction u = C + 2 - 2014 -12 -29
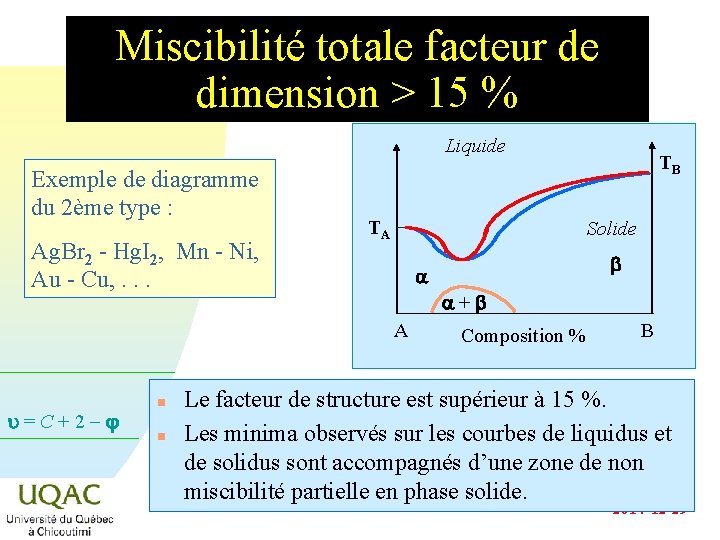
Miscibilité totale facteur de dimension > 15 % Liquide Exemple de diagramme du 2ème type : Ag. Br 2 - Hg. I 2, Mn - Ni, Au - Cu, . . . TA Solide u = C + 2 - n b a a + b A n TB Composition % B Le facteur de structure est supérieur à 15 %. Les minima observés sur les courbes de liquidus et de solidus sont accompagnés d’une zone de non miscibilité partielle en phase solide. 2014 -12 -29
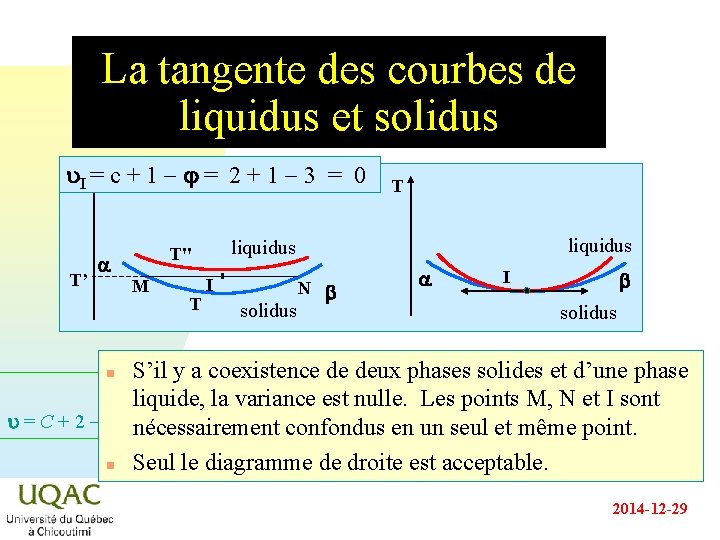
La tangente des courbes de liquidus et solidus u. I = c + 1 - = 2 + 1 - 3 = 0 T’ a T liquidus T" M T I solidus N b a I b solidus S’il y a coexistence de deux phases solides et d’une phase liquide, la variance est nulle. Les points M, N et I sont u = C + 2 - nécessairement confondus en un seul et même point. n Seul le diagramme de droite est acceptable. n 2014 -12 -29
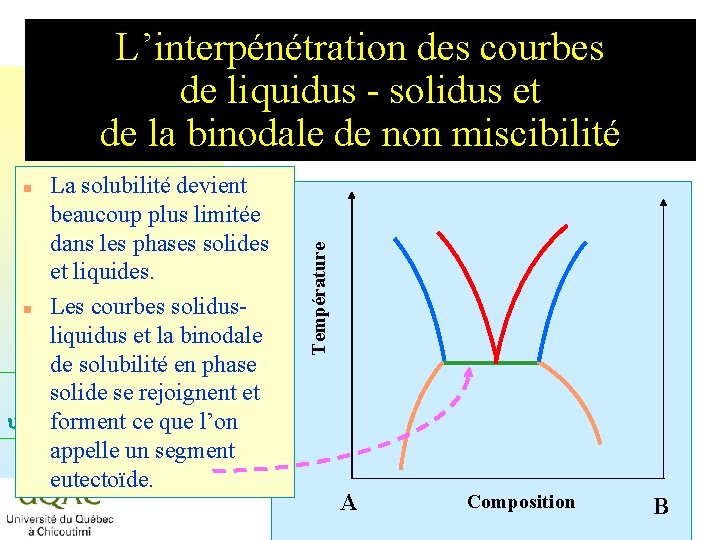
L’interpénétration des courbes de liquidus - solidus et de la binodale de non miscibilité La solubilité devient beaucoup plus limitée dans les phases solides et liquides. n Les courbes solidusliquidus et la binodale de solubilité en phase solide se rejoignent et u = C + 2 - forment ce que l’on appelle un segment eutectoïde. Température n A Composition 2014 -12 -29 B
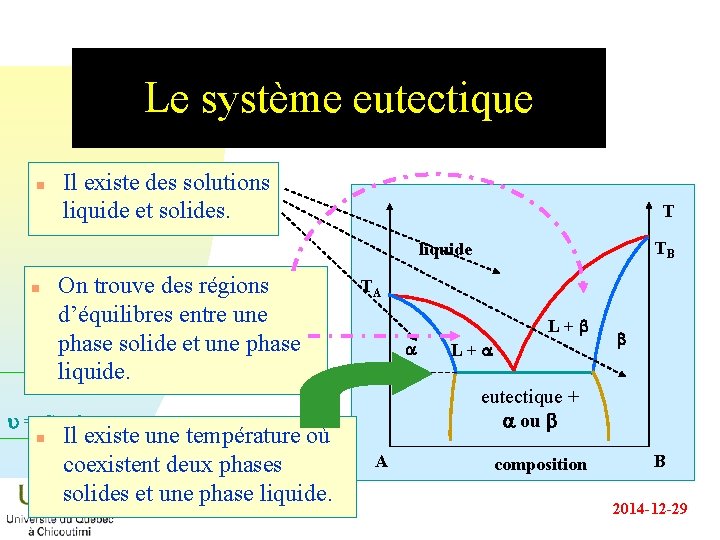
Le système eutectique n Il existe des solutions liquide et solides. T TB liquide n On trouve des régions d’équilibres entre une phase solide et une phase liquide. TA L+b a Il existe une température où coexistent deux phases solides et une phase liquide. b eutectique + a ou b u = C + 2 - n L+a A composition B 2014 -12 -29
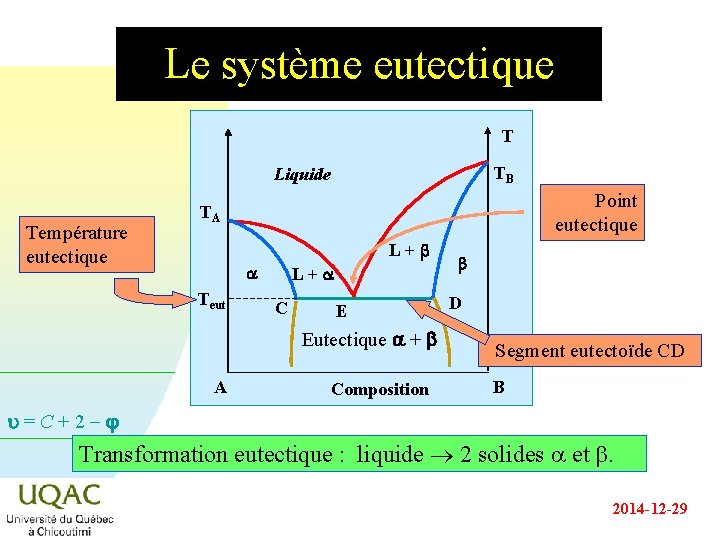
Le système eutectique T TB Liquide Température eutectique Point eutectique TA L+b a Teut L+a C E Eutectique a + b A Composition b D Segment eutectoïde CD B u = C + 2 - Transformation eutectique : liquide 2 solides a et b. 2014 -12 -29
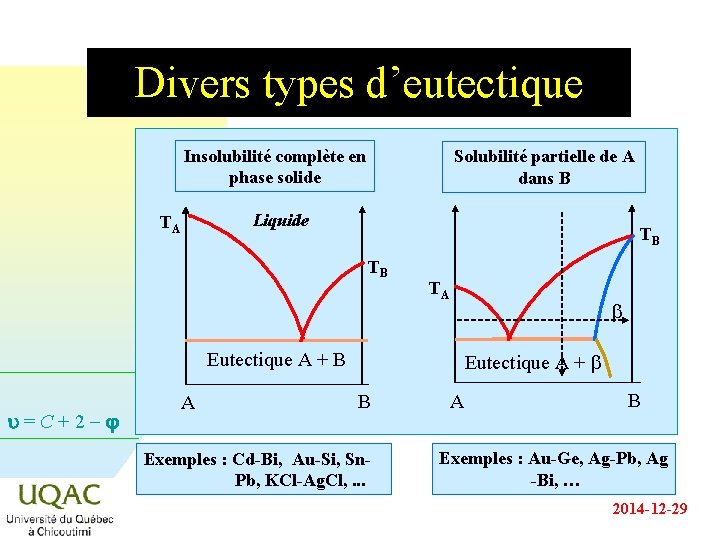
Divers types d’eutectique Insolubilité complète en phase solide TA Solubilité partielle de A dans B Liquide TB TB TA b Eutectique A + B u = C + 2 - A Eutectique A + b B Exemples : Cd-Bi, Au-Si, Sn. Pb, KCl-Ag. Cl, . . . A B Exemples : Au-Ge, Ag-Pb, Ag -Bi, … 2014 -12 -29
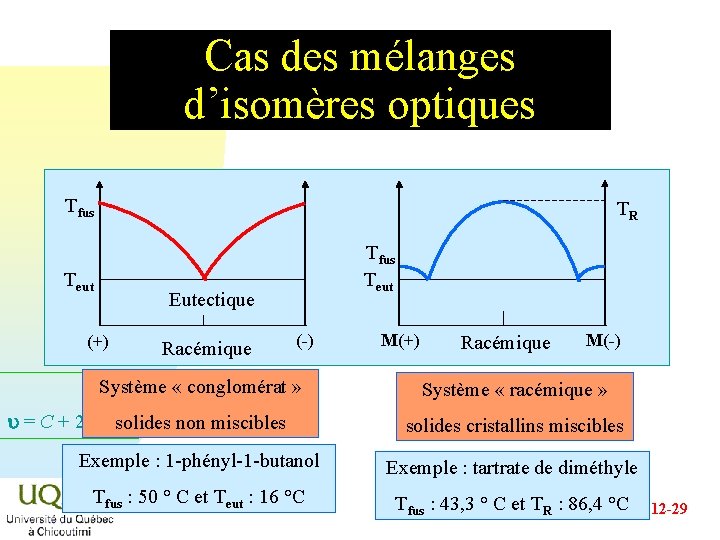
Cas des mélanges d’isomères optiques Tfus TR Teut Tfus Teut Eutectique (+) Racémique (-) Système « conglomérat » u = C + 2 - solides non miscibles Exemple : 1 -phényl-1 -butanol Tfus : 50 ° C et Teut : 16 °C M(+) Racémique M(-) Système « racémique » solides cristallins miscibles Exemple : tartrate de diméthyle Tfus : 43, 3 ° C et TR : 86, 4 °C 2014 -12 -29
Eutectiques eau-sel u = C + 2 - 2014 -12 -29

Le déglaçage des rues n Le choix d’un sel pour le déglaçage des rues en hiver doit obéir à un certain nombre de propriétés : u Il est exempt de propriétés adverses sur l’environnement. u L’abaissement cryoscopique doit être le plus prononcé possible. u Le plateau de fusion de l’eutectique soit le plus favorable possible. u = C + 2 - u Le coût du produit retenu soit le plus abordable possible (grande disponibilité au plus bas coût). 2014 -12 -29
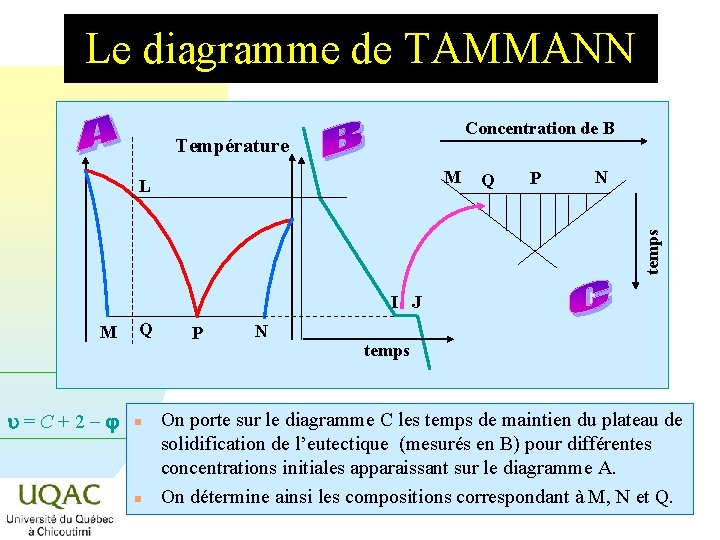
Le diagramme de TAMMANN Concentration de B Température M Q P N temps L I J M u = C + 2 - Q n n P N temps On porte sur le diagramme C les temps de maintien du plateau de solidification de l’eutectique (mesurés en B) pour différentes concentrations initiales apparaissant sur le diagramme A. On détermine ainsi les compositions correspondant à M, N et Q. 2014 -12 -29
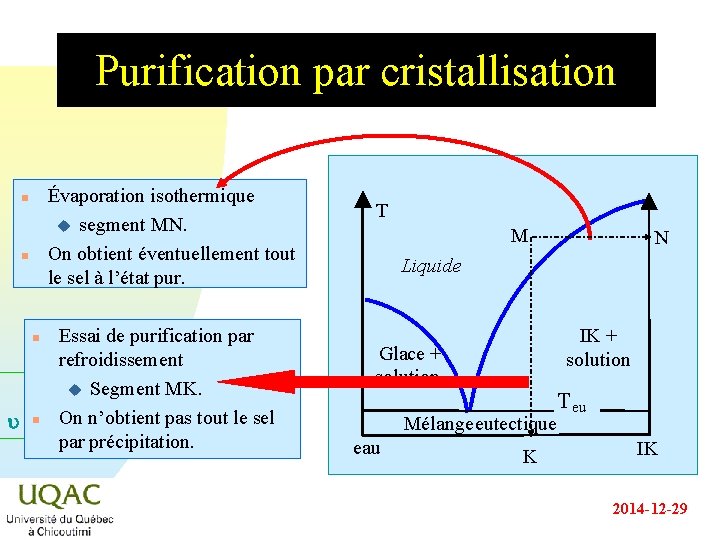
Purification par cristallisation Évaporation isothermique u segment MN. On obtient éventuellement tout le sel à l’état pur. n n Essai de purification par refroidissement u Segment MK. n On n’obtient pas tout le sel u = C + 2 - par précipitation. n T M N Liquide IK + solution Glace + solution Mélange eutectique eau K Teu IK 2014 -12 -29
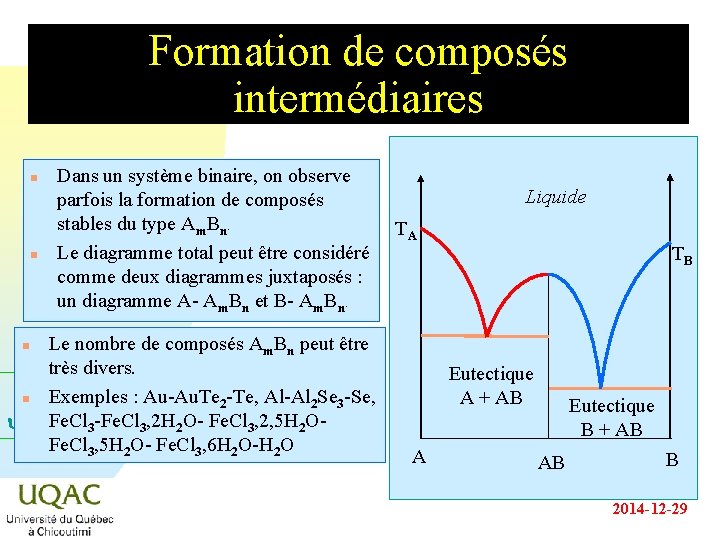
Formation de composés intermédiaires n n Dans un système binaire, on observe parfois la formation de composés stables du type Am. Bn. Le diagramme total peut être considéré comme deux diagrammes juxtaposés : un diagramme A- Am. Bn et B- Am. Bn. Le nombre de composés Am. Bn peut être très divers. n Exemples : Au-Au. Te 2 -Te, Al-Al 2 Se 3 -Se, Fe. Cl 3 -Fe. Cl 3, 2 H 2 O- Fe. Cl 3, 2, 5 H 2 O- u = C + 2 - Fe. Cl 3, 5 H 2 O- Fe. Cl 3, 6 H 2 O-H 2 O Liquide TA TB n Eutectique A + AB A AB Eutectique B + AB B 2014 -12 -29
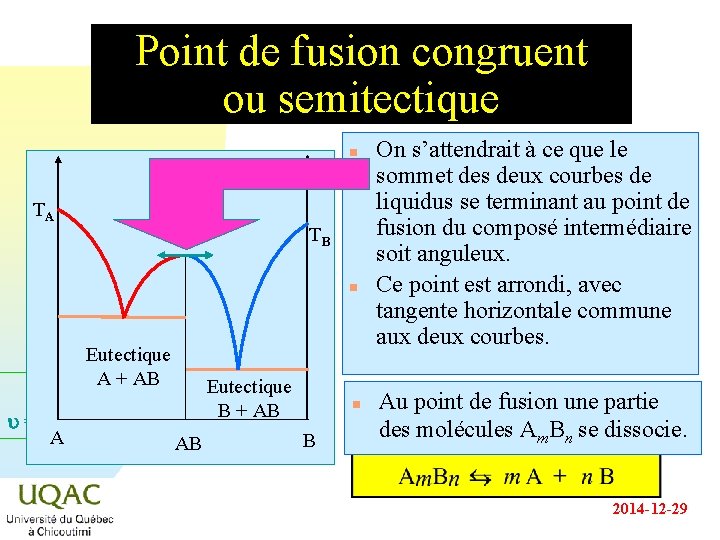
Point de fusion congruent ou semitectique n Liquide TA TB n Eutectique A + AB u = C + 2 - A AB Eutectique B + AB n B On s’attendrait à ce que le sommet des deux courbes de liquidus se terminant au point de fusion du composé intermédiaire soit anguleux. Ce point est arrondi, avec tangente horizontale commune aux deux courbes. Au point de fusion une partie des molécules Am. Bn se dissocie. 2014 -12 -29
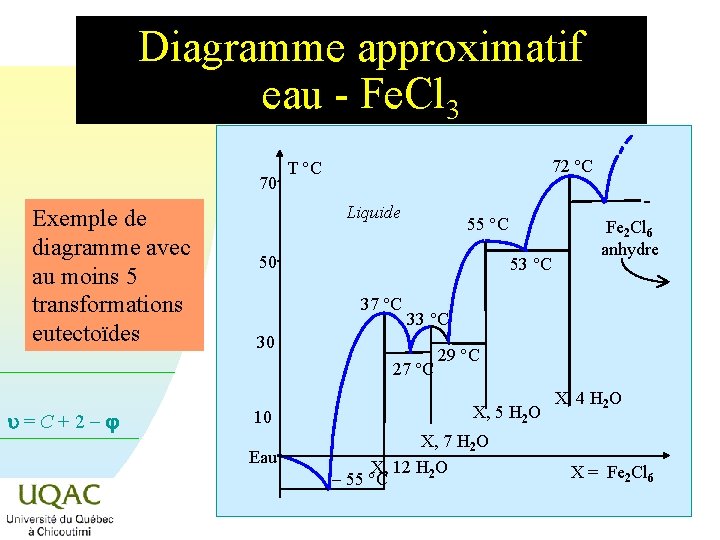
Diagramme approximatif eau - Fe. Cl 3 70 Exemple de diagramme avec au moins 5 transformations eutectoïdes 72 °C T °C Liquide 55 °C 50 53 °C 37 °C 33 °C 30 27 °C u = C + 2 - 10 Eau Fe 2 Cl 6 anhydre 29 °C X, 5 H 2 O X, 7 H 2 O X, 12 H 2 O - 55 °C X, 4 H 2 O X = Fe 2 Cl 6 2014 -12 -29
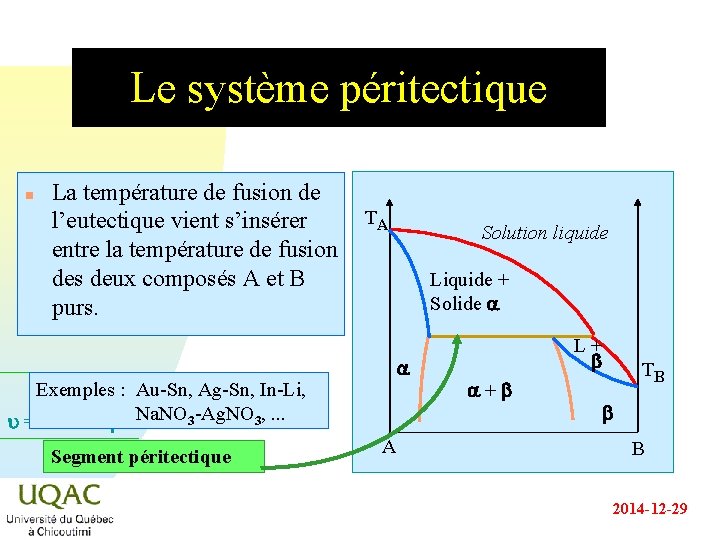
Le système péritectique n La température de fusion de TA l’eutectique vient s’insérer entre la température de fusion des deux composés A et B purs. Liquide + Solide a a Exemples : Au-Sn, Ag-Sn, In-Li, u = C + 2 - Na. NO 3 -Ag. NO 3, . . . Segment péritectique Solution liquide A L + b a+b TB b B 2014 -12 -29
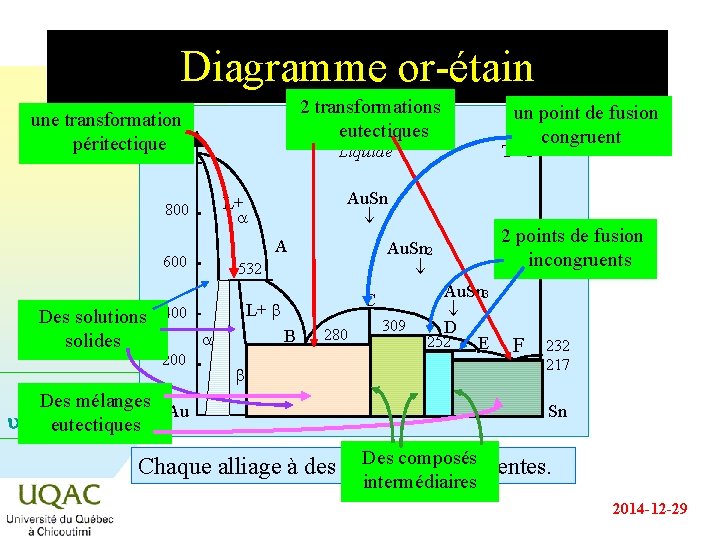
Diagramme or-étain 2 transformations eutectiques une transformation péritectique 1064 Liquide A 600 Des solutions solides Au. Sn 2 532 C L+ b 400 B a 200 Au. Sn L+ a 800 280 309 Au. Sn 3 D 252 E b Des mélanges Au u = C + 2 - eutectiques un point de fusion congruent T °C 2 points de fusion incongruents F 232 217 Sn Des composés Chaque alliage à des propriétés différentes. intermédiaires 2014 -12 -29
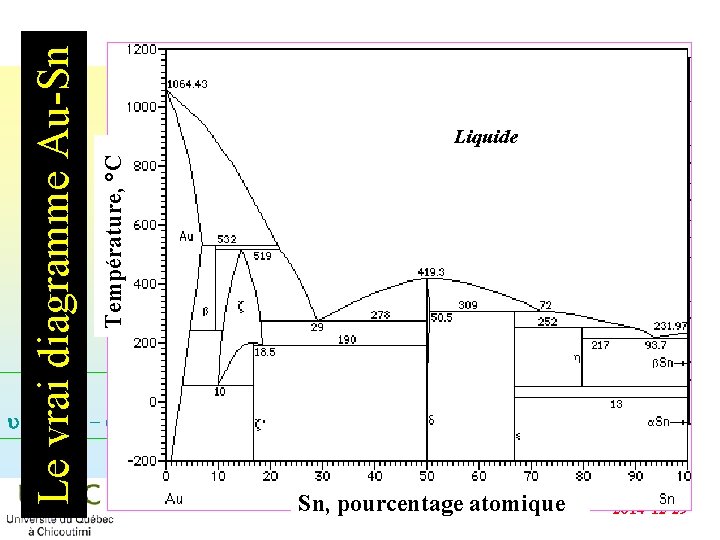
Température, °C Le vrai diagramme Au-Sn Liquide u = C + 2 - Sn, pourcentage atomique 2014 -12 -29

Transformations allotropiques dans une solution solide n Dans le cas de solution solide, par exemple d’une solution d’un peu de B dans un solvant A, l’application de la règle des phases montre que la température de transition de phase dépend de la composition : elle varie avec la teneur en soluté. n u = C + 1 - j = 2 + 1 - 2 = 1. u = C + 2 - 2014 -12 -29

Les alliages à base de cuivre n Laitons: alliages de cuivre et de zinc : u cuivre jaune. n Bronzes (Cu + Sn + Zn) : u monnaies, statues, cloches. n n Bronzes d’aluminium (Cu + Al, 90: 10). Maillechorts (ou argentan) (Cu + Zn + Ni) : u coutellerie (recouverte d’argent : argenterie). u = C + 2 - n Duralumin (Al + Cu, 97: 3). 2014 -12 -29
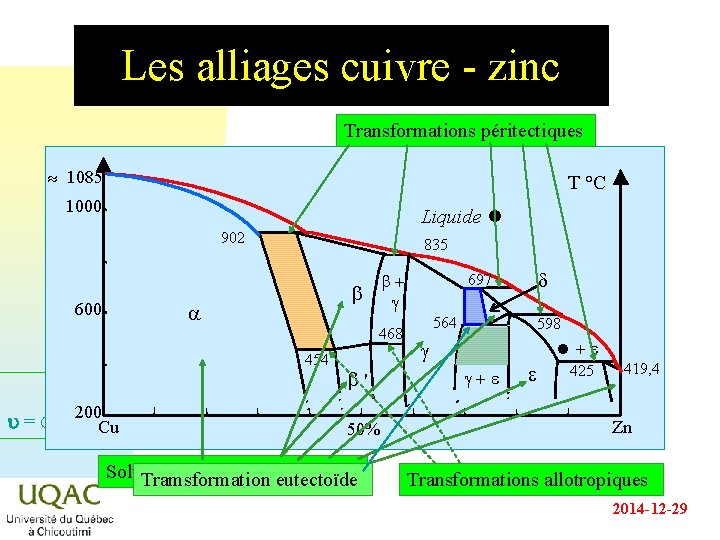
Les alliages cuivre - zinc Transformations péritectiques 1085 T °C 1000 Liquide 902 600 835 b+ g b a 468 454 200 u = C + 2 - Cu b' 50% Solutions solides a, b, g, d et e Tramsformation eutectoïde d 697 564 598 +e g g+e e 425 419, 4 Zn Transformations allotropiques 2014 -12 -29

Transformations allotropiques n n u = C + 2 - n Un solide (s) cristallise par exemple à partir de son liquide à la température ordinaire dans un système particulier. À une autre température, il peut cristalliser dans un autre système cristallin. L’application de la règle de la variance montre que la température de transition est unique et déterminée par le système. n u = C + 1 - j = 1 + 1 - 2 = 0 Fe (a, magnétique) Fe (a, paramagnétique) à 760 °C. n Fe (a) Fe (g) à 910 °C. Application la trempe physique. 2014 -12 -29
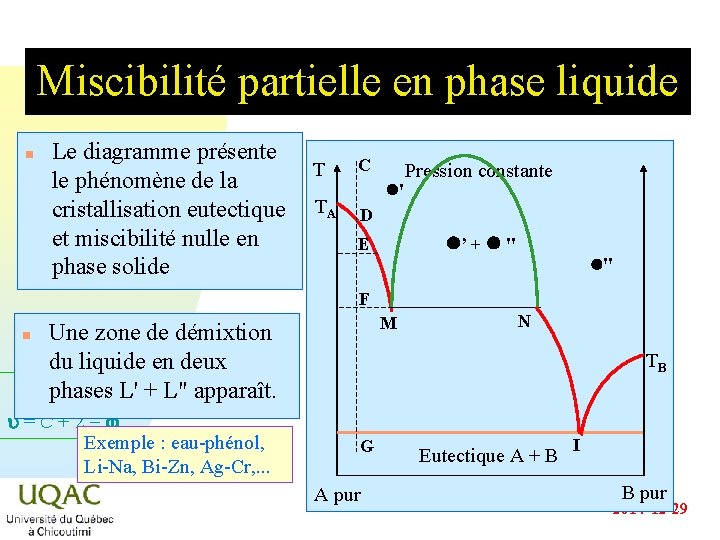
Miscibilité partielle en phase liquide n Le diagramme présente T le phénomène de la cristallisation eutectique TA et miscibilité nulle en phase solide C l' Pression constante D l’ + l " E l" F n M Une zone de démixtion du liquide en deux phases L' + L" apparaît. u = C + 2 - Exemple : eau-phénol, Li-Na, Bi-Zn, Ag-Cr, . . . N TB G A pur Eutectique A + B I B pur 2014 -12 -29

Le diagramme fer-carbone La fabrication des aciers est à l’évidence d’importance économique indiscutable. n La métallurgie du fer est tributaire de différents minerais, oxydes de fer, que sont : u la magnétite, Fe 3 O 4, u le sesquioxyde de fer, Fe 2 O 3, l’hématite rouge, u l’oxyde ferrique hydraté, 2 Fe 2 O 3, 3 H 2 O, l’hématite brune, u = C + 2 - u l’ilménite, Fe. Ti. O 3 que l’on trouve sur la Côte-Nord, u . . . n 2014 -12 -29
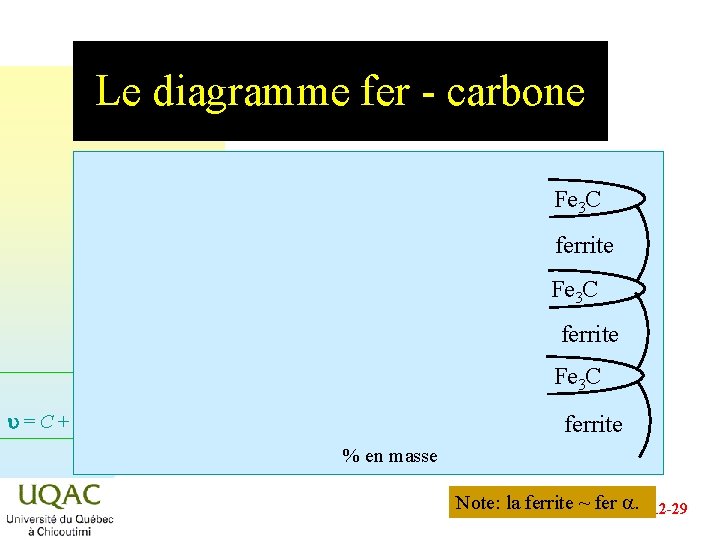
Le diagramme fer - carbone Fe 3 C ferrite Fe 3 C u = C + 2 - ferrite % en masse Note: la ferrite ~ fer a. 2014 -12 -29
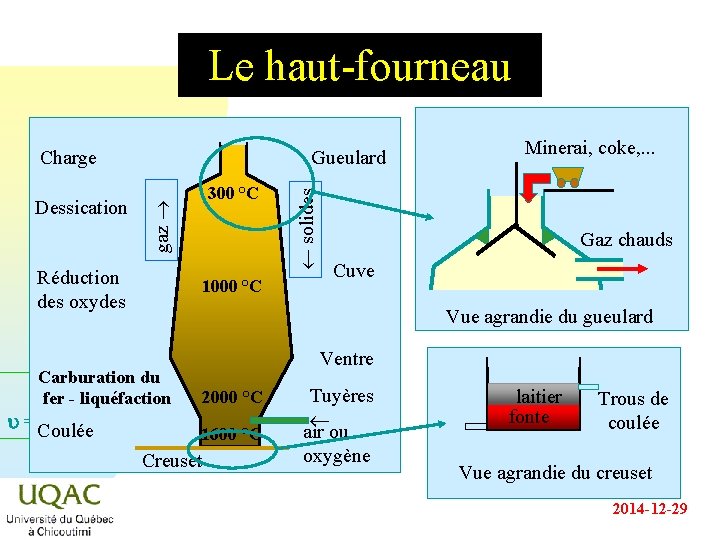
Le haut-fourneau Charge 1000 °C solides Réduction des oxydes Minerai, coke, . . . Gaz chauds Cuve Vue agrandie du gueulard Carburation du fer - liquéfaction u = C + 2 - Coulée 300 °C gaz Dessication Gueulard Ventre 2000 °C 1600 °C Creuset Tuyères air ou oxygène laitier fonte Trous de coulée Vue agrandie du creuset 2014 -12 -29

Le fonctionnement du haut fourneau n 300 °C n 1000 °C La formation de l’agent réducteur : u C(coke) + O 2 (air à 800 ºC) CO 2 + chaleur u réaction suivie de CO 2 + C(coke) 2 CO La réduction du minerai et la formation de la fonte : u Fe 3 O 4 + 4 CO 3 Fe ( ) + 4 CO 2 ( ) u Fe ( ) + C [Fe( ), Fe 3 C] u = C + 2 - 2000 °C 1600 °C n L’élimination des impuretés : u Ca. CO 3 + chaleur Ca. O + CO 2 ( ) u Ca. O + Si. O 2 Ca. Si. O 3 2014 -12 -29

Le fonctionnement du haut fourneau 0, 25 0, 5 PCO 300 °C Fe 600 1000 °C PCO + PCO 2 Fe 3 O 4 1000 1400 u = C + 2 - 0, 75 Fe. O 2000 °C 1600 °C 2014 -12 -29

De la fonte à l’acier n n n La fonte obtenue est cassante et peu malléable. Il faut éliminer le silicium et les traces de soufre et de phosphore. On peut procéder à leur oxydation. Deux procédés ont été développés : on oxyde le milieu directement à l’air (procédé BESSEMER), u ou on ajoutant de l’hématite (procédé MARTIN) + énergie d’appoint. u n Le procédé MARTIN permet un dosage plus fin des mélanges métalliques que l’on souhaite incorporer à l’acier. On peut ajouter du carbone pour obtenir l’acier désiré. u = C + 2 - n Fe 2 O 3 + 3 C 2 Fe + 3 CO ( ) 2014 -12 -29
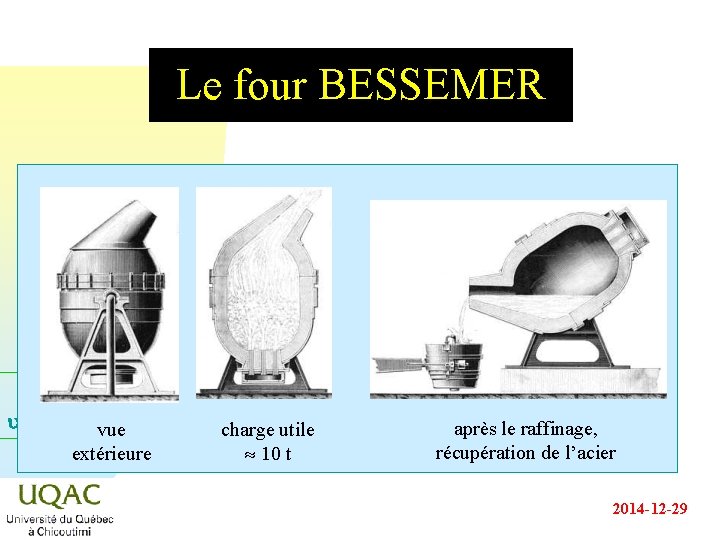
Le four BESSEMER u = C + 2 - vue extérieure charge utile 10 t après le raffinage, récupération de l’acier 2014 -12 -29
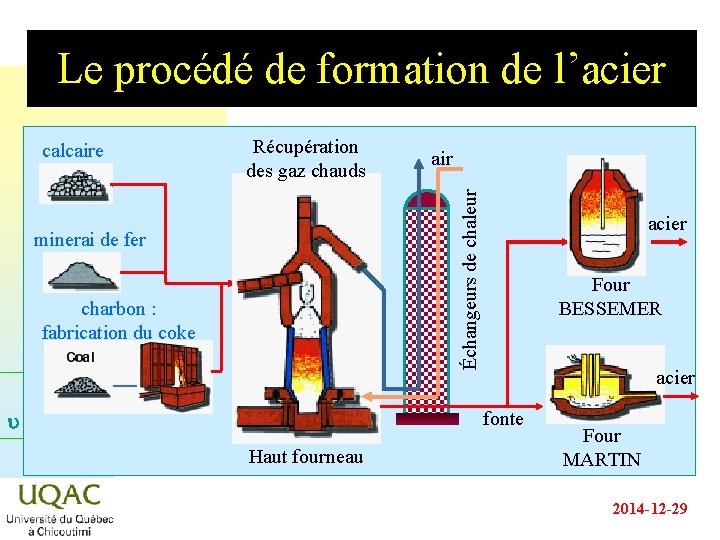
Le procédé de formation de l’acier Récupération des gaz chauds air Échangeurs de chaleur calcaire minerai de fer charbon : fabrication du coke acier Four BESSEMER acier fonte u = C + 2 - Haut fourneau Four MARTIN 2014 -12 -29
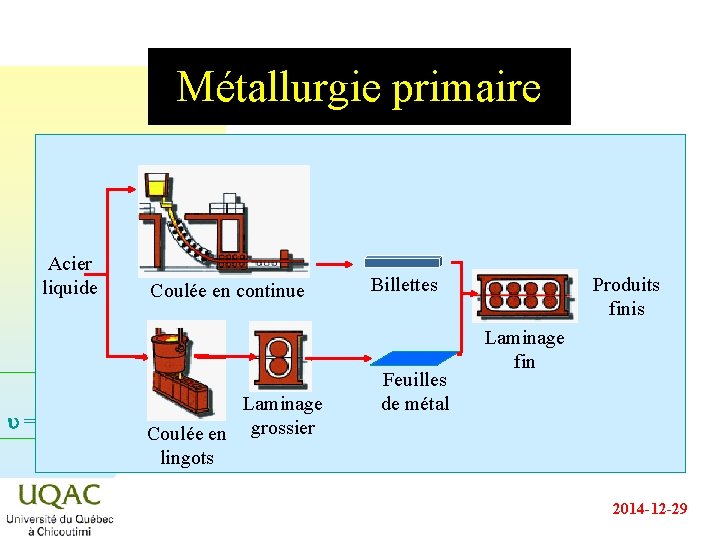
Métallurgie primaire Acier liquide u = C + 2 - Coulée en continue Laminage Coulée en grossier lingots Billettes Feuilles de métal Produits finis Laminage fin 2014 -12 -29

Conclusion La solubilité réciproque des constituants est fortement dépendante du diamètre des atomes ou des molécules constitutifs. n Dans le cas de mélanges de deux solides de diamètres semblables et dont le réseau cristallin est identique, les diagrammes solide - solide observés ressemblent à ceux des mélanges de deux liquides complètement miscibles. n Pour les mélanges plus difficilement miscibles on observe des diagrammes de plus en plus déformés au fur et à mesure de la décroissance de la miscibilité. u = C + 2 - n Apparaissent ainsi les diagrammes eutectiques et péritectiques. n 2014 -12 -29

Conclusion n n Des particularités viennent compliquer l’allure des diagramme comme par exemple la formation de composés intermédiaires. Les utilisations des mélanges binaires et surtout de leurs propriétés sont nombreux et variés : u l’épandage de sel sur la chaussée verglacée, u la fabrication d’alliages, u = C + 2 - u la fabrication de l’acier, . . . 2014 -12 -29
- Slides: 47