Les cycloadditions dipolaires prfrent la thorie valence bond
Les cycloadditions dipolaires préfèrent la théorie valence bond… P. C. Hiberty, LCP Orsay B. Braïda, LCT Jussieu C. Walter, stagiaire M 2
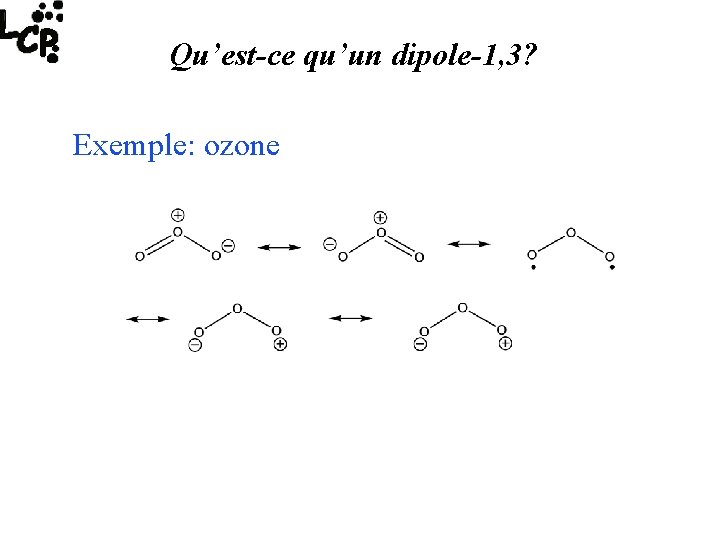
Qu’est-ce qu’un dipole-1, 3? Exemple: ozone
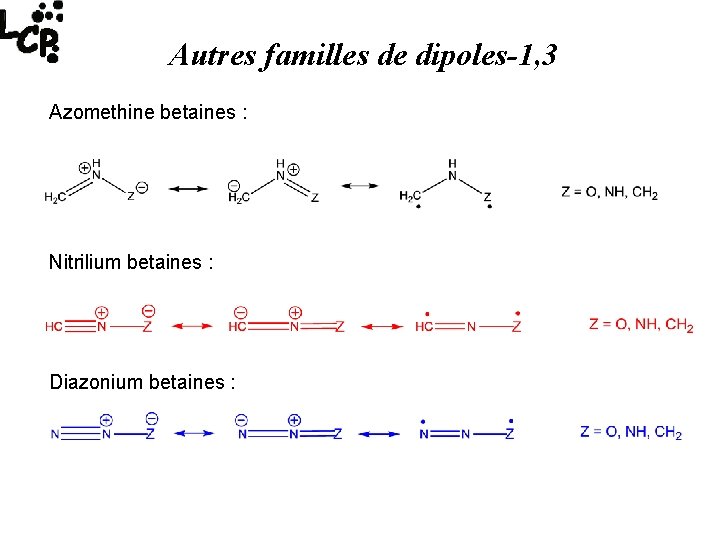
Autres familles de dipoles-1, 3 Azomethine betaines : Nitrilium betaines : Diazonium betaines :
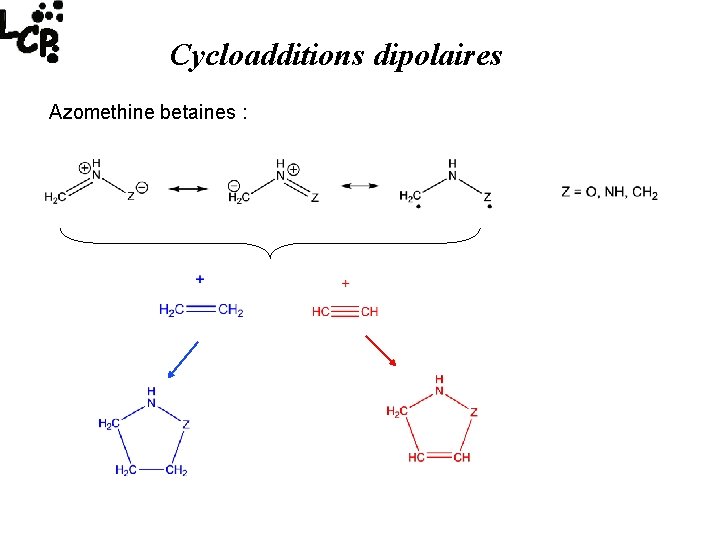
Cycloadditions dipolaires Azomethine betaines :
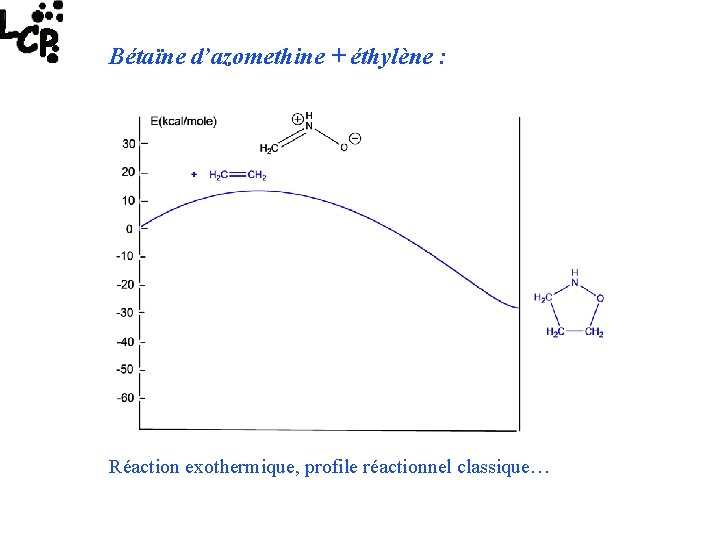
Bétaïne d’azomethine + éthylène : Réaction exothermique, profile réactionnel classique…
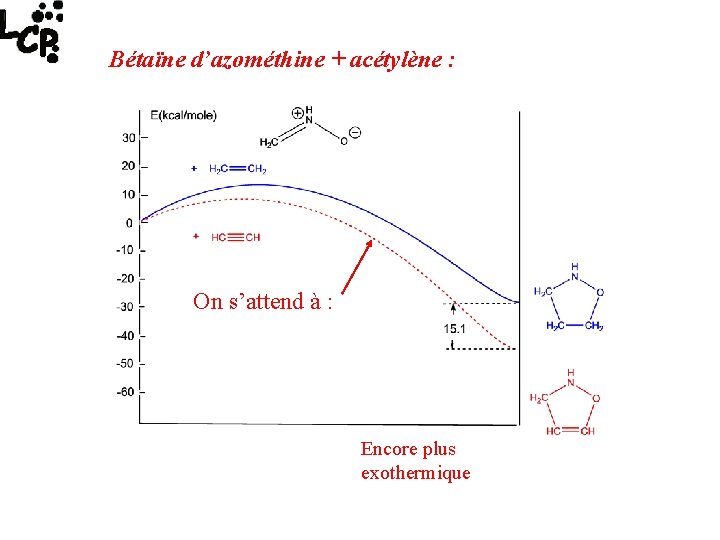
Bétaïne d’azométhine + acétylène : On s’attend à : Encore plus exothermique
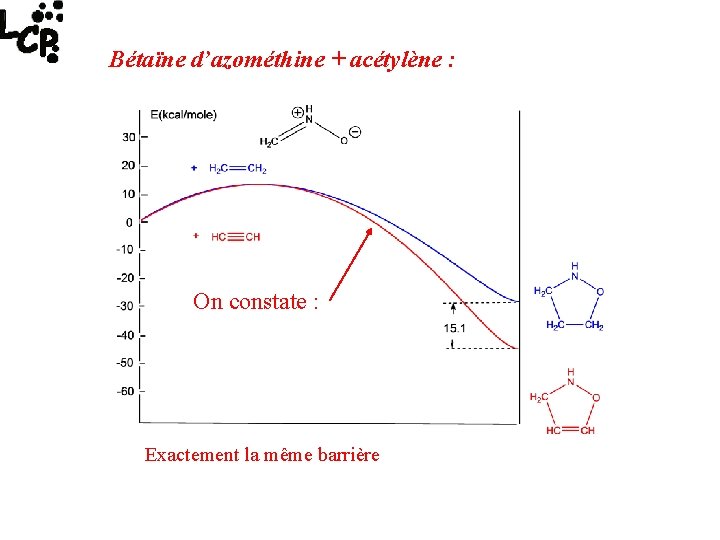
Bétaïne d’azométhine + acétylène : On constate : Exactement la même barrière
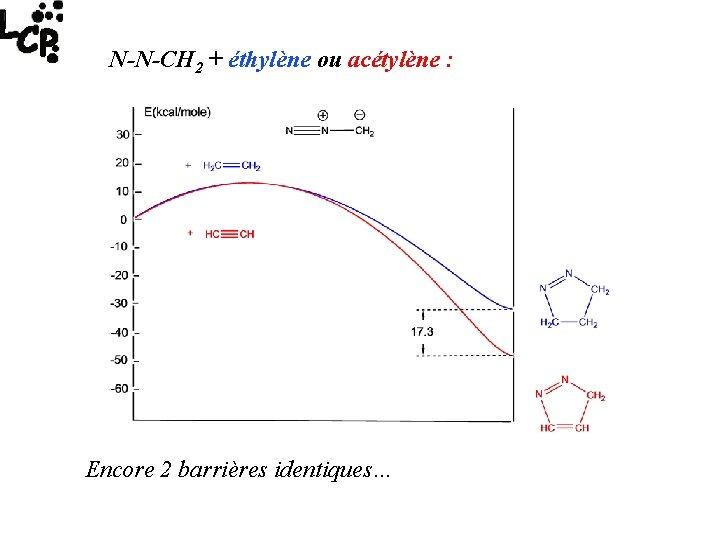
N-N-CH 2 + éthylène ou acétylène : Encore 2 barrières identiques…
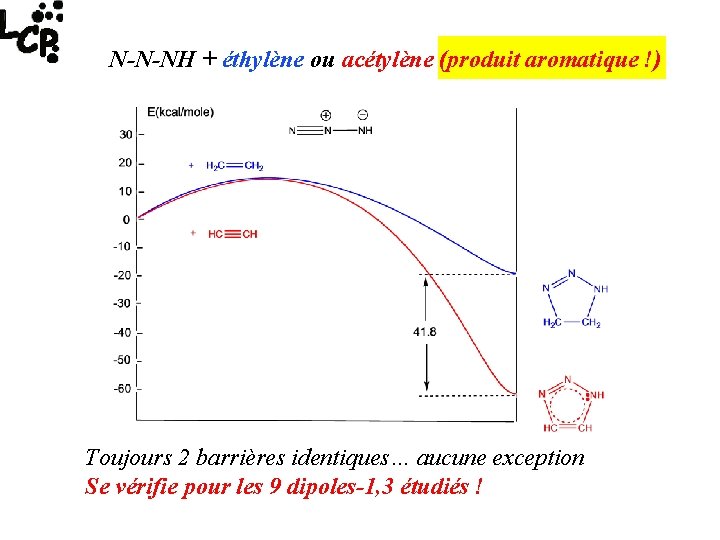
N-N-NH + éthylène ou acétylène (produit aromatique !) Toujours 2 barrières identiques… aucune exception Se vérifie pour les 9 dipoles-1, 3 étudiés !
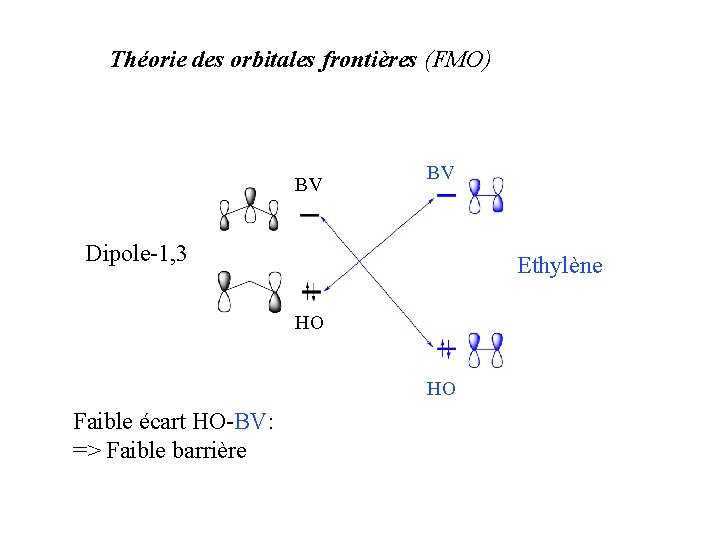
Théorie des orbitales frontières (FMO) BV BV Dipole-1, 3 Ethylène HO HO Faible écart HO-BV: => Faible barrière
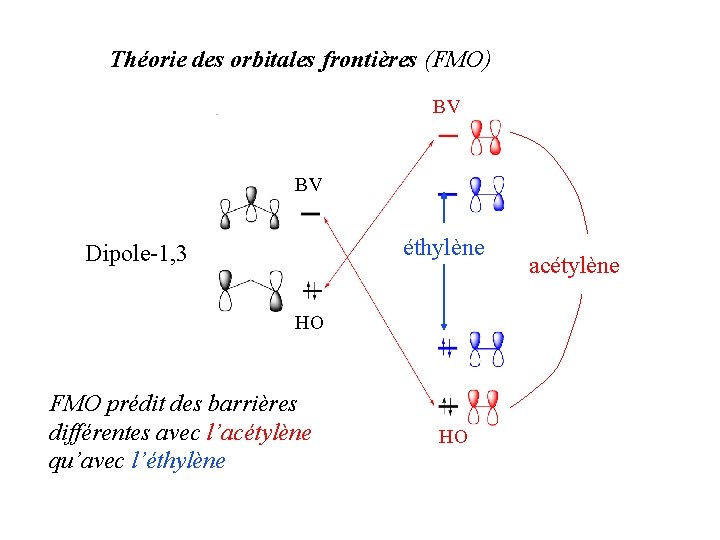
Théorie des orbitales frontières (FMO) BV BV éthylène Dipole-1, 3 HO FMO prédit des barrières différentes avec l’acétylène qu’avec l’éthylène HO acétylène
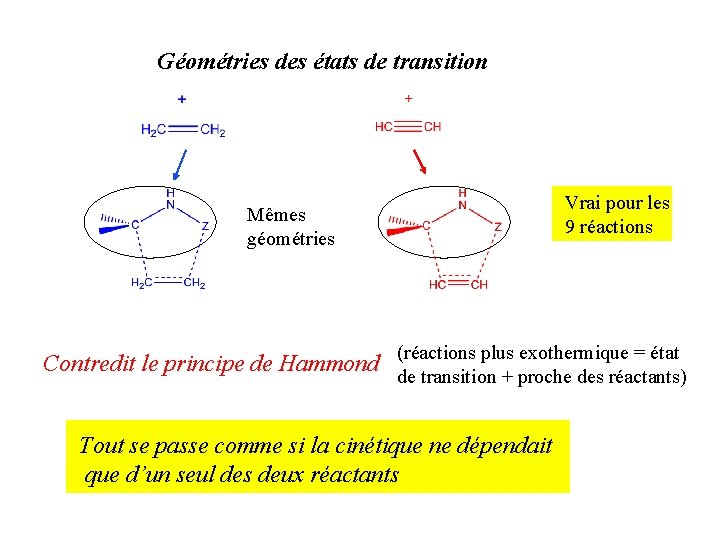
Géométries des états de transition Vrai pour les 9 réactions Mêmes géométries (réactions plus exothermique = état Contredit le principe de Hammond de transition + proche des réactants) Tout se passe comme si la cinétique ne dépendait que d’un seul des deux réactants
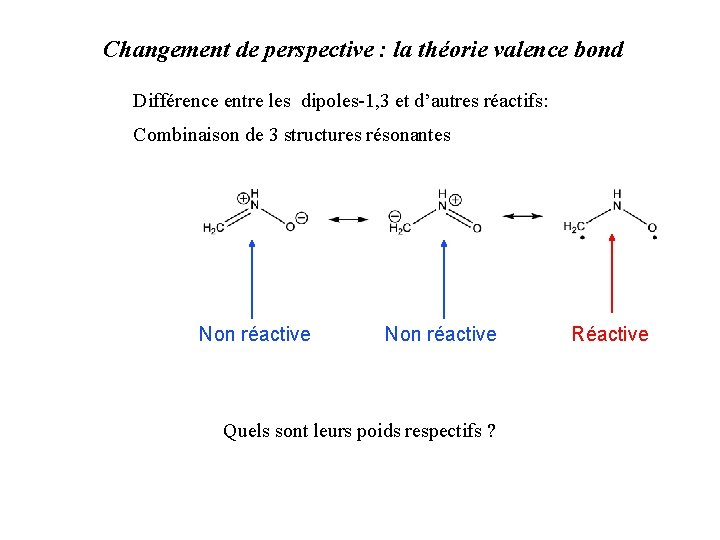
Changement de perspective : la théorie valence bond Différence entre les dipoles-1, 3 et d’autres réactifs: Combinaison de 3 structures résonantes Non réactive Quels sont leurs poids respectifs ? Réactive
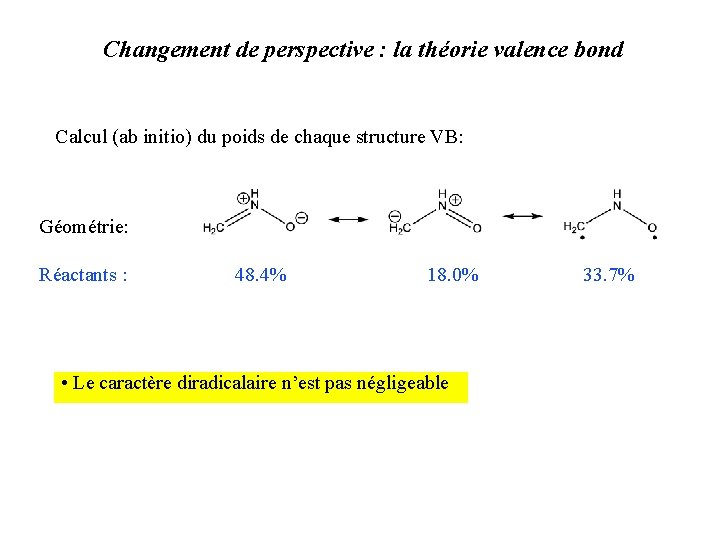
Changement de perspective : la théorie valence bond Calcul (ab initio) du poids de chaque structure VB: Géométrie: Réactants : 48. 4% 18. 0% • Le caractère diradicalaire n’est pas négligeable 33. 7%
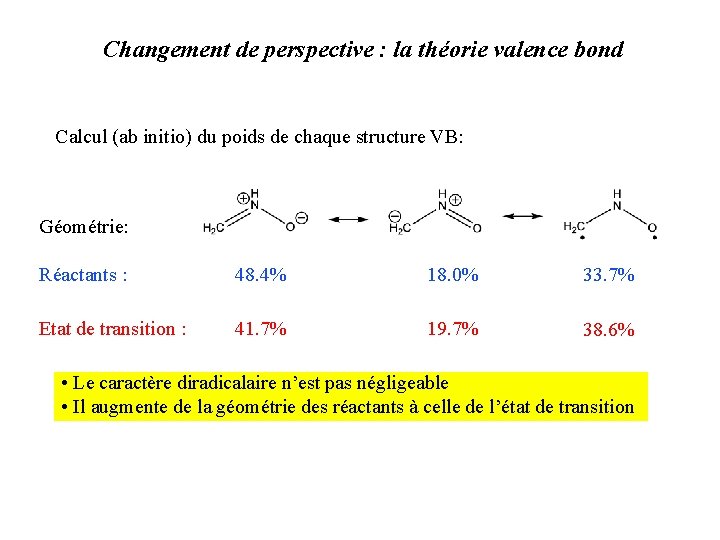
Changement de perspective : la théorie valence bond Calcul (ab initio) du poids de chaque structure VB: Géométrie: Réactants : 48. 4% 18. 0% 33. 7% Etat de transition : 41. 7% 19. 7% 38. 6% • Le caractère diradicalaire n’est pas négligeable • Il augmente de la géométrie des réactants à celle de l’état de transition
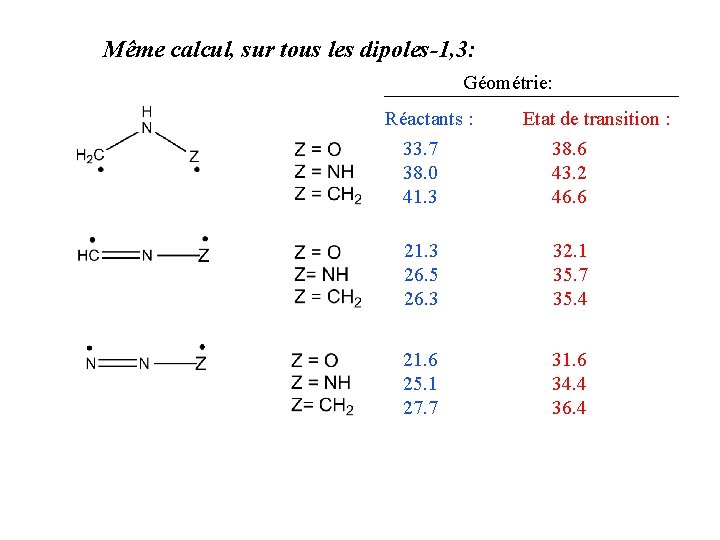
Même calcul, sur tous les dipoles-1, 3: Géométrie: Réactants : Etat de transition : 33. 7 38. 0 41. 3 38. 6 43. 2 46. 6 21. 3 26. 5 26. 3 32. 1 35. 7 35. 4 21. 6 25. 1 27. 7 31. 6 34. 4 36. 4
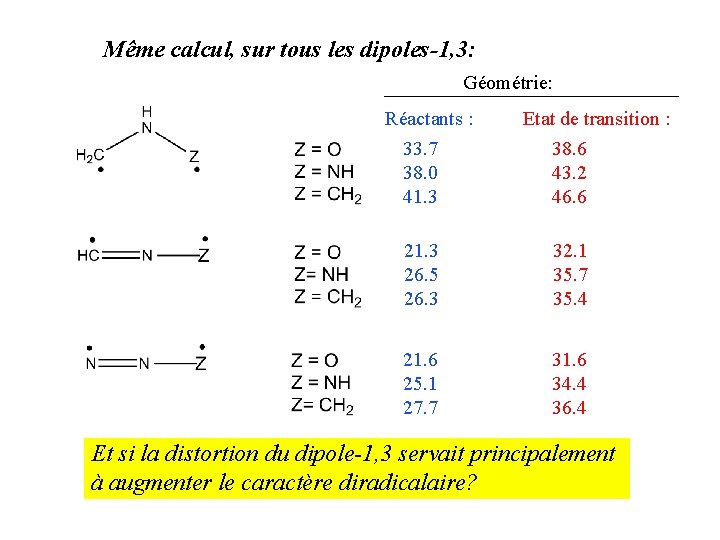
Même calcul, sur tous les dipoles-1, 3: Géométrie: Réactants : Etat de transition : 33. 7 38. 0 41. 3 38. 6 43. 2 46. 6 21. 3 26. 5 26. 3 32. 1 35. 7 35. 4 21. 6 25. 1 27. 7 31. 6 34. 4 36. 4 Et si la distortion du dipole-1, 3 servait principalement à augmenter le caractère diradicalaire?
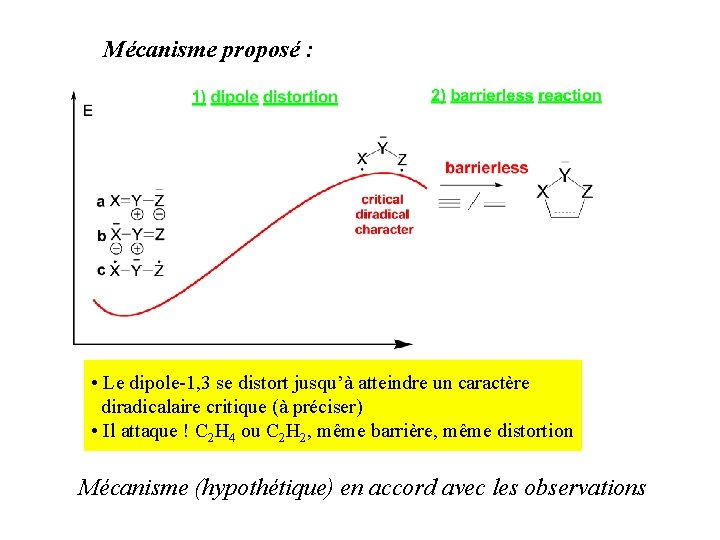
Mécanisme proposé : • Le dipole-1, 3 se distort jusqu’à atteindre un caractère diradicalaire critique (à préciser) • Il attaque ! C 2 H 4 ou C 2 H 2, même barrière, même distortion Mécanisme (hypothétique) en accord avec les observations
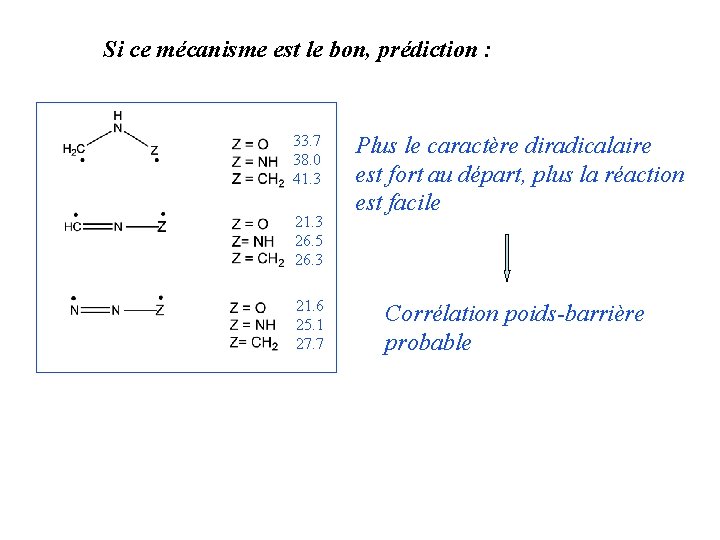
Si ce mécanisme est le bon, prédiction : 33. 7 38. 0 41. 3 26. 5 26. 3 21. 6 25. 1 27. 7 Plus le caractère diradicalaire est fort au départ, plus la réaction est facile Corrélation poids-barrière probable
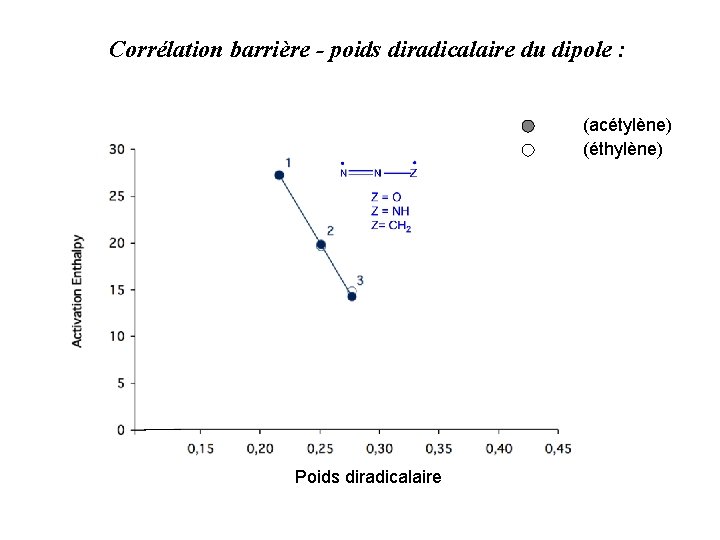
Corrélation barrière - poids diradicalaire du dipole : (acétylène) (éthylène) Poids diradicalaire
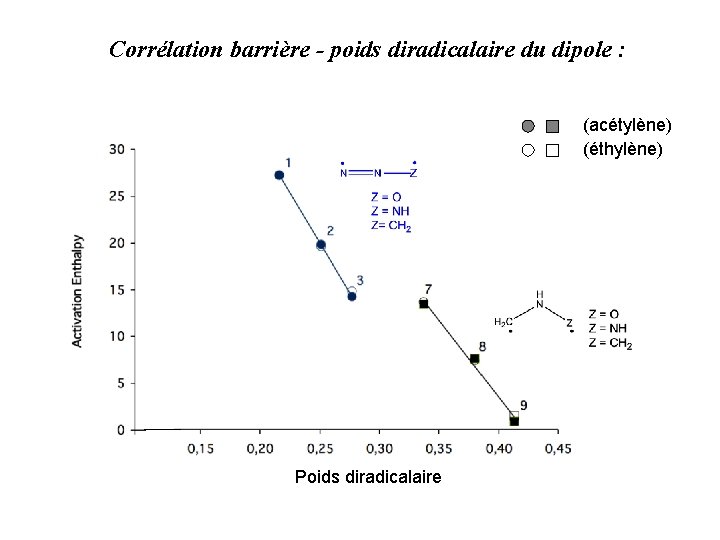
Corrélation barrière - poids diradicalaire du dipole : (acétylène) (éthylène) Poids diradicalaire
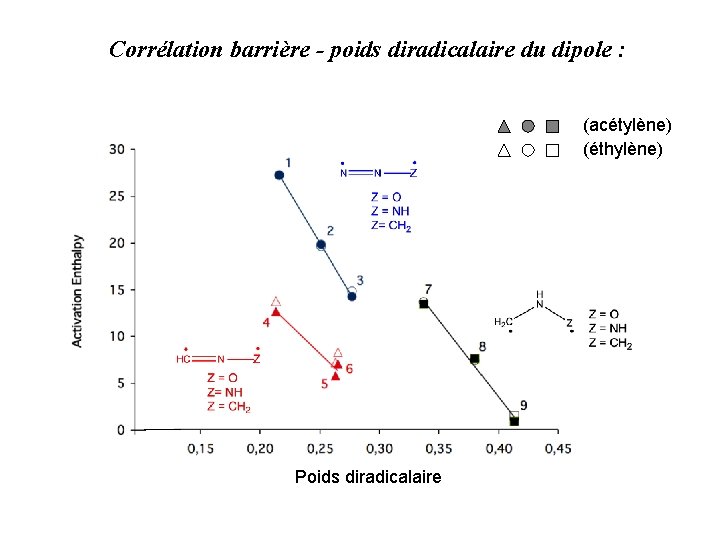
Corrélation barrière - poids diradicalaire du dipole : (acétylène) (éthylène) Poids diradicalaire
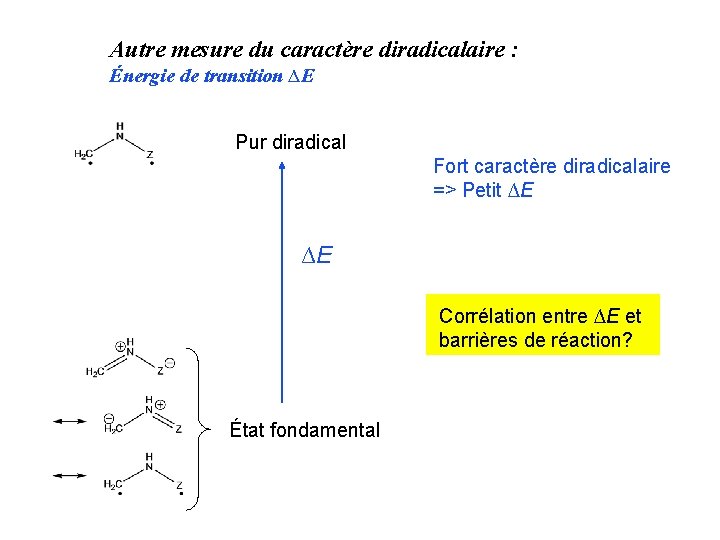
Autre mesure du caractère diradicalaire : Énergie de transition ∆E Pur diradical Fort caractère diradicalaire => Petit ∆E ∆E Corrélation entre ∆E et barrières de réaction? État fondamental
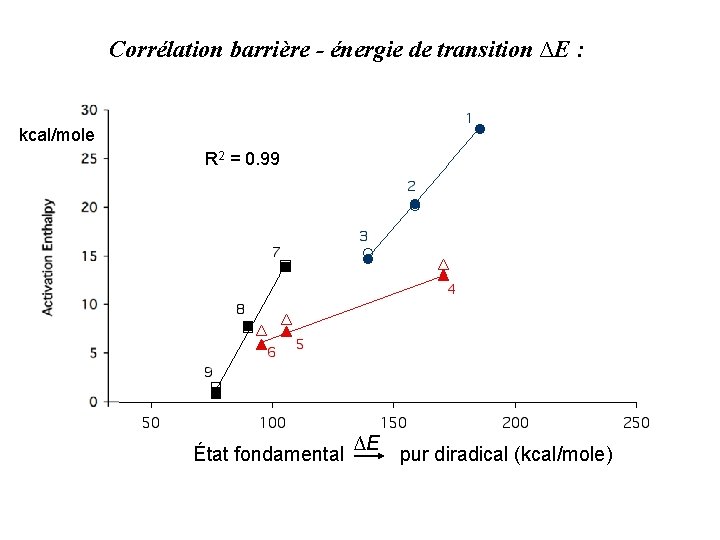
Corrélation barrière - énergie de transition ∆E : kcal/mole R 2 = 0. 99 État fondamental ∆E pur diradical (kcal/mole)

Énergie de transition ∆E (géométrie des réactants) ∆E ( ) plutôt dispersés ∆E État fondamental pur diradical (kcal/mole)

Énergie de transition ∆E ( = géométrie à l’état de transition) ∆E ( ) beaucoup moins dispersés ∆E État fondamental pur diradical (kcal/mole) Les dipoles ont ~ le même caractère diradicalaire une fois atteint l’état de transition
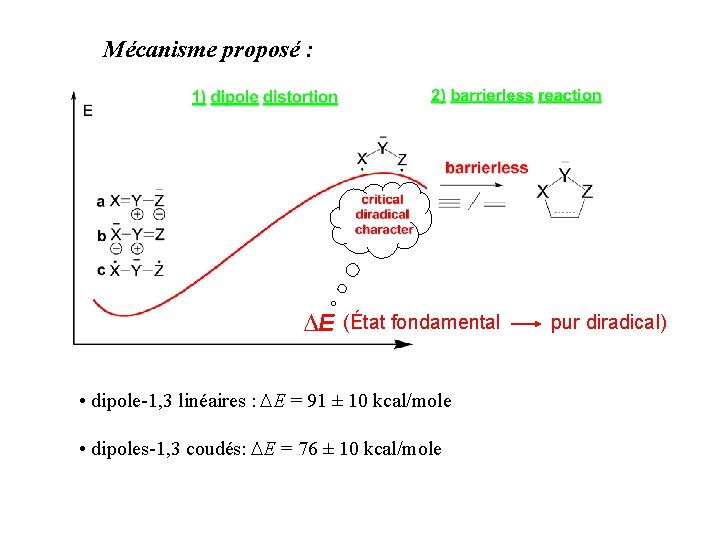
Mécanisme proposé : ∆E (État fondamental • dipole-1, 3 linéaires : ∆E = 91 ± 10 kcal/mole • dipoles-1, 3 coudés: ∆E = 76 ± 10 kcal/mole pur diradical)

« Give me insight, not numbers » (Charles Coulson) Cycloadditions dipolaires • Les dipoles-1, 3 sont des réactifs à part (violent les lois habituelles) • Le caractère diradicalaire est crucial • Un mécanisme est proposé, cohérent avec les observations • Barrières de réaction estimées à partir des propriétés des réactifs Valence bond et Orbitales moléculaires; 2 théories exactes • VB plus éclairante que les OM dans ce cas • VB vs OM: décrivent la réalité dans deux langages différents Valence bond, juste un changement de perspective

Try to see things from a different perspective (Prof. Keating, Dead Poets Society) Thanks to : B. Braida, Laboratoire de Chimie Théorique, Université de Paris 6, 75252 Paris, France C. Walter and B. Engels, Institut für Organische Chemie 97074 Würzburg, Germany
- Slides: 29