Les Cellules Souches Hmatopotiques CSH Dfinition Fonctions et






- Slides: 34

Les Cellules Souches Hématopoïétiques (CSH) - Définition - Fonctions et dévelopment - CSH en thérapies - Niche et motilité Isabelle Petit INSERM U 898 (D. Aberdam) ipetit@unice. fr

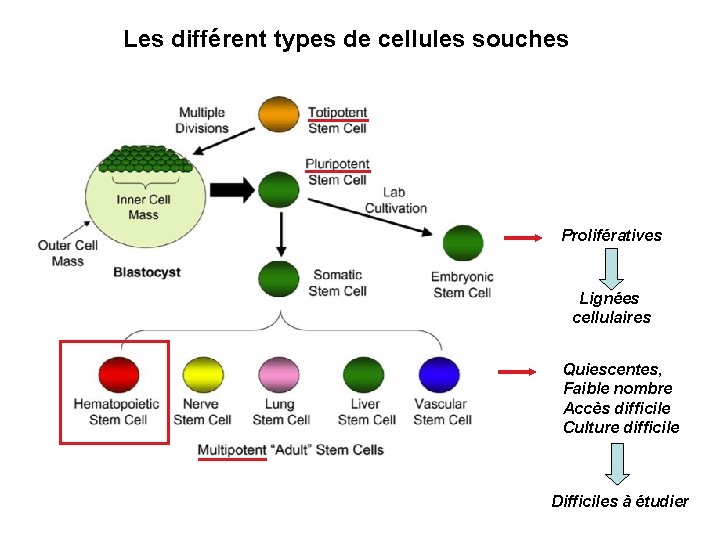
Les différent types de cellules souches Prolifératives Lignées cellulaires Quiescentes, Faible nombre Accès difficile Culture difficile Difficiles à étudier

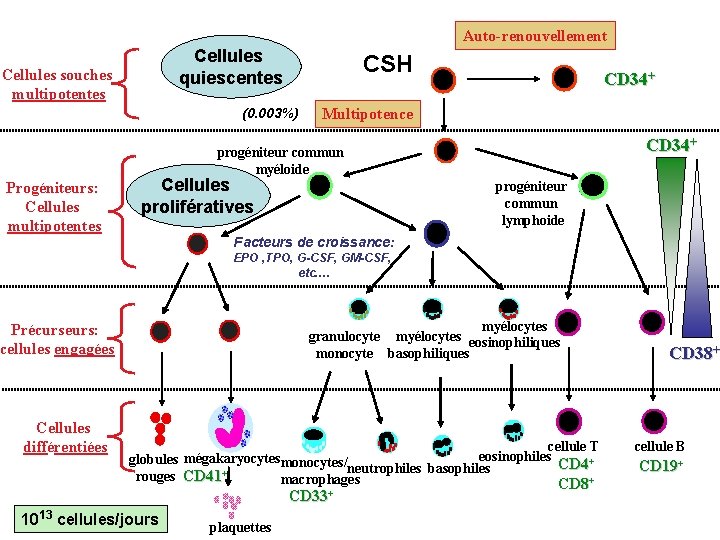
Auto-renouvellement Cellules quiescentes Cellules souches multipotentes CSH (0. 003%) CD 34+ Multipotence CD 34+ progéniteur commun myéloide Progéniteurs: Cellules multipotentes Cellules prolifératives progéniteur commun lymphoide Facteurs de croissance: EPO , TPO, G-CSF, GM-CSF, etc…. myélocytes granulocyte myélocytes eosinophiliques monocyte basophiliques Précurseurs: cellules engagées Cellules différentiées cellule T eosinophiles mégakaryocytes globules monocytes/neutrophiles basophiles CD 4+ + rouges CD 41 macrophages CD 8+ CD 33+ 1013 cellules/jours plaquettes CD 38+ cellule B CD 19+

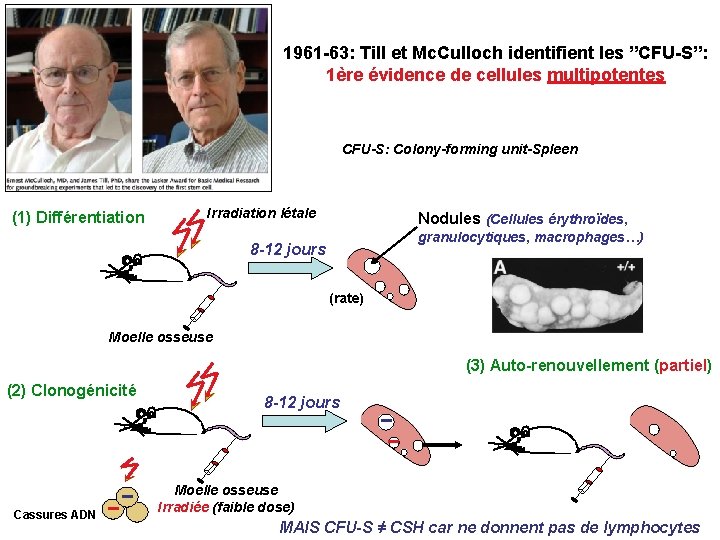
1961 -63: Till et Mc. Culloch identifient les ”CFU-S”: 1ère évidence de cellules multipotentes CFU-S: Colony-forming unit-Spleen (1) Différentiation Irradiation létale Nodules (Cellules érythroïdes, granulocytiques, macrophages…) 8 -12 jours (rate) Moelle osseuse (3) Auto-renouvellement (partiel) (2) Clonogénicité Cassures ADN 8 -12 jours Moelle osseuse Irradiée (faible dose) MAIS CFU-S ≠ CSH car ne donnent pas de lymphocytes

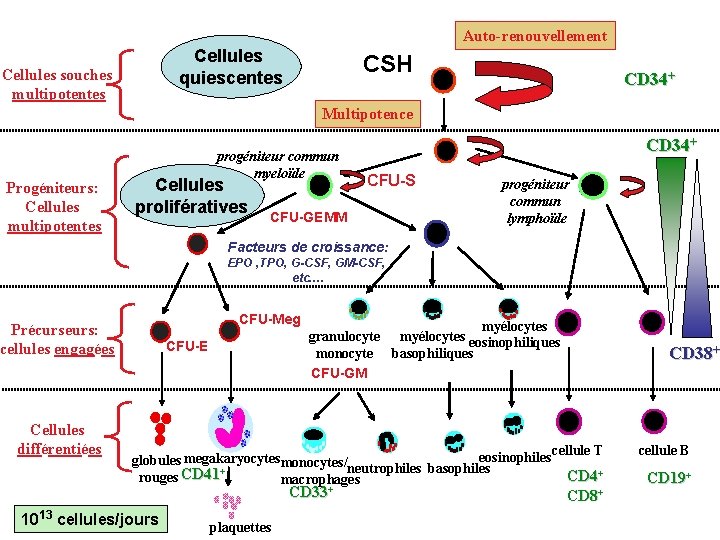
Auto-renouvellement Cellules quiescentes Cellules souches multipotentes CSH CD 34+ Multipotence Progéniteurs: Cellules multipotentes progéniteur commun myeloïde Cellules prolifératives CD 34+ CFU-S CFU-GEMM progéniteur commun lymphoïde Facteurs de croissance: EPO , TPO, G-CSF, GM-CSF, etc…. CFU-Meg Précurseurs: cellules engagées Cellules différentiées CFU-E myélocytes granulocyte myélocytes eosinophiliques monocyte basophiliques CFU-GM CD 38+ eosinophiles cellule T globules megakaryocytes monocytes/ neutrophiles basophiles + CD 4+ rouges CD 41 macrophages CD 33+ 1013 cellules/jours plaquettes CD 8+ cellule B CD 19+

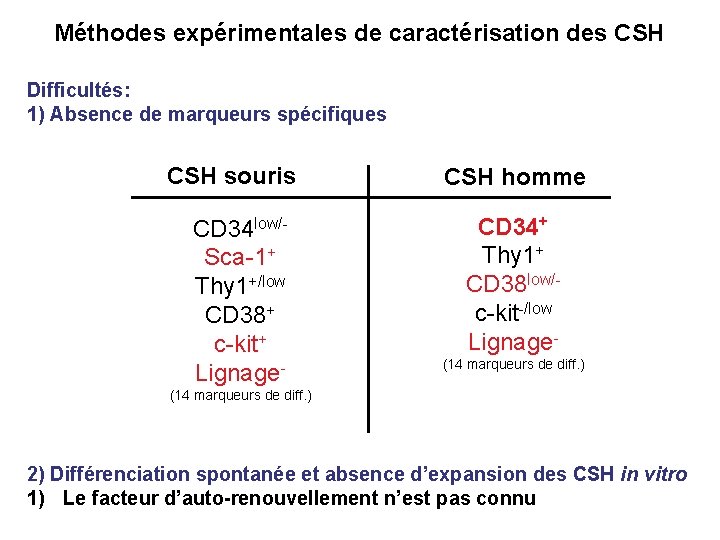
Méthodes expérimentales de caractérisation des CSH Difficultés: 1) Absence de marqueurs spécifiques CSH souris CD 34 low/Sca-1+ Thy 1+/low CD 38+ c-kit+ Lignage- CSH homme CD 34+ Thy 1+ CD 38 low/c-kit-/low Lignage(14 marqueurs de diff. ) 2) Différenciation spontanée et absence d’expansion des CSH in vitro 1) Le facteur d’auto-renouvellement n’est pas connu

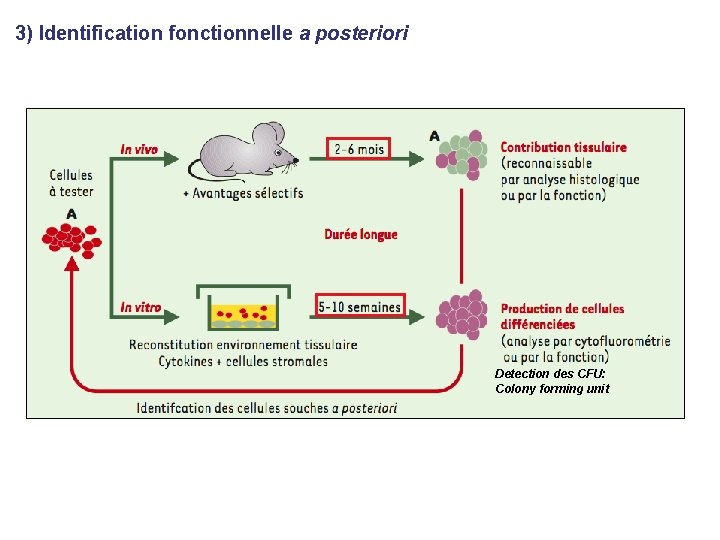
3) Identification fonctionnelle a posteriori Detection des CFU: Colony forming unit

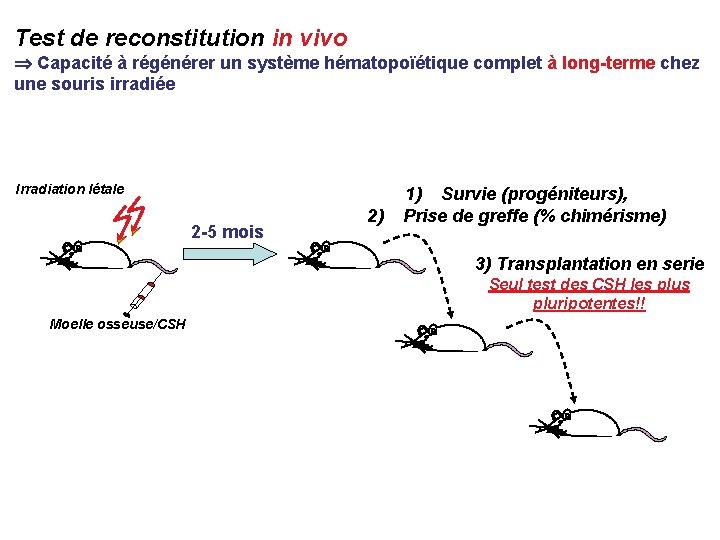
Test de reconstitution in vivo Capacité à régénérer un système hématopoïétique complet à long-terme chez une souris irradiée Irradiation létale 2 -5 mois 2) 1) Survie (progéniteurs), Prise de greffe (% chimérisme) 3) Transplantation en serie Seul test des CSH les pluripotentes!! Moelle osseuse/CSH

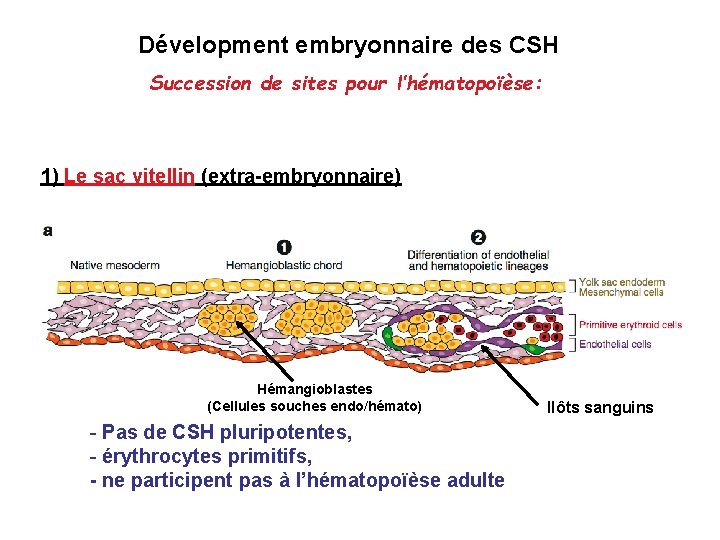
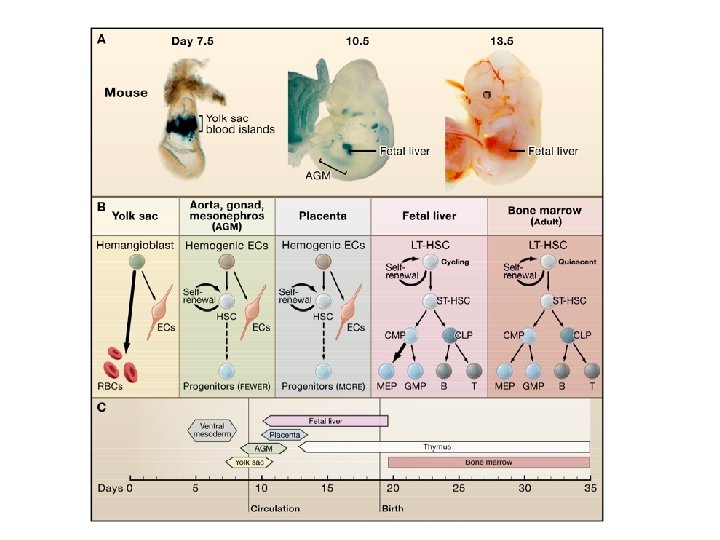
Dévelopment embryonnaire des CSH Succession de sites pour l’hématopoïèse: 1) Le sac vitellin (extra-embryonnaire) Hémangioblastes (Cellules souches endo/hémato) - Pas de CSH pluripotentes, - érythrocytes primitifs, - ne participent pas à l’hématopoïèse adulte Ilôts sanguins

2) La région aorte-gonade-mésonephros (AGM): 1 er site des CSH - CSH pluripotentes (faible nombre), - Progéniteurs multipotents, - pas de différenciation in situ - participent à l’hématopoïèse adulte 3) Le foie fetal: 1 er site d’une hématopoïèse complete - Colonization des CSH pluripotentes de l’AGM - expansion des CSH (nombre définitif) - différenciation importante Migration des cellules du foie vers: 4) Le thymus fétal 5) La rate fétale 6) La moelle osseuse fétale et adulte


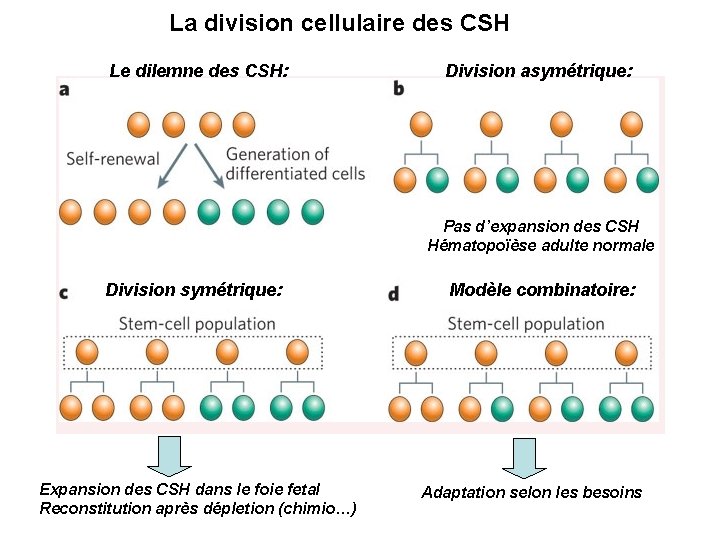
La division cellulaire des CSH Le dilemne des CSH: Division asymétrique: Pas d’expansion des CSH Hématopoïèse adulte normale Division symétrique: Expansion des CSH dans le foie fetal Reconstitution après dépletion (chimio…) Modèle combinatoire: Adaptation selon les besoins

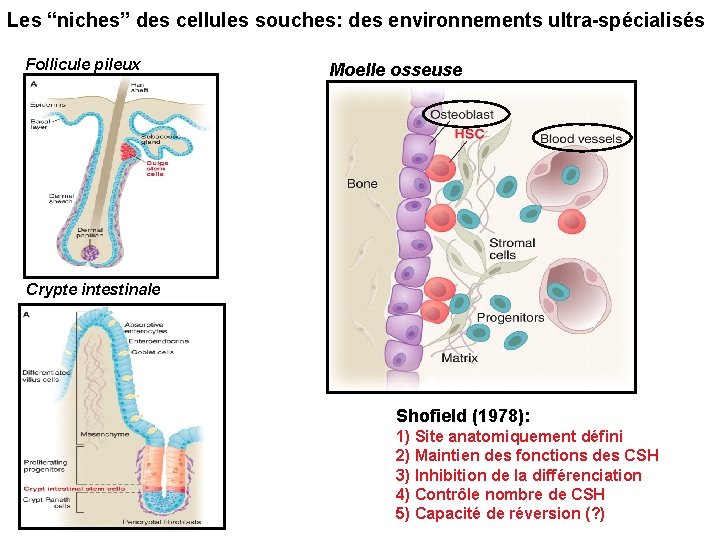
Les “niches” des cellules souches: des environnements ultra-spécialisés Follicule pileux Moelle osseuse Crypte intestinale Shofield (1978): 1) Site anatomiquement défini 2) Maintien des fonctions des CSH 3) Inhibition de la différenciation 4) Contrôle nombre de CSH 5) Capacité de réversion (? )

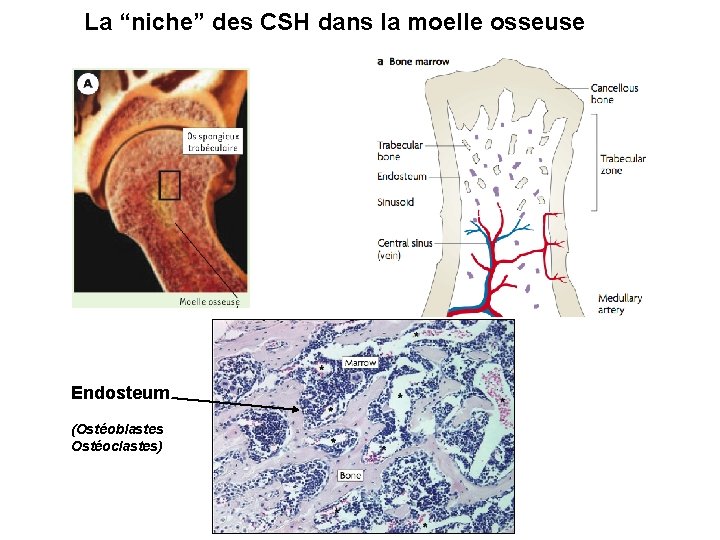
La “niche” des CSH dans la moelle osseuse Endosteum (Ostéoblastes Ostéoclastes)

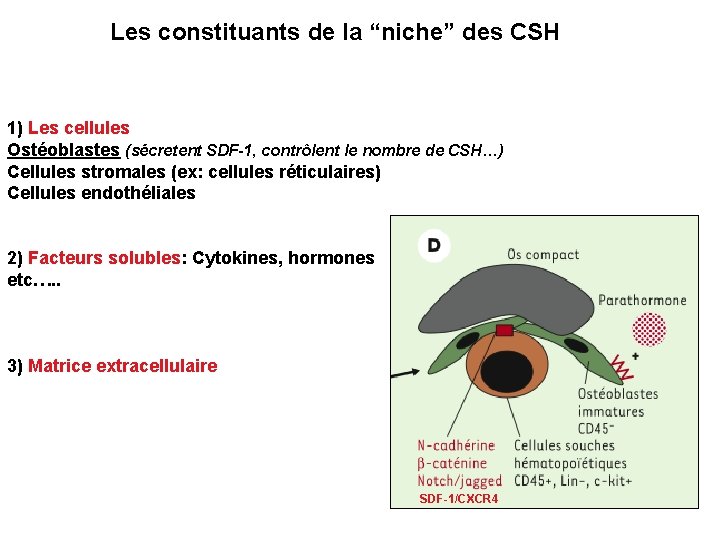
Les constituants de la “niche” des CSH 1) Les cellules Ostéoblastes (sécretent SDF-1, contrôlent le nombre de CSH…) Cellules stromales (ex: cellules réticulaires) Cellules endothéliales 2) Facteurs solubles: Cytokines, hormones etc…. . 3) Matrice extracellulaire SDF-1/CXCR 4

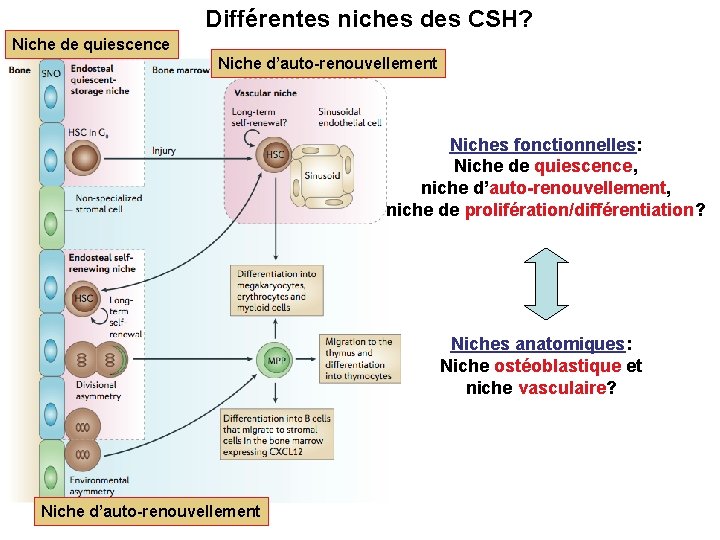
Différentes niches des CSH? Niche de quiescence Niche d’auto-renouvellement Niches fonctionnelles: Niche de quiescence, niche d’auto-renouvellement, niche de prolifération/différentiation? Niches anatomiques: Niche ostéoblastique et niche vasculaire? Niche d’auto-renouvellement

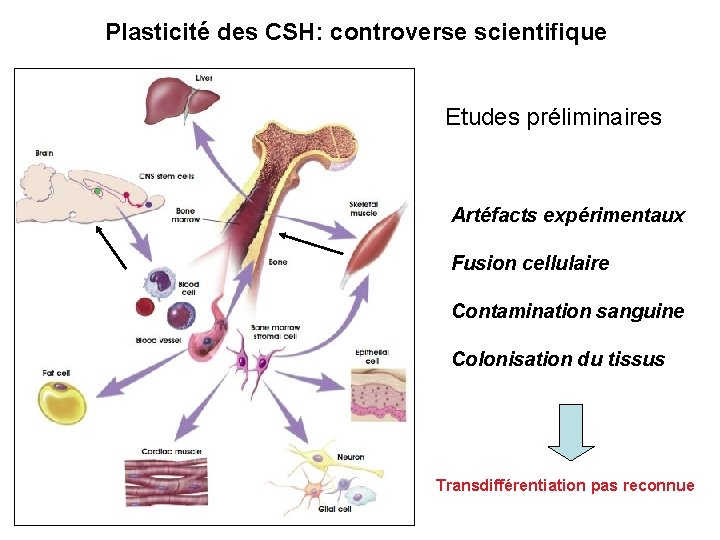
Plasticité des CSH: controverse scientifique Etudes préliminaires Artéfacts expérimentaux Fusion cellulaire Contamination sanguine Colonisation du tissus Transdifférentiation pas reconnue

Les CSH et thérapies cellulaires 1 - les transplantations 1) Restorer une fonction chez des patients avec mutations génétiques: Cancers du système hématopoïétique (leucémies) Maladies génétiques (immunologiques, métaboliques) Allogreffe 2) Conserver et re-injecter les CSH saines après traitement: Tumeurs solides, Lymphomes ou certaines leucémies Autogreffe

Autogreffe Allogreffe Maladies non-malignes • Aplasies médullaires (Fanconi) • Déficits immunitaires combinés sévères • Hémoglobinopathies • Déficit enzymatique (Gaucher) • Autres (ostéopétrose) • Maladies auto-immunes • Maladies génétiques+ thérapie génique Maladies malignes • Leucémies aiguës myeloïdes et lymphoblastiques • Leucémies myéloïdes chroniques • Syndromes myélodisplasiques • Lymphomes, Myélomes, • Leucémie lymphoïde chronique • Syndromes myéloprolifératifs • Tumeurs solides • Myélomes • Lymphomes non-hodgkiniens • Maladie de Hodgkin • Tumeurs solides (cancer du sein, neuroblastomes. . . )

3 propriétés fondamentales des CSH/progéniteurs pour la réussite de la greffe: 1) La pluripotence: Obtention de tous les types cellulaires hématopoiétiques 2) L’auto-renouvellement: Assure le maintien du système hématopoïétique reconstitué à long terme 3) La capacité de “homing” (domiciliation): Permet aux CSH de retourner dans la moelle osseuse après injection I. V. La présence des progéniteurs est importante pour la reconstitution à court-terme!

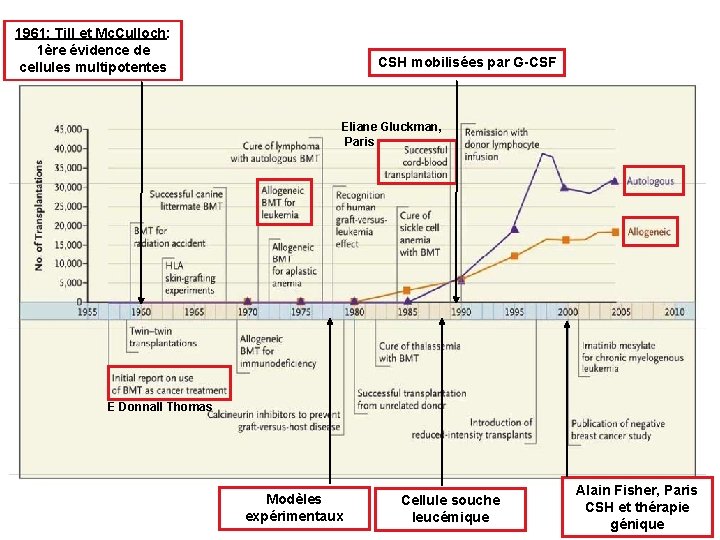
1961: Till et Mc. Culloch: 1ère évidence de cellules multipotentes CSH mobilisées par G-CSF Eliane Gluckman, Paris E Donnall Thomas Modèles expérimentaux Cellule souche leucémique Alain Fisher, Paris CSH et thérapie génique

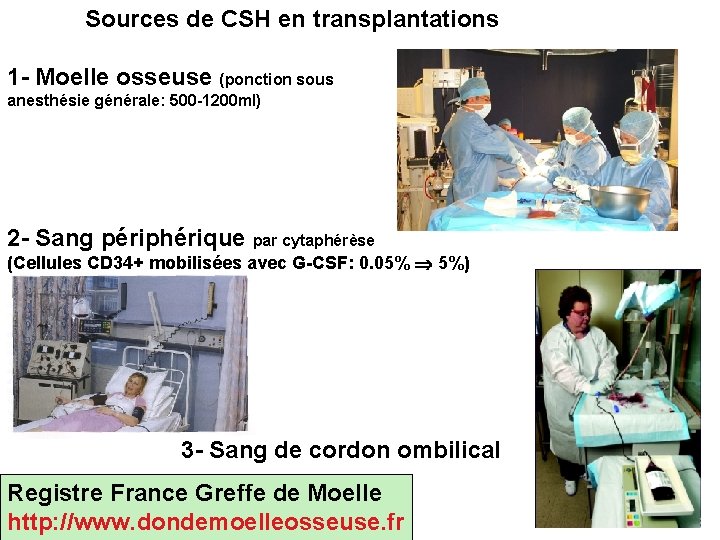
Sources de CSH en transplantations 1 - Moelle osseuse (ponction sous anesthésie générale: 500 -1200 ml) 2 - Sang périphérique par cytaphérèse (Cellules CD 34+ mobilisées avec G-CSF: 0. 05% 5%) 3 - Sang de cordon ombilical Registre France Greffe de Moelle http: //www. dondemoelleosseuse. fr

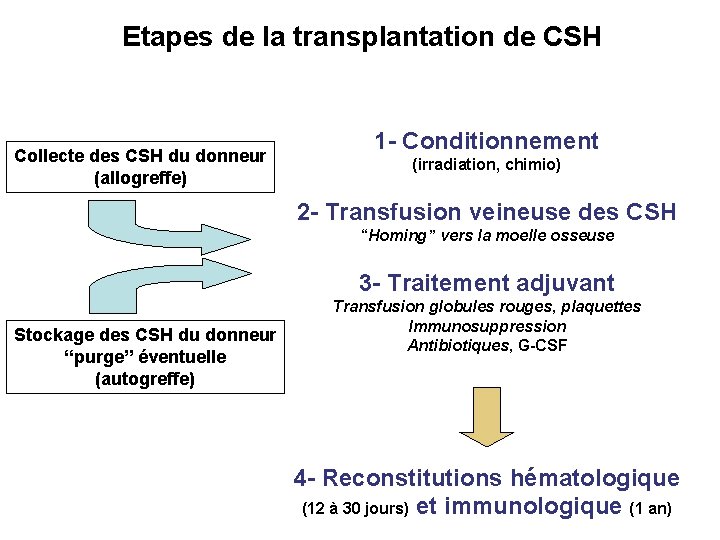
Etapes de la transplantation de CSH Collecte des CSH du donneur (allogreffe) 1 - Conditionnement (irradiation, chimio) 2 - Transfusion veineuse des CSH “Homing” vers la moelle osseuse 3 - Traitement adjuvant Stockage des CSH du donneur “purge” éventuelle (autogreffe) Transfusion globules rouges, plaquettes Immunosuppression Antibiotiques, G-CSF 4 - Reconstitutions hématologique (12 à 30 jours) et immunologique (1 an)

Les CSH et thérapies cellulaires 2 - Réparation cardiaque (essais cliniques 2005 - ) • Injectées au niveau de la lésion cardiaque après infarctus • Les CSH agissent en activant l’angiogénèse • Efficacité pas encore démontrée CSH et thérapies géniques (essais cliniques 2000 - ) Culture des CSH in vitro (cytokines) et transfert de gène (virus) Immunodéficiences (ADA-SCID, X linked-CGD) Maladies métaboliques Résultats: Bonne correction, Cellules T fonctionnelles MAIS: 4/10 enfants (Fisher, Paris) et 1/10 (Londres) ont développé des leucémies (LMO 2)

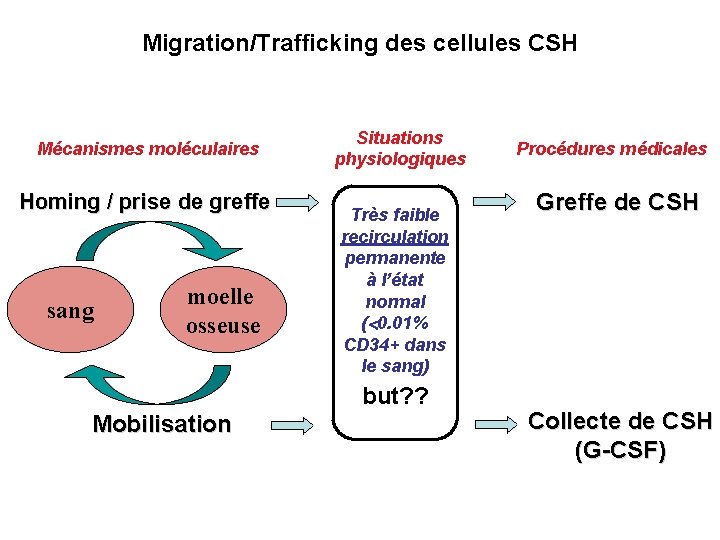
Migration/Trafficking des cellules CSH Mécanismes moléculaires Homing / prise de greffe sang moelle osseuse Situations physiologiques Très faible recirculation permanente à l’état normal ( 0. 01% CD 34+ dans le sang) but? ? Mobilisation Procédures médicales Greffe de CSH Collecte de CSH (G-CSF)

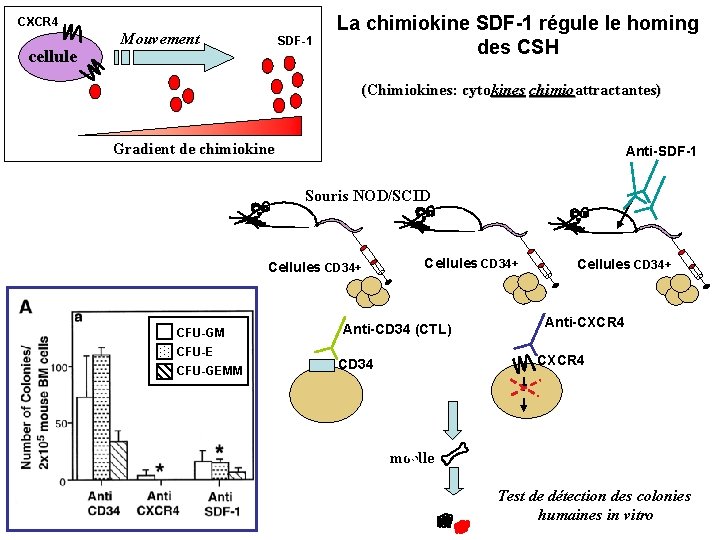
CXCR 4 cellule Mouvement SDF-1 La chimiokine SDF-1 régule le homing des CSH (Chimiokines: cytokines chimioattractantes) Gradient de chimiokine Anti-SDF-1 Souris NOD/SCID Cellules CD 34+ CFU-GM CFU-E CFU-GEMM Cellules CD 34+ Anti-CD 34 (CTL) Cellules CD 34+ Anti-CXCR 4 CD 34 moelle Test de détection des colonies humaines in vitro

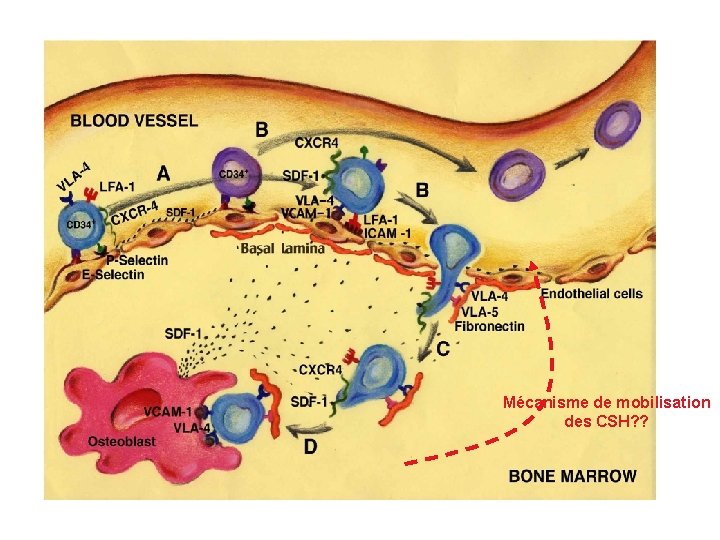
Mécanisme de mobilisation des CSH? ?

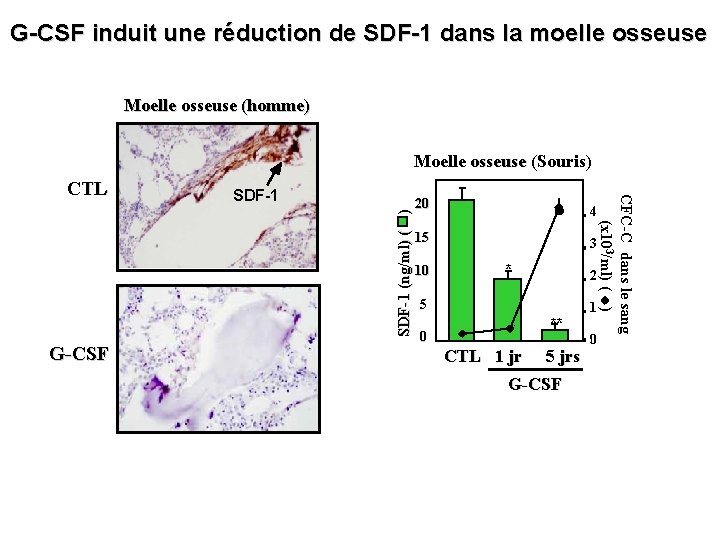
G-CSF induit une réduction de SDF-1 dans la moelle osseuse Moelle osseuse (homme) Moelle osseuse (Souris) SDF-1 (ng/ml) ( ) SDF-1 G-CSF 20 4 15 10 3 * 2 5 ** 0 CTL 1 jr 5 jrs G-CSF 1 0 CFC-C dans le sang (x 103/ml) ( ) CTL

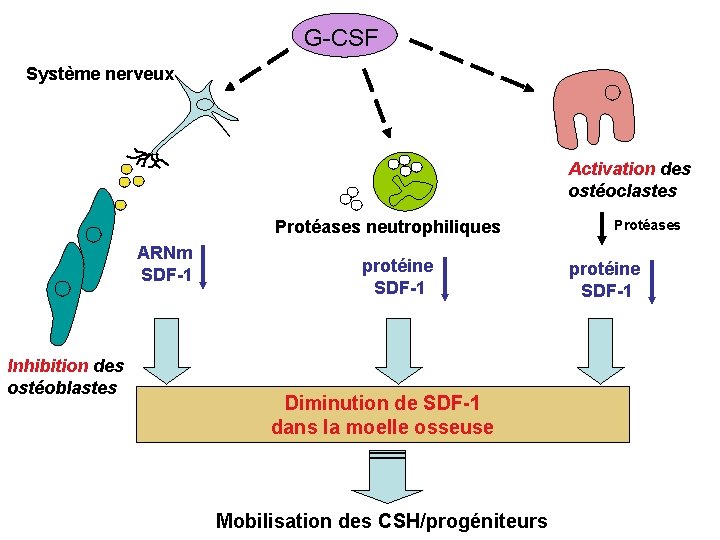
G-CSF Système nerveux Activation des ostéoclastes Protéases neutrophiliques ARNm SDF-1 Inhibition des ostéoblastes protéine SDF-1 Diminution de SDF-1 dans la moelle osseuse Mobilisation des CSH/progéniteurs Protéases protéine SDF-1

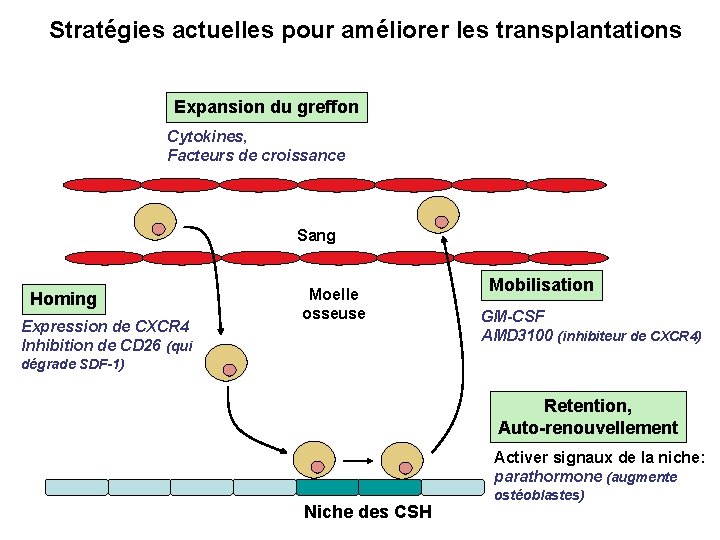
Stratégies actuelles pour améliorer les transplantations Expansion du greffon Cytokines, Facteurs de croissance Sang Homing Expression de CXCR 4 Inhibition de CD 26 (qui Moelle osseuse Mobilisation GM-CSF AMD 3100 (inhibiteur de CXCR 4) dégrade SDF-1) Retention, Auto-renouvellement Activer signaux de la niche: parathormone (augmente Niche des CSH ostéoblastes)

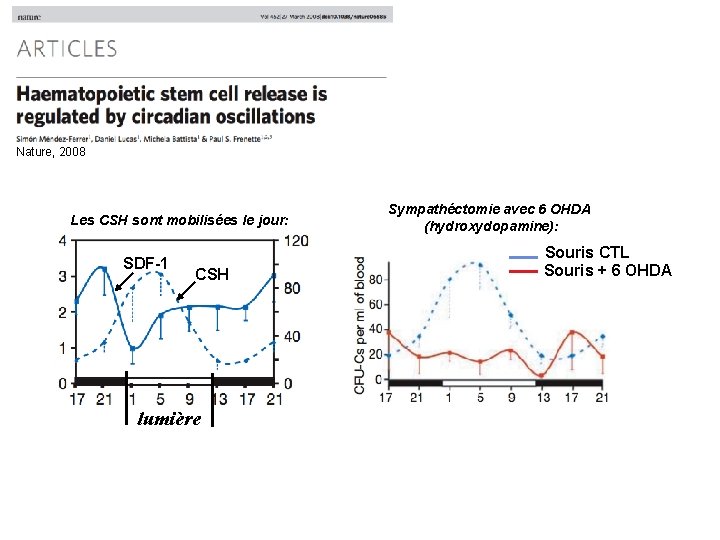
Nature, 2008 Les CSH sont mobilisées le jour: SDF-1 CSH lumière Sympathéctomie avec 6 OHDA (hydroxydopamine): Souris CTL Souris + 6 OHDA

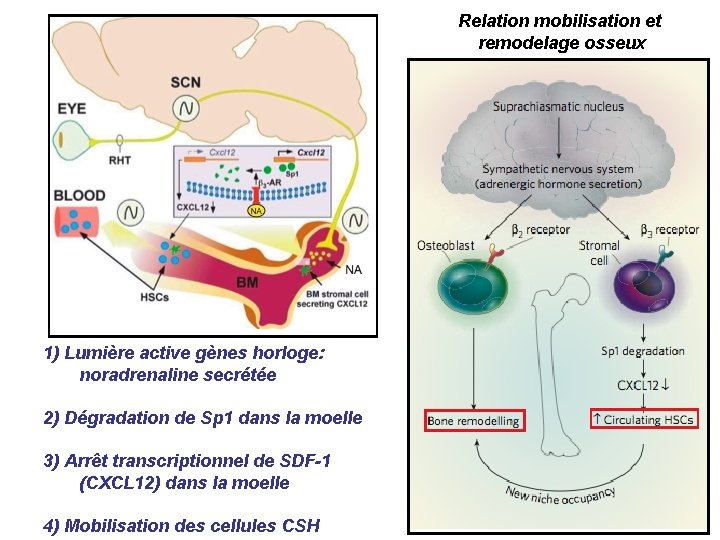
Relation mobilisation et remodelage osseux 1) Lumière active gènes horloge: noradrenaline secrétée 2) Dégradation de Sp 1 dans la moelle 3) Arrêt transcriptionnel de SDF-1 (CXCL 12) dans la moelle 4) Mobilisation des cellules CSH

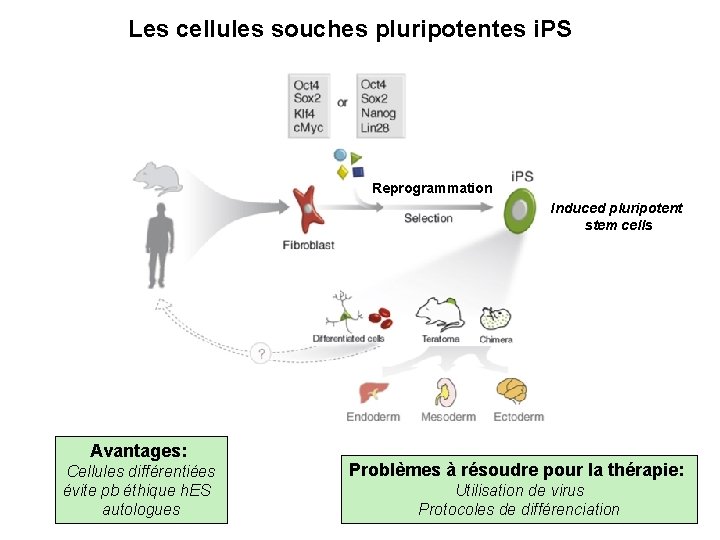
Les cellules souches pluripotentes i. PS Reprogrammation Induced pluripotent stem cells Avantages: Cellules différentiées évite pb éthique h. ES autologues Problèmes à résoudre pour la thérapie: Utilisation de virus Protocoles de différenciation

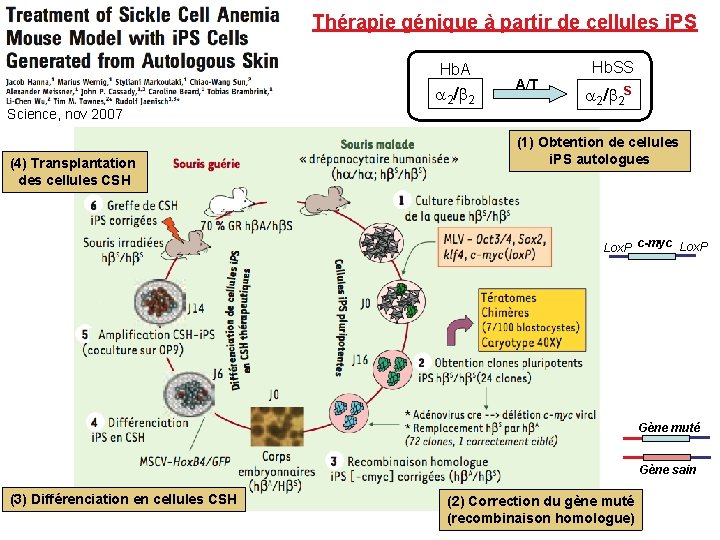
Thérapie génique à partir de cellules i. PS Hb. A 2/ 2 Science, nov 2007 (4) Transplantation des cellules CSH A/T Hb. SS 2/ 2 S (1) Obtention de cellules i. PS autologues Lox. P c-myc Lox. P Gène muté Gène sain (3) Différenciation en cellules CSH (2) Correction du gène muté (recombinaison homologue)