Les antiviraux tude dun cas particulier le VIH











- Slides: 23

Les antiviraux Étude d’un cas particulier : le VIH avec les antirétroviraux qui lui sont associés.

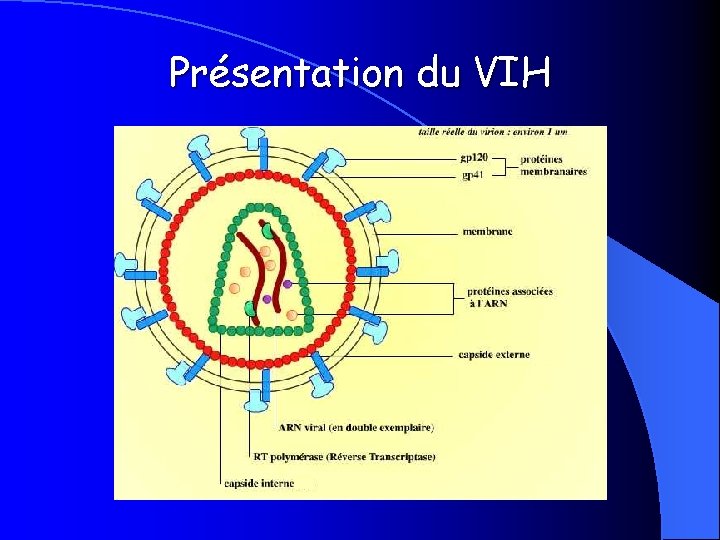
Présentation du VIH

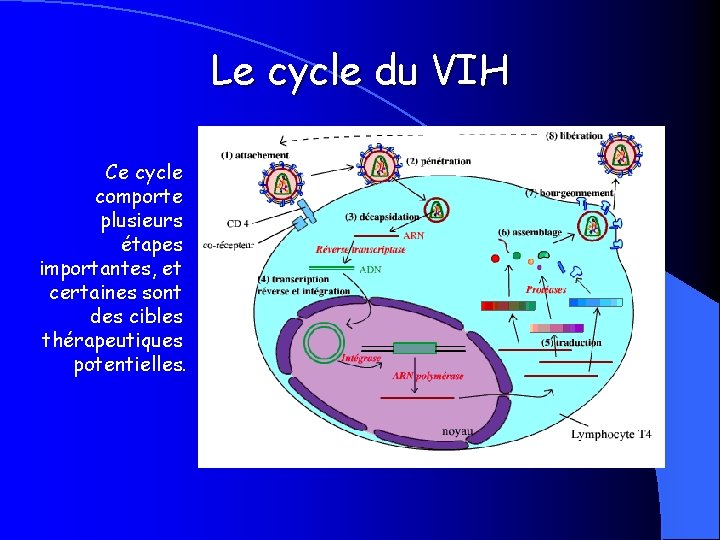
Le cycle du VIH Ce cycle comporte plusieurs étapes importantes, et certaines sont des cibles thérapeutiques potentielles.

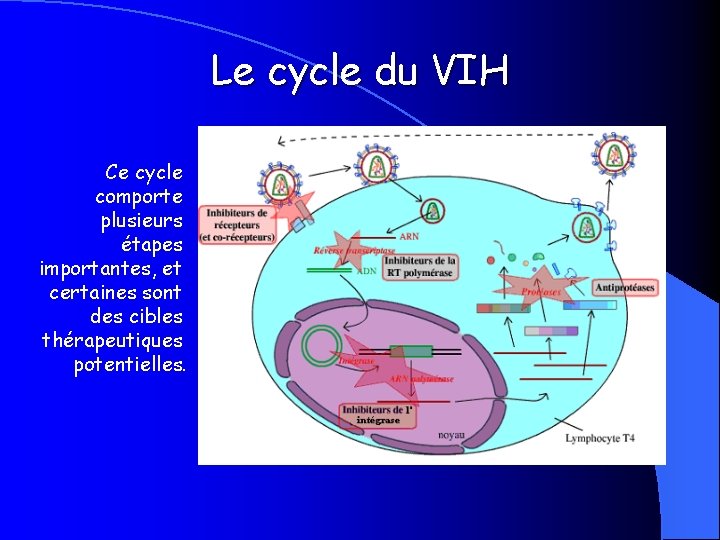
Le cycle du VIH Ce cycle comporte plusieurs étapes importantes, et certaines sont des cibles thérapeutiques potentielles.

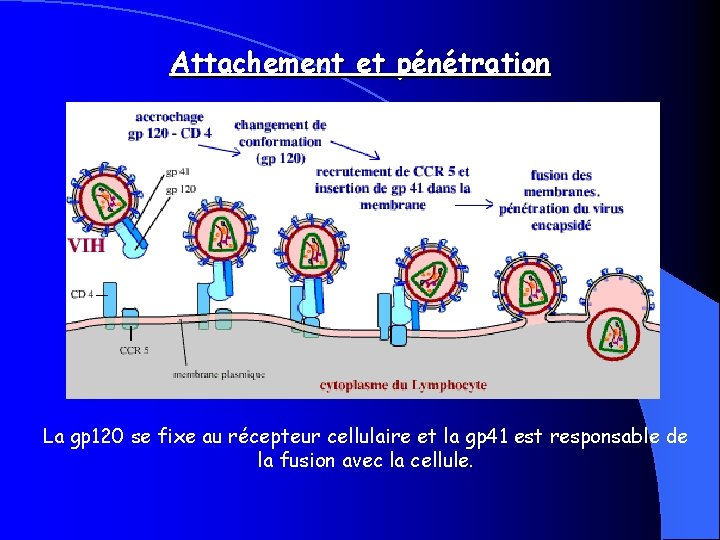
Attachement et pénétration La gp 120 se fixe au récepteur cellulaire et la gp 41 est responsable de la fusion avec la cellule.

La cible thérapeutique La gp 41 : les biologistes ont construit une petite protéine dont la structure ressemble à celle des hélices de la protéine gp 41. Cette protéine se fixe sur les hélices de la gp 41 et empêchent celles-ci de se replier pour faire fusionner les 2 membranes. L’entrée du rétrovirus est donc impossible. Pénétration du VIH dans une cellule humaine. Mais cette zone du virus mute facilement et de plus, ce processus mettant en jeu plusieurs protéines, parfois en inhiber une ne suffit pas.

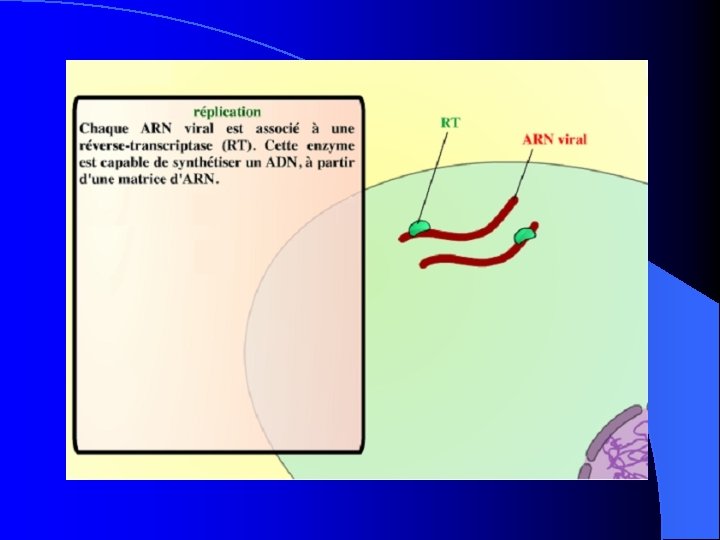
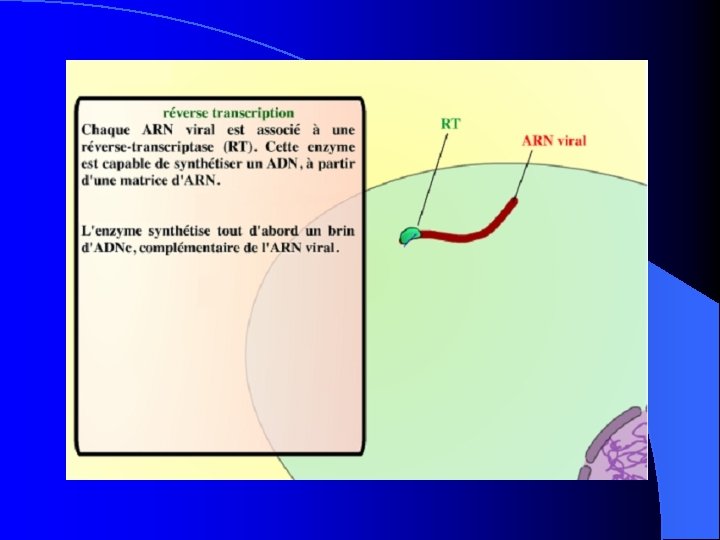
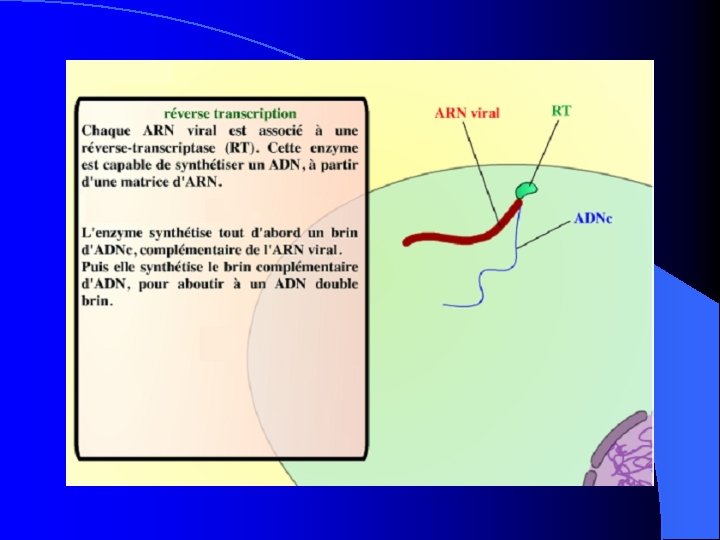
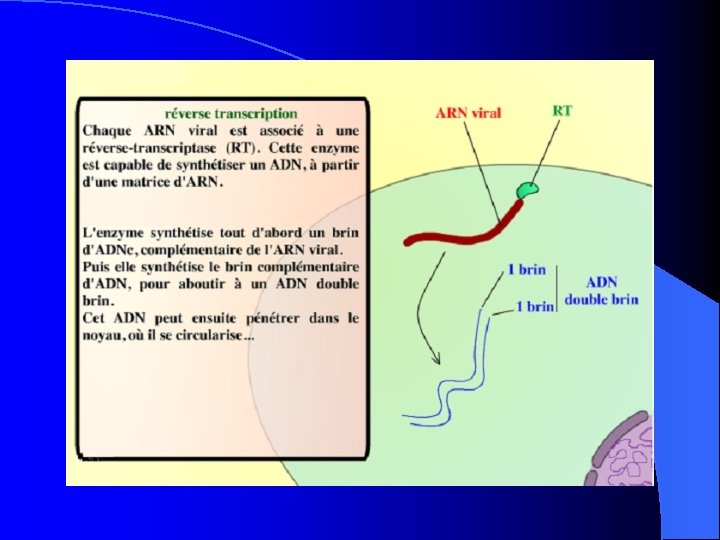
Transcription inverse Chacun des ARN viraux est associé à une RT polymérase, enzyme assurant la formation d’un brin transcrit d’ADN de l’ARN viral. Ces deux ADNc monobrins vont s’associer et former une molécule d’ADN, appelée provirale. L’information du virus est donc maintenant sous la forme d’ADN, séquence compréhensible et intégrable dans le programme génétique cellulaire.





La cible thérapeutique La transcriptase inverse : 2 types de molécules contre cette protéine Les inhibiteurs nucléotidiques et nucléosidiques de la transcriptase inverse (INTI) : Les nucléotides et nucléosides sont incorporés dans l'ADN viral à la place des synthons naturels de l'ADN, arrêtant ainsi toute réplication ultérieure par une terminaison de la chaîne peptidique. Les inhibiteurs non nucléosidiques de la transcriptase inverse (INNTI) : les INNTIs arrêtent l'activité de la transcriptase inverse du VIH en ralentissant le taux de certaines réactions chimiques importantes impliquées dans la synthèse de l'ADN.

Intégration L’ADN franchit la paroi du noyau, grâce à une enzyme : l’endonucléase. Une fois à l’intérieur, il se circularise et s’insert sous l’effet de l’intégrase dans le programme génétique de la cellule cible. L’intégration se déroule en 2 étapes : - l’intégrase élimine des nucléotides extrémités de l’ARN viral - puis l’insère au hasard dans le génome de la cellule infectée Une fois intégré l’ADN proviral s’exprime comme l’ADN cellulaire.

La cible thérapeutique L’intégrase : plusieurs inhibiteurs de l’intégrase sont en cours d’étude. On connaît aujourd’hui précisément les mécanismes moléculaires de l’insertion ainsi que la structure 3 D de l’enzyme. Des composés ont donc pu être mis au point afin de se fixer sur le site actif de l’enzyme afin d’inhiber son activité.

Traduction Une fois sortis du noyau par l’un des pores nucléaires, l’ARNm est lu par les ribosomes du Réticulum Endoplasmique Rugueux. L’ARNm vient en fait se glisser entre les deux sous unités du ribosome. Pour chaque codon (groupe de trois nucléotides) de l’ARNm, le ribosome attribuera un acide aminé. Ceux-ci se polymériseront au fur et à mesure de la lecture. Un codon initiateur AUG (Adénine-Uracile-Guanine) fera débuter la synthèse tandis qu’un codon stop (UAA ; UGA ; UAG) en marquera la fin. Le mécanisme de fabrication des protéines de la cellule est maintenant entièrement dédié à la fabrication de nouveaux virus.

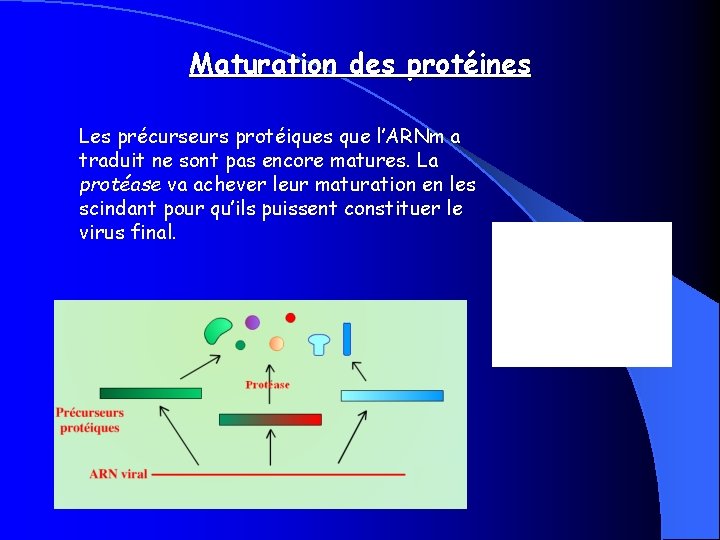
Maturation des protéines Les précurseurs protéiques que l’ARNm a traduit ne sont pas encore matures. La protéase va achever leur maturation en les scindant pour qu’ils puissent constituer le virus final.

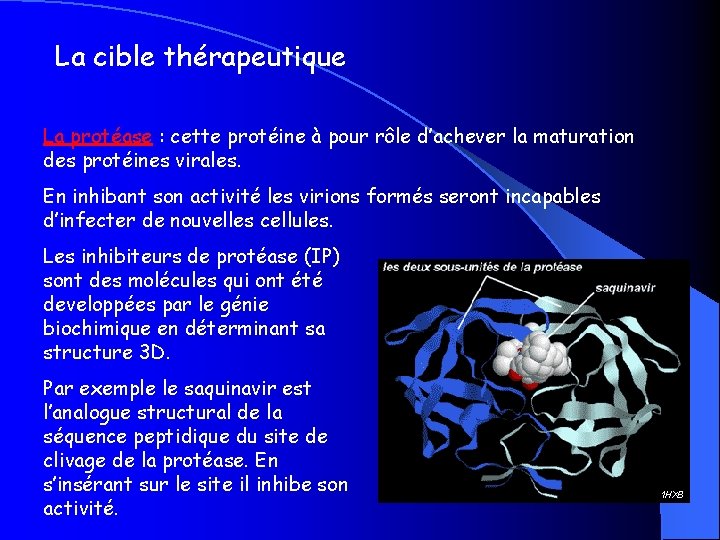
La cible thérapeutique La protéase : cette protéine à pour rôle d’achever la maturation des protéines virales. En inhibant son activité les virions formés seront incapables d’infecter de nouvelles cellules. Les inhibiteurs de protéase (IP) sont des molécules qui ont été developpées par le génie biochimique en déterminant sa structure 3 D. Par exemple le saquinavir est l’analogue structural de la séquence peptidique du site de clivage de la protéase. En s’insérant sur le site il inhibe son activité.

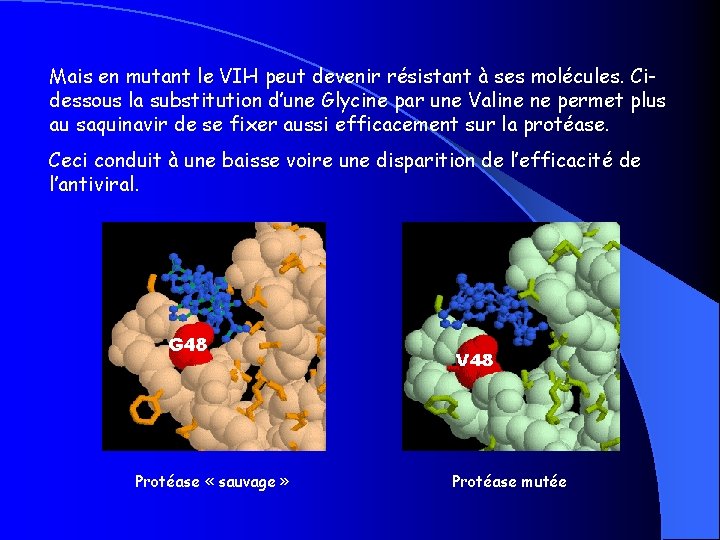
Mais en mutant le VIH peut devenir résistant à ses molécules. Cidessous la substitution d’une Glycine par une Valine ne permet plus au saquinavir de se fixer aussi efficacement sur la protéase. Ceci conduit à une baisse voire une disparition de l’efficacité de l’antiviral. Protéase « sauvage » Protéase mutée

Assemblage et Bourgeonnement Les différentes protéines du virus s’assemblent pour former de nouveaux virions. Des ARN proviraux rejoignent les enzymes virales. Les protéines constitutives s’assemblent pour former la capside, englobant cet ensemble. Ensuite la capside sort de la cellule infectée en arrachant une partie de la membrane cellulaire (ceci lui procurant une protection supplémentaire). Le virus est prêt a infecter de nouvelles cellules.

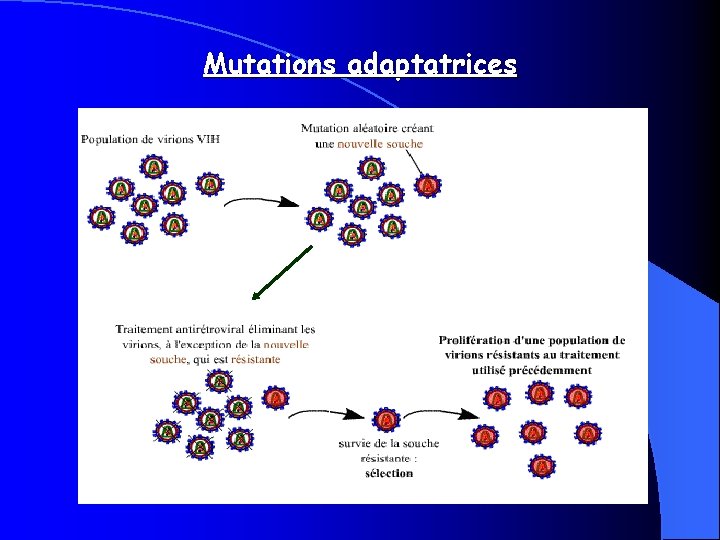
Les limites des antirétroviraux Les trithérapies ne guérissent en aucun cas du VIH ; et ce sont des traitements lourds et à vie. L'émergence de résistance virale aux trithérapies : des mutations adaptatrices. (vues précédemment avec l’exemple de mutants résistants au saquinavir) Les effets secondaires liés à leur utilisation.

Mutations adaptatrices

Quelques exemples d’effets secondaires Anémie Ø Hépatite Ø Hypercholestérolémie Ø Insuffisance hépatique Ø Confusion mentale Ø Douleurs Ø Nausées Ø Insuffisance rénale Ø Vomissements Ø Lipodystrophie (redistribution des graisses dans le corps) Ø

Bibliographie - "Pour la Science" n° 291 - http: //www. actions-traitements. org - http: //www. snv. jussieu. fr/vie/dossiers/tritherapie/ - http: //www. snv. jussieu. fr/vie/dossiers/SIDA/ - http: //fr. wikipedia. org/wiki/VIH