LES ACIDES ET LES BASES EN SOLUTIONS AQUEUSES

LES ACIDES ET LES BASES EN SOLUTIONS AQUEUSES 1

Introduction L’utilisation des termes « acide » et « base » (anciennement alcali), pour désigner certains groupes de substances date de plusieurs siècles; et pendant longtemps aucune théorie chimique cohérente ne pouvait encore définir un acide ou une base. La classification d’un composé en tant qu’acide ou en tant que base était fondée sur des propriétés communes aux substances de ce type, sans référence à une formule chimique. On se référait à certaines propriétés particulières et non à un concept général. 2

Les acides : - Saveur aigrelette - Colorent en rouge le papier tournesol - Réagissent avec les bases pour donner des sels et avec les métaux entrainant un dégagement d’hydrogène. Les bases : - Saveur caractéristique (amère) - Colorent en bleu le papier tournesol - Réagissent avec les acides pour donner des sels. Ces caractères, bien que souvent vérifiés, sont beaucoup trop qualitatifs pour définir les acides et les bases. 3

B-Théorie à l’origine de la définition d’un acide et d’une base : 1. Théorie d’Arrhenius l 887: Acide: HA → A- + H+ Exp : HCl → H + + Cl. Base: BOH →B+ + OH- Exp : Na. OH → Na+ + OH Limites: § Elle ne s’applique pas à tous les solvants; § L’ion H+ / H 3 O+ §Tous les acides ne contiennent pas d’Hydrogène, ex : BF 3, § Toutes les bases ne contiennent pas d’Hydroxyde, ex : NH 3 4

B-Théorie à l’origine de la définition d’un acide et d’une base : 2. Théorie de Bronsted et Lowry 1922: L’acide: HA ↔ H 3 O+ + ALa base: B + H 3 O+ ↔ BH+ En d’autres termes : Acide = Donneur de proton Base = Accepteur de proton 5

Avantages : - Valable que les substances soient en solution ou non; - Ne dépend pas de la nature de la solution ( aqueuse ou non aqueuse); - La particule de proton n’est pas libérée mais transférée. libérée - Les bases Limites Un rôle tout particulier au proton , alors que, certaines réactions conduisent à la formation de sel sans qu’il y ait transfert de proton entre un acide et une base exp: CO 2 + Ca. O → Ca. CO 3 6

Vocabulaire : § Acide => donneur du proton => protogénique § Base => accepteur du proton => protophilique § Les deux sont des protolytes § La réaction entre les deux est la neutralisation § La réaction qui mis en jeu un échange de proton est la protolyse 7
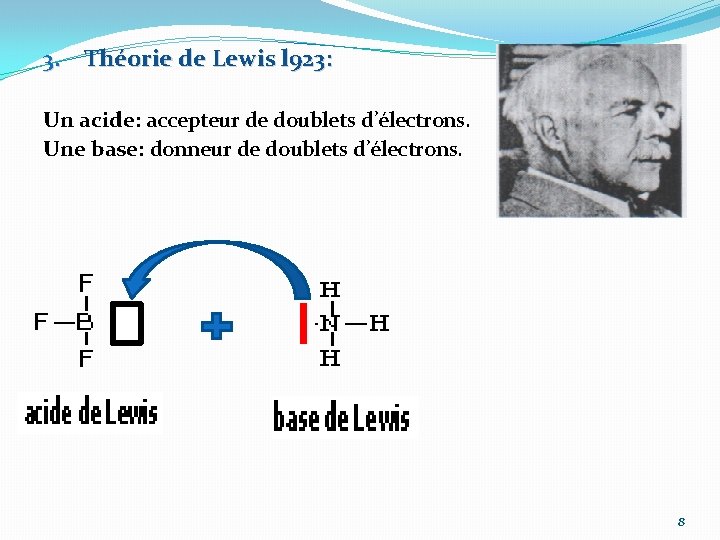
3. Théorie de Lewis l 923: Un acide: accepteur de doublets d’électrons. Une base: donneur de doublets d’électrons. 8

La théorie de Lewis présente un inconvénient majeur lorsqu’on se place sur le plan quantitatif : une série de acides (bases) ne serait pas classée dans le même ordre selon la base (acide) qui leur est opposée. En conclusion : si la théorie de Lewis, sur le plan En conclusion qualitatif, permet d’élargir considérablement les concepts d’acide et de base , il est préférable sur le plan quantitatif d’en rester à la théorie de Bronsted et Lowry, à qui aucun inconvénient majeur ne peut être fait 9

C. NOTION DE COUPLES ACIDE-BASE: AH H+ A- acidedans le sens inverse acide est lue Si la Base réaction Acide AH/A- Base + H+ un couple acide/base conjugué BH+/B un couple acide/base conjugué 10

La force d’un acide ou celle d’une base est ainsi liée à l’importance du transfert de protons; ü Pour un acide ou une base forts, le transfert est pratiquement total; pratiquement total ü Pour un acide ou une base faibles, le transfert est partiel 11

D-REACTION ACIDE-BASE: 1. Rôle du solvant : q Si le solvant est aprotique et apolaire (solvant inerte), il est nécessaire pour qu’il y ait réaction protolytique la présence d’un acide donneur de protons et d’une base qui les acceptant. q Si le solvant est protoactif, il va pouvoir se comporter lui-même comme donneur (acide) ou accepteur (base) de protons === le solvant va jouer le rôle du 2ème couple acido-basique. 12

2. Force des acides et des bases : a- Cas d’un acide HA dans un solvant S : HA + S A- + HS+ On peut écrire la constante suivante : K = [A- ][HS+]/[S][HA] K. [S] = [A- ][HS+]/[HA] = Ka = Constante d’acidité b- Cas d’un base B dans un solvant S : B + HS+ BH+ + S On peut écrire la constante suivante : K = [A- ][BH+]/[S][HA] K. [S] = [A- ][HS+]/[HA] = Kb = Constante de basicité 13

2. Force des acides et des bases : q Cas d’un acide HA dans un solvant S Acide + H 2 O ↔ Base + H 3 O+ +]/ [Acide]. = [Base]. [H O Ka 3. K [H 2 O] Ka = constante d’acidité On considère H 2 O comme constante et régulière en solution diluée. q Cas d’une base B dans un solvant S Base + H 2 O ↔ Acide + OH- Kb = [Acide]. [OH-]/ [Base] Kb = constante de basicité 14

REMARQUES : § Ka et Kb sont des constantes qui dépendent : - de la température - de la nature du solvant § pour les polyacides ou les polybases, on définit plusieurs constantes d’acidité et de basicité relative à chacune des fonctions acide ou basique : H 3 PO 4 + H 2 O ↔ H 3 O+ + H 2 PO 4 - Ka 1 H 2 PO 4 - + H 2 O ↔ H 3 O+ + HPO 4 -2 Ka 2 HPO 4 -2 + H 2 O ↔ H 3 O+ + PO 4 -3 Ka 3 15

§ p. Ka et p. Kb : ü p. Ka = - Log 10 Ka ü p. Kb = - Log 10 Kb Selon leur dissociation, les acides et les bases se classent en 2 groupes : Premier groupe : Acides et bases forts. o Réaction directe o Dissociation totale Deuxième groupe : Acides et bases faibles. o Réaction inverse o Dissociation partielle 16

Un acide est d’autant plus fort que : o Ka est grand , p. Ka est petit Une base est d’autant plus forte que : o Kb est grand , p. Kb est petit et p. Ka est grand Conclusion : o Si p. Ka< 0 ; l’acide est très fort o Si 0 p. Ka 4 ; l’acide est moyen; o Si 4 p. Ka 7 ; l’acide est moyennement faible o Si p. Ka > 7 ; l’acide est faible Les acides forts dans l’eau ont un p. Ka inférieur à celui de H 3 O+ Les bases fortes dans l’eau ont un p. Kb inférieur à celui de OH 17

Relation entre K Relation entre a et Kb d’un même couple acide-base Ka = [Base]. [H 3 O+]/ [Acide] Kb = [Acide]. [OH-]/ [Base] Ka. Kb = [H 3 O+]. [OH-] = Ke Ke le produit ionique de l’eau A 25°C , Ke = 10 -14 18

3. Degré d’avancement d’une réaction acidobasique : Travaux d’Arrhenius et Ostwald § Variation du coefficient de dissociation avec la dilution : loi d’Ostwald : HA A- + H+ § Quand la dilution augmente l’équilibre est déplacé vers la droite ; donc à dilution infinie ( C 0 ) l’ionisation est totale dans ces conditions : § La dilution augmente la dissociation d’un électrolyte faible ainsi un acide ou une base faible tend à ce comporter comme une base ou un acide fort et inversement § Variation de avec l’addition d’ion commun :

4. Facteurs intrinsèques d’acidité et de basicité Ils expriment une acidité ou une basicité latente qui ne peut se manifester qu’en présence d’un accepteur ou d’un donneur de protons ü Substances protogéniques: Acides La force d’un acide est liée à la structure de l’anion qui demeure après le départ de H 3 O+ , donc de la base conjuguée, et principalement à sa masse et à sa charge électrique. 20

§ Acides minéraux binaires : L’acidité croit avec : > - La diminution de la charge de l’anion : HCl H 2 S - L’augmentation de la masse de l’anion : HCl , HF, HI, HBr § Acides minéraux oxygénés : l’acidité croit avec la valence positive de l’élément et donc avec le nombre d’atomes d’oxygène. XOm(OH)n ; L’acidité augmente lorsque m augmente, ainsi : HCl. O, H 3 PO 4 , H 2 SO 4 , HCl. O 4 21

§ Acides organiques : En général, l’acidité est inférieure à celle des acides minéraux forts. Les acides organiques, les plus forts, portent des groupements fonctionnels sulfoniques ---SO 3 HB et carboxyliques ---COOH. ü Substances protophiliques : Bases Des règles comparables peuvent être établies. § Bases minérales § Bases organiques 22

5. Facteurs extrinsèques d’acidité et de basicité Ces facteurs sont relatifs au solvant Pouvoir prototropique du solvant (PP) Influence de la constante diélectrique La constante diélectrique => dissociation des paires d’ions PP => basique => révélera la force d’un acide plus qu’un solvant ayant un PP bas qui se comportera comme acide et révélera plus la force des bases. 23

6. Effet de nivellement limitation des échelles d'acidité ou de basicité par le solvant L’échelle d’acidité (de basicité) par rapport à l’eau est la plus utilisée car les solutions aqueuses sont les plus courantes. Il n’en est pas question de comparer la dissociation des électrolytes forts dans l’eau qui est pratiquement totale. 24
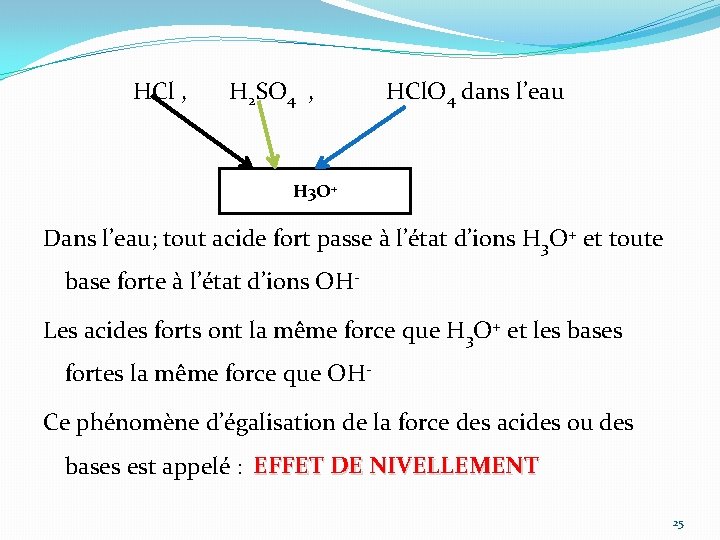
HCl , H 2 SO 4 , HCl. O 4 dans l’eau H 3 O+ Dans l’eau; tout acide fort passe à l’état d’ions H 3 O+ et toute base forte à l’état d’ions OH- Les acides forts ont la même force que H 3 O+ et les bases fortes la même force que OH- Ce phénomène d’égalisation de la force des acides ou des bases est appelé : EFFET DE NIVELLEMENT 25

Comment classer les acides et les bases très forts ? ? ? Cette comparaison n’étant pas possible dans l’eau, on utilise un solvant dans lequel l’acide ou la base sont peu dissociés 26

§ Dans l’eau, HCl est un acide fort : HCl + H 2 O H 3 O+ + Cl§ Dans l’acide acétique, HCl est un acide faible : HCl + CH 3 COOH CH 3 COOH+2 + Cl. On utilise donc l’échelle d’acidité par rapport à CH 3 COOH Pour classer HCl , H 2 SO 4 , HCl. O 4 qui sont des acides forts : HCl. O 4 > HCl > H 2 SO 4 27

7. Echelle d’acidité et de basicité : il est plausible de comparer entre eux différents acides ou différentes bases . Mais pour le faire valablement, il est nécessaire de faire réagir un même composé avec plusieurs antagonistes. 1. Echelle de basicité: • Référence → Acide perchlorique HCl. O 4 + B ↔ BH+ + Cl. O 4 p. K = p. HCl. O 4 – log ([B] / [BH+Cl. O 4 -]) A la demi neutralisation : p. K = p. HCl. O 4 2. Echelle de acidité: • Référence → Base RNH 2 p. K = p. B – log ([HA] / [BH+A-]) 28
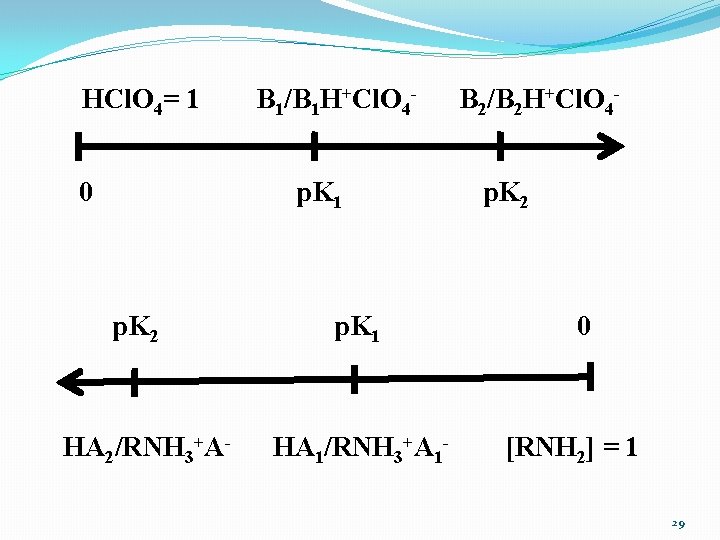
HCl. O 4= 1 0 B 1/B 1 H+Cl. O 4 p. K 1 p. K 2 HA 2/RNH 3+A- p. K 1 HA 1/RNH 3+A 1 - B 2/B 2 H+Cl. O 4 p. K 2 0 [RNH 2] = 1 29
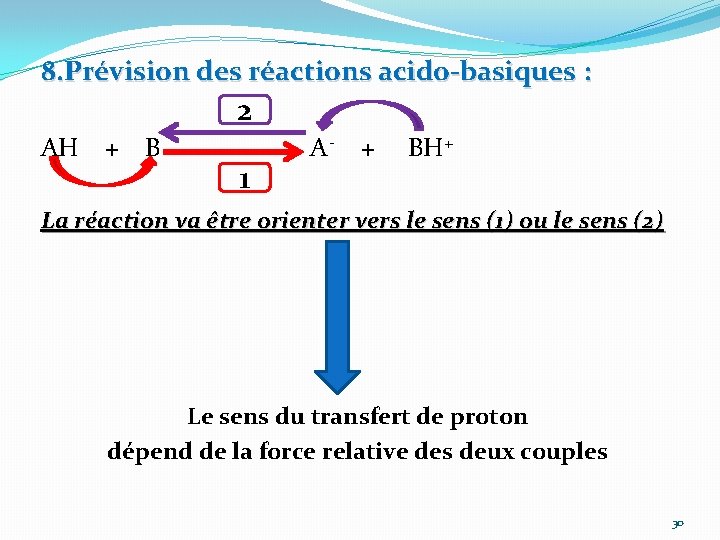
8. Prévision des réactions acido-basiques : 2 AH + B A - + BH+ 1 La réaction va être orienter vers le sens (1) ou le sens (2) Le sens du transfert de proton dépend de la force relative des deux couples 30

Considérons la réaction globale suivante : �HA + B BH+ + A- + H 2 O K Cet équilibre résulte de deux autres équilibres : �HA + H 2 O H 3 O+ + A- Ka 1 = [H 3 O+][ A-]/[ HA] �B + H 2 O BH+ + OH BH+ + H 2 O B + H 3 O+ Ka 2 = [H 3 O+][ B]/[BH+] �HA + B BH+ + A- + H 2 O K=[BH+]. [ A-]/[ HA]. [ B] �Ka 1/ Ka 2 = [H 3 O+]. [ A-]. [BH+]/[H 3 O+][ B]. [HA] =[BH+]. [ A-]/[ HA]. [ B] = K 31

La réaction dans le sens (1) sera d’autant plus totale que Ka 1 sera plus grand que Ka 2 Le transfert de protons se fait dans le sens de la disparition des espèces acides et basiques les plus fortes Exemple : 1) HCl + H 2 O H 3 O+ + Cl. HCl acide plus fort que H 3 O+. H 2 O base plus forte que Cl-. 2) C 2 H 5 OH + H 2 O C 2 H 5 O- + H 3 O+ C 2 H 5 O- base plus forte que H 2 O. H 3 O+ acide plus fort que C 2 H 5 OH. 32

9. Les réactions acido-basiques Ø Réaction de neutralisation : C’est l’action d’un acide sur une base Acide + Base → Sel + Eau. 2 Na. OH + H 2 SO 4 → Na 2 SO 4 + 2 H 2 O Ø Réaction d’hydrolyse : C’est la réaction, avec un excès d’eau, d’un acide ou une base faible. Dans une réaction de ce type l’eau joue à la fois le rôle de réactif et de solvant. 33

Les réactions acido-basiques Ø Réaction de déplacement : Un acide fort déplace un acide faible de son sel : CH 3 COONa + HCl ↔ Na. Cl + CH 3 COOH Une base forte déplace une base faible de son sel : Na. OH + NH 4 Cl ↔ Na. Cl + NH 4 OH 34

Conclusion Malgré la diversité des définitions des acides et des bases, chaque théorie est très utile lorsqu’elle est utilisée dans son propre terrain, autrement dit ces théories différent pour se compléter 35
- Slides: 35