LEQUILIBRIO IDROELETTROLITICO Prof M LOSPALLUTI Dipartimento Dellemergenza e

L’EQUILIBRIO IDROELETTROLITICO Prof. M. LOSPALLUTI Dipartimento Dell’emergenza e Dei Trapianti D’organo Sezione di Chirurgia d’Urgenza

L’equilibrio idro-elettrolitico e le sue alterazioni Il trattamento a base di liquidi elettroliti fa parte integrante dell’assistenza ai pazienti chirurgici. Molte malattie, molti traumi accidentali e i traumi chirurgici producono effetti notevoli sulla fisiologia dei liquidi e degli elettroliti dell’organismo. La conoscenza di questi meccanismi è premessa fondamentale per una corretta terapia.

L’acqua costituisce dal 50 al 70% del peso corporeo e le sue variazioni sono legate all’età ed al sesso. la quantità di acqua è massima nei primi anni di vita (fino all’ 80% alla nascita); si attesta sul 60% nei maschi e sul 50% nelle donne in età giovanile; si riduce, infine, in età avanzata fino a raggiungere, rispettivamente, il 50 e il 40%. Un’ulteriore variabile è data dalla quantità di tessuto adiposo (povero di acqua) e dalla quantità di massa muscolare (ricca di acqua). Liquidi corporei Liquido intra cellulare (40%) Plasma (5%) Liquido interstiziale (15%)

Il liquido interstiziale è composto da una componente funzionale (90%) che si equilibra con notevole rapidità; ed una parte non funzionale (10%) che non partecipa alle fasi di scambio con gli altri comparti. I componenti non funzionanti sono: L’acqua del tessuto connettivo Il liquor cefalorachidiano Il liquido delle articolazioni
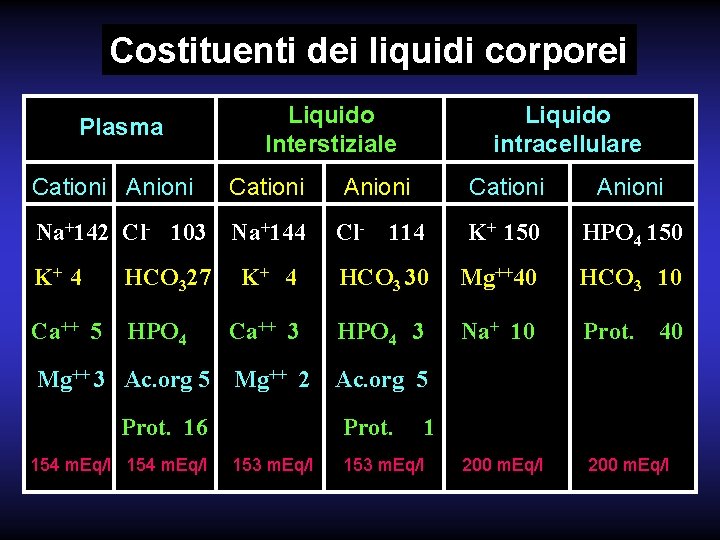
Costituenti dei liquidi corporei Plasma Liquido Interstiziale Liquido intracellulare Cationi Anioni Na+142 Cl- 103 Na+144 Cl- 114 K+ 150 HPO 4 150 K+ 4 HCO 3 30 Mg++40 HCO 3 10 Ca++ 3 HPO 4 3 Na+ 10 Prot. Mg++ 2 Ac. org 5 200 m. Eq/l K+ 4 HCO 327 Ca++ 5 HPO 4 Mg++ 3 Ac. org 5 Prot. 16 154 m. Eq/l Prot. 153 m. Eq/l 40 1

La diversa composizione chimica dei vari distretti dei liquidi dell’organismo è mantenuta in equilibrio dalla “Membrana cellulare” che si comporta come una membrana semipermeabile opponendosi alla libera diffusione dei vari componenti. I vari soluti hanno una pressione osmotica, che rappresenta la capacità di richiamare acqua, direttamente proporzionale al potere di dissociazione delle sostanze disciolte. In condizioni normali la pressione osmotica, nei vari comparti, oscilla intorno ai 290 -310 m. Osm. Il sodio e la quota proteica sono gli elementi che maggiormente contribuiscono al mantenimento della pressione osmotica nel comparto extra cellulare.

Alterazioni dei liquidi dell’organismo

Alterazioni del volume

Alterazioni della concentrazione

Alterazioni della composizione

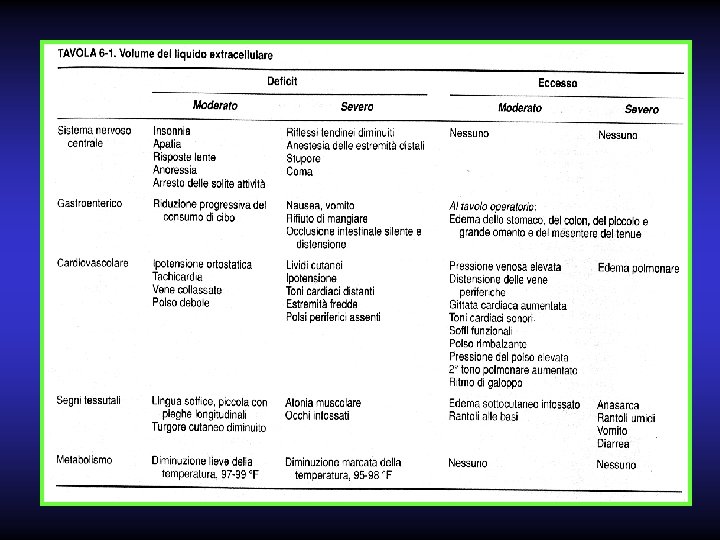
Alterazioni del volume Deficit di volume 1)Perdita di liquidi intestinali (vomito - diarrea) 2)Sequestro di liquidi nei traumi e nelle infezioni dei tessuti molli 3)Processi infiammatori endoaddominali 4)Peritonite 5)Occlusione intestinale 6)Ustioni 7)Emorragia Eccesso di volume 1)In genere iatrogeno 2)Secondario ad ins. renale

Alterazioni della concentrazione IPONATREMIA = Na IPERNATREMIA = Na

Iponatremia • Ridotta quantità di acqua nello spazio extracellulare • Compare con Na+<120 m. Eq/l • Oliguria per aumentato riassorbimento di Na+ • Edema dei tessuti • Pressione endocranica aumentata • Alterazioni della P. A.

Ipernatremia Riduzione dell’acqua intracellulare Compare con Na+>150 m. Eq/l Oliguria per aumentato riassorbimento di H 2 O Cute e mucose secche Pressione endocranica normale

Alterazioni miste a carico del volume e della concentrazione A) Paziente che continua a bere acqua dopo perdita di succhi gastroenterici. (riduzione del volume con iponatremia). B) Paziente diabetico con diuresi osmotica perdita di notevole quantità di urine ipotoniche. (riduzione del volume con ipernatremia)

Alterazioni della composizione Alterazioni dell’equilibrio acido-base Alterazioni della concentrazione di K+, Mg++, Ca++

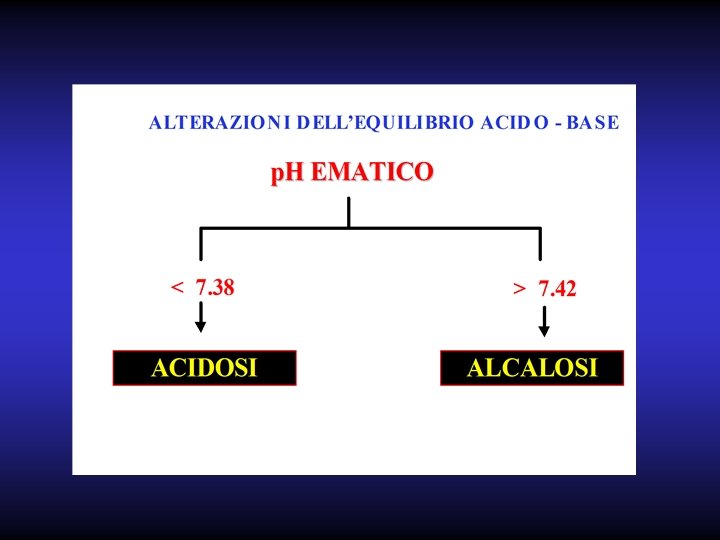
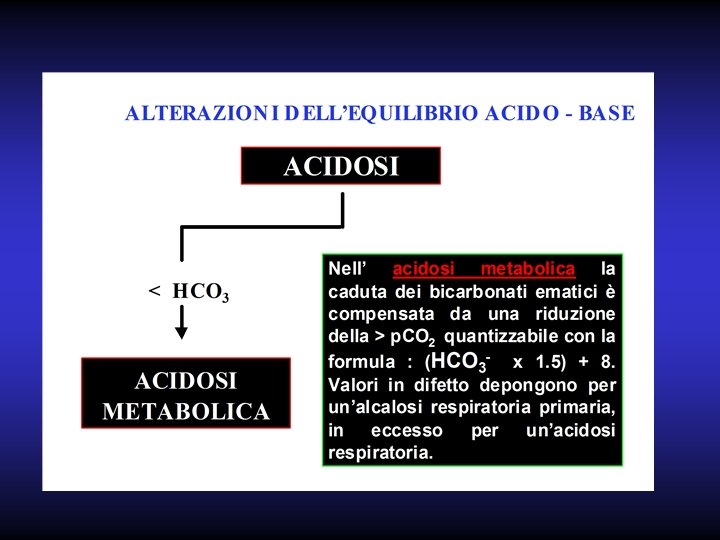
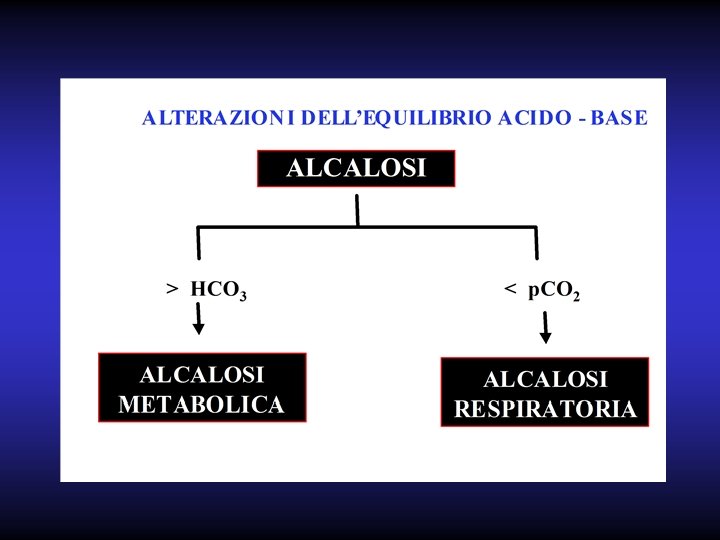
Alterazioni dell’equilibrio acido-base Il p. H dei liquidi dell’organismo è mantenuto costantemente entro certi limiti, nonostante la notevole produzione di acido derivante dal metabolismo corporeo.


Gli acidi sono neutralizzati in modo efficiente da numerosi sistemi tampone e successivamente eliminati attraverso il polmone ed il rene. Nel comparto intracellulare abbiamo le proteine ed i fosfati, mentre nel comparto extracellulare il sistema bicarbonato / acido carbonico.

Un sistema tampone è formato da un acido o da una base debole e dal sale di quell’acido o di quella base: (HCl + Na. HCO 3 = Na. Cl + H 2 CO 3) L’effetto tampone deriva dalla formazione di una quantità equivalente di acido debole a quella di acido forte aggiunta.

Il p. H è il logaritmo negativo della concentrazione di H+; Il suo valore è 7, 4. Rappresenta in sostanza il rapporto fra una base bicarbonato e la quantità di acido carbonico; tale rapporto è di 20 a 1. B)HCO 3 H 2 CO 3 20 1 Una variazione della quantità di acido o di base realizzerà uno squilibrio del rapporto conseguente abbassamento o innalzamento del p. H.

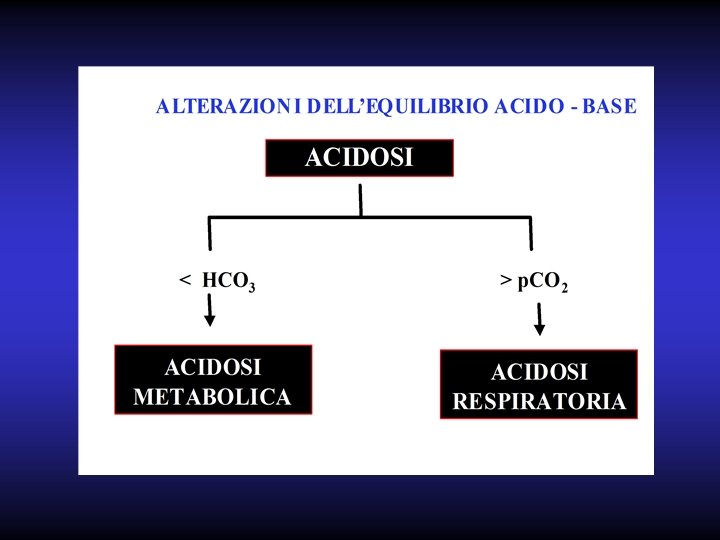





Alterazioni della concentrazione di K+, Mg++, Ca++ Il potassio rappresenta il principale catione del liquido intracellulare (150 m. Eq/l). La sua quantità nello spazio extra cellulare e modesta(4, 5 m. Eq/l); la sua esiguità però, rappresenta un fattore critico per una corretta funzione della muscolatura scheletrica e miocardica.

IPERKALIEMIA Gli effetti si manifestano a carico dell’apparato cardiovascolare e gastroenterico: Segni elettrocardiografici: Onde T con picchi elevati Complessi QRS allargati Tratto ST depresso Scomparsa dell’onda T Arresto cardiaco in diastole Sintomi gastro intestinali Nausea Vomito Diarrea

IPOKALIEMIA Gli effetti interessano la muscolatura striata quella liscia e l’apparato cardiovascolare Debolezza muscolare fino alla paralisi flaccida Diminuzione o scomparsa dei riflessi tendinei Ileo paralitico Segni elettrocardiografici di “basso voltaggio” Aritmie cardiache

La maggior parte del calcio (1000 -1200 gr. ) è depositato nelle ossa sotto forma di fosfato e carbonato. Il livello serico oscilla tra 8, 5 e 10, 5 mg/dl; la maggior parte si trova legata alle proteine plasmatiche (55%), la restante parte si trova libera in forma ionizzata ed è responsabile della stabilità neuro muscolare. E’ importante tenere conto del livello delle proteine totali nel valutare la frazione ionizzata! Occorre ricordare, anche, che la quota ionizzata è influenzata dall’equilibrio acidobase: l’acidosi aumenta il Ca++, mentre l’alcalosi lo diminuisce.

IPOCALCEMIA (Ca++<8 mg/dl) Intorpidimento e formicolio della regione periorale, della punta delle dita di mani e piedi. Iperattività dei riflessi tendinei. Crampi muscolari e addominali. Tetania. Convulsioni.

IPERCALCEMIA Affaticamento e stanchezza. Anoressia, nausea e vomito. Sonnambulismo, stupore. Coma.

Il Magnesio è indispensabile per il corretto funzionamento di quasi tutti i sistemi enzimatici. Gli effetti legati all’alterazione di concentrazione sono simili a quelli del calcio. Colpisce i pazienti con storia clinica di digiuno protratto e sostenuti con nutrizione artificiale; l’insufficienza renale cronica determina spesso un innalzamento della concentrazione di questo ione.

- Slides: 39