Lentropia Marina Cobal Dipt di Fisica Universita di

L’entropia Marina Cobal - Dipt. di Fisica Universita' di Udine 1

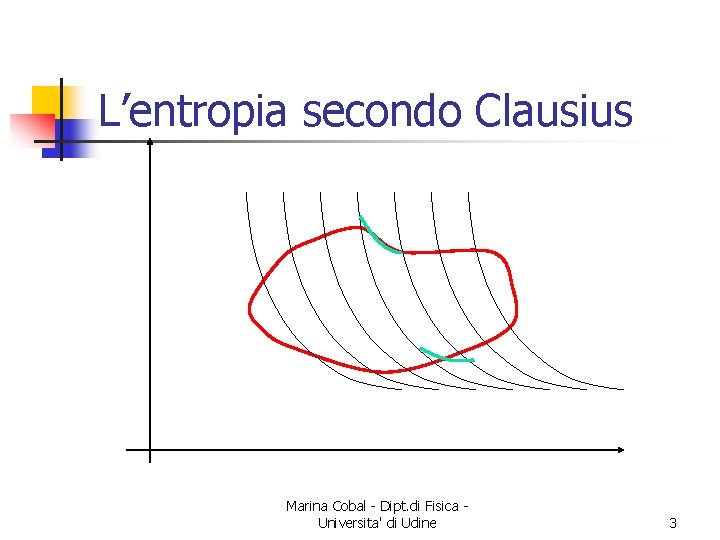
L’entropia secondo Clausius n Prendiamo un ciclo reversibile qualunque n n n ricopriamolo con una rete di adiabatiche i trattini del ciclo li sostituiamo con trattini di isoterme Possiamo quindi sostituire il ciclo con una serie di cicli di Carnot Marina Cobal - Dipt. di Fisica Universita' di Udine 2
L’entropia secondo Clausius Marina Cobal - Dipt. di Fisica Universita' di Udine 3

L’entropia secondo Clausius n Per ogni ciclo, in modulo n e se teniamo conto dei segni dei calori Marina Cobal - Dipt. di Fisica Universita' di Udine 4

L’entropia secondo Clausius n Questo vuol dire che per tutta la rete n Il ciclo vero può essere sostituito dalla rete n n I calori ceduti ed assorbiti nelle isoterme sostituiscono quelli dei trattini del ciclo reale All’interno le adiabatiche non assorbono calore ed il bilancio dei lavori è sempre nullo Marina Cobal - Dipt. di Fisica Universita' di Udine 5

L’entropia secondo Clausius n n n Ora “infittiamo” le adiabatiche Arriviamo agli infinitesimi… …e scopriamo di aver trovato una nuova funzione di stato! Marina Cobal - Dipt. di Fisica Universita' di Udine 6

L’entropia secondo Clausius È l’entropia di Clausius Marina Cobal - Dipt. di Fisica Universita' di Udine 7

L’entropia secondo Clausius n n n L’entropia è definita a meno di una costante additiva Clausius si accorge che l’entropia aumenta in ogni processo irreversibile Per far diminuire l’entropia occorre lavoro Marina Cobal - Dipt. di Fisica Universita' di Udine 8

L’entropia secondo Clausius n n Quando l’entropia è massima nessuna trasformazione è più possibile L’entropia “misura” l’utilizzabilità dell’energia! Marina Cobal - Dipt. di Fisica Universita' di Udine 9

Il calcolo dell’entropia Marina Cobal - Dipt. di Fisica Universita' di Udine 10

Calcolo di entropie n n L’entropia è una funzione di stato Quindi per calcolarla possiamo scegliere le trasformazioni a noi più comode n n per esempio quelle reversibili… Applichiamo la definizione Marina Cobal - Dipt. di Fisica Universita' di Udine 11

Seconda Legge Termodinamica L’entropia di un sistema isolato durante un processo spontaneo aumenta Marina Cobal - Dipt. di Fisica Universita' di Udine 12

DSamb n n n L’entropia totale dell’Universo è la somma dell’entropia del sistema e di quella dell’Ambiente Stot = Samb + Ssis Quindi DStot = DSamb + DSsis Consideriamo un trasferimento di calore dqrev, amb Possiamo considerare l’ambiente a volume costante. Quindi dqrev, amb= durev, amb U è una funzione di stato: durev, amb = duamb Marina Cobal - Dipt. di Fisica Quindi dqrev, amb = dq Universita' 13 ambdi Udine

DSamb n Possiamo considerare l’ambiente a temperatura costante, quindi DSamb = qamb/Tamb Sia che il processo sia reversibile o meno n Per un processo adiabatico, qamb = 0, quindi DSamb = 0 Marina Cobal - Dipt. di Fisica Universita' di Udine 14

Processo Isotermo per un gas Ideale n n n Calcoliamo il DS per una espansione isoterma di un gas ideale tra Vi e Vf Per una espansione isoterma, d. U=0, quindi dqrev = -dwrev = p d. V Allora Marina Cobal - Dipt. di Fisica Universita' di Udine 15

Variazioni di Entropia per passaggi di Fase Marina Cobal - Dipt. di Fisica Universita' di Udine 16
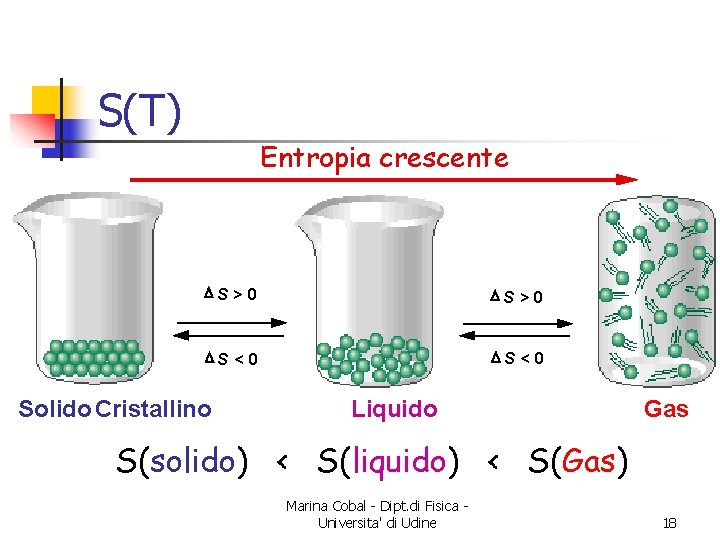
S(T) Entropia crescente DS > 0 DS < 0 Solido Cristallino Liquido Gas S(solido) < S(liquido) < S(Gas) Marina Cobal - Dipt. di Fisica Universita' di Udine 18

Calcolo di entropie Marina Cobal - Dipt. di Fisica Universita' di Udine 19

Calcolo di entropie Marina Cobal - Dipt. di Fisica Universita' di Udine 20

Calcolo di entropie n e questa potremo semplificarla con l’equazione di stato e la relazione di Meyer Marina Cobal - Dipt. di Fisica Universita' di Udine 21

Calcolo di entropie Marina Cobal - Dipt. di Fisica Universita' di Udine 22

Calcolo di entropie n Ad esempio per l’espansione libera di un gas biatomico, in un volume doppio Marina Cobal - Dipt. di Fisica Universita' di Udine 23

Entropia: Riassunto n n S e’ una funzione di stato! DStot = DSsis + DSamb Se DStot e’ positivo il processo e’ spontaneo Se DStot e’ negativo, il processo e’ spontaneo nella direzione opposta. In un processo spontaneo, l’Entropia dell’universo aumenta sempre

Entropia per processi spontanei n n n Per processi spontanei DStot = DSsis + DSamb > 0 D’ora in poi, chiamiamo DSsis = DS Processo Esotermico n n Processo Endotermico n n q < 0, qamb > 0 quindi DSamb > 0 q > 0, qamb < 0 quindi DSamb < 0 In ogni caso DStot > 0
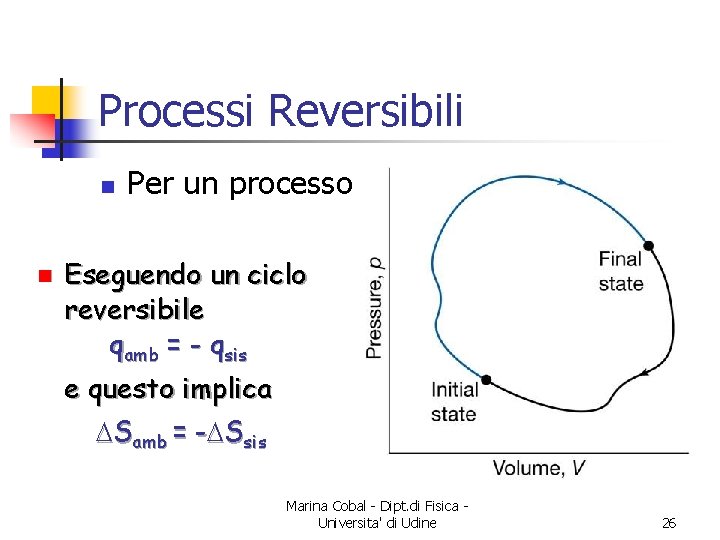
Processi Reversibili n n Per un processo reversibile, DStot = 0 Eseguendo un ciclo reversibile qamb = - qsis e questo implica DSamb = -DSsis Marina Cobal - Dipt. di Fisica Universita' di Udine 26

Variazioni di Entropia DStot 0 n n n DStot > 0 Processo Irreversibile DStot = 0 Processo Reversibile In forma differenziale d. Samb+ d. S 0 Marina Cobal - Dipt. di Fisica Universita' di Udine 27

Il 2° principio e la statistica Marina Cobal - Dipt. di Fisica Universita' di Udine 28

Entropia e disordine n n n Supponiamo di avere una scatola con 2 molecole identiche Dividiamola con un setto immaginario Saranno possibili le seguenti configurazioni Marina Cobal - Dipt. di Fisica Universita' di Udine 29
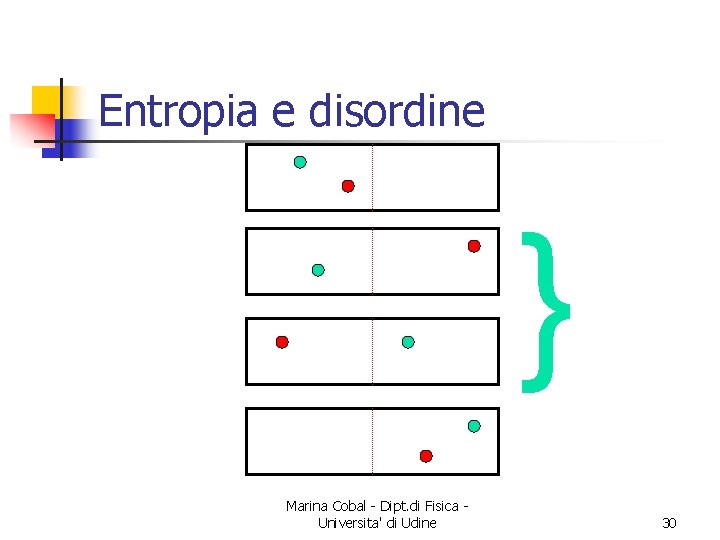
Entropia e disordine } Marina Cobal - Dipt. di Fisica Universita' di Udine 30

Entropia e disordine n n Lo stato con una molecola per parte può essere raggiunto in 2 modi diversi E con 3 molecole la cosa si ripete e si estende. . . Marina Cobal - Dipt. di Fisica Universita' di Udine 31
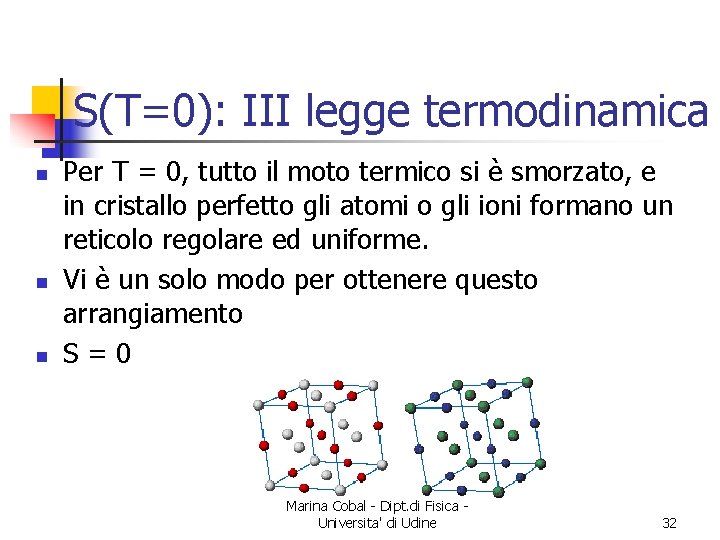
S(T=0): III legge termodinamica n n n Per T = 0, tutto il moto termico si è smorzato, e in cristallo perfetto gli atomi o gli ioni formano un reticolo regolare ed uniforme. Vi è un solo modo per ottenere questo arrangiamento S=0 Marina Cobal - Dipt. di Fisica Universita' di Udine 32

III Legge della Termodinamica l’Entropia di un cristallo perfetto a 0 K è 0 n le entropie hanno una scala assoluta, grazie alla Terza Legge. Marina Cobal - Dipt. di Fisica Universita' di Udine 33

E’ possibile definire funzioni di stato, genericamente chiamati “potenziali termodinamici”, che, poiche’: 1 o Principio Þ 2 o Principio Þ assumono il valore minimo, in determinati tipi di trasformazione, quando il sistema raggiunge l’equilibrio termodinamico ( in analogia con i sistemi meccanici, che sono in una posizione di equilibrio stabile quando è minima l’energia potenziale) Per qualsiasi trasformazione: ( 1 o Principio) ( 2 o Principio : disuguaglianza di Clausius ) Marina Cobal - Dipt. di Fisica Universita' di Udine 34

Entalpia n n n Definiamo l’Entalpia come L’Entalpia è una funzione di stato in quanto somma di funzioni di stato. Una volta era chiamata contenuto di calore D H = Hf - H i Calcoliamo la variazione infinitesima Marina Cobal - Dipt. di Fisica Universita' di Udine 35

d. H e DH ü ü Utilizziamo ora il primo principio Per un sistema in equilibrio in un processo reversibile Marina Cobal - Dipt. di Fisica Universita' di Udine 36

Calore e Entalpia n n n in condizioni di pressione costante dp = 0. . . Quindi il calore infinitesimo scambiato a pressione costante è pari alla variazione infinitesima di Entalpia Per una variazione finita, a pressione costante. . Marina Cobal - Dipt. di Fisica Universita' di Udine 37

DH Per un gas ideale n n H = U + p. V DH = DU + D(p. V) n n Ma per un processo isotermo n n n Per un gas ideale, p. V = n RT allora D(p. V) = D(n RT) Ma D(n RT) = n R DT DU = 0 n R DT = 0 Quindi DH = 0 38

Entalpia n n In un certo senso, l’Entalpia non è una funzione termodinamica “fondamentale”. È una nostra comoda invenzione, dovuta al fatto che viviamo su un pianeta dove la pressione è praticamente costante. Se incontrassimo dei Chimici alieni, che vivono su un pianeta dove la pressione subisce forti variazioni in poco tempo, probabilmente la loro Termodinamica conterrebbe U ma non H Marina Cobal - Dipt. di Fisica Universita' di Udine 39

Potenziali termodinamici “Energia libera “(o “potenziale di Helmotz”): Nelle trasf. isocore e isoterme, dalla disuguaglianza: d. V=0 d. T=0 l’energia libera assume il valore minimo nelle trasformazioni isocore e isoterme “Entalpia libera” (o “potenziale di Gibbs”) : Nelle trasf. isobare e isoterme, dalla disuguaglianza: dp=0, d. T=0 Þ l’entalpia libera assume il valore minimo nelle Marina Cobalisobare - Dipt. di Fisica trasformazioni e isoterme Universita' di Udine 40
- Slides: 39