Lek generyczny Lek referencyjny i leki generyczne zawieraj









- Slides: 12

Lek generyczny

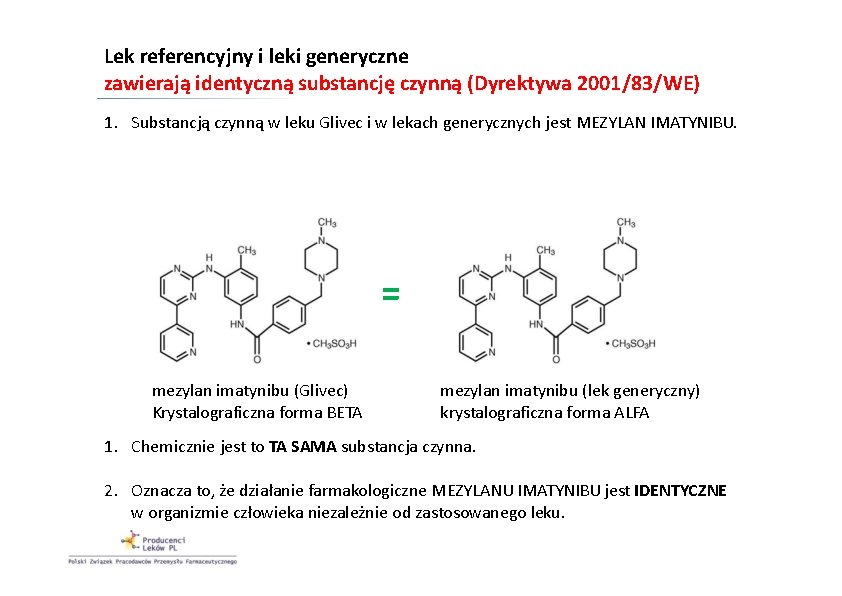
Lek referencyjny i leki generyczne zawierają identyczną substancję czynną (Dyrektywa 2001/83/WE) 1. Substancją czynną w leku Glivec i w lekach generycznych jest MEZYLAN IMATYNIBU. = mezylan imatynibu (Glivec) Krystalograficzna forma BETA mezylan imatynibu (lek generyczny) krystalograficzna forma ALFA 1. Chemicznie jest to TA SAMA substancja czynna. 2. Oznacza to, że działanie farmakologiczne MEZYLANU IMATYNIBU jest IDENTYCZNE w organizmie człowieka niezależnie od zastosowanego leku.

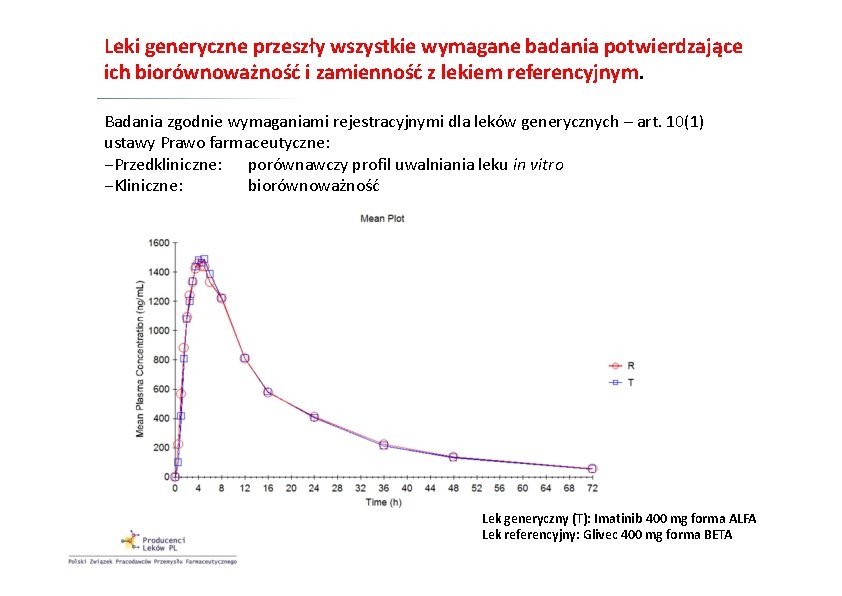
Leki generyczne przeszły wszystkie wymagane badania potwierdzające ich biorównoważność i zamienność z lekiem referencyjnym. Badania zgodnie wymaganiami rejestracyjnymi dla leków generycznych – art. 10(1) ustawy Prawo farmaceutyczne: −Przedkliniczne: porównawczy profil uwalniania leku in vitro −Kliniczne: biorównoważność Lek generyczny (T): Imatinib 400 mg forma ALFA Lek referencyjny: Glivec 400 mg forma BETA

Podstawą dopuszczenia do obrotu wszystkich produktów generycznych Imatynibu, będących odpowiednikami leku Glivec we wszystkich zarejestrowanych wskazaniach, były badania kliniczne biorównoważności, które dowiodły ponad wszelką wątpliwość, iż leki generyczne dostarczają do organizmu tę samą substancję czynną w takiej samej ilości i czasie, jak lek referencyjny.

Wszystkie generyczne Imatyniby otrzymały pozwolenia od agencji europejskich i pozaeuropejskich. Są zarejestrowane w procedurach: centralnej, zdecentralizowanej i narodowych – co gwarantuje ich identyczną skuteczność i bezpieczeństwo co lek referencyjny. − − − Wszystkie kraje UE Bośnia i Hercegowina Macedonia Ukraina Korea Południowa Nowa Zelandia

Wszystkie odpowiedniki produkowane przez firmy członkowskie Związku produkowane są w fabrykach o najwyższych światowych standardach, spełniających wymogi Dobrej Praktyki Wytwarzania (GMP) i dystrybuowane są na całą UE oraz inne kraje świata

Czym się różnimy? Tylko ceną ‐ zwiększając dostępność leku w systemach refundacyjnych dla większej liczby pacjentów!

„Podważanie równoważności terapeutycznej leku generycznego nie ma podstaw naukowych i jest efektem braku wiedzy merytorycznej, przesądów, uprzedzeń (…). ” Instytut Farmaceutyczny, pismo do MZ z 11. 04. 2014



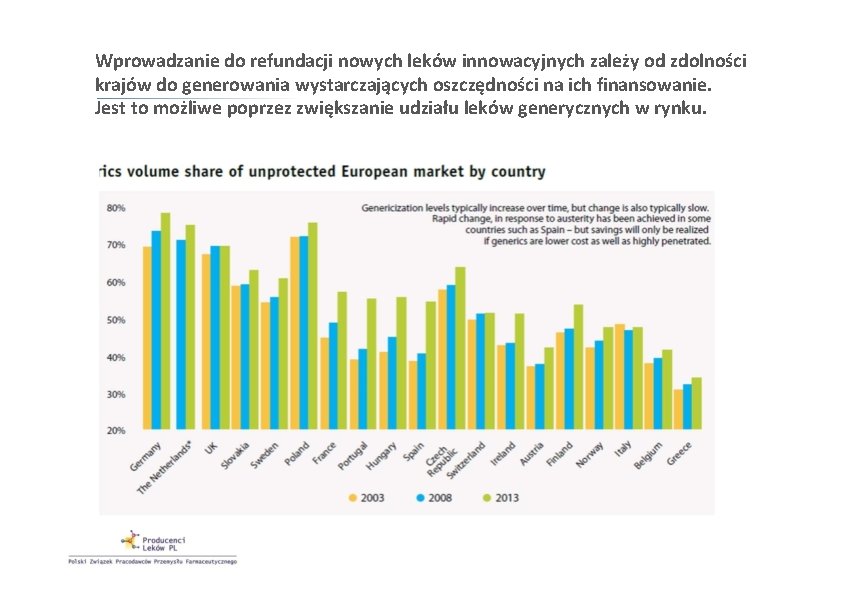
Wprowadzanie do refundacji nowych leków innowacyjnych zależy od zdolności krajów do generowania wystarczających oszczędności na ich finansowanie. Jest to możliwe poprzez zwiększanie udziału leków generycznych w rynku.

Dziękuję za uwagę!