LEGTURI CHIMICE PROF ELENA CIOBANU GRUP COLAR ENERGETIC
LEGĂTURI CHIMICE PROF. ELENA CIOBANU GRUP ŞCOLAR ENERGETIC NR. 1 TG-JIU
DEFINIŢIE Sunt interacţiunile între atomi, care se realizează prin intermediul electronilor din învelişul exterior al atomului numiţi electroni de valenţă.
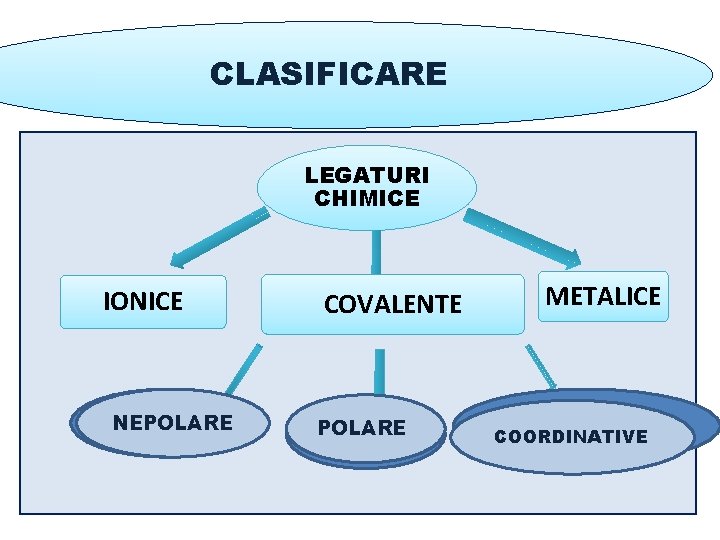
CLASIFICARE LEGATURI CHIMICE IONICE NEPOLARE COVALENTE POLARE METALICE COORDINATIVE

LEGĂTURA IONICĂ Este atracţia electrostatică ce se stabileşte între ionii de semn contrar, formaţi prin transfer de electroni de la metal la nemetal. Produşii obţinuţi se numesc compuşi ionici. Modelarea formării legăturii ionice în Na. Cl: Na + Cl → Na+ + Cl- → Na+Cl-
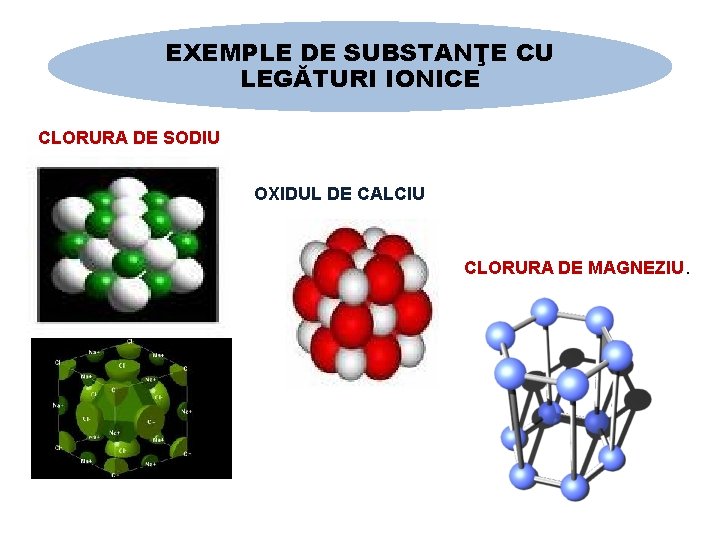
EXEMPLE DE SUBSTANŢE CU LEGĂTURI IONICE CLORURA DE SODIU OXIDUL DE CALCIU CLORURA DE MAGNEZIU.

LEGĂTURA COVALENTĂ q. Se formează prin punerea în comun de electroni între atomi identici sau diferiţi de nemetale. q Compuşii rezultaţi se numesc molecule. Legătura covalentă nepolară: atomii participanţi sunt identici: H 2 , O 2, N 2 , F 2 , Cl 2 , Br 2, I 2 , O 3, P 4. Poate fi: Simplă-fiecare atom pune în comun câte un electron: H – H , H 3 C – CH 3 Dublă-fiecare atom pune în comun câte doi electroni: O=O , H 2 C=CH 2 Triplă-fiecare atom pune în comun câte trei electroni: N≡N, HC≡CH
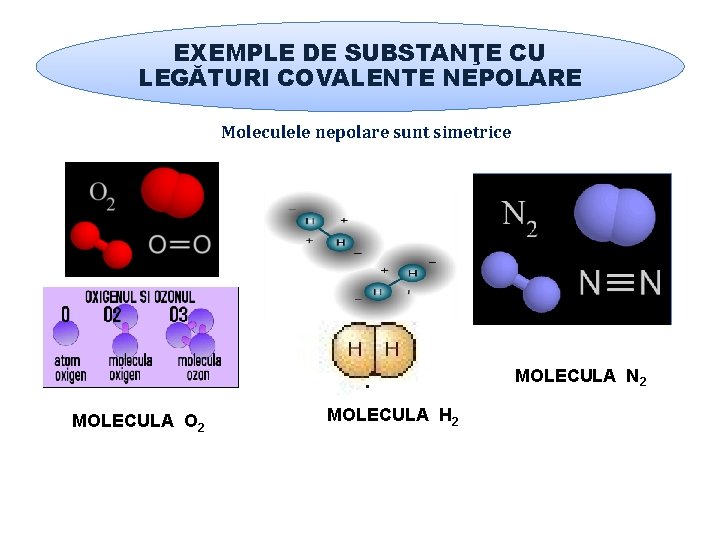
EXEMPLE DE SUBSTANŢE CU LEGĂTURI COVALENTE NEPOLARE Moleculele nepolare sunt simetrice MOLECULA N 2 MOLECULA O 2 MOLECULA H 2

LEGĂTURA COVALENTĂ POLARĂ Legătura covalentă polară: atomii participanţi sunt diferiţi şi se formează molecule polare: HCl , HF, HBr, HI , NH 3 , CH 4 , CO 2, HNO 3, HNO 2 , H 2 CO 3, H 2 SO 4, H 2 SO 3, H 3 PO 4 Moleculele polare sunt asimetrice (atomii diferiţi sunt legaţi prin legătură covalentă polară ce determină apariţia unui moment de dipol, motiv pentru care se mai numesc şi dipoli): Hδ+ Clδ-
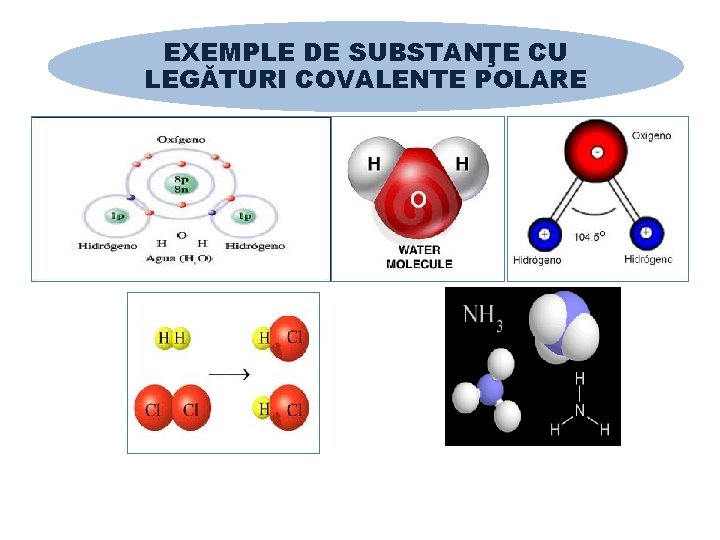
EXEMPLE DE SUBSTANŢE CU LEGĂTURI COVALENTE POLARE
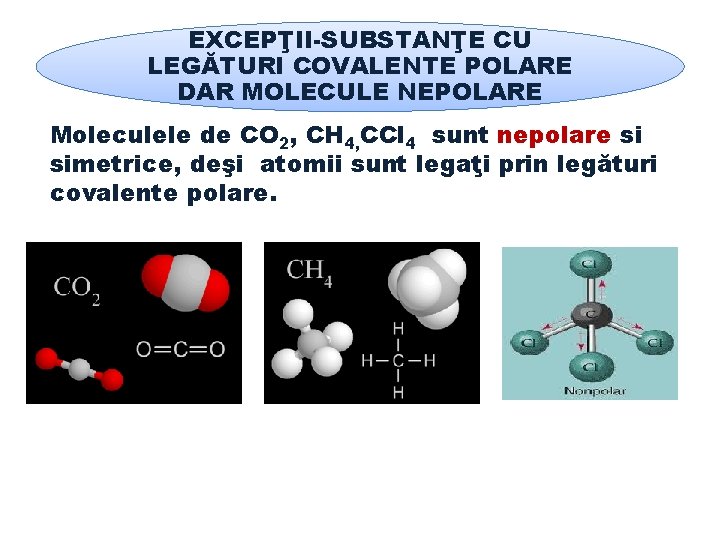
EXCEPŢII-SUBSTANŢE CU LEGĂTURI COVALENTE POLARE DAR MOLECULE NEPOLARE Moleculele de CO 2, CH 4, CCl 4 sunt nepolare si simetrice, deşi atomii sunt legaţi prin legături covalente polare.

LEGĂTURA COVALENTĂ COORDINATIVĂ (DONOR –ACCEPTOR) • Se formează prin punerea în comun de electroni proveniţi de la un singur atom de nemetal (care cel puţin un dublet de electroni liber, numit donor), cu un alt atom (care orbitali atomici liberi şi nu participă cu electroni, numit acceptor). • Modelarea formării ionilor de hidroniu şi amoniu: H 2Ö: + H+ → H 3Ö+ : NH 3 + H+ → NH 4+
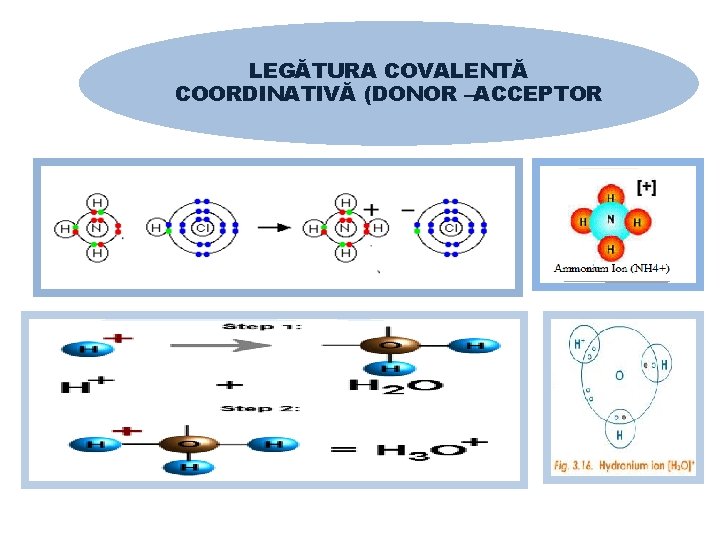
LEGĂTURA COVALENTĂ COORDINATIVĂ (DONOR –ACCEPTOR
SUBSTANŢE CU LEGĂTURA COVALENTĂ COORDINATIVĂ q Săruri de amoniu: ~ clorura de amoniu, NH 4 Cl ~ carbonatul de amoniu, (NH 4)2 CO 3 q Combinaţii complexe: ~ hidroxid de tetraamino. Cu(II) [Cu(NH 3)4](OH)2 ~ clorura de diamino. Cu(I) [Cu(NH 3)2]Cl ~ hidroxid de diamino. Ag(I) [Ag(NH 3)2]OH

- Slides: 14