Leccin 4 Equilibrios en disolucin Redox y precipitacin

Lección 4 Equilibrios en disolución: Redox y precipitación

Capítulo Final. Equilibrios en disolución: Redox y precipitación Ø Ø Ø Generalidades: conceptos básicos Celda electroquímica Potencial de una pila Ø Ø Ø Ø Ø Electrodo estándar de hidrógeno Medida de potenciales normales de electrodos Espontaneidad de las reacciones redox La Ecuación de Nernst Equilibrios de precipitación Solubilidad Efecto del ión común Diagramas de Latimer Diagramas de Frost 2

Generalidades: reacciones redox Ø Ø Una reacción redox es un proceso químico en el que se transfieren electrones La especie química que pierde electrones se oxida (su número de oxidación aumenta) La especie química que gana electrones se reduce (su número de oxidación disminuye) P. Ej, la adición de Zn a una disolución de HCl conduce a la reacción espontánea: Se oxida Zn(s) + 2 H+(ac) Zn 2+(ac) + H 2(g) Se reduce Ø Ø Ø El Zn es capaz de reducir al H+ y es el agente reductor El H+ es capaz de oxidar al Zn y es el agente oxidante El agente reductor se oxida mientras que el agente oxidante se reduce en el proceso redox 3

Generalidades: ecuaciones redox Ø Ø La reacción redox se puede descomponer, convenientemente, en dos semirreacciones Las semirreacciones para: Sn 2+(ac) + 2 Fe 3+(ac) Sn 4+(ac) + 2 Fe 2+(ac) son Semirreacción de oxidación: Sn 2+(ac) Sn 4+(ac) +2 e. Semirreacción de reducción: 2 Fe 3+(ac) + 2 e- 2 Fe 2+(ac) La suma de las dos semirreacciones ajustadas debe ser igual a la reacción redox Una reacción redox se puede realizar de dos maneras: Ø Ø mediante contacto directo entre los reactivos en el mismo recipiente Separación de los reactivos en recipientes distintos, fluyendo los electrones a través de un circuito celda galvánica 4

Celda electroquímica Ø Ø La energía que se libera en un proceso redox espontáneo se utiliza para producir un trabajo eléctrico Una celda electroquímica o pila galvánica es un dispositivo en el que la transferencia de electrones ocurre mediante un circuito externo La celda electroquímica está constituida por dos semicéldas conectadas mediante un puente salino Una semicélda está formada por un electrodo (pieza de metal) sumergido en una disolución que contiene iones del mismo metal Reacción de la pila Zn(s) + Cu 2+(ac) Zn 2+(ac) + Cu(s) 5
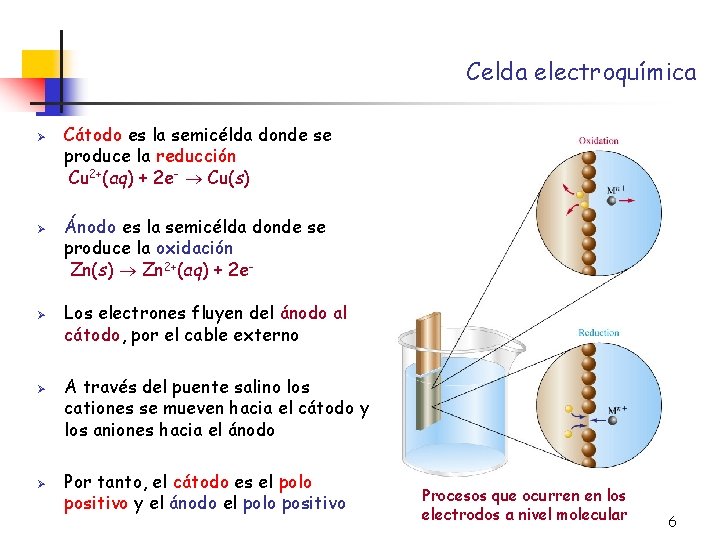
Celda electroquímica Ø Ø Ø Cátodo es la semicélda donde se produce la reducción Cu 2+(aq) + 2 e- Cu(s) Ánodo es la semicélda donde se produce la oxidación Zn(s) Zn 2+(aq) + 2 e. Los electrones fluyen del ánodo al cátodo, por el cable externo A través del puente salino los cationes se mueven hacia el cátodo y los aniones hacia el ánodo Por tanto, el cátodo es el polo positivo y el ánodo el polo positivo Procesos que ocurren en los electrodos a nivel molecular 6

Potencial de una pila (Epila) Ø Ø La fuerza electromotriz (fem) de una pila es la energía requerida para mover los electrones por el circuito externo El potencial de una celda o pila, Epila, es la fem de la pila Para disoluciones 1 M a 25 ºC (condiciones estándar), la fuerza electromotriz estándar o potencial estándar de la pila se denomina Eºpila El potencial de una pila se expresa en función de los potenciales estándar de los electrodos que forman la pila Eºpila = Eºcátodo - Eºánodo 7

Potencial de una pila (Epila) Ø No se puede obtener el potencial de un electrodo aislado. Ejemplo Eºpila = Eºcátodo - Eºlánodo = 1. 0 V posibles soluciones Eºcátodo=3. 5 V, Eºánodo= 2. 5 V Eºcátodo=3. 0 V, Eºánodo= 2. 0 V Eºcátodo=10. 0 V, Eºánodo= 9. 0 V ad infinitum. . . Ø Ø Ø Para poder hacerlo se asigna a una determinado electrodo el valor de referencia de cero. Dicho electrodo es el electrodo estándar de hidrógeno (EEH) Los potenciales estándar de electrodo Eºelect se miden frente al potencial del electrodo estándar de hidrógeno Los potenciales estándar de electrodos se ordenan convenientemente en una tabla, siempre en sentido de reducción. 8

Electrodo estándar de hidrógeno Reacción que tiene lugar en el electrodo estándar de hidrógeno: 2 H+ (1 M) + 2 e- H 2(g) (1 atm) Eº 2 H+/H 2 = 0 V Ø Para medir el potencial estándar de un electrodo, p. ej de la reacción Cu 2+(ac) + 2 e- Cu(s) EºCu 2+/Cu Ø Ø Se construye una pila formada por el electrodo de hidrógeno y el electrodo cuyo potencial queremos conocer 9
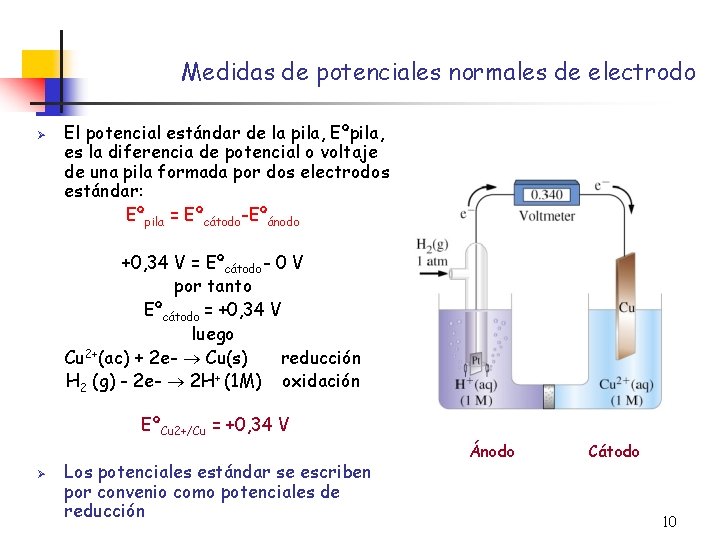
Medidas de potenciales normales de electrodo Ø El potencial estándar de la pila, Eºpila, es la diferencia de potencial o voltaje de una pila formada por dos electrodos estándar: Eºpila = Eºcátodo-Eºánodo +0, 34 V = Eºcátodo- 0 V por tanto Eºcátodo = +0, 34 V luego Cu 2+(ac) + 2 e- Cu(s) reducción H 2 (g) - 2 e- 2 H+ (1 M) oxidación EºCu 2+/Cu = +0, 34 V Ø Los potenciales estándar se escriben por convenio como potenciales de reducción Ánodo Cátodo 10
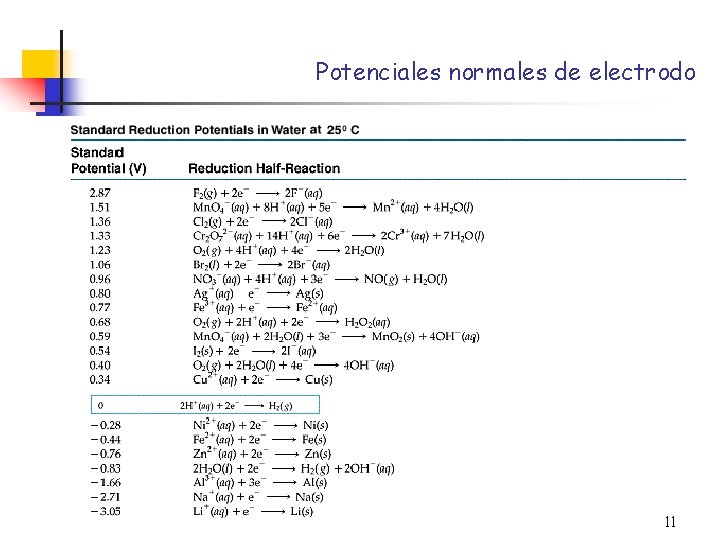
Potenciales normales de electrodo 11

Oxidantes y reductores Ø Ø Cuanto más positivo es Eº más fuerte es el agente oxidante (lado izquierdo de las reacciones) Cuanto más negativo es Eº más fuerte es el agente reductor (lado derecho de las reacciones) Agentes oxidantes más fuertes: lado izquierdo y parte superior de la tabla Agentes reductores más fuertes: lado derecho y parte inferior de la tabla 12

Oxidantes y reductores Ø Ø Una especie química reactiva que se encuentre en la parte superior (y esté en el lado izquierdo) de la tabla oxidará, espontáneamente, a la otra especie química reactiva que se encuentre por debajo de ella (y esté en el lado derecho de la misma). O lo que es lo mismo, cualquier especie que se encuentre en el lado derecho de una reacción química reducirá, espontáneamente, cualquier otra que se encuentre a la izquierda por encima de ella Ø Ejemplos: Ø Ø 3 Fe 3+ + Al(s) 3 Fe 2+ + Al 3+ Zn(s) + Cu 2+ Zn 2+ + Cu(s) 13
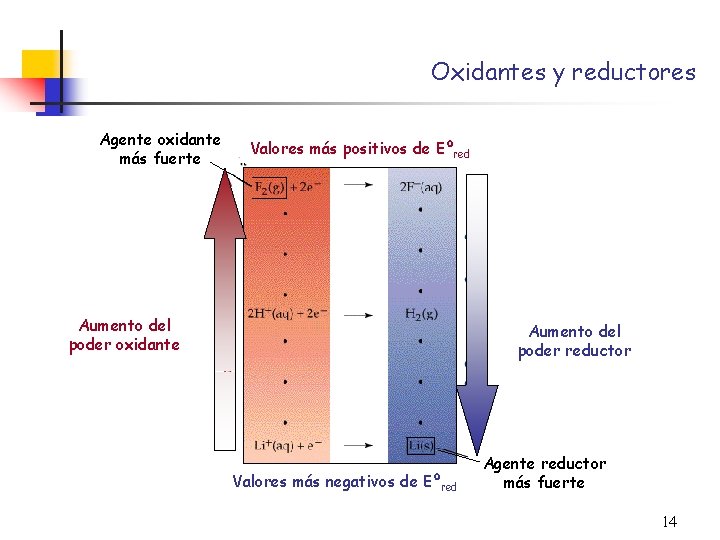
Oxidantes y reductores Agente oxidante más fuerte Valores más positivos de Eºred Aumento del poder oxidante Aumento del poder reductor Valores más negativos de Eºred Agente reductor más fuerte 14

Espontaneidad de las reacciones redox Ø Ø Ø En una pila galvánica el potencial Eº del cátodo es siempre más positivo que Eº del ánodo Eºpila = Eº(cátodo) –Eº(ánodo) De forma general, para cualquier proceso electroquímico: Eºpila = Eºred(proceso de reducción) –Eºred(proceso de oxidación) Un valor positivo de Eºpila indica que el proceso es espontáneo Un valor negativo de Eºpila indica que el proceso no es espontáneo Por ejemplo, consideremos el desplazamiento de la plata por el níquel Ni(s) + 2 Ag+(aq) Ni 2+(aq) + 2 Ag(s) tiene E = E red(Ag+/Ag) - E red(Ni 2+/Ni) = (0. 80 V) - (-0. 28 V) = 1. 08 V Ø Lo cual indica que el proceso es espontáneo 15

Espontaneidad de las reacciones redox Ø Ø Ø Ø Eºpila está relacionada con la energía libre DG mediante la expresión: DG = -n. FEºpila Dond n es el número de moles de electrones transferidos, F es la constante de Faraday (96500 C) y Eºpila es potencial de la pila Como n y F son valores positivos, si DG>0 entonces E<0 Una pila funciona hasta que E = 0, momento en el que se ha alcanzado el equilibrio El punto en el cual E = 0 viene determinado, para una pila dada, por el valor de las concentraciones de las especies que están implicadas en el proceso redox Para calcular el potencial de una pila en condiciones que no sean las estándar hay que utilizar la ecuación de Nernst La ecuación de Nernst relaciona la fem de la pila concentración 16

Ecuación de Nernst DG = DGº + RTln. Q Luego -n. FE = -n. FEº + RTln. Q Ø Ø Esta expresión se puede reorganizar para dar E = Eº- (RT/n. F)ln. Q La ecuación de Nernst puede simplificarse reemplazando las constantes por una sola especificando la temperatura de 298 K E = Eº -(0, 0592/n)log. Q Ø En el equilibrio E = 0 , entonces Eº = (0, 0592/n)log. K Cte de equilibrio 17

Equilibrios de precipitación Ø Cuando se satura una disolución en una sal, se establece un equilibrio entre el sólido y los iones en disolución Ejemplo Ø Ba(IO 3)2 (s) Ba 2+(aq) + 2 IO 3 - (aq) La constante de equilibrio viene dada por Ø K= [Ba 2+][IO 3 -]2 [Ba(IO 3)2 ] ya que [Ba(IO 3)2] = cte Ø K[Ba(IO 3)2 ] = [Ba 2+][IO 3 -]2 Kps = [Ba 2+][IO 3 -]2 Constante de equilibrio de solubilidad o Producto de solubilidad Kps 18

Equilibrios de precipitación Ø Para un compuesto An. Bm Ø Ø Ø An. Bm(s) n. Am- + m. Bn+ Kps = [Am-]n[Bn+]m si [Am-]n[Bn+]m < Kps disolución no saturado si [Am-]n[Bn+]m = Kps disolución saturada si [Am-]n[Bn+]m > Kps precipita An. Bm hasta que se [A]n[B]m = Kps compuesto Ba(IO 3)2 Ag. Cl Ag. Br Ag. I Fe(OH)2 Al(OH)3 Fe(OH)3 Ag 2 S Hg. S Kps 1. 57 x 10 -9 1. 82 x 10 -10 5. 0 x 10 -13 8. 3 x 10 -17 4. 1 x 10 -15 3 x 10 -34 2 x 10 -39 8 x 10 -51 2 x 10 -53 Compuestos más insolubles 19
![Solubilidad Para un compuesto An. Bm(s) n. Am- + m. Bn+ Kps = [Am-]n[Bn+]m Solubilidad Para un compuesto An. Bm(s) n. Am- + m. Bn+ Kps = [Am-]n[Bn+]m](http://slidetodoc.com/presentation_image_h/2c7815977bd9f604bc8249ad58b0120c/image-20.jpg)
Solubilidad Para un compuesto An. Bm(s) n. Am- + m. Bn+ Kps = [Am-]n[Bn+]m Ø La solubilidad iónica o molar s = [Am-]/n ó s = [Bn+]/m Ø s se puede calcular a partir de Kps [Am-] = ns [Bn+]= ms Kps = [Am-]n[Bn+]m = (ms)m(ns)n = mm · nn · sm+n 20

Efecto del ión común Ø Ø El efecto del ión común es una reducción en la solubilidad de un precipitado iónico al añadir un compuesto soluble que contiene uno de los iones del precipitado Ejemplo Calcular la solubilidad del Ba(IO 3)2 en i) agua y ii) una disolución que es 0. 02 M en Ba(NO 3)2. Kps 1. 57 x 10 -9 i) Ba(IO 3)2 (s) Ba 2+(aq) + 2 IO 3 - (aq) Kps= [Ba 2+][IO 3 -]2 = s· (2 s)2= 4 s 3 = 1. 57 x 10 -9 s = (1. 57 x 10 -9/4)1/3= 7. 32 x 10 -4 M 21

Efecto del ión común Ø ii) Ba(IO 3)2 (s) Ba 2+(aq) + 2 IO 3 - (aq) Kps Ba(NO 3)2(aq) Ba 2+(aq) + 2 NO 3 - (aq) Implica resolver una ecuación de 3º grado Kps= [Ba 2+][IO 3 -]2 = (s + 0. 02)· (2 s)2= 1. 57 x 10 -9 simplificación: suponer que s<< 0. 02 M, entonces s+0. 02 M Kps= (s + 0. 02)· (2 s)2 0. 02· 4 s 2= 1. 57 x 10 -9 s = (1. 57 x 10 -9/0. 02· 4 )1/2= 1. 40 x 10 -4 M 22
- Slides: 22