Leccin 3 Equilibrios en disolucin y valoraciones I

Lección 3 Equilibrios en disolución y valoraciones (I): Ácidos y Bases. Sales poco solubles.

Lección 3. Equilibrios en disolución y valoraciones (I): Ácidos y bases. Sales poco solubles. Índice Ø Ø Ø Propiedades de los ácidos y las bases Teorías ácido-base: Ø Definiciones de Arrhenius. Ø Definiciones de Brønsted-Lowry. Propiedades ácido-base del agua y la escala de p. H. Fuerza de los ácidos y las bases. Ácidos y bases débiles. Constantes de ionización ácidas y básica. Vamos a usar Balances de Masa y Carga. Aplicación para diferentes sistemas ácido-base. Propiedades ácido-base de las sales: Hidrólisis. Ácidos y bases de Lewis. El efecto de ion común en los equilibrios ácido-base. Disoluciones reguladoras de p. H. Las sales poco solubles. Ejercicios de aplicación. 2

Índice Ø Valoraciones: Ø Ø Ø Introducción Términos relacionados con las volumetrías Punto de equivalencia y punto final Curvas de valoración Valoraciones ácido-base Ø Ø Ø Indicadores ácido-base Valoración de un ácido fuerte con una base fuerte Valoración de un ácido débil con una base fuerte 3

Ácidos y Bases ÁCIDOS Ø Ø BASES Tienen sabor agrio Reaccionan con metales (Zn, Mg, Fe, . . ) para producir H 2 gaseoso Son conductores de la electricidad (electrolitos) Colorean de rojo el papel de tornasol Ø Ø Tienen sabor amargo Tienen tacto resbaladizo, como el de los jabones (bases) Son conductores de la electricidad (electrolitos) Colorean de azul el papel de tornasol Deterjentes y jabones Limpiadores amoniacales cítricos aspirina Fármacos Antiácidos 4

Teorías ácido-base Teoría de Arrhenius Ø Ácidos son sustancias que se ionizan en agua para formar iones H + HCl Ø H+ + Cl Bases son sustancias que se ionizan en agua para formar iones OH Na. OH Ø H 2 O Na+ + OH Limitaciones de la teoría: Ø Ø Ø Sólo aplicable a disoluciones acuosas No explica la basicidad del amoniaco (NH 3) y de bases aminadas orgánicas (no contienen OH ) No reconoce el papel fundamental del disolvente en los equilibrios ácidobase 5
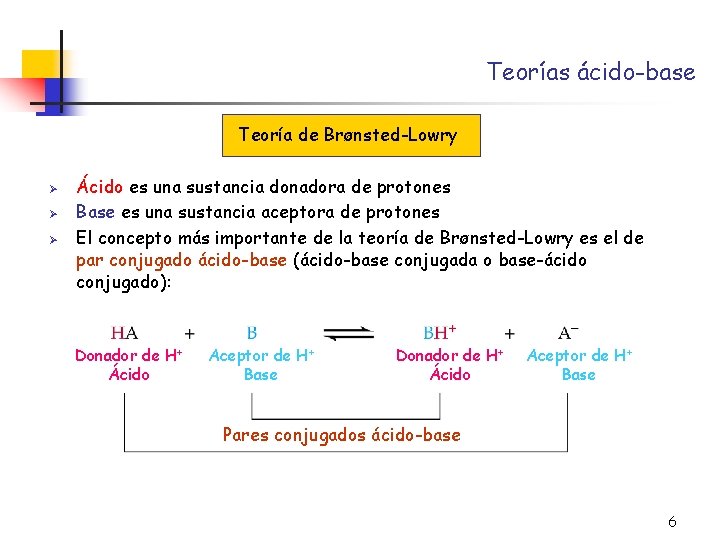
Teorías ácido-base Teoría de Brønsted-Lowry Ø Ø Ø Ácido es una sustancia donadora de protones Base es una sustancia aceptora de protones El concepto más importante de la teoría de Brønsted-Lowry es el de par conjugado ácido-base (ácido-base conjugada o base-ácido conjugado): Donador de H+ Ácido Aceptor de H+ Base Pares conjugados ácido-base 6
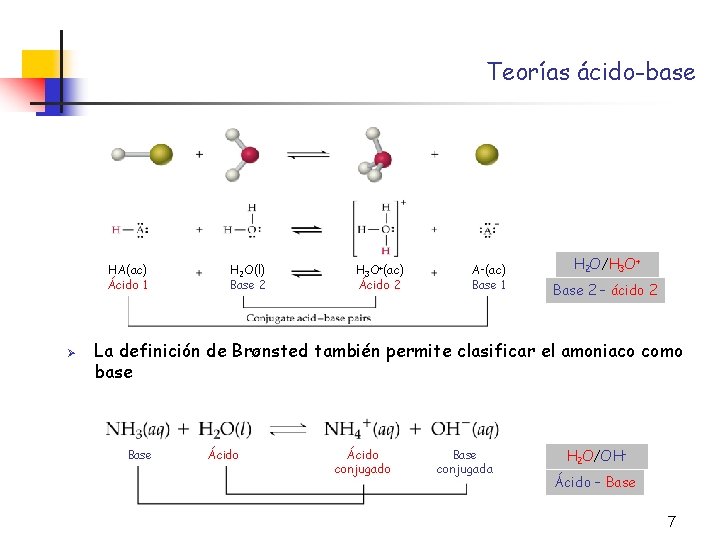
Teorías ácido-base HA(ac) Ácido 1 Ø H 2 O(l) Base 2 H 3 O+(ac) Ácido 2 A (ac) Base 1 H 2 O/H 3 O+ Base 2 – ácido 2 La definición de Brønsted también permite clasificar el amoniaco como base Base Ácido conjugado Base conjugada H 2 O/OHÁcido – Base 7
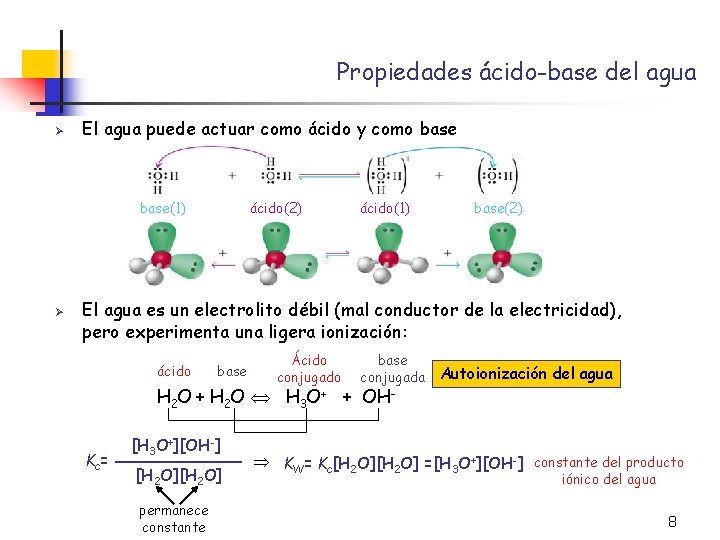
Propiedades ácido-base del agua Ø El agua puede actuar como ácido y como base(1) Ø ácido(2) ácido(1) base(2) El agua es un electrolito débil (mal conductor de la electricidad), pero experimenta una ligera ionización: ácido base Ácido conjugado base conjugada Autoionización del agua H 2 O + H 2 O H 3 O+ + OHKc= [H 3 O+][OH-] [H 2 O] permanece constante KW= Kc[H 2 O] = [H 3 O+][OH-] constante del producto iónico del agua 8
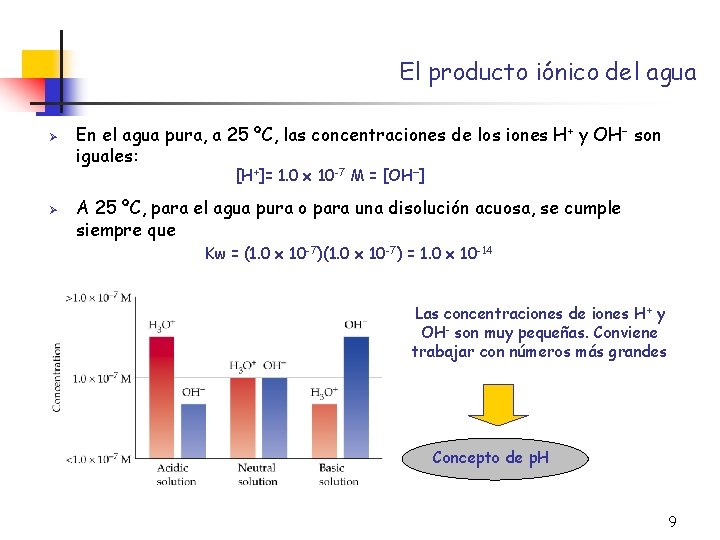
El producto iónico del agua Ø En el agua pura, a 25 ºC, las concentraciones de los iones H + y OH son iguales: [H+]= 1. 0 x 10 -7 M = [OH ] Ø A 25 ºC, para el agua pura o para una disolución acuosa, se cumple siempre que Kw = (1. 0 x 10 -7) = 1. 0 x 10 -14 Las concentraciones de iones H+ y OH- son muy pequeñas. Conviene trabajar con números más grandes Concepto de p. H 9

El p. H y su escala Ø S. Sorensen introduce en 1909 el concepto de p. H (potencial del ion hidrógeno): p. H = -log[H 3 O+] p. OH = -log[OH ] KW = [H 3 O+][OH-]= 1. 0 x 10 -14 -log. KW = -log[H 3 O+]-log[OH-]= -log(1. 0 x 10 -14) p. KW = p. H + p. OH= -(-14) p. KW = p. H + p. OH = 14 Ø El p. H es una forma de expresar la concentración de [H 3 O+]. Las disoluciones ácidas y básicas se identifican por sus valores de p. H: Neutra Escala de p. H ácido p. H < 7 básico p. H > 7 10
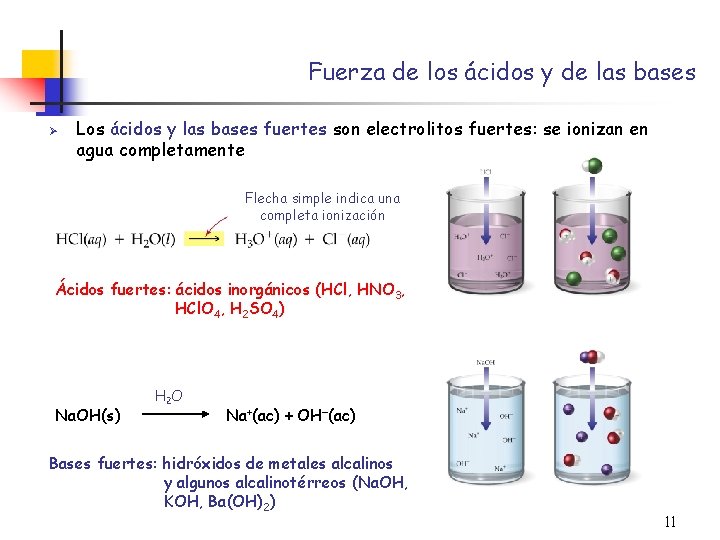
Fuerza de los ácidos y de las bases Ø Los ácidos y las bases fuertes son electrolitos fuertes: se ionizan en agua completamente Flecha simple indica una completa ionización Ácidos fuertes: ácidos inorgánicos (HCl, HNO 3, HCl. O 4, H 2 SO 4) Na. OH(s) H 2 O Na+(ac) + OH (ac) Bases fuertes: hidróxidos de metales alcalinos y algunos alcalinotérreos (Na. OH, KOH, Ba(OH)2) 11
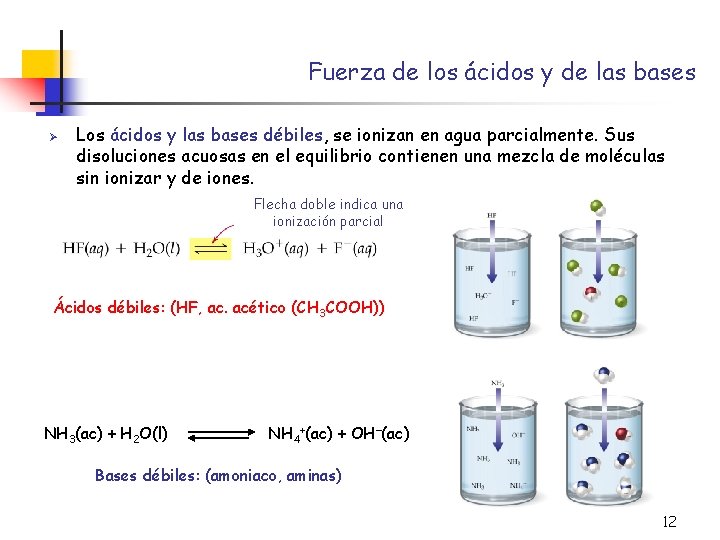
Fuerza de los ácidos y de las bases Ø Los ácidos y las bases débiles, se ionizan en agua parcialmente. Sus disoluciones acuosas en el equilibrio contienen una mezcla de moléculas sin ionizar y de iones. Flecha doble indica una ionización parcial Ácidos débiles: (HF, ac. acético (CH 3 COOH)) NH 3(ac) + H 2 O(l) NH 4+(ac) + OH (ac) Bases débiles: (amoniaco, aminas) 12

Fuerza de los ácidos y de las bases Ácidos y bases fuertes comunes 13
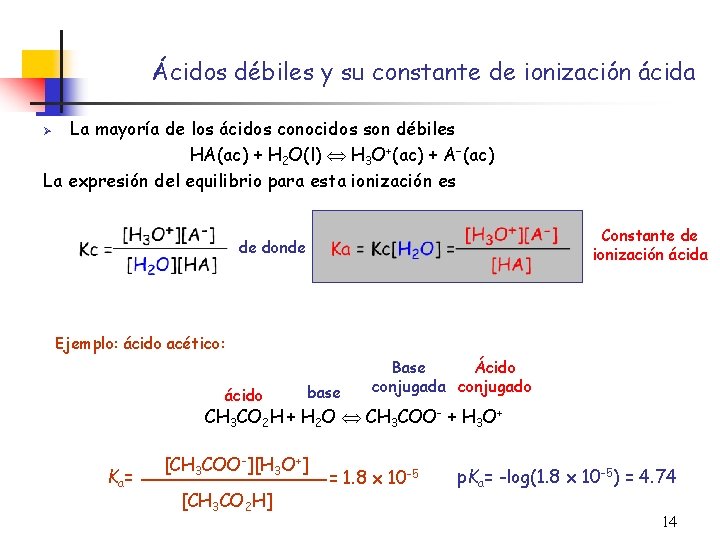
Ácidos débiles y su constante de ionización ácida La mayoría de los ácidos conocidos son débiles HA(ac) + H 2 O(l) H 3 O+(ac) + A (ac) La expresión del equilibrio para esta ionización es Ø Constante de ionización ácida de donde Ejemplo: ácido acético: ácido base Base Ácido conjugada conjugado CH 3 CO 2 H + H 2 O CH 3 COO- + H 3 O+ Ka = [CH 3 COO-][H 3 O+] [CH 3 CO 2 H] = 1. 8 x 10 -5 p. Ka= -log(1. 8 x 10 -5) = 4. 74 14
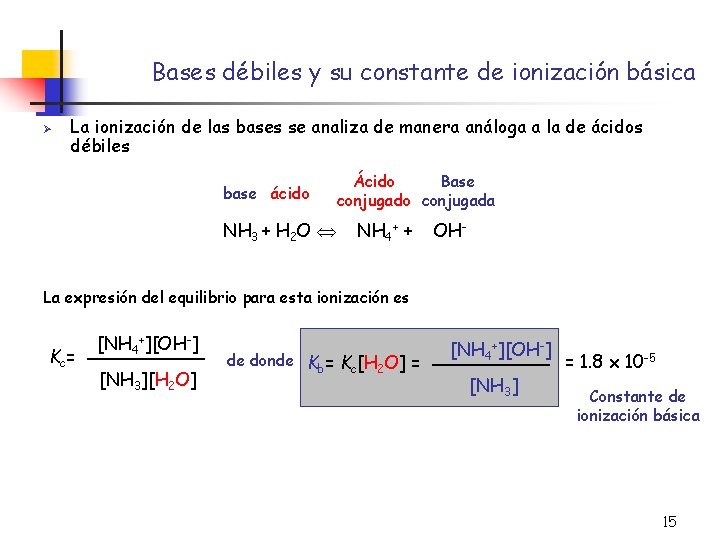
Bases débiles y su constante de ionización básica Ø La ionización de las bases se analiza de manera análoga a la de ácidos débiles base ácido NH 3 + H 2 O Ácido Base conjugado conjugada NH 4+ + OH- La expresión del equilibrio para esta ionización es Kc = [NH 4+][OH-] [NH 3][H 2 O] de donde Kb= Kc[H 2 O] = [NH 4+][OH-] [NH 3] = 1. 8 x 10 -5 Constante de ionización básica 15
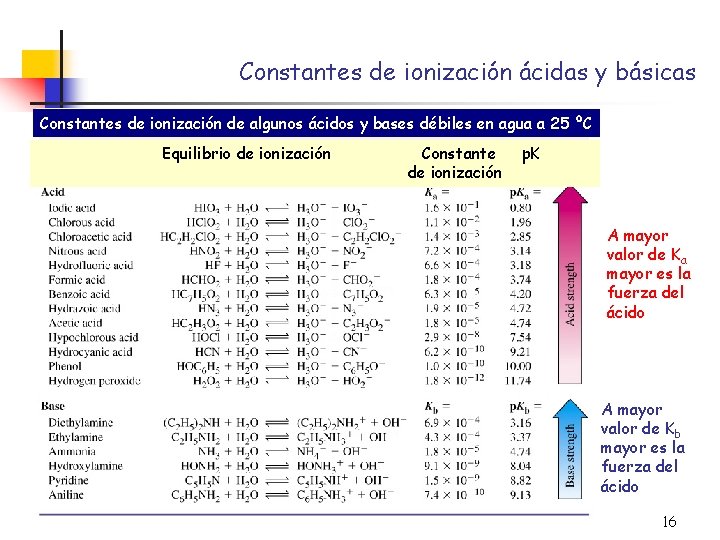
Constantes de ionización ácidas y básicas Constantes de ionización de algunos ácidos y bases débiles en agua a 25 ºC Equilibrio de ionización Constante de ionización p. K A mayor valor de Ka mayor es la fuerza del ácido A mayor valor de Kb mayor es la fuerza del ácido 16

Porcentaje de ionización Ø Ka indica la fuerza de un ácido. Otra forma de medirla es mediante el porcentaje de ionización: La proporción en que un ácido débil se ioniza depende de su concentración inicial. Molaridad del ácido ( ) representa el p. H de la disolución Cuanto más diluida sea la disolución mayor será el porcentaje de ionización. 17

Relación entre las constantes de ionización de los ácidos y sus bases conjugadas Ø La constante de ionización ácida (Ka) está relacionada con la constante de ionización de su base conjugada CH 3 CO 2 H + H 2 O CH 3 COO- + H 3 O+ Ka= [CH 3 COO-][H 3 O+] [CH 3 CO 2 H] Ø La base conjugada, CH 3 COO , reacciona con agua: CH 3 COO + H 2 O CH 3 COOH + OH Kb= Ø [CH 3 COOH][OH ] [CH 3 COO ] El producto de estas dos constantes está dado por Ka x K b = [CH 3 COO-][H 3 O+] [CH 3 CO 2 H] x [CH 3 COOH][OH ] Para cualquier par conjugado [CH 3 COO ] = [H 3 O+][OH ] = Kw Ka x Kb = Kw 18
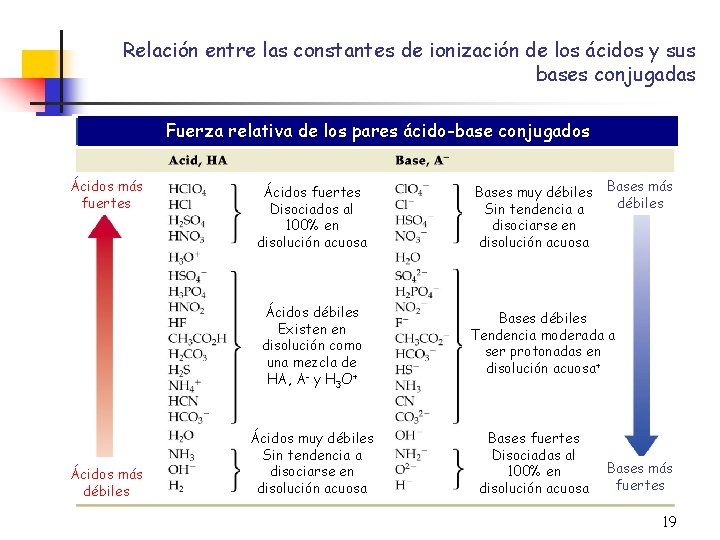
Relación entre las constantes de ionización de los ácidos y sus bases conjugadas Fuerza relativa de los pares ácido-base conjugados Ácidos más fuertes Ácidos fuertes Disociados al 100% en disolución acuosa Ácidos débiles Existen en disolución como una mezcla de HA, A- y H 3 O+ Ácidos más débiles Ácidos muy débiles Sin tendencia a disociarse en disolución acuosa Bases más fuertes débiles Bases débiles Tendencia moderada a ser protonadas en disolución acuosa+ Bases fuertes Disociadas al 100% en disolución acuosa Bases más fuertes 19
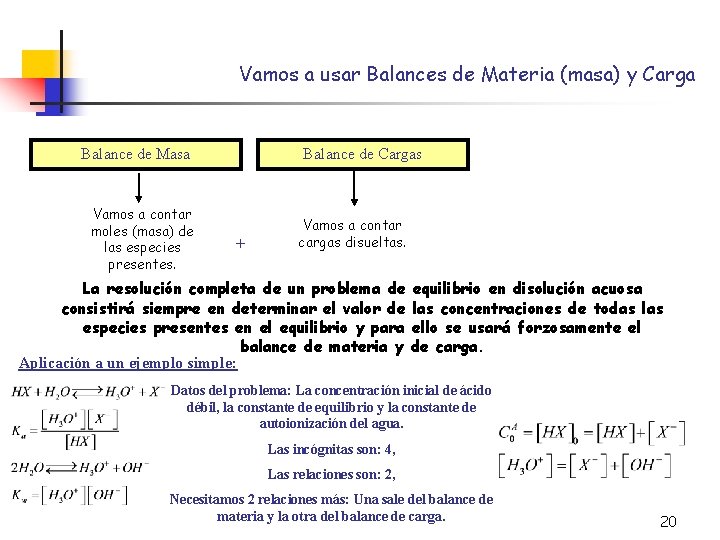
Vamos a usar Balances de Materia (masa) y Carga Balance de Masa Vamos a contar moles (masa) de las especies presentes. Balance de Cargas + Vamos a contar cargas disueltas. La resolución completa de un problema de consistirá siempre en determinar el valor de especies presentes en el equilibrio y para balance de materia y Aplicación a un ejemplo simple: equilibrio en disolución acuosa las concentraciones de todas las ello se usará forzosamente el de carga. Datos del problema: La concentración inicial de ácido débil, la constante de equilibrio y la constante de autoionización del agua. Las incógnitas son: 4, Las relaciones son: 2, Necesitamos 2 relaciones más: Una sale del balance de materia y la otra del balance de carga. 20

Propiedades ácido-base de las sales Ø Ø Ø Las sales son electrolitos fuertes que se disocian por completo para dar sus iones en agua Hidrólisis de una sal es la reacción de un anión o catión de la sal, o ambos, con el agua. La hidrólisis de una sal afecta al p. H de la disolución SALES QUE PRODUCEN DISOLUCIONES NEUTRAS: Formadas por un ion alcalino o alcalinotérreo (excepto Be 2+) y la base conjugada de un ácido fuerte (Cl , Br , NO 3 ) No sufre hidrólisis y sus disoluciones son neutras Base conjugada de un ácido muy fuerte. Sin Ej: Na. NO 3 afinidad por H+ Na. NO 3(s) Na+(ac) + NO 3 (ac) No dona ni acepta H+ Ø SALES QUE PRODUCEN DISOLUCIONES BÁSICAS: La disolución de una sal que deriva de una base fuerte y un ácido débil, es básica. P. Ej. Acetato de Sodio (CH 3 COONa) 21
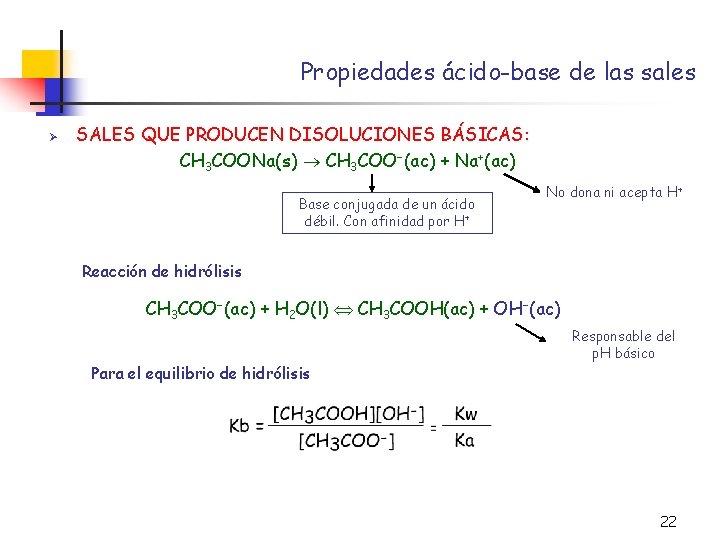
Propiedades ácido-base de las sales Ø SALES QUE PRODUCEN DISOLUCIONES BÁSICAS: CH 3 COONa(s) CH 3 COO (ac) + Na+(ac) Base conjugada de un ácido débil. Con afinidad por H+ No dona ni acepta H+ Reacción de hidrólisis CH 3 COO (ac) + H 2 O(l) CH 3 COOH(ac) + OH (ac) Para el equilibrio de hidrólisis Responsable del p. H básico 22
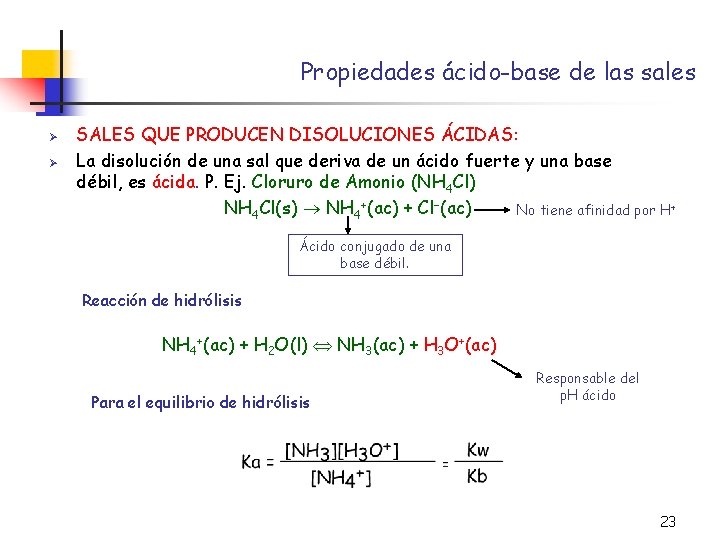
Propiedades ácido-base de las sales Ø Ø SALES QUE PRODUCEN DISOLUCIONES ÁCIDAS: La disolución de una sal que deriva de un ácido fuerte y una base débil, es ácida. P. Ej. Cloruro de Amonio (NH 4 Cl) NH 4 Cl(s) NH 4+(ac) + Cl (ac) No tiene afinidad por H+ Ácido conjugado de una base débil. Reacción de hidrólisis NH 4+(ac) + H 2 O(l) NH 3(ac) + H 3 O+(ac) Para el equilibrio de hidrólisis Responsable del p. H ácido 23

Propiedades ácido-base de las sales Ø SALES EN LAS QUE SE HIDROLIZA EL CATIÓN Y EL ANIÓN La disolución de una sal que deriva de una ácido débil y una base débil, puede ser ácida, básica o neutra. Sólo se pueden hacer predicciones cualitativas teniendo en cuenta lo siguiente: v v v Si Kb > Ka. La disolución de be ser básica, porque el anión se hidrolizará en mayor proporción que el catión. Habrá más iones OH- en el equilibrio Si Kb < Ka. La disolución de be ser ácida, porque el catión se hidrolizará en mayor proporción que el anión. Habrá más H+ en el equilibrio Si Kb = Ka. La disolución será casi neutra 24
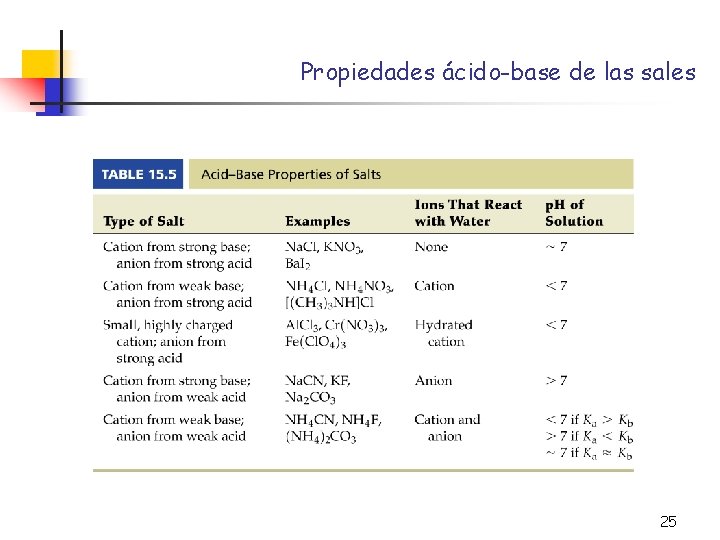
Propiedades ácido-base de las sales 25
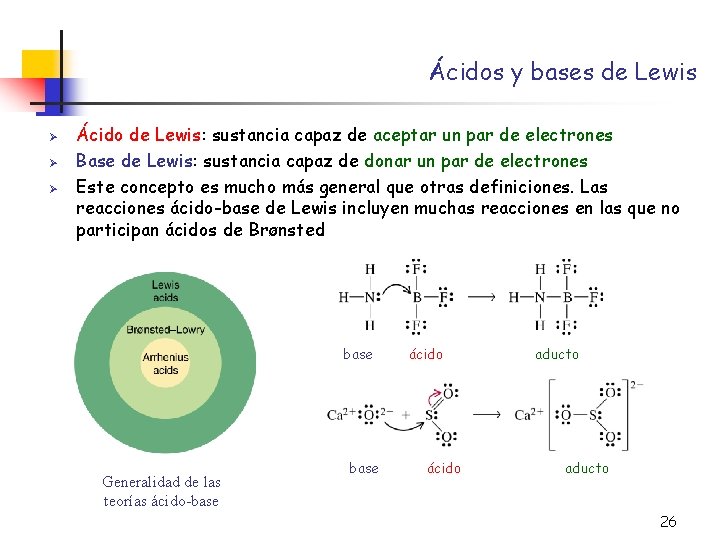
Ácidos y bases de Lewis Ø Ø Ø Ácido de Lewis: sustancia capaz de aceptar un par de electrones Base de Lewis: sustancia capaz de donar un par de electrones Este concepto es mucho más general que otras definiciones. Las reacciones ácido-base de Lewis incluyen muchas reacciones en las que no participan ácidos de Brønsted base Generalidad de las teorías ácido-base ácido aducto 26

El efecto de ion común Ø Ø El efecto de ion común es el desplazamiento del equilibrio causado por la adición de un compuesto que tiene un ion común con la sustancia disuelta. Es un caso especial del principio de Le Chatelier La presencia de un ion común suprime la ionización de un ácido débil o una base débil Ejemplo: una disolución de ácido acético y de acetato sódico Ion común CH 3 COONa(s) CH 3 COO (ac) + Na+(ac) CH 3 CO 2 H (ac)+ H 2 O(l) CH 3 COO-(ac) + H 3 O+(ac) La adición de iones acetato desplaza el equilibrio hacia la izquierda, esto es, se suprime la ionización del ácido 27

El efecto de ion común Ø p. H de un disolución formada por un ácido débil (HA) y una sal soluble del ácido (Na. A) Na. A Na+ + AHA(ac) + H 2 O(l) H 3 O+(ac) + A (ac) Ka - Ø Ø Tomando logaritmos negativos a ambos lados de la ecuación: Luego Ecuación de Henderson. Hasselbach 28
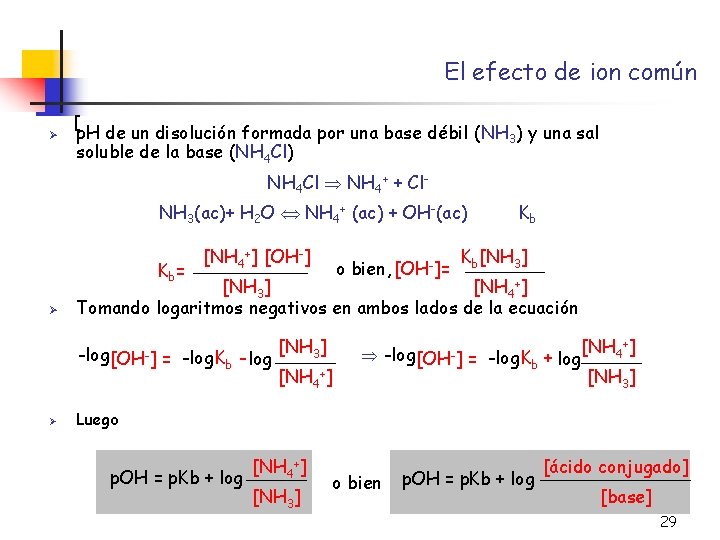
El efecto de ion común Ø [ p. H de un disolución formada por una base débil (NH 3) y una sal soluble de la base (NH 4 Cl) NH 4 Cl NH 4+ + Cl. NH 3(ac)+ H 2 O NH 4+ (ac) + OH-(ac) Kb= Ø o bien, [OH-]= Kb[NH 3] [NH 4+] Tomando logaritmos negativos en ambos lados de la ecuación -log [OH-] Ø [NH 4+] [OH-] Kb = -log Kb - log [NH 3] [NH 4 +] -log [OH-] = -log Kb + log [NH 4+] [NH 3] Luego p. OH = p. Kb + log [NH 4+] [NH 3] o bien p. OH = p. Kb + log [ácido conjugado] [base] 29
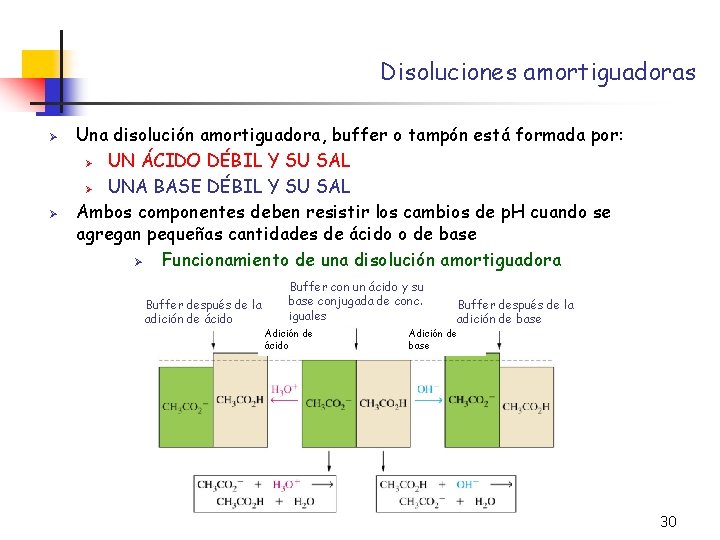
Disoluciones amortiguadoras Ø Ø Una disolución amortiguadora, buffer o tampón está formada por: Ø UN ÁCIDO DÉBIL Y SU SAL Ø UNA BASE DÉBIL Y SU SAL Ambos componentes deben resistir los cambios de p. H cuando se agregan pequeñas cantidades de ácido o de base Ø Funcionamiento de una disolución amortiguadora Buffer después de la adición de ácido Buffer con un ácido y su base conjugada de conc. iguales Adición de ácido Buffer después de la adición de base Adición de base 30

Preparación de una disolución amortiguadora de p. H específico Qué masa de Na. C 2 H 3 O 2 debe disolverse en 0. 3 L de una disolución 0. 25 M de HC 2 H 3 O 2 para producir una disolución de p. H = 5. 09? (Asumir que el volumen de la disolución permanece constante e igua a 0, 3 L) CH 3 CO 2 H + H 2 O CH 3 COO- + H 3 O+ Ka = [H 3 O+] [C 2 H 3 O 2 -] [HC 2 H 3 O 2] = 1. 8 x 10 -5 o Ka= [H 3 O+] [C 2 H 3 O 2 -] [HC 2 H 3 O 2] = 1. 8 x 10 -5 p. H = 5, 09 luego, [H 3 O+] = 10 -5, 09 = 8 x 10 -6 M [HC 2 H 3 O 2] = 0. 25 M, concentración inicial de ácido [C 2 H 3 O 2 -] = Ka Masa de C 2 H 3 O 2 - = 0. 300 L [HC 2 H 3 O 2] [H 3 O+ ] 0. 56 mol 1 L x = 1. 8 x 10 -5 0. 25 8. 1 x 10 -6 1 mol Na. C 2 H 3 O 2 1 mol C 2 H 3 O 2 = 14 g Na. C 2 H 3 O 2 - x = 0. 56 M 82. 0 g Na. C 2 H 3 O 2 1 mol Na. C 2 H 3 O 2 31 =

Introducción a las volumetrías Ø Volumetrías o Métodos volumétricos de análisis Ø “Medida del volumen de una disolución de reactivo de concentración conocida, necesario para reaccionar cuantitativamente con el analito” Las volumetrías permiten calcular la concentración desconocida de una sustancia en disolución a partir del volumen de una disolución de un reactivo de concentración conocida Ø Ø Características de las reacciones químicas empleadas en volumetrías: Ø Completas Ø Estequiometría definida Ø Rápidas no se cumple siempre Reacciones químicas empleadas en volumetrías: Ø Ácido-base Precipitación Ø Complejos Redox 32

Términos relacionados Ø Términos relacionados con las volumetrías: Ø Ø Ø Valoración: proceso de medida del volumen en una volumetría Valorante o disolución patrón: disolución de reactivo de concentración conocida Patrón primario: reactivo empleado para preparar el valorante y que cumple una serie de requisitos: Máxima pureza (>99. 9%) Peso molecular elevado Estabilidad atmosférica Ausencia de agua de hidratación Ø No higroscópico Soluble Disolución estable Fácil adquisición y precio razonable Patrón secundario: reactivo que no cumple los requisitos de un patrón primario. Su disoluciones deben ser estandarizadas frente a un patrón primario Ejemplo. Valoración de la acidez de un vinagre (CH 3 COOH) con una disolución de Na. OH, estandarizada frente a biftalato potásico 33

Volumetrias: términos relacionados Ø Bureta: instrumento para la medida del volumen 34

Volumetrías: punto de equivalencia y punto final Ø Punto de equivalencia (PE) Ø Se alcanza cuando la cantidad de valorante añadido es químicamente equivalente a la cantidad de analito presente en la muestra Resultado teórico Ø Punto final (PF) Ø Se alcanza cuando la cantidad de valorante añadido da lugar un cambio observable asociado a la condición de equivalencia Resultado real visualmente Un cambio de color debido a los propios reactivos Un cambio de color de un INDICADOR añadido a la disolución instrumentalmente (potencial A partir de la CURVA DE VALORACIÓN: un cambio en el registro de una propiedad de la disolución eléctrico, intensidad eléctrica, colorímetría) La diferencia entre PE y PF es el error en la valoración, debe ser lo menor posible 35

Volumetrías: punto de equivalencia y punto final Ø Ejemplo de valoración con cambio de color de los propios reactivos 5 (COOH)2 + 2 Mn. O 4 - 10 CO 2 + 2 Mn 2+ + 8 H 2 O Ø Ø Cantidad de analito: 40 mmoles (COOH)2 Concentración del valorante: 1 mmol Mn. O 4 -/ml El PE se alcanza cuando se han añadido 16. 0 ml de valorante El PF se alcanza cuando se la disolución del erlenmeyer cambia de incolora a la primera tonalidad morada (16. 0 ml+ 1 gota) 36
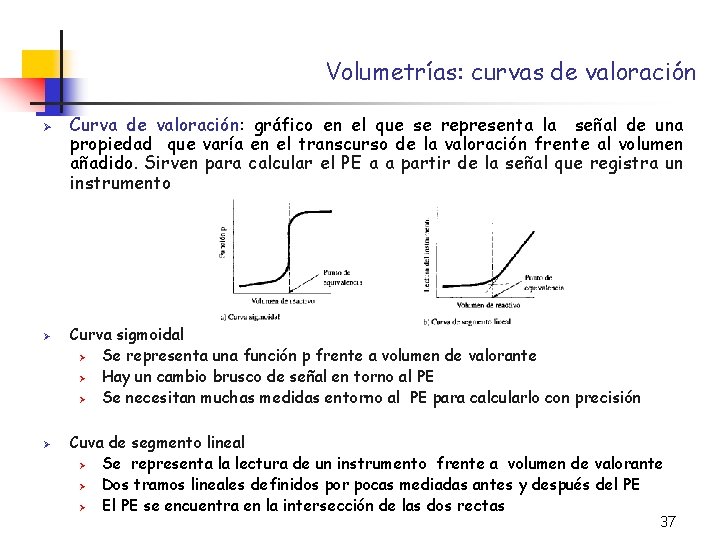
Volumetrías: curvas de valoración Ø Ø Ø Curva de valoración: gráfico en el que se representa la señal de una propiedad que varía en el transcurso de la valoración frente al volumen añadido. Sirven para calcular el PE a a partir de la señal que registra un instrumento Curva sigmoidal Ø Se representa una función p frente a volumen de valorante Ø Hay un cambio brusco de señal en torno al PE Ø Se necesitan muchas medidas entorno al PE para calcularlo con precisión Cuva de segmento lineal Ø Se representa la lectura de un instrumento frente a volumen de valorante Ø Dos tramos lineales definidos por pocas mediadas antes y después del PE Ø El PE se encuentra en la intersección de las dos rectas 37

Volumetrias: clasificación Ø Clasificación de las volumetrías: Ø Ø Volumetrías directas: adición de la cantidad exacta de valorante hasta reacción completa con el analito Volumetrías por retroceso: adición de un exceso medido de disolución patrón hasta reacción completa con el analito, y posterior valoración del exceso con un segundo reactivo valorante 38
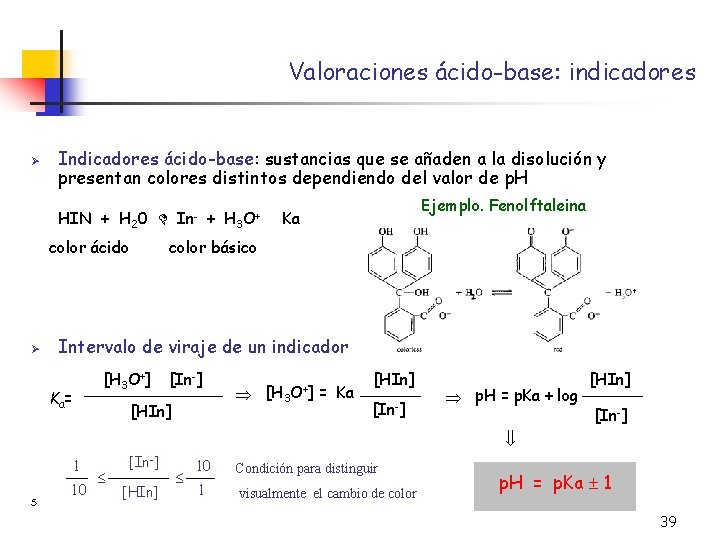
Valoraciones ácido-base: indicadores Ø Indicadores ácido-base: sustancias que se añaden a la disolución y presentan colores distintos dependiendo del valor de p. H HIN + H 20 color ácido Ø In- + H 3 O+ Ejemplo. Fenolftaleina Ka color básico Intervalo de viraje de un indicador [H 3 O+] Ka= [In-] [HIn] [H 3 O+] = Ka [HIn] [In-] p. H = p. Ka + log [HIn] [In-] 1 S 10 [In-] [HIn] 10 Condición para distinguir 1 visualmente el cambio de color p. H = p. Ka 1 39
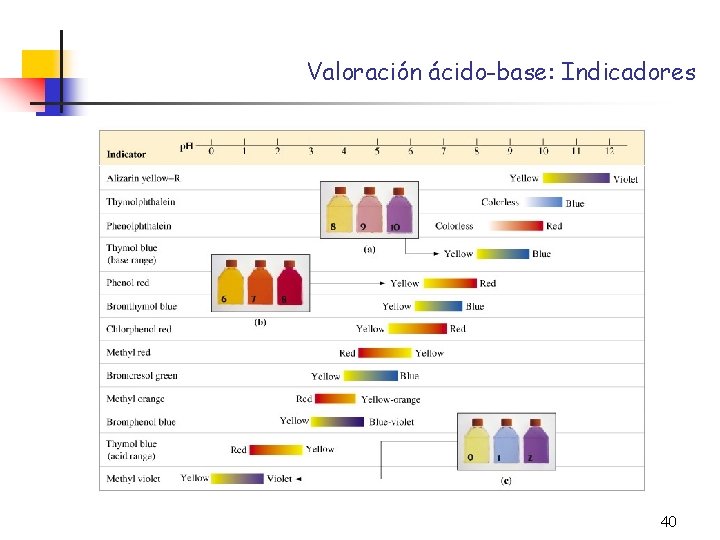
Valoración ácido-base: Indicadores 40

Valoraciones ácido-base Ø Valoración de un ácido fuerte con una base fuerte Ø Ejemplo: valoración de una disolución de HCl con otra de Na. OH HCl + Na. OH Na. Cl + H 2 O H+ + OH- H 2 O Ø Kw (reacción iónica neta) Se produce una variación de p. H a lo largo de la valoración Ø Antes del PE: disolución de p. H ácido [H+] > [OH-] Ø En el PE: el p. H es exactamente 7. 0 [H+] = [OH-] Ø Pasado el PE: disolución de p. H básico [H+] < [OH-] 41
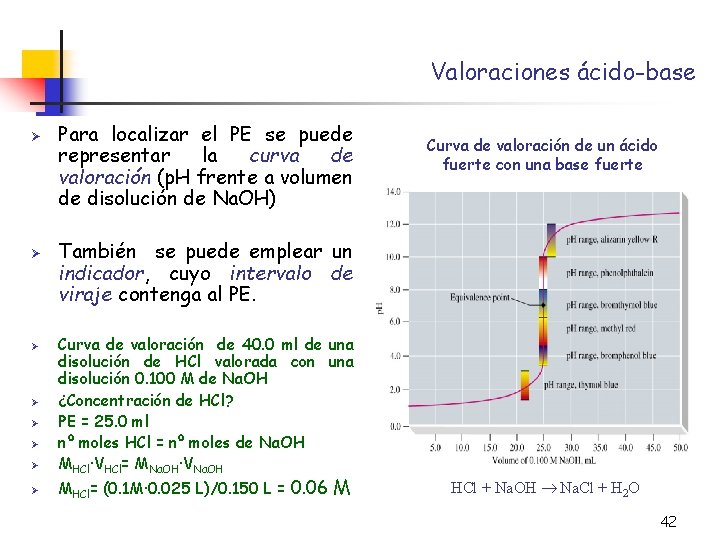
Valoraciones ácido-base Ø Ø Ø Ø Para localizar el PE se puede representar la curva de valoración (p. H frente a volumen de disolución de Na. OH) Curva de valoración de un ácido fuerte con una base fuerte También se puede emplear un indicador, cuyo intervalo de viraje contenga al PE. Curva de valoración de 40. 0 ml de una disolución de HCl valorada con una disolución 0. 100 M de Na. OH ¿Concentración de HCl? PE = 25. 0 ml nº moles HCl = nº moles de Na. OH MHCl·VHCl= MNa. OH·VNa. OH MHCl= (0. 1 M· 0. 025 L)/0. 150 L = 0. 06 M HCl + Na. OH Na. Cl + H 2 O 42

Valoraciones ácido-base Ø Valoración de un ácido débil con una base fuerte Ø Ejemplo: valoración de una disolución de CH 3 COOH con otra de Na. OH CH 3 COOH + Na. OH CH 3 COO Na + H 2 O H+ + OH- H 2 O Ø Kw (reacción iónica neta) Se produce una variación de p. H a lo largo de la valoración Ø Antes del PE: disolución de p. H ácido y luego básico [H+] > [OH-] Ø En el PE: el p. H es mayor que 7. 0 pero CH 3 COONa CH 3 COO- + Na+ CH 3 COO- + H 2 O CH 3 COOH + OH- Ø Pasado el PE: disolución de p. H básico [H+]Ac. H = [OH-]Na. OH p. H básico [H+] < [OH-] 43
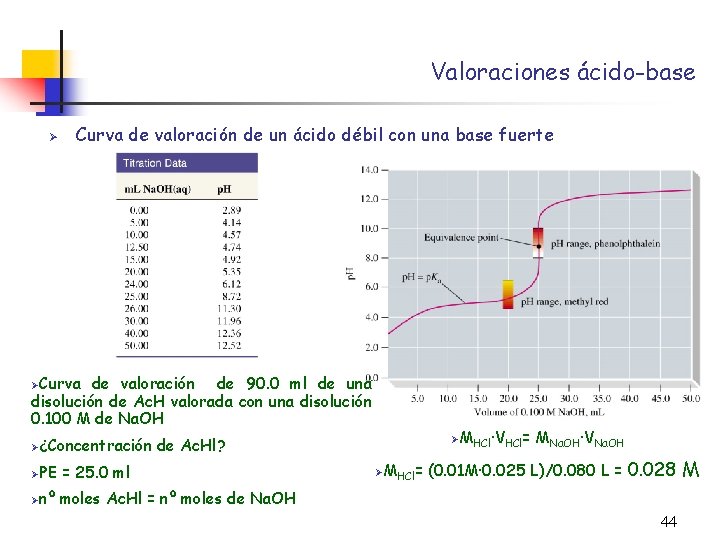
Valoraciones ácido-base Ø Curva de valoración de un ácido débil con una base fuerte ØCurva de valoración de 90. 0 ml de una disolución de Ac. H valorada con una disolución 0. 100 M de Na. OH Ø¿Concentración ØMHCl·VHCl= de Ac. Hl? ØPE = 25. 0 ml Ønº moles Ac. Hl = nº moles de Na. OH ØMHCl= MNa. OH·VNa. OH (0. 01 M· 0. 025 L)/0. 080 L = 0. 028 44 M

Las Sales poco solubles. Equilibrio de precipitación. Ø Disolución Saturada: Cuando a una determinada cantidad de disolvente se le añaden sucesivas cantidades de soluto, se llega a un punto en el que ya no se disuelve más soluto. En ese momento, la disolución está saturada: Ø Ø Depende de la temperatura. Depende de la naturaleza del soluto. Depende de la naturaleza del disolvente. Solubilidad: Es el valor de la concentración de soluto en una disolución saturada de éste. Es conveniente tener una idea sobre qué tipos de sustancias son solubles y cuáles lo son muy poco. 45

Generalización de las solubilidades. Ø Ø Ø Ø Todas las sales de Na+, K+ y NH 4+ son solubles. Todos los nitratos son solubles. Todos los cloruros son solubles a excepción del Ag. Cl, Hg 2 Cl 2, Pb. Cl 2 y Cu. Cl. Todos los sulfatos son solubles excepto el de Ca, Sr, Ba , Pb, Hg(I), Hg(II) y Ag. Todos los hidróxidos son poco solubles salvo los alcalinos, Sr(OH)2, Ba(OH)2 y NH 4 OH. Todos los carbonatos son poco solubles a excepción de los alcalinos y el de amonio. Todos los sulfuros son poco solubles, con excepción de los alcalinos, alcalino-térreos y amonio. 46

Producto de Solubilidad Ø Imaginemos que tenemos una disolución saturada de una sal del tipo An. Bm. En disolución existe el siguiente equilibrio: Ø A partir del equilibrio es posible definir: Ø El producto de solubilidad rige el equilibrio: Ø Ø Cuando el producto iónico es mayor que el Kps precipita. Cuando el producto iónico es menor que el Kps no precipita. 47

Consideraciones finales Ø Ø Ø La presencia de un ion común a los que forman la sal poco soluble, provoca la disminución de la solubilidad. Si en una disolución existen varios iones que precipitan con un ion común a todos ellos (calcio, bario, estroncio y plomo con sulfato), tiene interés el hecho de intentar precipitar cada uno de ellos de forma escalonada. Esta técnica se conoce con el nombre de precipitación fraccionada, y se emplea en el análisis químico. Si a alguno de los iones que forman parte del equilibrio de solubilidad se les hace participar en otro equilibrio, la concentración de este ion disminuye y puede hacer que se produzca la disolución del precipitado. Ø Ø Ø Formación de un ácido débil. Formación de una base débil. Por un proceso Redox Formación de un compuesto menos soluble. Formación de un complejo. 48
- Slides: 48