Le second principe de la thermodynamique 1 Ncessit














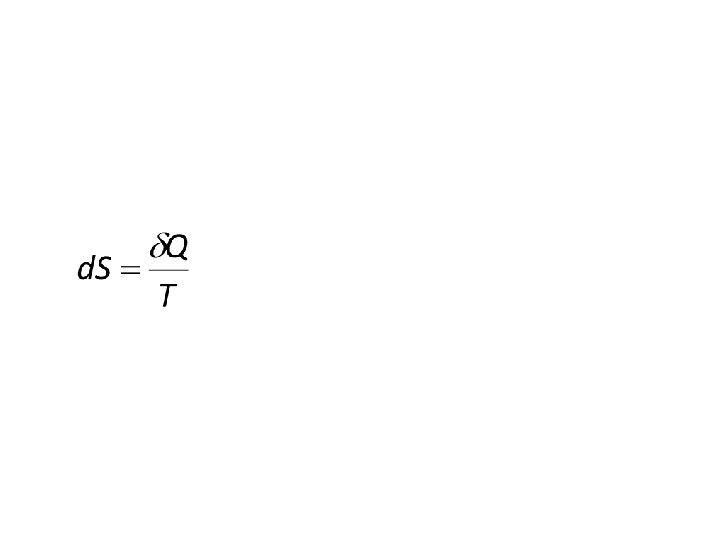






















- Slides: 43

Le second principe de la thermodynamique

1. Nécessité du second principe de la thermodynamique.

Premier principe : DU = W + Q

Premier principe : DU = W + Q Principe de conservation de l’énergie.

Premier principe : DU = W + Q Principe de conservation de l’énergie. Ne fixe pas le sens des échanges d’énergie.

Mélange de 100 g d’eau à 10 °C et de 100 g d’eau à 50 °C dans un calorimètre. Température finale : TF = 30 °C Q 1 = m 1. c. DT 1 = 0, 1*4185*(30 -10) = + 9370 J Q 2 = m 2. c. DT 2 = 0, 1*4185*(30 -50) = -9370 J DU = Q 1 +Q 2 = 0

On peut imaginer que les 100 g d’eau à 10 °C passent à 0 °C et les 100 g à 50 °C passent à 60 °C. Q 1 = m 1. c. DT 1 = 0, 1*4185*(0 -10) = - 4185 J Q 2 = m 2. c. DT 2 = 0, 1*4185*(60 -50) = +4185 J DU = Q 1 +Q 2 = 0

Les deux hypothèses vérifient le premier principe.

Il faut donc compléter le premier principe pour pouvoir rendre compte du sens des transformations (fixer le sens de la « flèche du temps » ).

2. Le second principe de la thermodynamique et la fonction entropie.

2. 1. Énoncé. À tout système fermé est associée la fonction d’état entropie S dont les variations sont données par :

Fonction définie par Clausius (1865). Je préfère emprunter aux langues anciennes les noms des quantités scientifiques importantes, afin qu'ils puissent rester les mêmes dans toutes langues vivantes; je proposerai donc d'appeler la quantité S l'entropie du corps, d'après le mot grec η τροπη une transformation. C'est à dessein que j'ai formé ce mot entropie, de manière qu'il se rapproche autant que possible du mot énergie; car ces deux quantités ont une telle analogie dans leur signification physique qu'une analogie de dénomination m'a paru utile.

d. Q : chaleur reçue par le système. Te : température de la source de chaleur. di. S, Di. S : termes positifs ou nuls.

2. 2. Commentaires et propriétés.
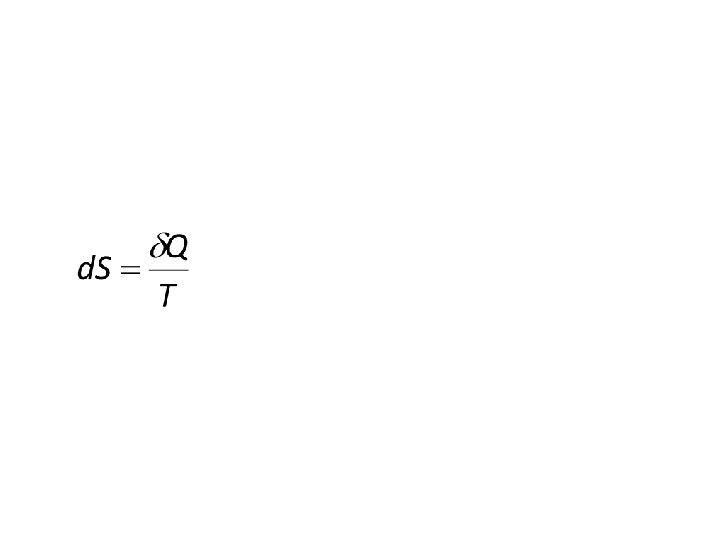

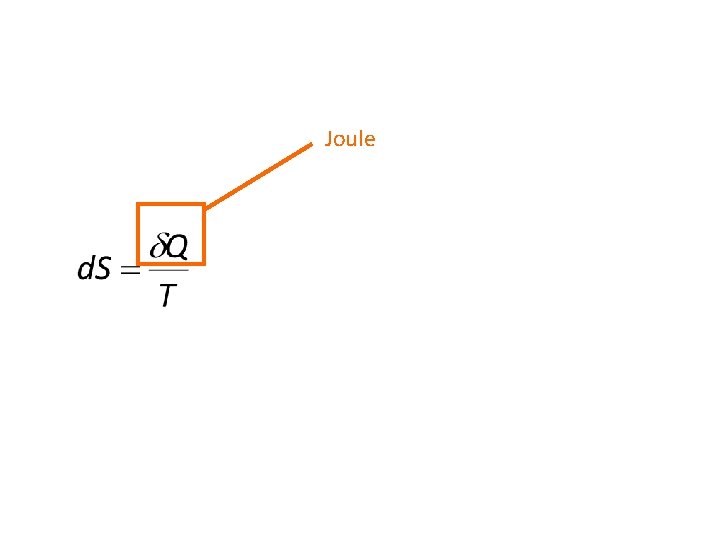
Joule

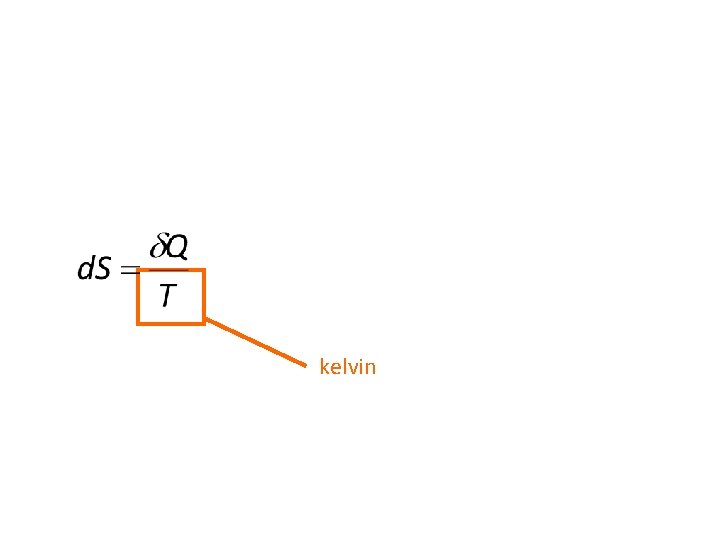
kelvin

L’entropie est en joules par kelvin (J. K-1).

Cas d’un système isolé : d. Q = 0 : pas de chaleur reçue de l’extérieur. d. S = di. S

Cas d’un système isolé : d. Q = 0 : pas de chaleur reçue de l’extérieur. d. S = di. S est positive

Cas d’un système isolé : d. Q = 0 : pas de chaleur reçue de l’extérieur. d. S = di. S est positive

Cas d’un système isolé : d. Q = 0 : pas de chaleur reçue de l’extérieur. d. S = di. S est positive L’entropie d’un système isolé ne peut qu’augmenter.

Pour l’Univers : L’entropie de l’Univers ne peut qu’augmenter.

Prévision des évolutions d’un système : Les seules transformations possibles sont celles qui font augmenter l’entropie de l’Univers.

Prévision des évolutions d’un système : Les seules transformations possibles sont celles qui font augmenter l’entropie de l’Univers. Un système cesse d’évoluer (équilibre) quand l’entropie de l’Univers n’augmente plus : d. S = 0

Transformation réversible : Une transformation réversible est une transformation infiniment lente renversable à chaque instant. On a alors : di. S = 0 Donc :

On sait donc calculer la variation d’entropie dans le cas d’une transformation réversible.

S est une fonction d’état. S est extensive : DSA+B = DSA + DSB

2. 3. Signification physique de l’entropie.

Entropie = mesure du désordre

Entropie = mesure du désordre Une transformation quelconque ne peut qu’augmenter le désordre de l’Univers.

2. 4. Principe de détermination de l’entropie. Identité thermodynamique.

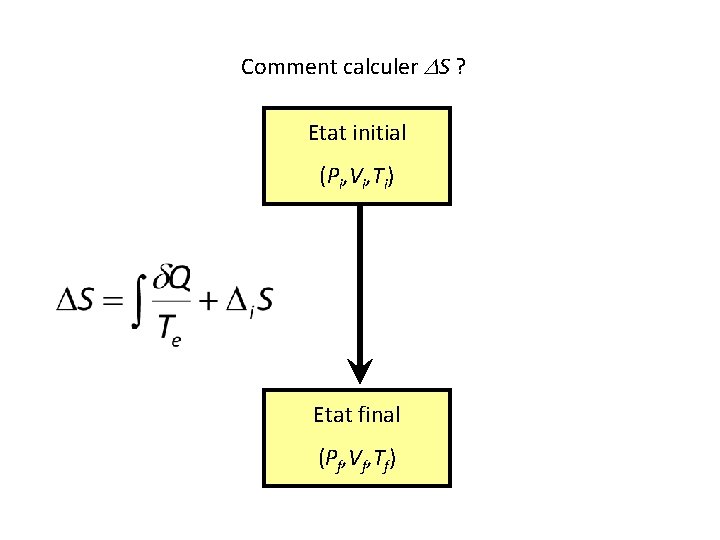
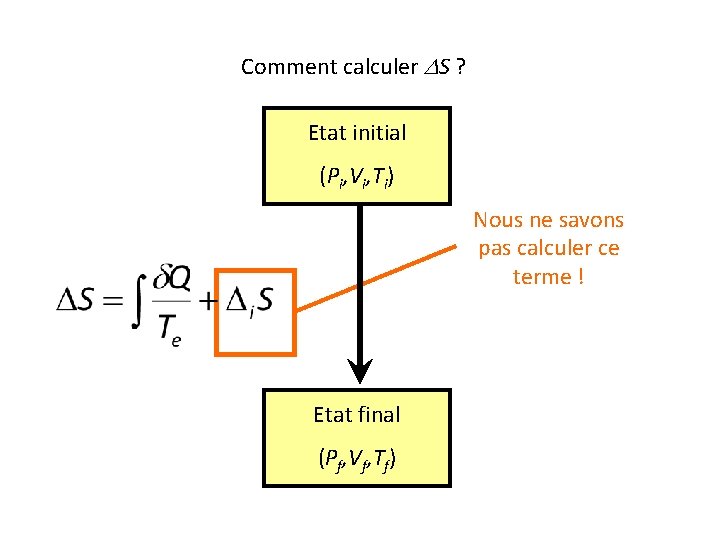
Comment calculer DS ? Etat initial (Pi, Vi, Ti) Etat final (Pf, Vf, Tf)

Comment calculer DS ? Etat initial (Pi, Vi, Ti) Nous ne savons pas calculer ce terme ! Etat final (Pf, Vf, Tf)

Mais S est une fonction d’état !

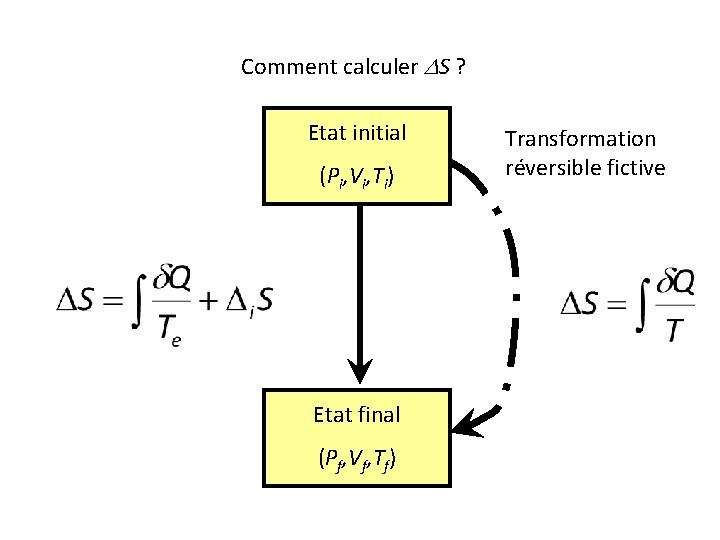
Comment calculer DS ? Etat initial (Pi, Vi, Ti) Etat final (Pf, Vf, Tf) Transformation réversible fictive

Utilisation de l’identité thermodynamique.

3. Exemple d’utilisation de l’entropie : étude du contact thermique entre deux corps.

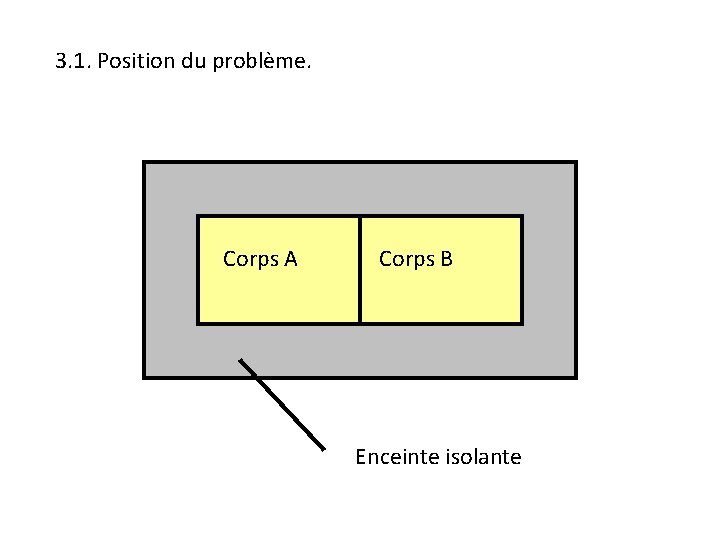
3. 1. Position du problème. Corps A Corps B Enceinte isolante

Corps A : masse m, capacité thermique c, température initiale TA. Corps B : masse m, capacité thermique c, température initiale TB.

3. 2. Sens de l’évolution.

3. 3. Variation d’entropie.

4. Entropie du gaz parfait.