Le KPS Questce quun compos ionique Rappel Cest











- Slides: 13

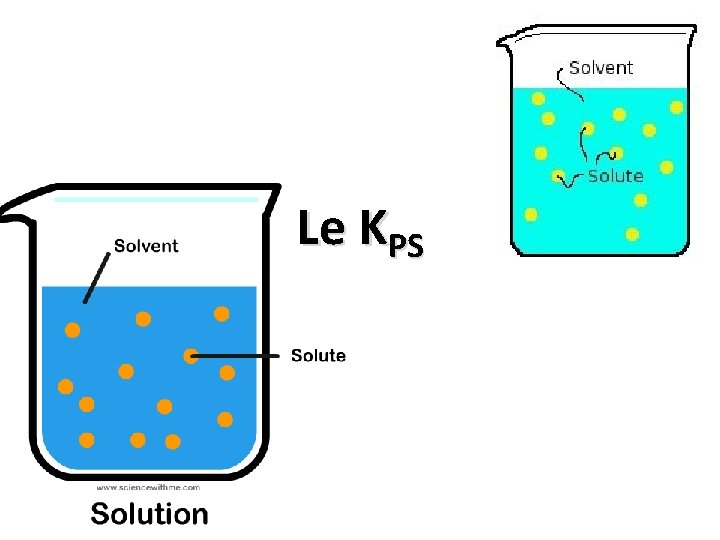
Le KPS

Qu’est-ce qu’un composé ionique? Rappel: C’est une molécule ayant 1 ou plusieurs liens ioniques entre un métal et un non-métal. Nous appelons généralement ces substances des sels, mais elles peuvent aussi être des hydroxydes métalliques (ex. hydroxyde de calcium, de magnésium, de plomb ou de fer, etc. )

Qu’est-ce que la solubilité? La solubilité d'un composé ionique ou moléculaire, appelé soluté, est la concentration maximale de ce composé que l'on peut dissoudre ou dissocier dans un solvant, à une température donnée. La solution ainsi obtenue est alors saturée (https: //www. google. ca/url? sa=t&rct=j&q=&esrc=s&source=web&cd=1&ved=0 CB 4 Qk. A 4 o. ADAA&url=http%3 A%2 F%2 Ffr. wikipedi a. org%2 Fwiki%2 FSolubilite&ei=lhl. IVZe 7 DIu. Ry. QTn 4 ICIAQ&usg=AFQj. CNE 5 Dd. Ysj. VAR 8 Zd. Wwij. ZQX 3 ha 0 oz. NA&sig 2=xlh. SN 7 qzac. Fa 1 EKFQl 9 tg&bvm=bv. 92291466, d. a. Ww) On l’exprime en g/L, en % ou en mol/L

Qu’est-ce qu’une réaction de précipitation?

Démonstrations:

ANNEXE 2: La solubilité de divers composées ioniques Souvenez-vous que tous les nitrates sont solubles et consultez cette annexe au besoin. Cahier des savoirs p. ___406____

Exemple d’applications des substances peu solubles: 1 - Stalactites et stalagmites (Ca. CO 3); 2 - Fabrication du fromage (caillette ou chymosine); 3 - Traitement des eaux (ajout de coagulants= sulfate d’aluminium et sulfate de fer pour coagulation et stabilisation du p. H); 4 - Les «pierres aux reins» (calculs rénaux = Ca. C 2 O 4 ou oxalate de calcium); 5 - En connaissez-vous d’autres?

La constante du produit de solubilité Pour les substances peu solubles, on utilise la «constante du produit de solubilité» , le KPS. Selon l’équation suivantes: Xn. Ym(s) ↔ n. X+(aq) + m. Y-(aq) KPS = [X+]n·[Y-]m

Écrire l’équation de dissociation et le KPS de certaines réactions: p. 383 #1

La solubilité molaire du solide à dissoudre (s): Ici, avec les KPS, on ne tient pas toujours compte des ions dissouts, mais seulement de la concentration de la substance dissoute. ENRICHISSEMENT: Comme on fait un «essai» , on calcule «Q» . Puis on essaie de voir si la solution est: saturée (Q = KPS); insaturée (Q KPS); ou si le point de saturation a été dépassé (Q KPS). S = la concentration du solide qui se trouve en solution.

Exercices p. 383 à 386 #2 à 6

Exercices p. 389 à 394 #1 à 10

Exercices défis ++ p. 395 à 398 #1 à 5