Le Alterazioni del Protidogramma Bibbiena 17 04 2010

Le Alterazioni del Protidogramma Bibbiena , 17 -04 -2010 Dr. Stefano Gambineri
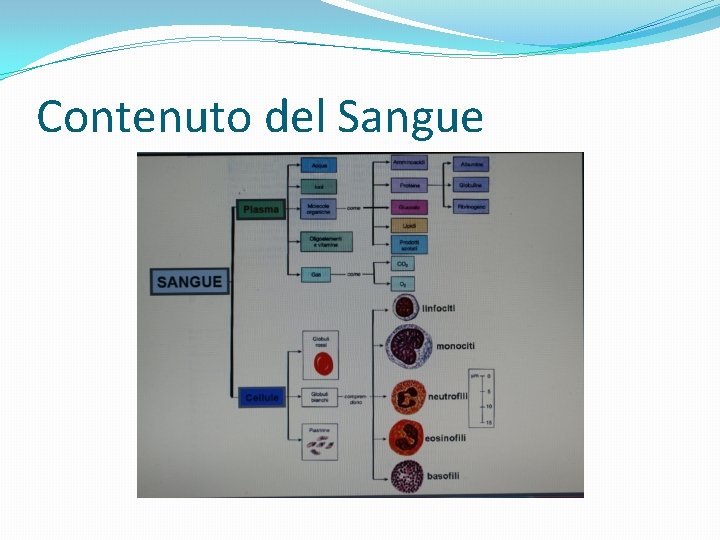
Contenuto del Sangue

Proteine Plasmatiche Classificazione

Le Proteine Plasmatiche Funzioni

Proteine plasmatiche e quadro proteico elettroforetico � V. N. 6 -8 g/dl 8, 3 g/dl �Albumine �Alfa 1 globuline �Alfa 2 globuline �Beta globuline �Gamma globuline 6, 63, 6 -4, 9 g/dl 55 -64% 55, 1 -65, 7% 0, 2 -0, 4 g/dl 4, 2 -7, 2% 3, 1 -5, 6% 0, 4 -0, 8 g/dl 7 -9% 8 -12, 7% 0, 6 -1 g/dl 9 -13% 8 -13, 30% 0, 9 -1, 4 g/dl 13 -21% 10, 3 -18, 8% �A/G 1, 2 -1, 7

Elettroforesi delle proteine e scansione Densitometrica

Archi e linee di precipitazione nella Immunoelettroforesi

Proteine totali. Aumento e Diminuzione. � Aumento : emoconcentrazione, gammopatie mono e policlonali. � Diminuzione : � Insufficiente apporto � Digiuno prolungato, dieta ipoproteica. � Ridotto assorbimento � Vomito, diarrea, s. da malassorbimento � Perdita � S. nefrosica, enteropatie, ustioni estese, emorragie � Ridotta sintesi � Epatopatie acute e croniche � Ipercatabolismo � Ipertiroidismo, febbre, infez. acute, traumi, interventi chirugici, neoplasie � Emodiluizione � Emorragie profuse, scompenso cardiaco congestizio, terapie idratanti

Albumina �E’ una proteina di PM 65. 000 D che costituisce la frazione sieroproteica + abbondante. Le sue funzioni sono essenzialmente di mantenimento della P osmotica del sangue e di trasporto di acidi grassi, bilirubina, ormoni e farmaci. L’ ipoalbuminemia è responsabile di ipoproteinemia, costituendo da sola il 60% delle proteine plasmatiche.
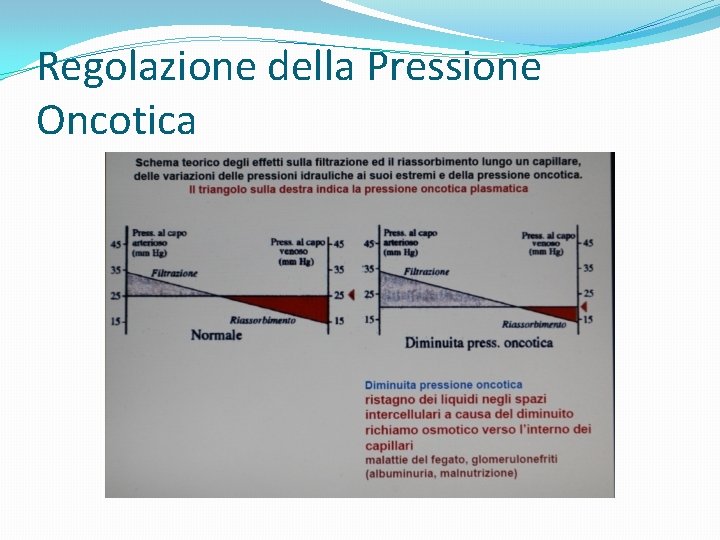
Regolazione della Pressione Oncotica

Albumina. Aumento e diminuzione. �Aumento : Emoconcentrazione ( Diarrea, vomito, sudorazione ); infusione di albumina. �Diminuzione : vedi cause di diminuzione delle proteine totali

Indicazioni al trattamento con Albumina �Shock ipovolemico, ma in seconda scelta se vi sono controindicazioni e non responsività ai cristalloidi e plasma expanders vari �Ustioni con grave proteinodispersione ad es. per ustioni > 50% del corpo ( Come sopra ) �Cirrosi epatica : nelle asciti dopo paracentesi evacuativa ( per es. 4 l ); se il paziente non risponde a terapia diuretica per es. per iponatriemia �Peritonite batterica spontanea insieme ad atb �Plasmaferesi �Emorragia subaracnoidea in caso di vasospasmo sintomatico �Iperbilirubinemia del neonato �Enteropatie proteinodisperdenti o malnutrizione : se il tasso è < 2 gr/dl, se c’ è diarrea grave.

Albumina prescrizione a carico del SSN. �La prescrizione di Albumina a carico del SSN, su diagnosi e PT di strutture specialistiche delle Aziende Sanitarie, è limitata alle seguenti condizioni: �Dopo paracentesi evacuativa a largo volume nella Cirrosi Epatica �Grave ritenzione idrosalina nella Cirrosi ascitica, nella sindrome nefrosica o nelle sindromi da malassorbimento ( Ad. Es. intestino corto post-chirurgico o da proteinodispersione ), non responsiva a un trattamento diuretico appropriato, specie se associata ad ipoalbuminemia ed in particolare a segni clinici di ipovolemia

Alfa 1 Globuline. Aumento Diminuzione. �Alfa 1 antitripsina ( Anti Proteasi come at III), alfa 1 glicoproteina acida ( Mucoproteine ), alfa 1 fetoproteina ( Gravid. Ed estroprog. , Marker epatok. e tumori germinali ), alfa 1 lipoproteina �Aumento : gravidanza, terapia contraccettiva, malattie infettive, malattie infiammatorie croniche, necrosi tissutale ( Infarto miocardico , neoplasie ) �Diminuzione : carenzacongenita di alfa 1 antitripsina, sclerodermia, sindrome nefrosica

Alfa 2 globuline. Aumento e diminuzione. �Alfa 2 macroglobulina (Antiproteasi, trasporto insulina e GH ), Aptoglobina ( Lega l’ Hgb in corso di emolisi ), Antitrombina III, Protrombina, Ceruloplasmina, Colinesterasi ( Indice di attività protidosintetica epatica > sensibil. ai narcotici mediante N° di dibucaina), pre-beta lipoproteine , alcune Ig. A �Aumento : infezioni acute batteriche, traumi, interv. chirurgici, s. nefrosica, necrosi tissutale, epatopatie croniche, DM, collagenopatie, M. di Hodgkin, Sarcoidosi, S. di Down ( alfa 2 macroglobulina ) �Diminuzione : alcune collagenopatie, epatite virale, pancreatite, DM

Beta globuline. Aumento e diminuzione. �Molti laboratori separano frazioni beta 1 e beta 2 ( Non differenze concettuali dal punto di vista interpretativo ) �Transferrina, C 3, emopessina ( Lega il gruppo EME liberato dalla Hgb dopo ossidazione ), pcr, beta 2 microglobulina ( Espressione di turn-over cellulare), beta-lipoproteine, alcune Ig. M �Aumento: gravidanza, beta-disliproteinemie primitive e secondarie, cirrosi epatica ( Fusione beta-gamma ), s. nefrosica, macroglobulinemia �Diminuzione : a-betalipoproteinemia congenita, atransferrinemia congenita, enteropatie essudative

Quadro elettroforetico di Sindrome Nefrosica
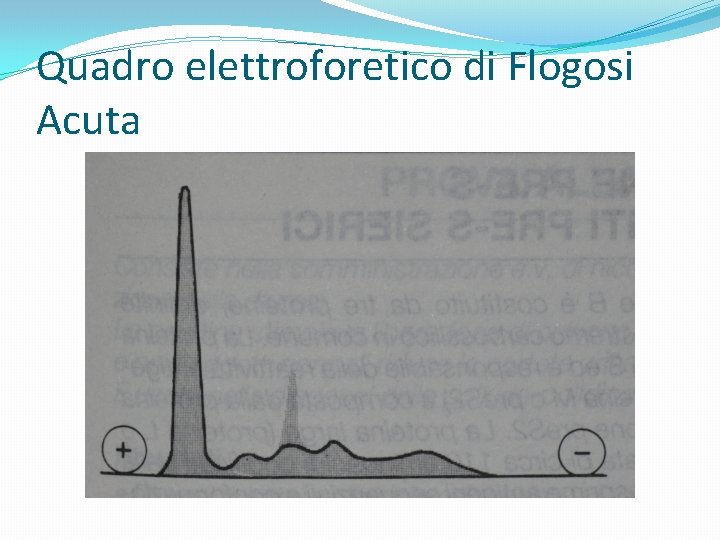
Quadro elettroforetico di Flogosi Acuta
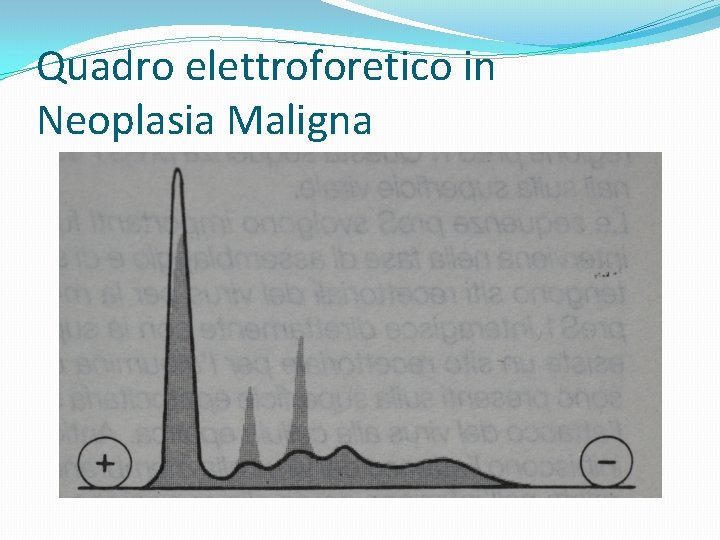
Quadro elettroforetico in Neoplasia Maligna

Immunoglobuline �Sono formate da 4 subunità polipeptidiche , 2 catene pesanti e 2 catene leggere legate tra loro con legame disolfuro; le catene pesanti sono di 5 tipi principali cui corrispondono altrettante classi di Ig ( G, M, D, A, E ). Le catene leggere sono di 2 tipi, kappa o lambda, però ciascuna Ig è formata da una sola classe di esse ( Ig di tipo kappa o di tipo lambda)

Struttura delle Immunoglobuline 2

Gamma globuline. Aumento e diminuzione. �Aumento. Policlonale : epatopatie croniche. , infezioni batteriche, collagenopatie e m. autoimmuni, sarcoidosi, neoplasie, tossicodipendenza. �Monoclonale : MGUS, gammopatie monoclonali �Diminuzione : malnutrizione, ipogammaglobulinemie congenite, sindrome nefrosica, enteropatia protidodisperdente, ustioni, terapia immunosoppressiva, giardiasi ( Diminuzione di Ig. A, Ig. M e livelli variabili di Ig. G )
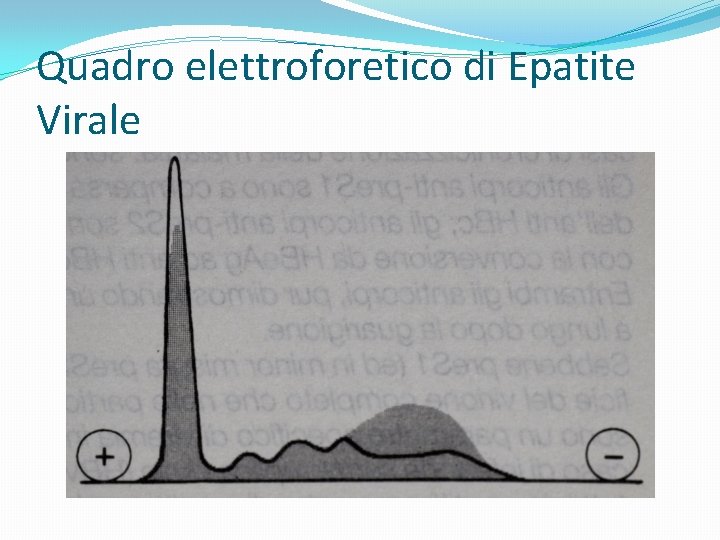
Quadro elettroforetico di Epatite Virale
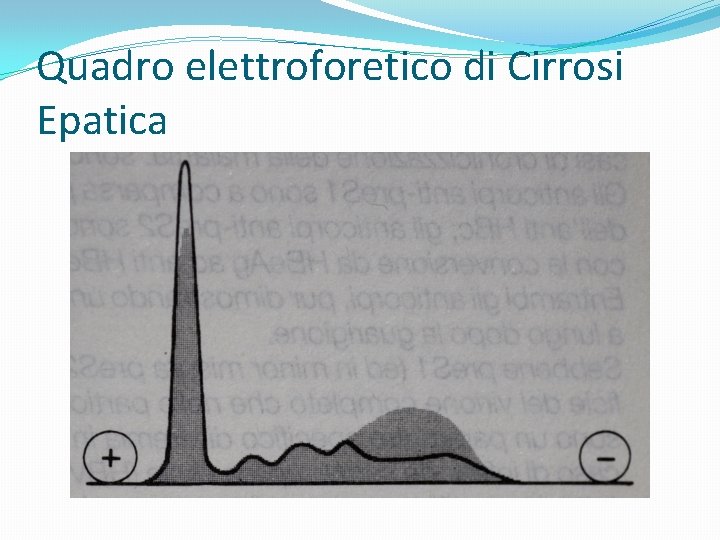
Quadro elettroforetico di Cirrosi Epatica
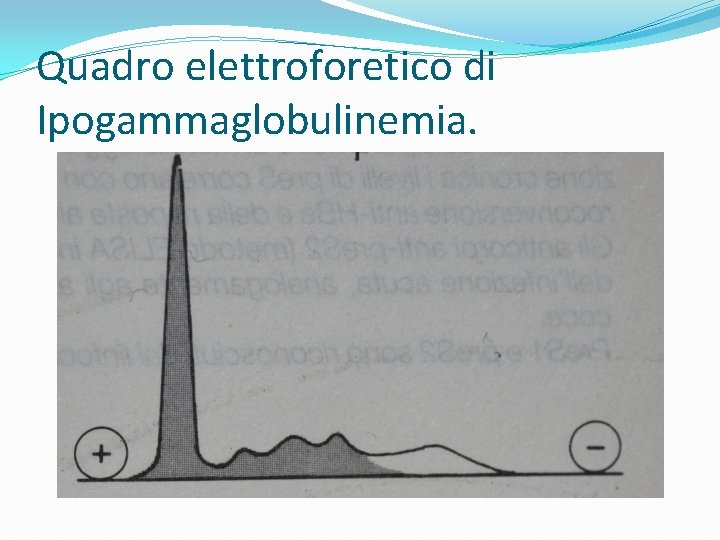
Quadro elettroforetico di Ipogammaglobulinemia.

Gammopatie Monoclonali ( Aumento di un solo tipo di Ig caratterizzata da un unico tipo di catena leggera - kappa o lambda- ) �Forme clinicamente occulte. MGUS : gammopatie monocl. benigne ; associate a infiammazioni o infezioni croniche , leucosi , sarcoma di Kaposi e AIDS, tumori intestinali, del tratto biliare, della mammella, polineuropatie idiopatiche, a lipodistrofie tipo M. di Gaucher. �Gammopatie monoclonali transitorie : associate a trattamento con farmaci ( Idantoina, sulfonamidi, immunodepressori ) ; assoc. a infezioni virali; assoc. a protesi valvolari cardiache

. Gammopatie Monoclonali Forme clinicamente manifeste dovute alla proliferazione del clone neoplastico: MM; leucemia plasmacellulare; macroglobulinemia di Waldenstrom ; malattie delle catene pesanti. Forme clinicamente manifeste dovute agli effetti patologici delle componenti monoclonali. Malattia cronica da Crioagglutinine ; amiloidosi ; sindrome di Fanconi dell’ adulto ; polineuropatie ; Lichen myxedematosus.

MGUS ( Monoclonal Gammopathy of Undetermined Significance ) Diagnosi �Presenza di proteina serica monoclonale ( Proteina M, o Ig. G, o Ig. A, o Ig. M) ad una concentrazione < rispett. a 3 gr/d. L, 2 gr/d. L, 1 gr/d. L �Numero di Plasmacellule <10% nel midollo osseo �Assenza o piccola presenza di proteine M nelle urine ( Proteinuria di Bence Jones ) �Assenza di lesioni ossee litiche, anemia, ipercalcemia ed insuff. Renale �Proteina M stabile nel tempo �Esclusione di disordini proliferativi di beta-cellule �Circa il 25% delle MGUS evolve in MM entro 10 aa dalla diagnosi �La parte più cospicua è espressione del fisiol. invecchiamento del sist. immunitario con indebolimento del controllo T sulla proliferazione B HP(? )

Quadro elettroforetico di Gammopatia Monoclonale.
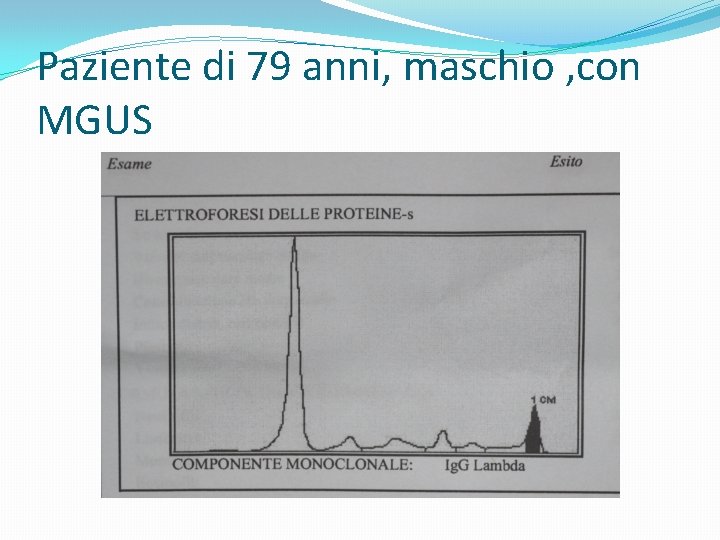
Paziente di 79 anni, maschio , con MGUS
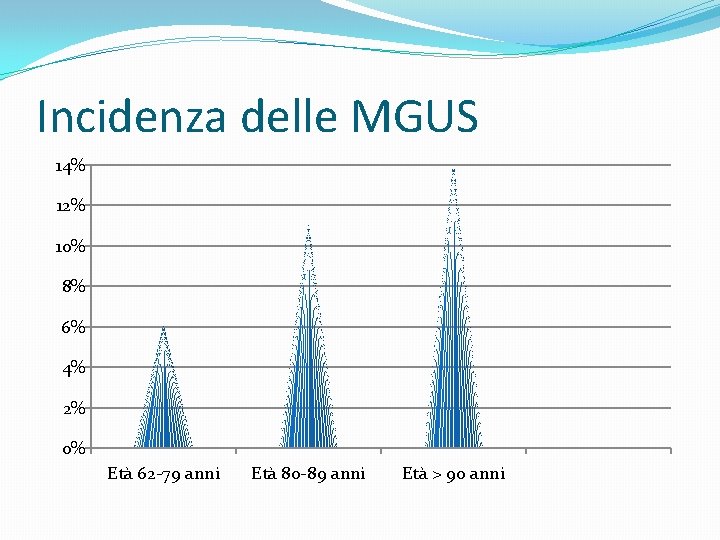
Incidenza delle MGUS 14% 12% 10% 8% 6% 4% 2% 0% Età 62 -79 anni Età 80 -89 anni Età > 90 anni
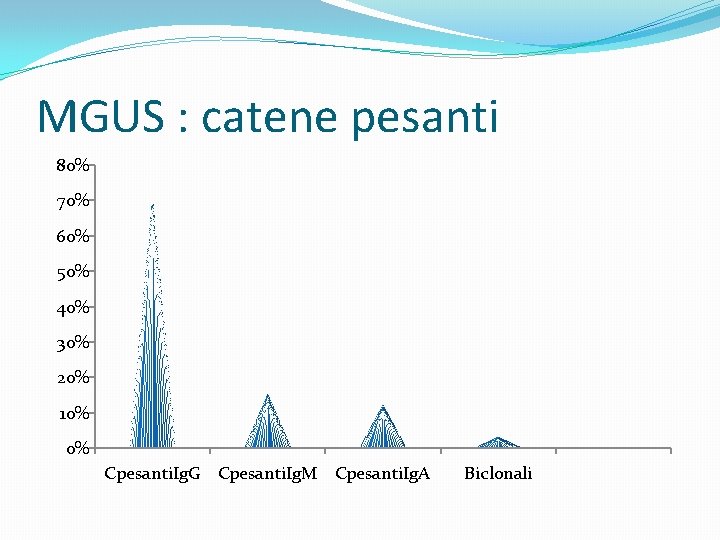
MGUS : catene pesanti 80% 70% 60% 50% 40% 30% 20% 10% 0% Cpesanti. Ig. G Cpesanti. Ig. M Cpesanti. Ig. A Biclonali

MGUS Catene leggere 70% 60% 50% 40% 30% 20% 10% 0% Cat. Kappa Cat. Lambda Cat. u kappa Cat. ulambda

Mieloma Multiplo incidenza �Incidenza annua 4 per 100. 000 �Costituisce l’ 1% di tutte le neoplasie maligne nella razza bianca , il 2% nella razza nera �Costituisce il 13% di tutte le neoplasie ematologiche �Inizia sempre come MGUS (? )
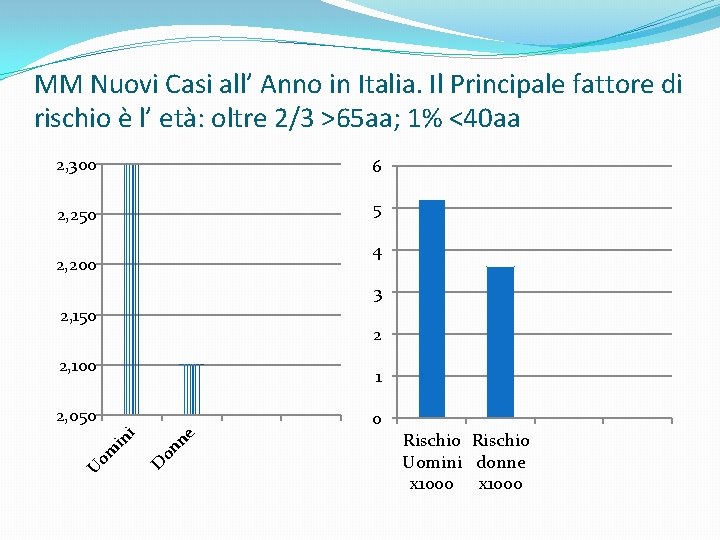
MM Nuovi Casi all’ Anno in Italia. Il Principale fattore di rischio è l’ età: oltre 2/3 >65 aa; 1% <40 aa 2, 300 6 2, 250 5 4 2, 200 3 2, 150 2 2, 100 1 2, 050 on D U om in i ne 0 Rischio Uomini donne x 1000

Mieloma Multiplo : tipologie �Mieloma Multiplo “ Classico “ �Mieloma Micromolecolare ( Le plasmacellule producono solo catene leggere ) 20% dei Mielomi �Mieloma non secernente ( Le Plasmacellule non producono Ig ma sono presenti in numero eccessivo ) �Plasmocitoma Solitario ( Unica localizzazione in un osso o a livello extramidollare ) �Leucemia Plasmacellulare ( Le plasmacellule sono elevate anche nel sangue ) �Mieloma Indolente ( Malattia asintomatica senza lesioni a carico di ossa o altri organi ) “ Smouldering “

Mieloma Multiplo : presentazione clinica �Anemia ( Normocromica e normocitica ) �Epistassi �Minore resistenza alle infezioni �Ipercalcemia �Dolore a carico di vari distretti osteoarticolari �Sintomi da Iperviscosità : confusione, annebbiamento della vista, vertigine �Insufficienza renale
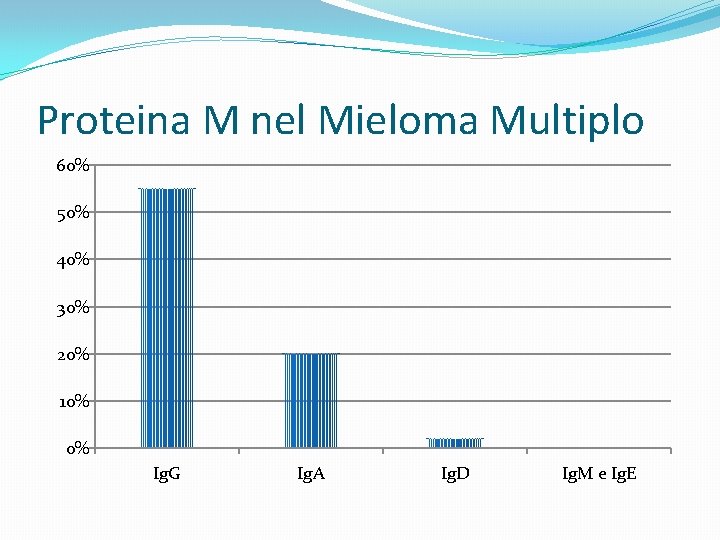
Proteina M nel Mieloma Multiplo 60% 50% 40% 30% 20% 10% 0% Ig. G Ig. A Ig. D Ig. M e Ig. E

Percentuali MM
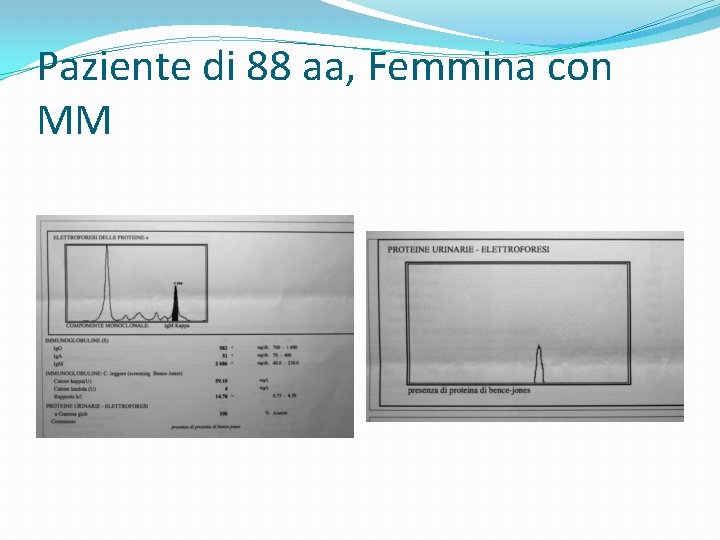
Paziente di 88 aa, Femmina con MM

Criteri Diagnostici del MM

DD tra MGUS e MM �Il modo migliore per differenziare le due patologie è la determinazione seriata della proteina M nel siero e la periodica rivalutazione dei parametri clinici e di laboratorio pertinenti ( Anche beta 2 microglobulina ) �Il razionale della diagnosi e del Follow-up dei pazienti con MGUS è la possibile progressione neoplastica �Frequenza di monitoraggio della proteina M : Ig monoclonale <20 g/L 6 mesi dopo il I° riscontro e, se stabile, annualmente. Ig monoclonale >20 gr/L da 3 a 6 mesi dopo il primo riscontro e , se stabile, ogni 6 -12 mesi �Le MGUS Ig. G o Ig. A tendono a progredire in MM o amiloidosi primaria o in discrasie plasmacellulari; le MGUS Ig. M tendono a progredire in disordini linfoproliferativi ( Linfoma di Hodgkin, LLc, Macroglobulinemia di Waldestrom)
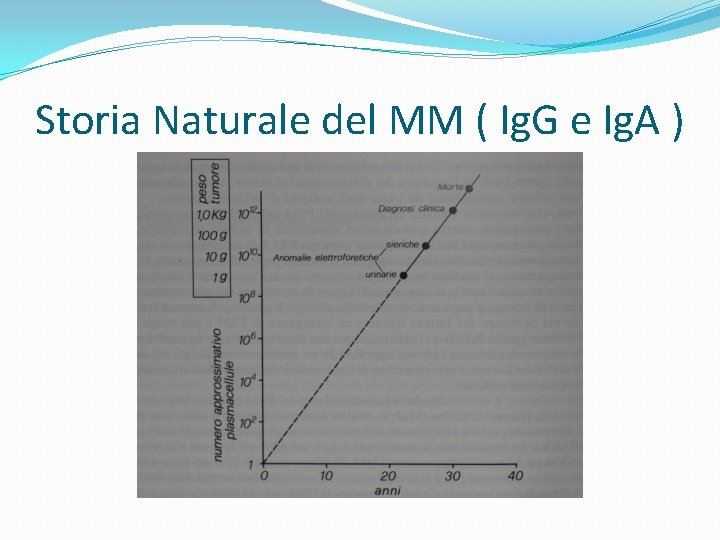
Storia Naturale del MM ( Ig. G e Ig. A )

MM : Prognosi �Il 10% dei MM ha un decorso torpido, una progress. molto lenta , si trattano solo quando la proteina mielomatosa > 5 gr/dl o si presentano lesioni ossee progressive �La maggior parte dei MM richiede un intervento terapeutico sia Antitumorale che di Supporto; i pazienti spesso rispondono alla terapia ma la durata della risposta progressivamente diminuisce �Il 15% dei paz. muore entro pochi mesi dalla diagnosi poi la mortalità si attesta attorno al 15% per anno

MM Terapia �Cicli intermittenti di agenti alchilanti ( Melphalan, Ciclofosfamide, Clorambucil ) + Prednisone �Nuovi farmaci : Talidomide, Lenalinomide, Bortezomib �Radioterapia �Trapianto di cellule staminali autologhe o eterologhe �Terapia di supporto : bifosfonati, eritropoietina, plasmaferesi etc.

Indicazioni per la richiesta di Elettroforesi Sieroproteica (SIBio. C 2008) �Valutazione dell’ Albumina (? ) �Valutazione del deficit di alfa 1 -antitripsina (? ) �Evidenza-monitoraggio di una condizione di flogosi (? ) �Evidenza-monitoraggio di condizioni di ipoipergammaglobulinemia (? ) �Rilevazione delle componenti monoclonali ( > 50 aa ) �Monitoraggio dei pazienti con trapianto d’ organo e con neuropatia periferica demielinizzante �Monitoraggio delle componenti monoclonali , la determinazione della loro concentrazione e tipo soddisfano i criteri per la definizione di Marker Tumorale ideale.
- Slides: 46