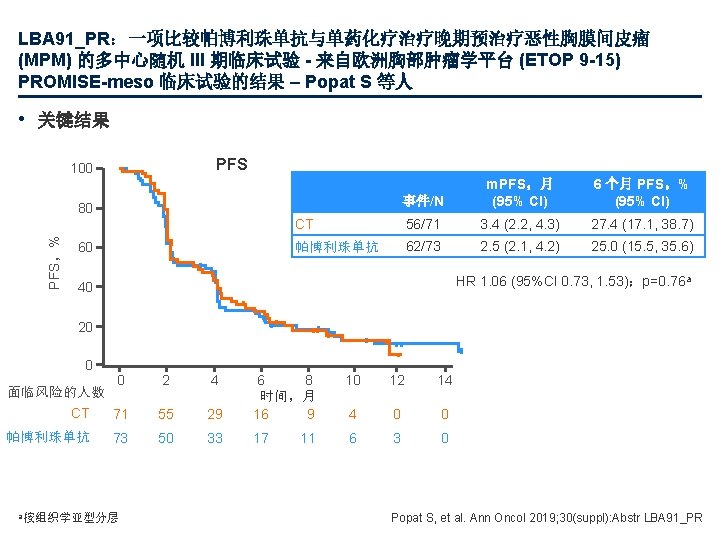
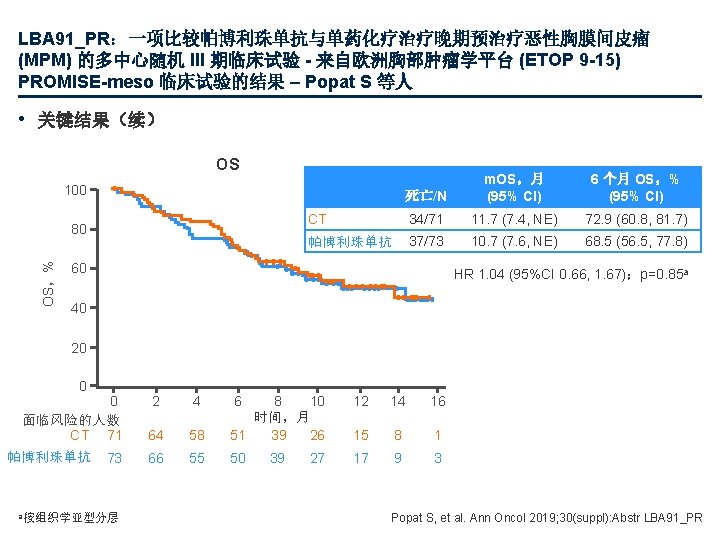
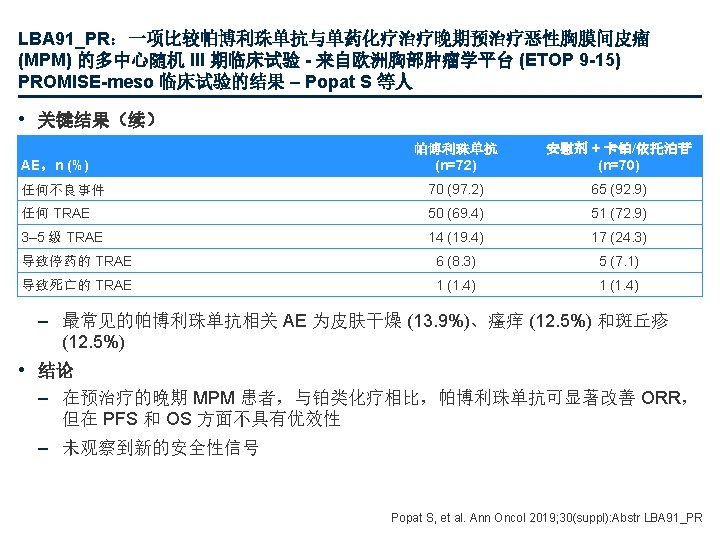
LBA 17 NSCLC GarridoMartin EM 100 TMB TML






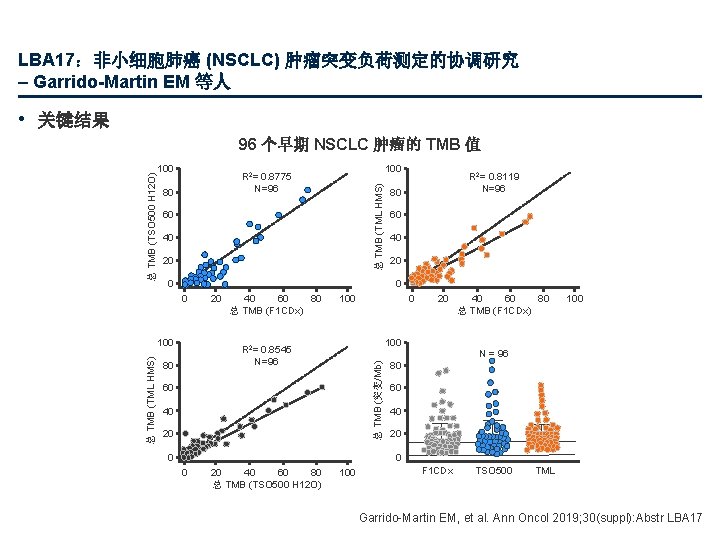
LBA 17:非小细胞肺癌 (NSCLC) 肿瘤突变负荷测定的协调研究 – Garrido-Martin EM 等人 • 关键结果 100 总 TMB (TML HMS) 80 60 40 20 0 R 2= 0. 8119 N=96 80 60 40 20 0 0 100 总 TMB (TML HMS) 100 R 2= 0. 8775 N=96 20 80 40 60 总 TMB (F 1 CDx) 100 20 100 R 2= 0. 8545 N=96 80 0 总 TMB (突变/Mb) 总 TMB (TSO 500 H 12 O) 96 个早期 NSCLC 肿瘤的 TMB 值 60 40 20 80 40 60 总 TMB (F 1 CDx) 100 N = 96 80 60 40 20 0 80 20 60 40 总 TMB (TSO 500 H 12 O) 100 F 1 CDx TSO 500 TML Garrido-Martin EM, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 17


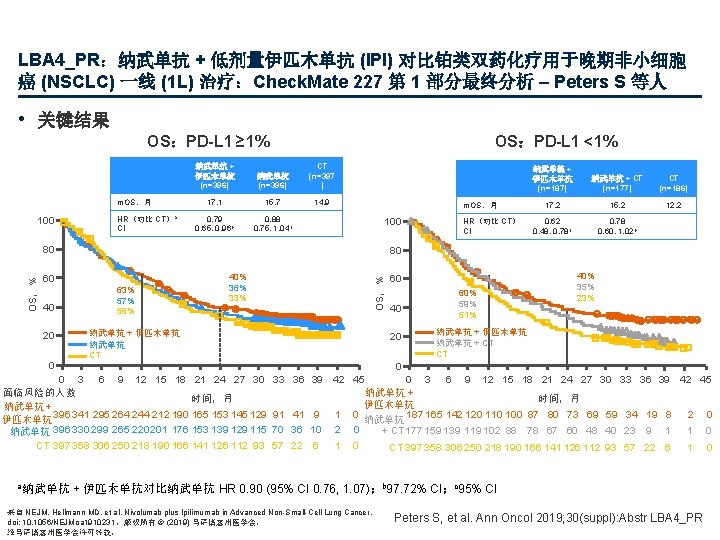
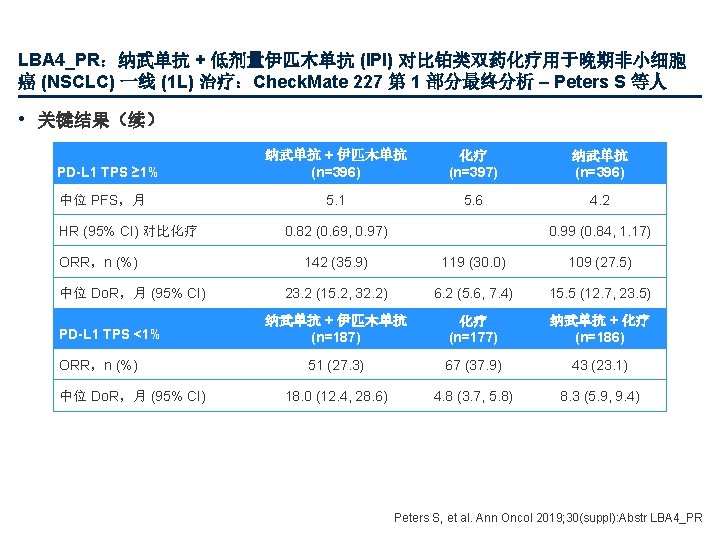
LBA 4_PR:纳武单抗 + 低剂量伊匹木单抗 (IPI) 对比铂类双药化疗用于晚期非小细胞 癌 (NSCLC) 一线 (1 L) 治疗:Check. Mate 227 第 1 部分最终分析 – Peters S 等人 • 关键结果 OS:PD-L 1 ≥ 1% m. OS,月 100 HR(对比 CI CT)a OS:PD-L 1 <1% 纳武单抗 + 伊匹木单抗 (n=396) 纳武单抗 (n=396) CT (n=397 ) 17. 1 15. 7 14. 9 0. 79 0. 65, 0. 96 b 0. 88 0. 75, 1. 04 c m. OS,月 100 60 40 20 0 63% 57% 56% 40% 36% 33% 纳武单抗 + 伊匹木单抗 纳武单抗 CT CT (n=186) 17. 2 15. 2 12. 2 0. 62 0. 48, 0. 78 c 0. 78 0. 60, 1. 02 b 40% 35% 23% 60 60% 59% 51% 40 纳武单抗 + 伊匹木单抗 纳武单抗 + CT CT 20 0 0 3 6 9 12 15 18 21 24 27 30 面临风险的人数 时间,月 纳武单抗 + 伊匹木单抗 396 341 295 264 244 212 190 165 153 145 129 纳武单抗 396 330 299 265 220201 176 153 139 129 115 CT 397 358 306 250 218 190 166 141 126 112 93 a纳武单抗 + CT (n=177) 80 OS,% 80 HR(对比 CT) CI 纳武单抗 + 伊匹木单抗 (n=187) 33 36 39 42 45 0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 91 41 9 70 36 10 1 2 纳武单抗 + 时间,月 伊匹木单抗 0 纳武单抗 187 165 142 120 110 100 87 80 73 69 59 34 19 8 0 + CT 177 159 139 119 102 88 78 67 60 48 40 23 9 1 57 22 6 1 0 CT 397 358 306 250 218 190 166 141 126 112 93 57 22 6 2 0 1 0 + 伊匹木单抗对比纳武单抗 HR 0. 90 (95% CI 0. 76, 1. 07);b 97. 72% CI;c 95% CI 来自 NEJM, Hellmann MD, et al, Nivolumab plus Ipilimumab in Advanced Non-Small-Cell Lung Cancer, doi: 10. 1056/NEJMoa 1910231 。版权所有 © (2019) 马萨诸塞州医学会。 经马萨诸塞州医学会许可转载。 Peters S, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 4_PR
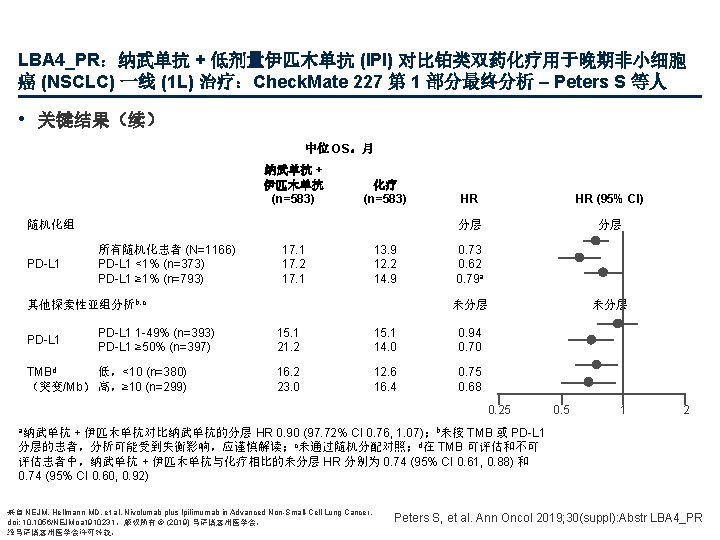
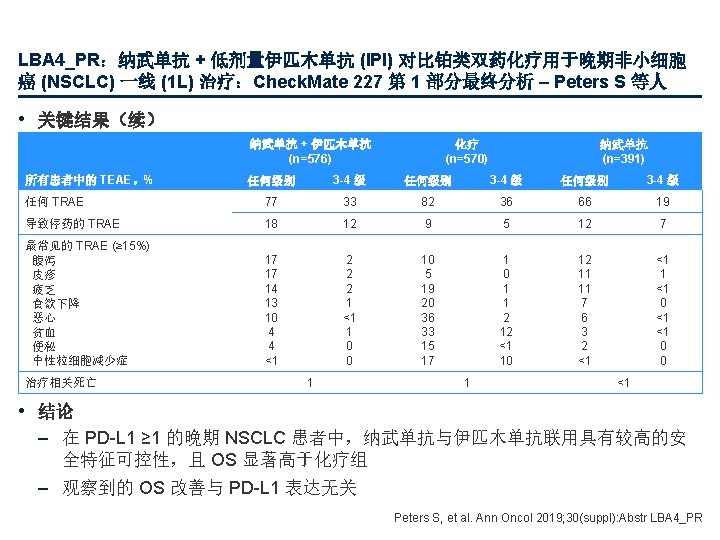
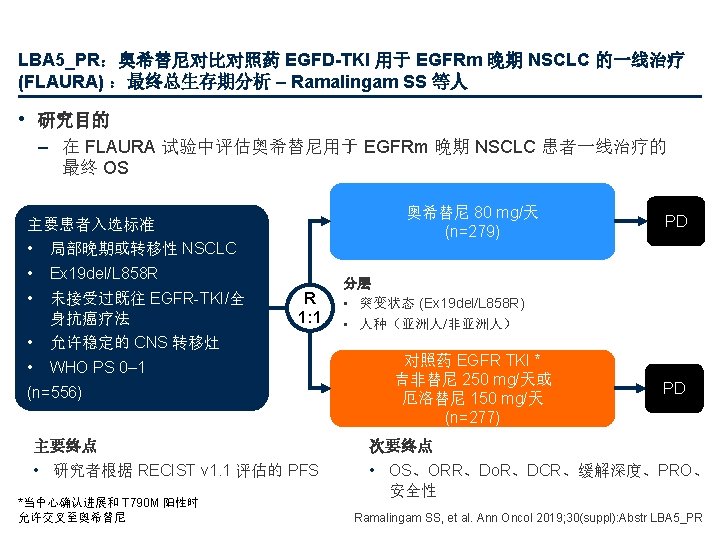
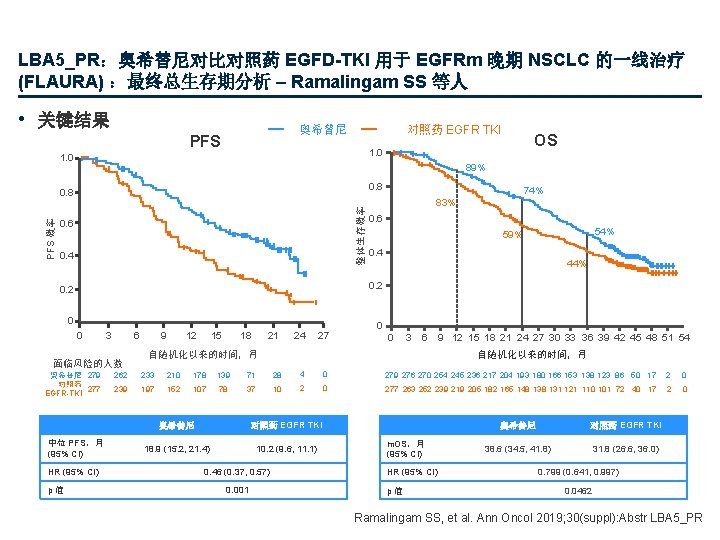
LBA 5_PR:奥希替尼对比对照药 EGFD-TKI 用于 EGFRm 晚期 NSCLC 的一线治疗 (FLAURA) :最终总生存期分析 – Ramalingam SS 等人 • 关键结果 对照药 EGFR TKI 奥希替尼 PFS 1. 0 89% 0. 8 整体生存概率 PFS 概率 0. 8 0. 6 0. 4 74% 83% 0. 6 54% 59% 0. 4 44% 0. 2 0 0 3 6 面临风险的人数 奥希替尼 279 对照药 277 EGFR-TKI 中位 PFS,月 (95% CI) HR (95% CI) p值 OS 1. 0 9 12 15 18 21 24 27 0 0 3 6 自随机化以来的时间,月 9 12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 自随机化以来的时间,月 262 233 210 178 139 71 28 4 0 279 276 270 254 245 236 217 204 193 180 166 153 138 123 86 50 17 2 0 239 197 152 107 78 37 10 2 0 277 263 252 239 219 205 182 165 148 131 121 110 101 72 40 17 2 0 奥希替尼 对照药 EGFR TKI 18. 9 (15. 2, 21. 4) 10. 2 (9. 6, 11. 1) 0. 46 (0. 37, 0. 57) 0. 001 m. OS,月 (95% CI) HR (95% CI) p值 奥希替尼 对照药 EGFR TKI 38. 6 (34. 5, 41. 8) 31. 8 (26. 6, 36. 0) 0. 799 (0. 641, 0. 997) 0. 0462 Ramalingam SS, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 5_PR
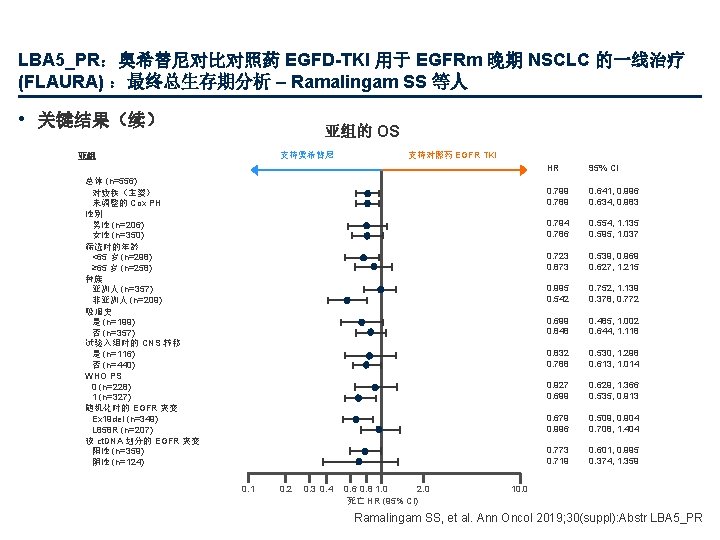
LBA 5_PR:奥希替尼对比对照药 EGFD-TKI 用于 EGFRm 晚期 NSCLC 的一线治疗 (FLAURA) :最终总生存期分析 – Ramalingam SS 等人 • 关键结果(续) 亚组的 OS 支持奥希替尼 亚组 支持对照药 EGFR TKI 总体 (n=556) 对数秩(主要) 未调整的 Cox PH 性别 男性 (n=206) 女性 (n=350) 筛选时的年龄 <65 岁 (n=298) ≥ 65 岁 (n=258) 种族 亚洲人 (n=357) 非亚洲人 (n=209) 吸烟史 是 (n=199) 否 (n=357) 试验入组时的 CNS 转移 是 (n=116) 否 (n=440) WHO PS 0 (n=228) 1 (n=327) 随机化时的 EGFR 突变 Ex 19 del (n=349) L 858 R (n=207) 按 ct. DNA 划分的 EGFR 突变 阳性 (n=359) 阴性 (n=124) 0. 1 0. 2 0. 3 0. 4 0. 6 0. 8 1. 0 2. 0 死亡 HR (95% CI) HR 95% CI 0. 799 0. 789 0. 641, 0. 996 0. 634, 0. 983 0. 794 0. 786 0. 554, 1. 135 0. 595, 1. 037 0. 723 0. 873 0. 539, 0. 969 0. 627, 1. 215 0. 995 0. 542 0. 752, 1. 139 0. 378, 0. 772 0. 699 0. 848 0. 485, 1. 002 0. 644, 1. 118 0. 832 0. 788 0. 530, 1. 298 0. 613, 1. 014 0. 927 0. 699 0. 629, 1. 366 0. 535, 0. 913 0. 679 0. 996 0. 509, 0. 904 0. 708, 1. 404 0. 773 0. 719 0. 601, 0. 995 0. 374, 1. 359 10. 0 Ramalingam SS, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 5_PR
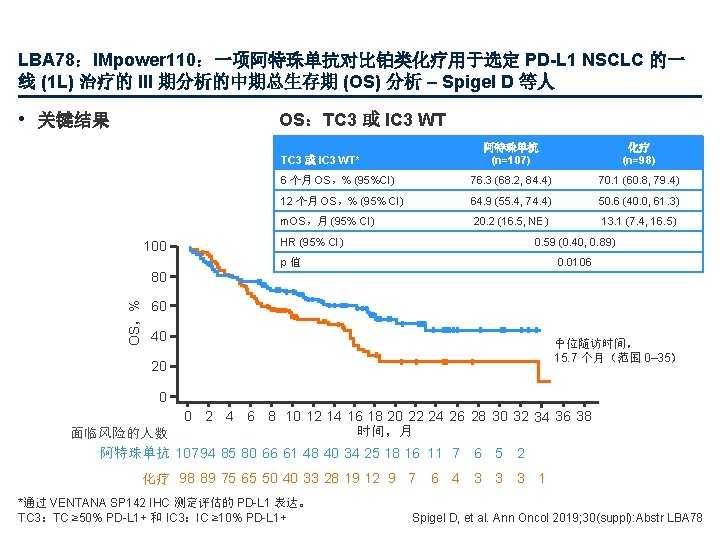
LBA 78:IMpower 110:一项阿特珠单抗对比铂类化疗用于选定 PD-L 1 NSCLC 的一 线 (1 L) 治疗的 III 期分析的中期总生存期 (OS) 分析 – Spigel D 等人 • 关键结果 OS:TC 3 或 IC 3 WT 阿特珠单抗 (n=107) 化疗 (n=98) 6 个月 OS,% (95%CI) 76. 3 (68. 2, 84. 4) 70. 1 (60. 8, 79. 4) 12 个月 OS,% (95% CI) 64. 9 (55. 4, 74. 4) 50. 6 (40. 0, 61. 3) m. OS,月 (95% CI) 20. 2 (16. 5, NE) 13. 1 (7. 4, 16. 5) TC 3 或 IC 3 WT* 100 HR (95% CI) 0. 59 (0. 40, 0. 89) p值 0. 0106 OS,% 80 60 40 中位随访时间, 15. 7 个月(范围 0– 35) 20 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 32 34 36 38 时间,月 面临风险的人数 阿特珠单抗 107 94 85 80 66 61 48 40 34 25 18 16 11 7 6 化疗 98 89 75 65 50 40 33 28 19 12 9 7 *通过 VENTANA SP 142 IHC 测定评估的 PD-L 1 表达。 TC 3:TC ≥ 50% PD-L 1+ 和 IC 3:IC ≥ 10% PD-L 1+ 6 4 3 5 2 3 3 1 Spigel D, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 78
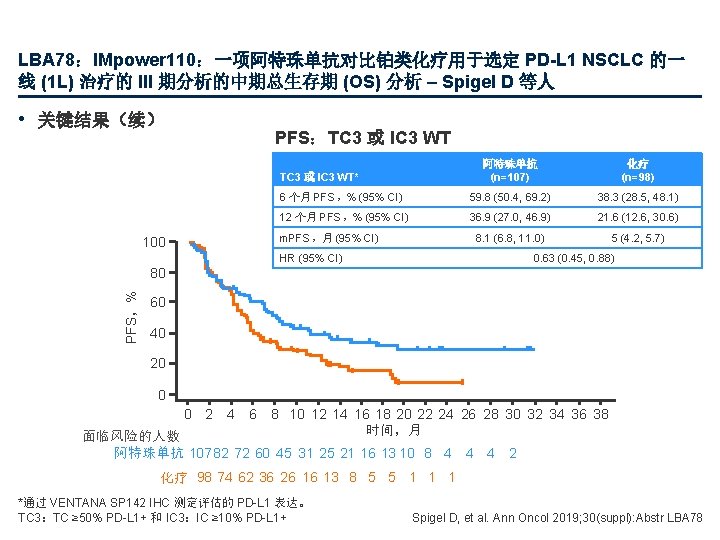
LBA 78:IMpower 110:一项阿特珠单抗对比铂类化疗用于选定 PD-L 1 NSCLC 的一 线 (1 L) 治疗的 III 期分析的中期总生存期 (OS) 分析 – Spigel D 等人 • 关键结果(续) PFS:TC 3 或 IC 3 WT 阿特珠单抗 (n=107) 化疗 (n=98) 6 个月 PFS,% (95% CI) 59. 8 (50. 4, 69. 2) 38. 3 (28. 5, 48. 1) 12 个月 PFS,% (95% CI) 36. 9 (27. 0, 46. 9) 21. 6 (12. 6, 30. 6) 8. 1 (6. 8, 11. 0) 5 (4. 2, 5. 7) TC 3 或 IC 3 WT* m. PFS,月 (95% CI) 100 HR (95% CI) 0. 63 (0. 45, 0. 88) PFS,% 80 60 40 20 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 32 34 36 38 时间,月 面临风险的人数 阿特珠单抗 107 82 72 60 45 31 25 21 16 13 10 8 4 4 4 2 化疗 98 74 62 36 26 16 13 8 5 5 1 1 1 *通过 VENTANA SP 142 IHC 测定评估的 PD-L 1 表达。 TC 3:TC ≥ 50% PD-L 1+ 和 IC 3:IC ≥ 10% PD-L 1+ Spigel D, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 78
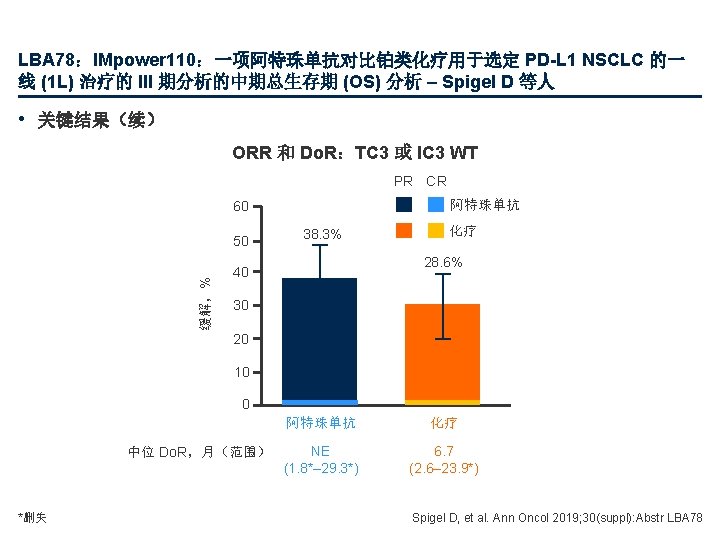
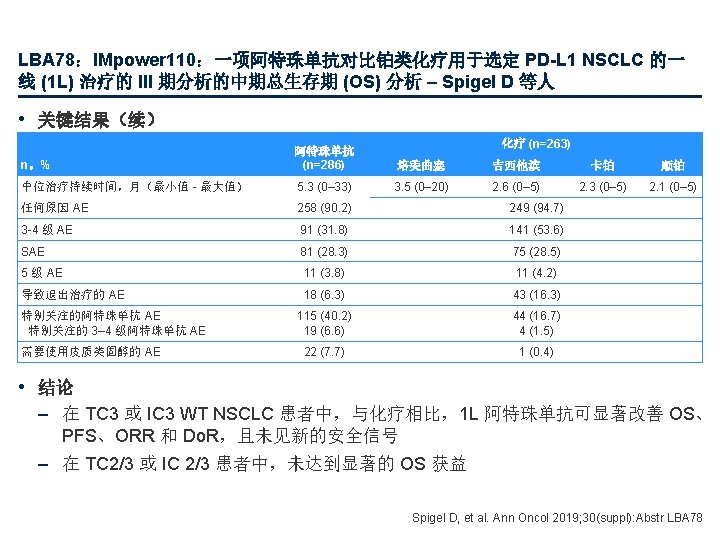
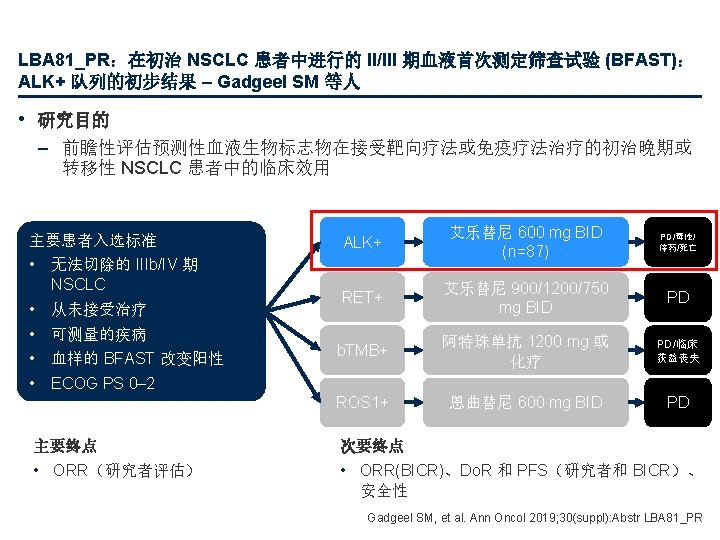
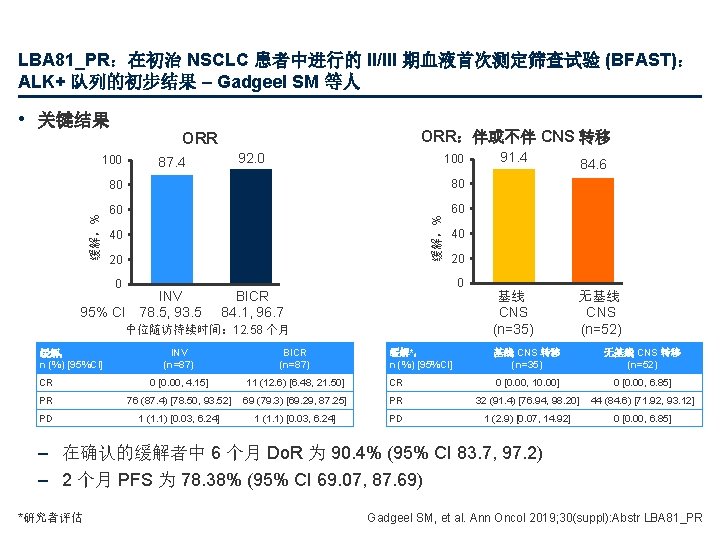
LBA 81_PR:在初治 NSCLC 患者中进行的 II/III 期血液首次测定筛查试验 (BFAST): ALK+ 队列的初步结果 – Gadgeel SM 等人 • 关键结果 100 92. 0 87. 4 100 80 80 60 60 缓解,% ORR:伴或不伴 CNS 转移 ORR 40 20 0 INV 95% CI 78. 5, 93. 5 20 0 BICR 84. 1, 96. 7 INV (n=87) BICR (n=87) CR 0 [0. 00, 4. 15] PR PD 84. 6 40 中位随访持续时间: 12. 58 个月 缓解, n (%) [95%CI] 91. 4 基线 CNS (n=35) 无基线 CNS (n=52) 缓解*, n (%) [95%CI] 基线 CNS 转移 (n=35) 无基线 CNS 转移 (n=52) 11 (12. 6) [6. 48, 21. 50] CR 0 [0. 00, 10. 00] 0 [0. 00, 6. 85] 76 (87. 4) [78. 50, 93. 52] 69 (79. 3) [69. 29, 87. 25] PR 32 (91. 4) [76. 94, 98. 20] 44 (84. 6) [71. 92, 93. 12] 1 (1. 1) [0. 03, 6. 24] PD 1 (2. 9) [0. 07, 14. 92] 0 [0. 00, 6. 85] – 在确认的缓解者中 6 个月 Do. R 为 90. 4% (95% CI 83. 7, 97. 2) – 2 个月 PFS 为 78. 38% (95% CI 69. 07, 87. 69) *研究者评估 Gadgeel SM, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 81_PR
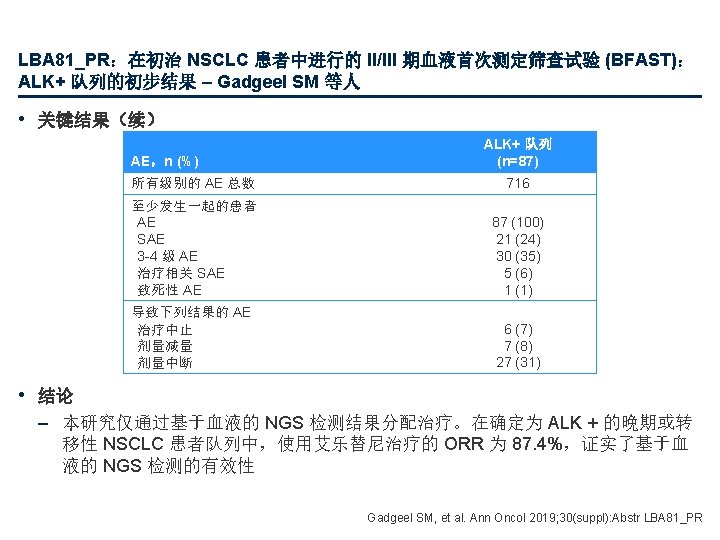
LBA 82:帕博利珠单抗 + 化疗治疗转移性鳞状 NSCLC:KEYNOTE-407 的最终分析 和下一线治疗后的进展 (PFS 2) – Paz-Ares L 等人 • 关键结果 m. OS,月 (95% CI) 安慰剂 + CT (n=281) 100 17. 1 (14. 4, 19. 9) 11. 6 (10. 1, 13. 7) 80 HR (95% CI) 中位 PFS,月 (95% CI) 0. 71 (0. 58, 0. 88) 8. 0 (6. 3, 8. 4) HR (95% CI) ORR,% 中位 Do. R,月( 范围) 5. 1 (4. 3, 6. 0) PFS 2,% 更新的生存结局 PFS 2 帕博利珠单抗 + CT (n=278) 0. 57 (0. 47, 0. 69) 81. 7% 69. 5% 60 40 20 62. 6 38. 4 8. 8 (1. 3+ – 28. 4+) 4. 9 (1. 3+ – 28. 3+) 0 0 面临风险的人数 帕博利珠单抗 + CT 安慰剂 + CT +数据截止日期前无疾病进展 中位数,月 (95% CI) 13. 8 (12. 2, 15. 9) 9. 1 (8. 2, 10. 2) HR 0. 59 (95% CI 0. 49, 0. 72) 3 6 9 12 15 21 24 27 30 33 时间,月 278 256 227 189 157 127 98 67 39 10 4 0 281 241 193 142 99 24 9 2 0 74 18 62 42 Paz-Ares L, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 82
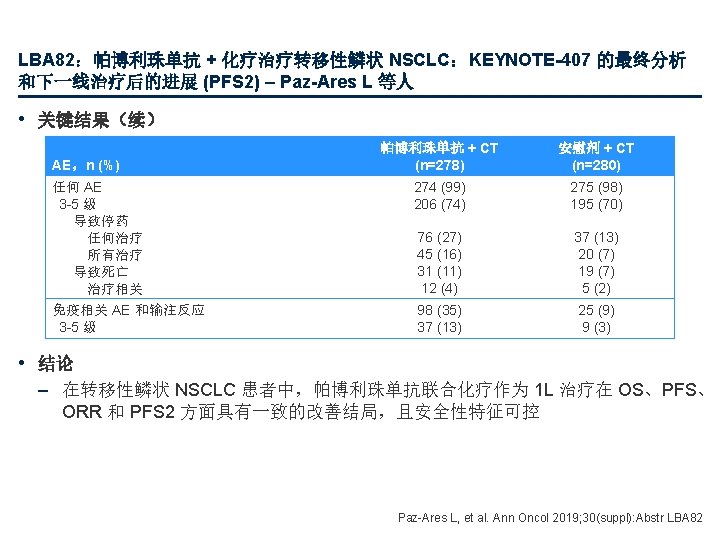
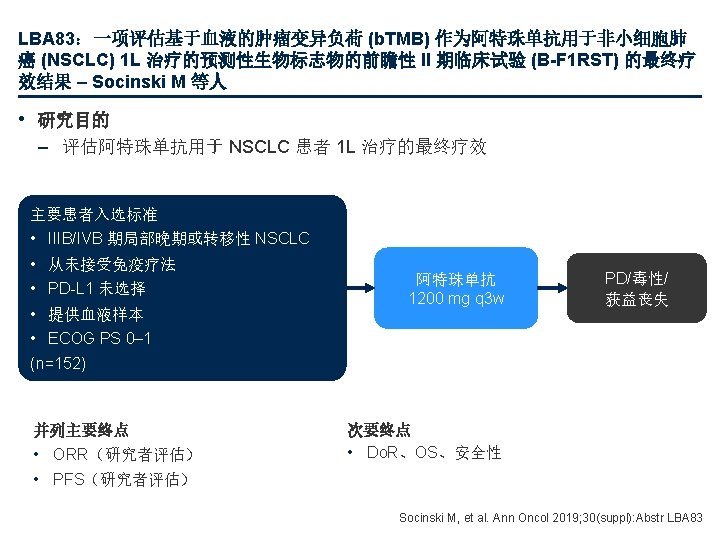
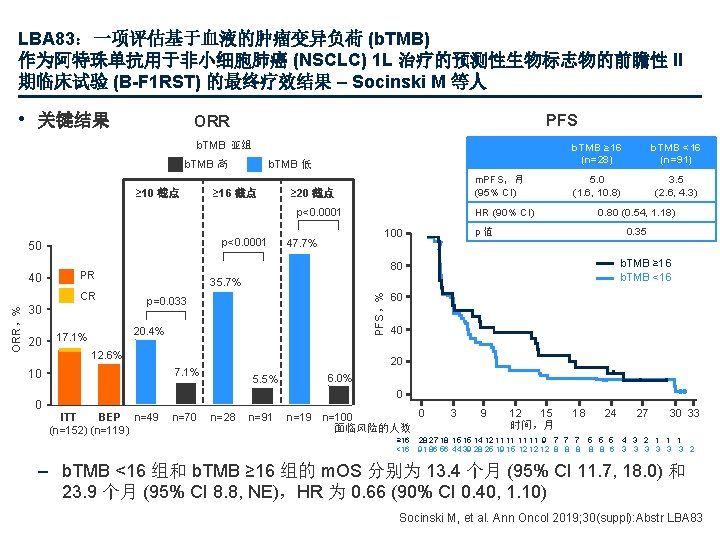
LBA 83:一项评估基于血液的肿瘤变异负荷 (b. TMB) 作为阿特珠单抗用于非小细胞肺癌 (NSCLC) 1 L 治疗的预测性生物标志物的前瞻性 II 期临床试验 (B-F 1 RST) 的最终疗效结果 – Socinski M 等人 • 关键结果 PFS ORR b. TMB 亚组 b. TMB 高 ≥ 10 截点 b. TMB 低 ≥ 16 截点 m. PFS,月 (95% CI) ≥ 20 截点 p<0. 0001 50 ORR,% CR 30 20 p=0. 033 12. 6% 0. 80 (0. 54, 1. 18) p值 0. 35 b. TMB ≥ 16 b. TMB <16 60 40 20 7. 1% 10 0 3. 5 (2. 6, 4. 3) 35. 7% 20. 4% 17. 1% 5. 0 (1. 6, 10. 8) 80 PR PFS,% 40 b. TMB <16 (n=91) HR (90% CI) 100 47. 7% b. TMB ≥ 16 (n=28) 5. 5% 6. 0% 0 ITT BEP n=49 (n=152) (n=119) n=70 n=28 n=91 0 n=19 n=100 面临风险的人数 ≥ 16 <16 3 9 12 15 时间,月 18 24 27 30 33 28 27 18 15 15 14 12 11 11 9 7 7 7 5 5 5 4 3 2 1 1 1 91 86 56 44 39 28 25 19 15 12 12 12 8 8 8 6 3 3 3 2 – b. TMB <16 组和 b. TMB ≥ 16 组的 m. OS 分别为 13. 4 个月 (95% CI 11. 7, 18. 0) 和 23. 9 个月 (95% CI 8. 8, NE),HR 为 0. 66 (90% CI 0. 40, 1. 10) Socinski M, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 83
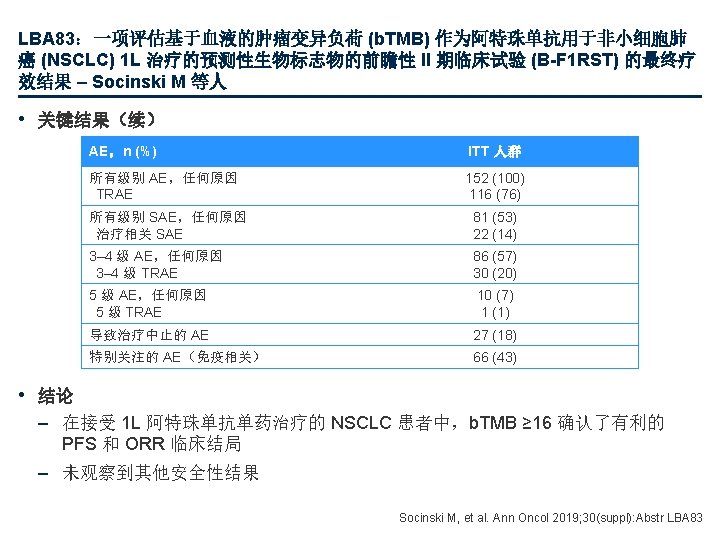
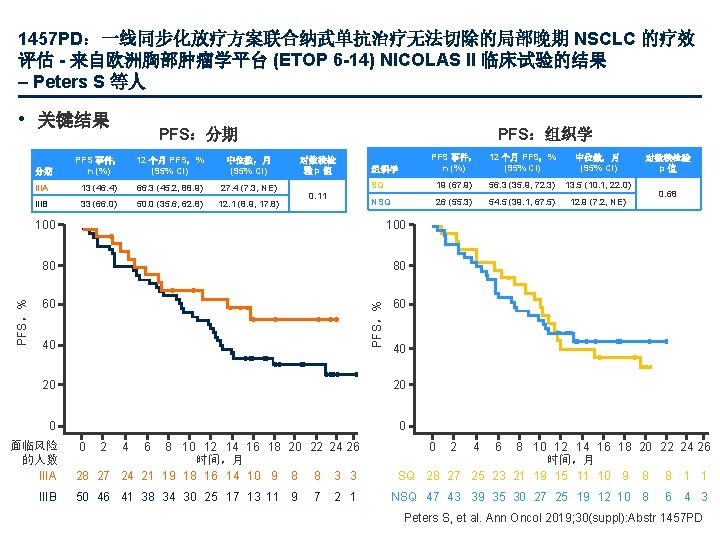
1457 PD:一线同步化放疗方案联合纳武单抗治疗无法切除的局部晚期 NSCLC 的疗效 评估 - 来自欧洲胸部肿瘤学平台 (ETOP 6 -14) NICOLAS II 临床试验的结果 – Peters S 等人 PFS:分期 分期 PFS 事件, n (%) 12 个月 PFS,% (95% CI) 中位数,月 (95% CI) IIIA 13 (46. 4) 66. 3 (45. 2, 88. 9) 27. 4 (7. 3, NE) IIIB 33 (66. 0) 50. 0 (35. 6, 62. 8) 12. 1 (8. 9, 17. 8) PFS:组织学 对数秩检 验p值 0. 11 PFS 事件, n (%) 12 个月 PFS,% (95% CI) 中位数,月 (95% CI) SQ 19 (67. 9) 56. 3 (35. 9, 72. 3) 13. 5 (10. 1, 22. 0) NSQ 26 (55. 3) 54. 5 (39. 1, 67. 5) 12. 9 (7. 2, NE) 组织学 100 80 80 60 60 PFS,% • 关键结果 40 20 0 0 IIIB 0 2 4 6 8 10 12 14 16 18 20 22 24 26 时间,月 28 27 24 21 19 18 16 14 10 9 8 8 3 3 50 46 41 38 34 30 25 17 13 11 9 7 2 1 0. 68 40 20 面临风险 的人数 IIIA 对数秩检验 p值 0 2 4 6 8 10 12 14 16 18 20 22 24 26 时间,月 SQ 28 27 25 23 21 19 15 11 10 9 8 8 1 1 NSQ 47 43 39 35 30 27 25 19 12 10 8 6 4 3 Peters S, et al. Ann Oncol 2019; 30(suppl): Abstr 1457 PD

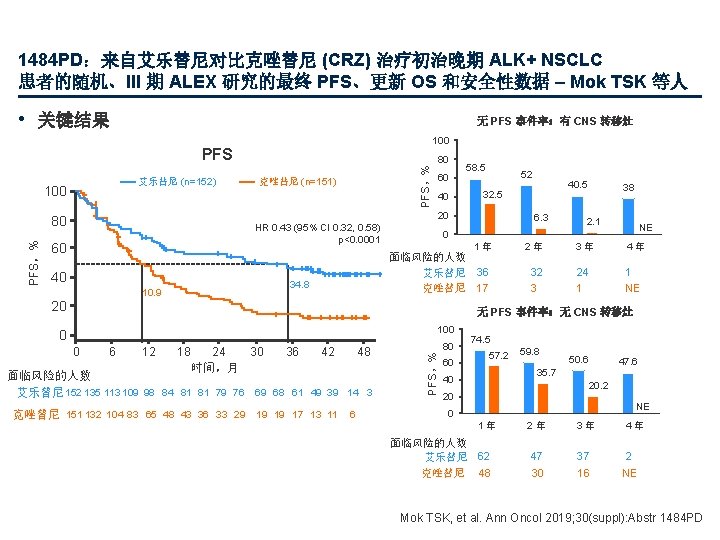
1484 PD:来自艾乐替尼对比克唑替尼 (CRZ) 治疗初治晚期 ALK+ NSCLC 患者的随机、III 期 ALEX 研究的最终 PFS、更新 OS 和安全性数据 – Mok TSK 等人 • 关键结果 无 PFS 事件率:有 CNS 转移灶 100 PFS 100 克唑替尼 (n=151) 60 40 58. 5 52 HR 0. 43 (95% CI 0. 32, 0. 58) p<0. 0001 60 40 6. 3 38 2. 1 NE 0 1年 面临风险的人数 艾乐替尼 36 克唑替尼 17 34. 8 10. 9 40. 5 32. 5 20 80 PFS,% 艾乐替尼 (n=152) 80 20 2年 3年 4年 32 3 24 1 1 NE 无 PFS 事件率:无 CNS 转移灶 100 0 6 12 18 24 30 时间,月 36 42 48 面临风险的人数 艾乐替尼 152 135 113 109 98 84 81 81 79 76 69 68 61 49 39 14 3 克唑替尼 151 132 104 83 65 48 43 36 33 29 19 19 17 13 11 6 80 PFS,% 0 60 74. 5 57. 2 59. 8 50. 6 47. 6 35. 7 40 20. 2 20 NE 0 1年 面临风险的人数 艾乐替尼 62 克唑替尼 48 2年 3年 4年 47 30 37 16 2 NE Mok TSK, et al. Ann Oncol 2019; 30(suppl): Abstr 1484 PD
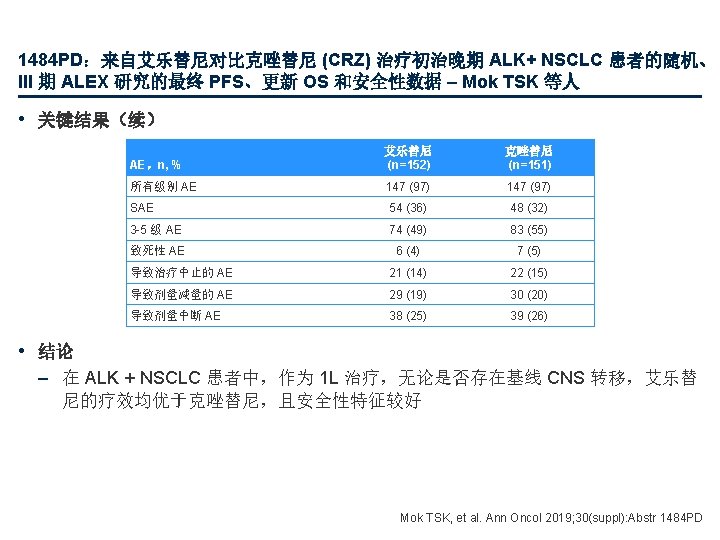

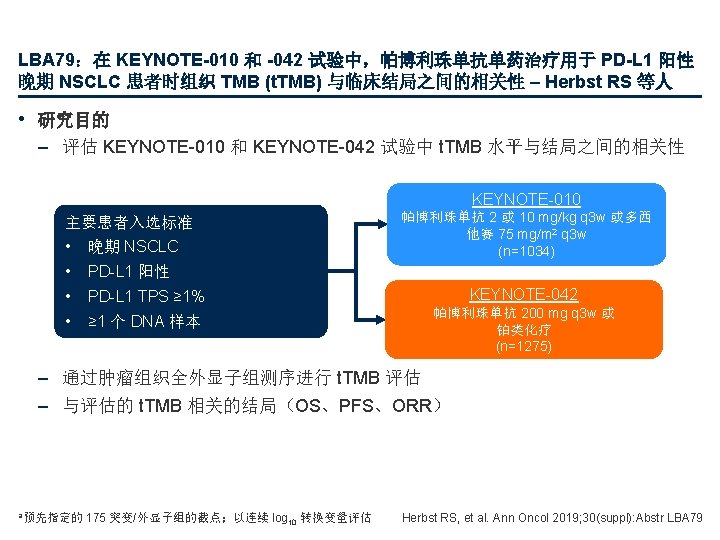
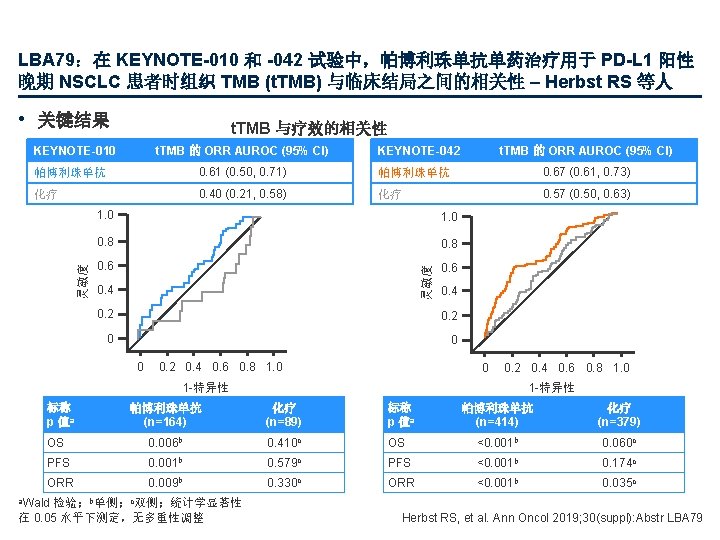
LBA 79:在 KEYNOTE-010 和 -042 试验中,帕博利珠单抗单药治疗用于 PD-L 1 阳性 晚期 NSCLC 患者时组织 TMB (t. TMB) 与临床结局之间的相关性 – Herbst RS 等人 • 关键结果 t. TMB 与疗效的相关性 KEYNOTE-010 t. TMB 的 ORR AUROC (95% CI) KEYNOTE-042 t. TMB 的 ORR AUROC (95% CI) 0. 61 (0. 50, 0. 71) 帕博利珠单抗 0. 67 (0. 61, 0. 73) 化疗 0. 40 (0. 21, 0. 58) 化疗 0. 57 (0. 50, 0. 63) 1. 0 0. 8 0. 6 灵敏度 帕博利珠单抗 0. 4 0. 2 0. 4 0. 6 0. 8 1. 0 0 0. 2 0. 4 0. 6 0. 8 1. 0 1 -特异性 标称 p 值a 1 -特异性 帕博利珠单抗 (n=164) 化疗 (n=89) 标称 p 值a OS 0. 006 b 0. 410 c PFS 0. 001 b ORR 0. 009 b 帕博利珠单抗 (n=414) 化疗 (n=379) OS <0. 001 b 0. 060 c 0. 579 c PFS <0. 001 b 0. 174 c 0. 330 c ORR <0. 001 b 0. 035 c a. Wald 检验;b单侧;c双侧;统计学显著性 在 0. 05 水平下测定,无多重性调整 Herbst RS, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 79

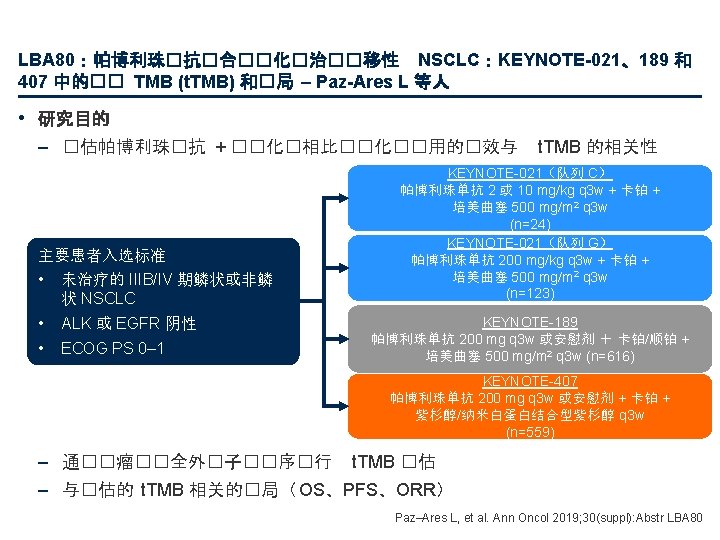
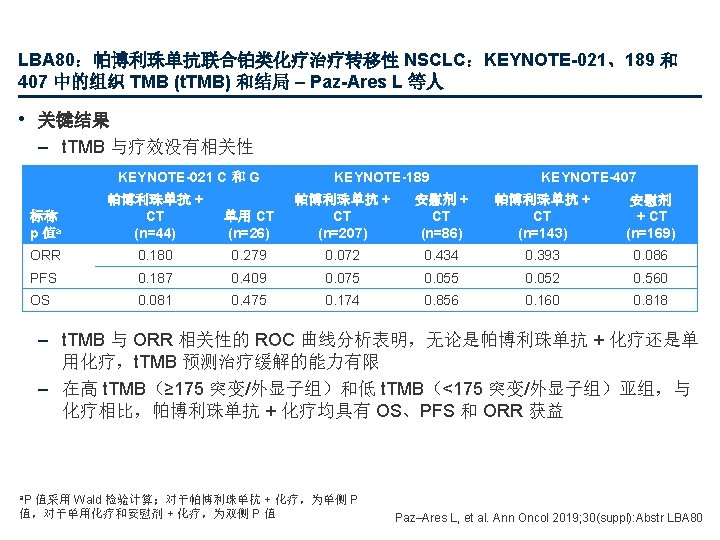

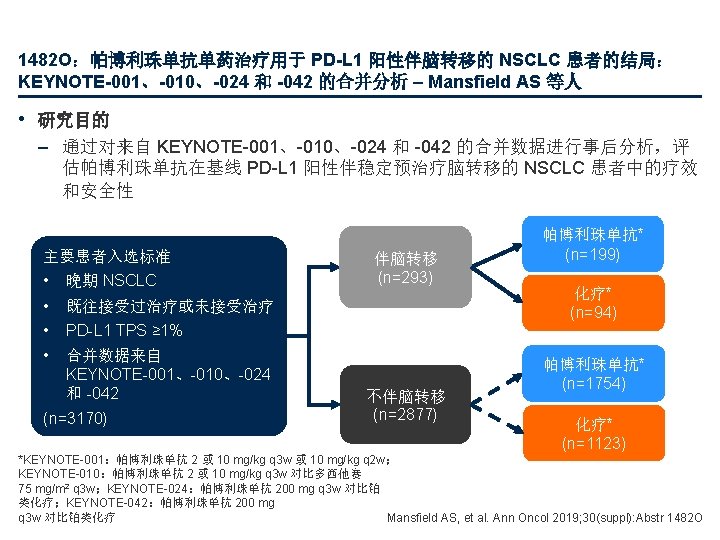
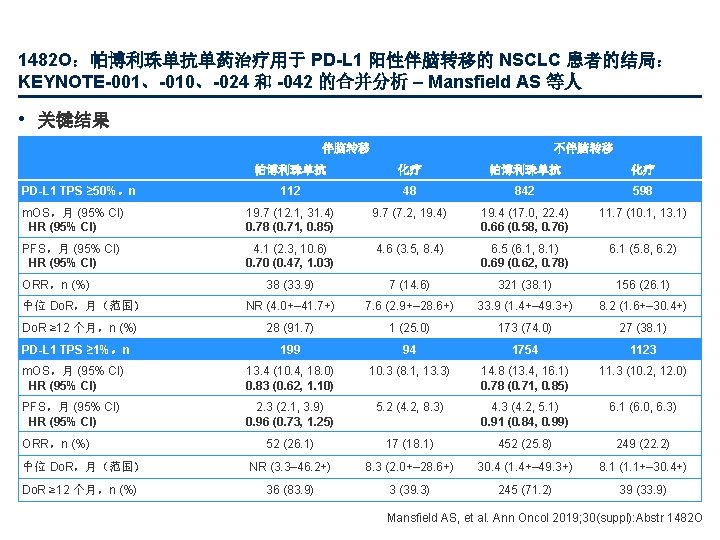
1482 O:帕博利珠单抗单药治疗用于 PD-L 1 阳性伴脑转移的 NSCLC 患者的结局: KEYNOTE-001、-010、-024 和 -042 的合并分析 – Mansfield AS 等人 • 关键结果 伴脑转移 不伴脑转移 帕博利珠单抗 化疗 112 48 842 598 m. OS,月 (95% CI) HR (95% CI) 19. 7 (12. 1, 31. 4) 0. 78 (0. 71, 0. 85) 9. 7 (7. 2, 19. 4) 19. 4 (17. 0, 22. 4) 0. 66 (0. 58, 0. 76) 11. 7 (10. 1, 13. 1) PFS,月 (95% CI) HR (95% CI) 4. 1 (2. 3, 10. 6) 0. 70 (0. 47, 1. 03) 4. 6 (3. 5, 8. 4) 6. 5 (6. 1, 8. 1) 0. 69 (0. 62, 0. 78) 6. 1 (5. 8, 6. 2) 38 (33. 9) 7 (14. 6) 321 (38. 1) 156 (26. 1) NR (4. 0+– 41. 7+) 7. 6 (2. 9+– 28. 6+) 33. 9 (1. 4+– 49. 3+) 8. 2 (1. 6+– 30. 4+) 28 (91. 7) 1 (25. 0) 173 (74. 0) 27 (38. 1) PD-L 1 TPS ≥ 1%,n 199 94 1754 1123 m. OS,月 (95% CI) HR (95% CI) 13. 4 (10. 4, 18. 0) 0. 83 (0. 62, 1. 10) 10. 3 (8. 1, 13. 3) 14. 8 (13. 4, 16. 1) 0. 78 (0. 71, 0. 85) 11. 3 (10. 2, 12. 0) PFS,月 (95% CI) HR (95% CI) 2. 3 (2. 1, 3. 9) 0. 96 (0. 73, 1. 25) 5. 2 (4. 2, 8. 3) 4. 3 (4. 2, 5. 1) 0. 91 (0. 84, 0. 99) 6. 1 (6. 0, 6. 3) 52 (26. 1) 17 (18. 1) 452 (25. 8) 249 (22. 2) NR (3. 3– 46. 2+) 8. 3 (2. 0+– 28. 6+) 30. 4 (1. 4+– 49. 3+) 8. 1 (1. 1+– 30. 4+) 36 (83. 9) 3 (39. 3) 245 (71. 2) 39 (33. 9) PD-L 1 TPS ≥ 50%,n ORR,n (%) 中位 Do. R,月(范围) Do. R ≥ 12 个月,n (%) Mansfield AS, et al. Ann Oncol 2019; 30(suppl): Abstr 1482 O
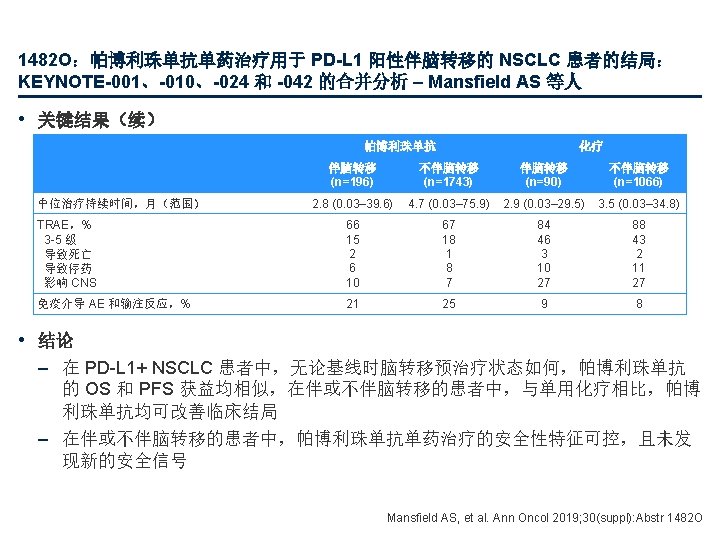
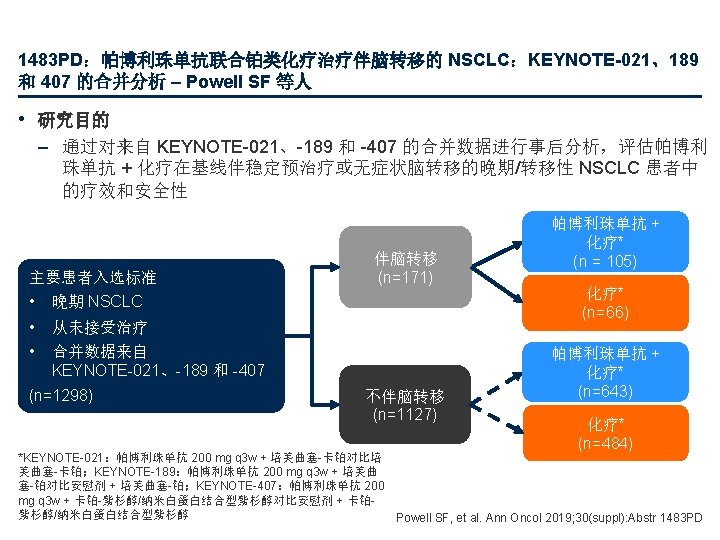
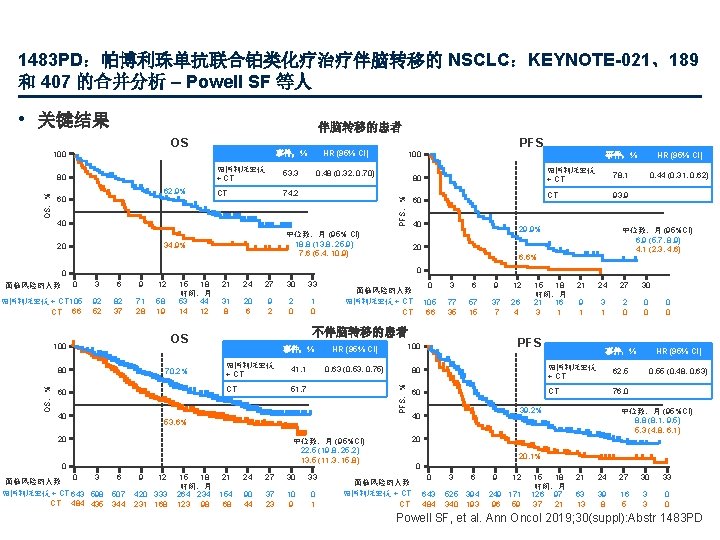
1483 PD:帕博利珠单抗联合铂类化疗治疗伴脑转移的 NSCLC:KEYNOTE-021、189 和 407 的合并分析 – Powell SF 等人 • 关键结果 伴脑转移的患者 OS OS,% 80 62. 9% 60 事件,% HR (95% CI) 帕博利珠单抗 + CT 53. 3 0. 48 (0. 32, 0. 70) CT 74. 2 40 80 60 40 中位数,月 (95% CI) 18. 8 (13. 8, 25. 9) 7. 6 (5. 4, 10. 9) 34. 9% 20 PFS 100 PFS,% 100 帕博利珠单抗 + CT 78. 1 0. 44 (0. 31, 0. 62) CT 93. 9 29. 9% 中位数,月 (95%CI) 6. 9 (5. 7, 8. 9) 4. 1 (2. 3, 4. 6) 6. 6% 0 3 6 9 12 92 52 82 37 71 28 58 19 15 18 时间,月 53 44 14 12 21 24 27 30 33 31 8 20 6 9 2 2 0 1 0 80 70. 2% 60 40 事件,% HR (95% CI) 100 帕博利珠单抗 + CT 41. 1 0. 63 (0. 53, 0. 75) 80 CT 51. 7 60 53. 6% 20 9 12 420 333 231 168 3 6 9 12 105 66 77 35 57 15 37 7 26 4 15 18 21 时间,月 264 234 154 123 98 68 24 27 30 33 90 44 37 23 10 9 0 1 15 18 时间,月 21 16 3 1 21 24 27 30 9 1 3 1 2 0 0 0 PFS HR (95% CI) 帕博利珠单抗 + CT 62. 5 0. 55 (0. 48, 0. 63) CT 76. 0 39. 2% 40 0 0 事件,% 中位数,月 (95%CI) 8. 8 (8. 1, 9. 5) 5. 3 (4. 8, 6. 1) 20 中位数,月 (95%CI) 22. 5 (19. 8, 25. 2) 13. 5 (11. 3, 15. 8) 0 0 3 6 面临风险的人数 帕博利珠单抗 + CT 643 598 507 CT 484 435 344 0 不伴脑转移的患者 OS 100 面临风险的人数 帕博利珠单抗 + CT CT PFS,% 0 帕博利珠单抗 + CT 105 CT 66 OS,% HR (95% CI) 20 0 面临风险的人数 事件,% 20. 1% 0 面临风险的人数 帕博利珠单抗 + CT CT 0 643 484 3 6 525 394 340 193 9 12 249 171 96 59 15 18 时间,月 126 97 37 21 21 24 27 30 33 63 13 39 8 16 5 3 3 0 0 Powell SF, et al. Ann Oncol 2019; 30(suppl): Abstr 1483 PD
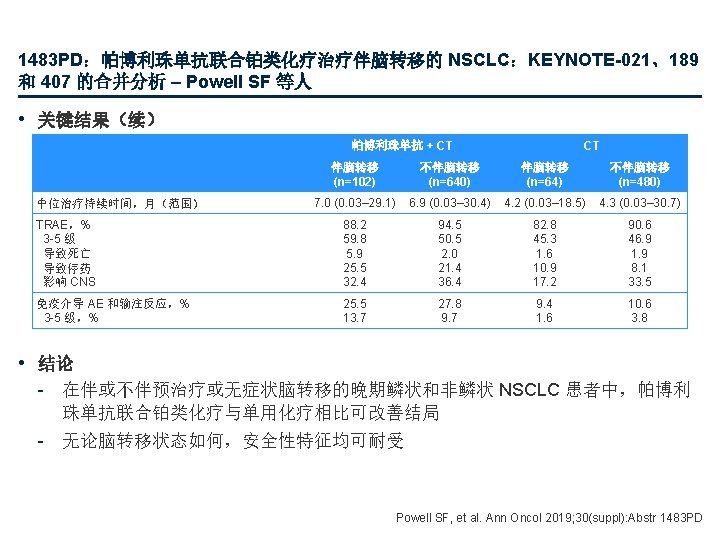
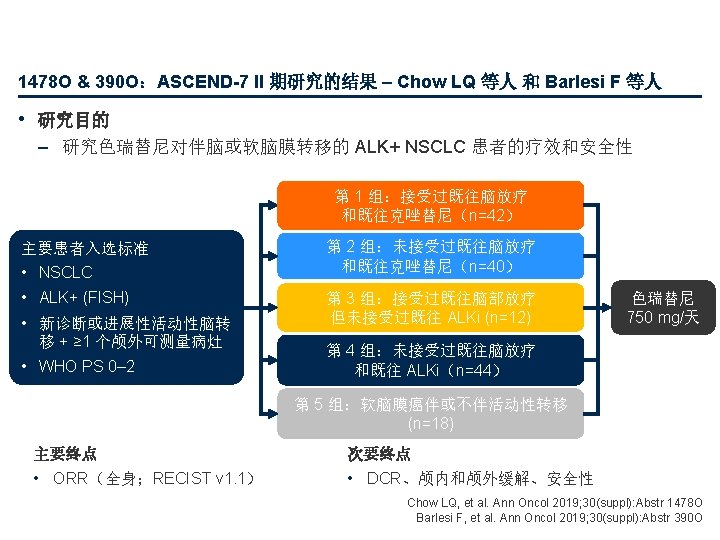
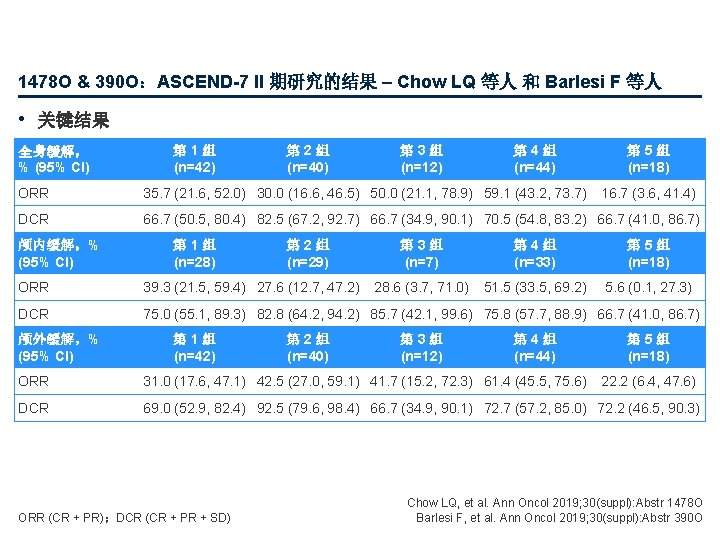
1478 O & 390 O:ASCEND-7 II 期研究的结果 – Chow LQ 等人 和 Barlesi F 等人 • 关键结果 全身缓解, % (95% CI) 第 1组 (n=42) 第 2组 (n=40) 第 3组 (n=12) 第 4组 (n=44) 第 5组 (n=18) ORR 35. 7 (21. 6, 52. 0) 30. 0 (16. 6, 46. 5) 50. 0 (21. 1, 78. 9) 59. 1 (43. 2, 73. 7) DCR 66. 7 (50. 5, 80. 4) 82. 5 (67. 2, 92. 7) 66. 7 (34. 9, 90. 1) 70. 5 (54. 8, 83. 2) 66. 7 (41. 0, 86. 7) 颅内缓解,% (95% CI) 第 1组 (n=28) 第 2组 (n=29) 16. 7 (3. 6, 41. 4) 第 3组 (n=7) 第 4组 (n=33) 第 5组 (n=18) 28. 6 (3. 7, 71. 0) 51. 5 (33. 5, 69. 2) 5. 6 (0. 1, 27. 3) ORR 39. 3 (21. 5, 59. 4) 27. 6 (12. 7, 47. 2) DCR 75. 0 (55. 1, 89. 3) 82. 8 (64. 2, 94. 2) 85. 7 (42. 1, 99. 6) 75. 8 (57. 7, 88. 9) 66. 7 (41. 0, 86. 7) 颅外缓解,% (95% CI) 第 1组 (n=42) 第 2组 (n=40) 第 3组 (n=12) 第 4组 (n=44) 第 5组 (n=18) ORR 31. 0 (17. 6, 47. 1) 42. 5 (27. 0, 59. 1) 41. 7 (15. 2, 72. 3) 61. 4 (45. 5, 75. 6) DCR 69. 0 (52. 9, 82. 4) 92. 5 (79. 6, 98. 4) 66. 7 (34. 9, 90. 1) 72. 7 (57. 2, 85. 0) 72. 2 (46. 5, 90. 3) ORR (CR + PR);DCR (CR + PR + SD) 22. 2 (6. 4, 47. 6) Chow LQ, et al. Ann Oncol 2019; 30(suppl): Abstr 1478 O Barlesi F, et al. Ann Oncol 2019; 30(suppl): Abstr 390 O
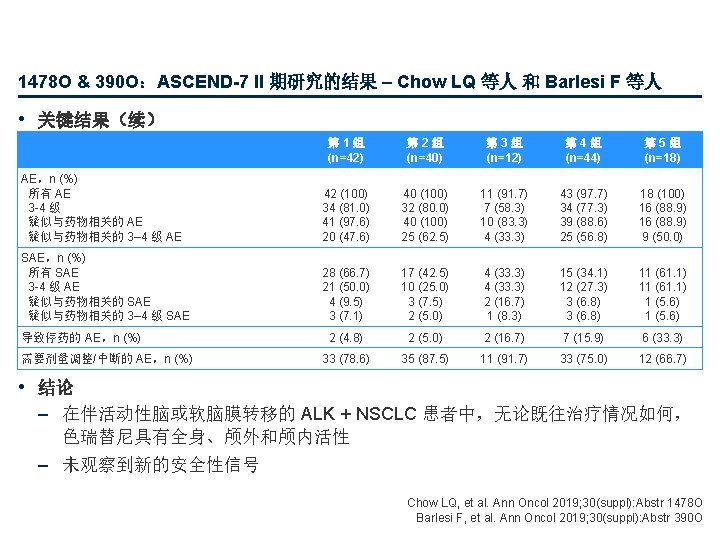

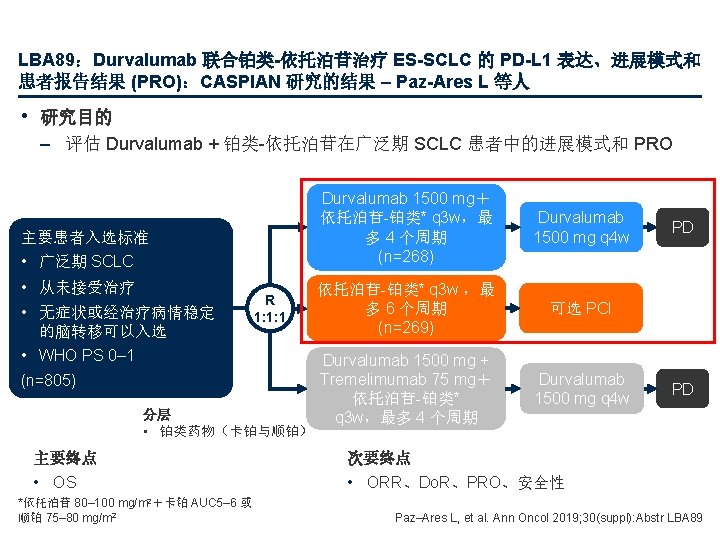

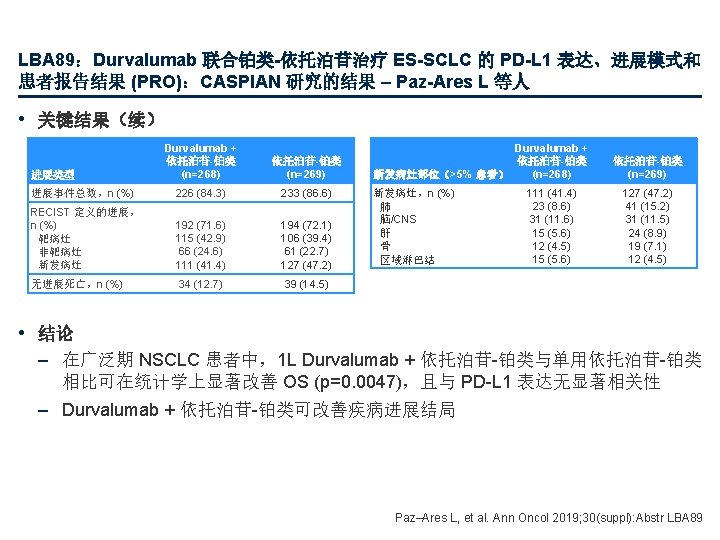
LBA 89:Durvalumab 联合铂类-依托泊苷治疗 ES-SCLC 的 PD-L 1 表达、进展模式和 患者报告结果 (PRO):CASPIAN 研究的结果 – Paz-Ares L 等人 • 关键结果 – Durvalumab + 依托泊苷-铂类的中位 OS 为 13. 0 个月 (95%CI 11. 5, 14. 8), 依托泊苷-铂类单用的中位 OS 为 10. 3 个月 (95%CI 9. 3, 11. 2),(HR 0. 73 [95%CI 0. 591, 0. 909]) – 两组中 277 名 (51. 6%) 患者的 PD-L 1 可评估* • 94. 9% 的 TC PD-L 1 <1%,77. 6% 的 IC PD-L 1 <1% – 未观察到 PD-L 1 表达对 OS、PFS 或 ORR 的显著影响 基于 PD-L 1 表达的 OS ITT (n=537) HR (95% CI) 0. 73 (0. 591, 0. 910) PD-L 1 可评估 (n=277) IC <1 (n=215) IC ≥ 1 (n=62) TC <1 (n=263) TC ≥ 1 (n=14) 0. 65 (0. 482, 0. 864) 0. 64 (0. 462, 0. 897) 0. 69 (0. 370, 1. 283) 0. 66 (0. 491, 0. 896) 0. 46 (0. 119, 1. 793) 0. 10 0. 25 0. 5 1. 0 支持 Durvalumab + 依托泊苷-铂类 *通过 VENTANA PD-L 1 (SP 263) 测定评估的 PD-L 1 2. 0 支持依托泊苷-铂类 Paz–Ares L, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 89
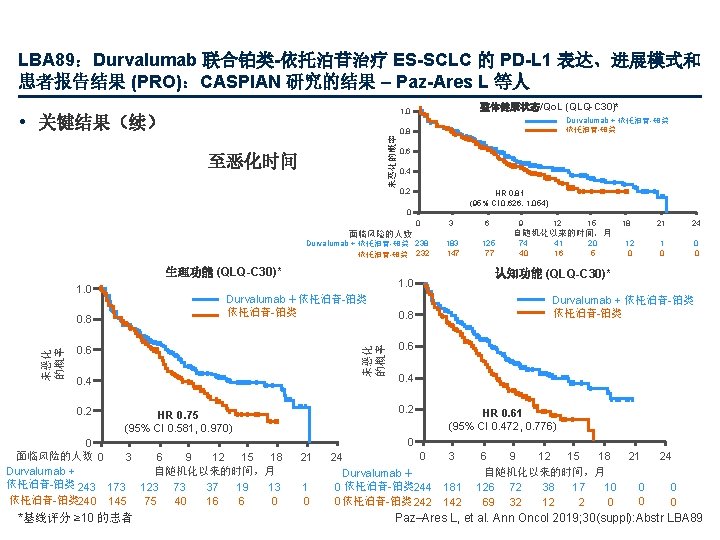
LBA 89:Durvalumab 联合铂类-依托泊苷治疗 ES-SCLC 的 PD-L 1 表达、进展模式和 患者报告结果 (PRO):CASPIAN 研究的结果 – Paz-Ares L 等人 整体健康状态/Qo. L (QLQ-C 30)* 1. 0 未恶化的概率 • 关键结果(续) 至恶化时间 Durvalumab + 依托泊苷-铂类 0. 8 0. 6 0. 4 0. 2 HR 0. 81 (95% CI 0. 626, 1. 054) 0 0 3 6 9 Durvalumab + 依托泊苷-铂类 238 依托泊苷-铂类 232 生理功能 (QLQ-C 30)* 1. 0 未恶化 的概率 0. 8 0. 6 0. 4 0. 2 *基线评分 ≥ 10 的患者 15 18 21 24 125 77 74 40 41 16 20 5 12 0 1 0 0 0 认知功能 (QLQ-C 30)* Durvalumab + 依托泊苷-铂类 0. 8 0. 6 0. 4 0. 2 HR 0. 75 (95% CI 0. 581, 0. 970) 0 面临风险的人数 0 3 6 9 12 15 18 自随机化以来的时间,月 Durvalumab + 依托泊苷-铂类 243 173 123 73 37 19 13 依托泊苷-铂类 240 145 75 40 16 6 0 183 147 1. 0 Durvalumab+依托泊苷-铂类 12 自随机化以来的时间,月 面临风险的人数 HR 0. 61 (95% CI 0. 472, 0. 776) 0 21 1 0 24 0 Durvalumab+ 0 依托泊苷-铂类 244 0 依托泊苷-铂类 242 3 181 142 6 9 12 15 18 自随机化以来的时间,月 126 72 38 17 10 69 32 12 2 0 21 0 0 24 0 0 Paz–Ares L, et al. Ann Oncol 2019; 30(suppl): Abstr LBA 89


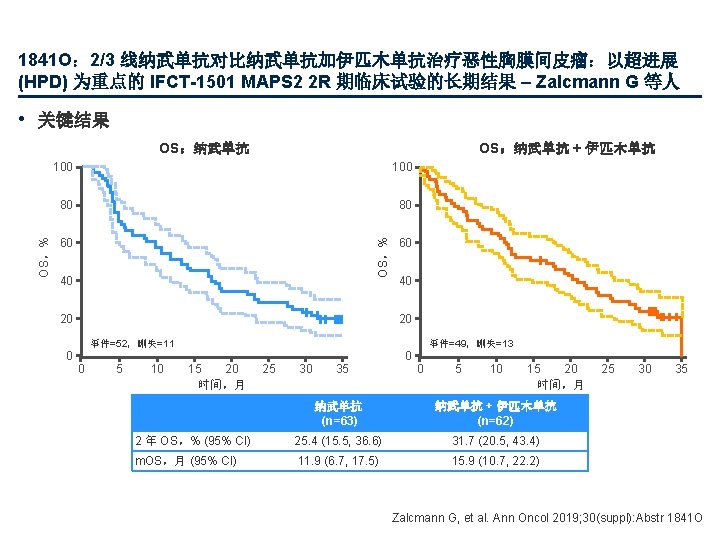

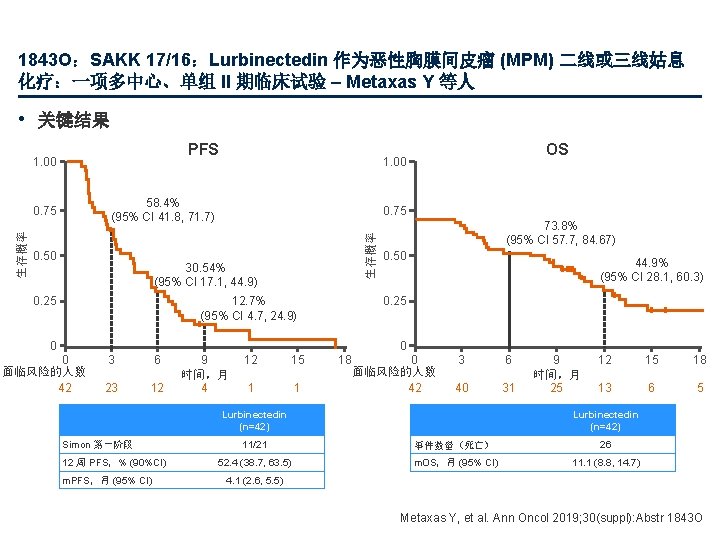
1843 O:SAKK 17/16:Lurbinectedin 作为恶性胸膜间皮瘤 (MPM) 二线或三线姑息 化疗:一项多中心、单组 II 期临床试验 – Metaxas Y 等人 • 关键结果 PFS 1. 00 58. 4% (95% CI 41. 8, 71. 7) 0. 50 0. 75 生存概率 0. 75 30. 54% (95% CI 17. 1, 44. 9) 12. 7% (95% CI 4. 7, 24. 9) 0. 25 OS 1. 00 73. 8% (95% CI 57. 7, 84. 67) 0. 50 44. 9% (95% CI 28. 1, 60. 3) 0. 25 0 0 0 面临风险的人数 42 3 6 23 12 9 时间,月 4 12 15 1 1 18 0 面临风险的人数 42 3 6 40 31 12 周 PFS,% (90%CI) m. PFS,月 (95% CI) 12 15 18 13 6 5 Lurbinectedin (n=42) Simon 第一阶段 9 时间,月 25 11/21 事件数量(死亡) 26 52. 4 (38. 7, 63. 5) m. OS,月 (95% CI) 11. 1 (8. 8, 14. 7) 4. 1 (2. 6, 5. 5) Metaxas Y, et al. Ann Oncol 2019; 30(suppl): Abstr 1843 O



- Slides: 80