Lattivazione dellO 2 nelle reazioni di biodegradazione Utilizzo

L’attivazione dell’O 2 nelle reazioni di biodegradazione Utilizzo di O 2 Respirazione Piu’ del 90 % dell’ossigeno è consumato dagli organismi nella catena respiratoria O 2 + 4 H+ + 4 e 2 H 2 O E° = 0. 815 V Questa reazione rappresenta la maggiore sorgente di energia negli organismi aerobici, quando accoppiata all’ossidazione di composti organici ricchi di elettroni, come il gluclosio. Ossigenazione L’ossigeno viene utilizzato per la biosintesi di varie molecole nei pathways metabolici; uno o due atomi di O vengono incorporati nel substrato Monoossigenazione RH + ½ O 2 ROH Diossigenazione Perche’ le reazioni di ossigenazione devono essere catalizzate da enzimi ?

L’attivazione dell’O 2 nelle reazioni di biodegradazione Aspetti termodinamici della riduzione di O 2 Potenziali standard di riduzione di O 2 E°, V vs. NHE, p. H 7, 25 °C O 2 + e O 2 - + e- + 2 H+ H 2 O 2 + e - + H + OH + e- + H+ O 2 + 2 e- + 2 H+ H 2 O 2 + 2 e- + 2 H+ O 2 + 4 H+ + 4 e- O 2 + - e , 2 H O 2 H 2 O + OH H 2 O 2 2 H 2 O H 2 O 2 e - , H+ H 2 O + OH· -0. 33 (1) +0. 89 +0. 38 +2. 31 +0. 281 (2) +1. 349 +0. 815 e - , H+ 2 H 2 O La completa riduzione di O 2 richiede 4 elettroni, ma la maggior parte dei riducenti può trasferire 1 o 2 elettroni per volta

L’attivazione dell’O 2 nelle reazioni di biodegradazione Aspetti termodinamici della riduzione di O 2 La reazione (1), monoelettronica, richiede riducenti molto forti. La reazione (2), bielettronica, è termodicamente più favorita. Le sostanze organiche sono generalmente riducenti deboli per reazioni che coinvolgono 1 elettrone. R· + e- + H+ R-H pot. rid. elevato La riduzione a 2 e- (reazione 2) è perciò quella termodinamicamente favorita dalle sostanze organiche. Le reazioni a 2 e- sono però reazioni molto lente

L’attivazione dell’O 2 nelle reazioni di biodegradazione Aspetti termodinamici della riduzione di O 2 Esempi di reazioni di idrossilazione ed epossidazione di sostanze organiche Queste reazioni sono termodinamicamente permesse tuttavia sono molto lente in assenza di catalizzatori CH 4 + ½ O 2 C 6 H 6 + ½ O 2 C 6 H 5 OH + ½ O 2 C 2 H 4 + ½ O 2 C 5 H 5 N + ½ O 2 CH 3 OH C 6 H 5 OH CH 4(OH)2 C 2 H 4 O C 5 H 5 NO H (kcal/mol) -30 -43 -42 -25 -13

L’attivazione dell’O 2 nelle reazioni di biodegradazione Aspetti cinetici della riduzione di O 2 Barriera cinetica alla reazione diretta di O 2 con substrati organici O 2 – stato fondamentale: tripletto (2 e- spaiati) RH – stato fondamentale: singoletto (no e- spaiati) ROOH (prodotto) – stato fondamentale: singoletto (no e- spaiati) La reazione può avvenire solo con Eatt. molto elevata che consenta di portare il prodotto in stato di tripletto O 2 + RH ROOH non puo’ avvenire in un unico stadio veloce ma attraverso 2 passaggi successivi con Eatt alta O 2 + RH ROOH lenta ROOH oppure O 2 potrebbe passare a stato di singoletto O 2 + 22. 5 Kcal/mol O 2+ RH O 2 ROOH


L’attivazione dell’O 2 nelle reazioni di biodegradazione L’ossigeno nello stato di tripletto può partecipare a reazioni di ossidazione monoelettroniche di sostanze organiche, senza alterare la molteplicità di spin; tali reazioni sono però termodinamicamente sfavorite O 2 + RH O 2 - + R· + H+ Reazioni bielettroniche sono termodinamicamente favorite, ma violano la molteplicità di spin O 2 + RH ROOH Ossidazioni monoelettroniche coinvolgono uno ione metallico sono favorite e spin permesse O 2 + Mn+1 -O 2 - O 2 + Fe 2+ Fe 3+-O 2 -
L’attivazione dell’O 2 da parte del ferro in ossigenazioni bielettroniche E’ necessario Fe 2+ + O 2 Fe 2+-O 2 Fe 3+-O 2 -· potrebbe essere la specie attiva, invece Fe 3+-O 2 -· + e- Fe 2+-O 2 -· Fe 3+-O 22 - Fe 3+-O 22è preferita monoossigenasi diossigenasi
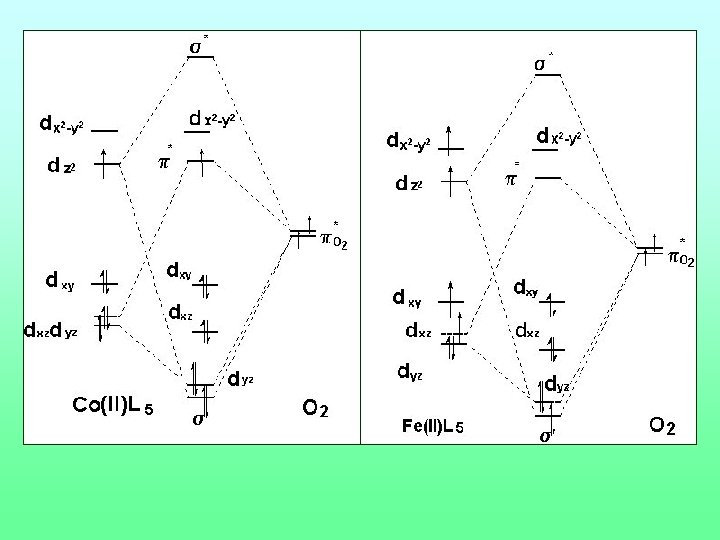

L’attivazione dell’O 2 da parte del ferro in ossigenazioni bielettroniche Fe 3+-O 2 -· Fe 2+-O (1) 2 Fe 2+ + O 2 (2) Fe 3+ + O 2 -· perdita di controllo Fe 3+-O 2 -· + e- Fe 2+-O 2 -· Fe 3+-O 22 - Un elettrone in più deve essere immediatamente disponibile. Occorrono in totale 2 e- (o almeno devono essere disponibili ad una velocità che sia maggiore delle reazioni 1 e 2) Chi fornisce l’elettrone addizionale? Enzimi idrossilanti centro Fe 2 S 2 MMO Fe(II) adiacente Cit P 450 flavoproteina
L’attivazione dell’O 2 da parte del ferro in ossigenazioni bielettroniche Fe 3+enzimi Fe 2+ enzimi (resting state) cit P 450 s. MMO Alcano monoossig. (putida monoossina) la riduzione precede sempre il legame dell’O 2 Fe 3+-O 22 Specie comune Fe. IV=O diossigenasi idrossilanti il ferro è già pronto per legare O 2
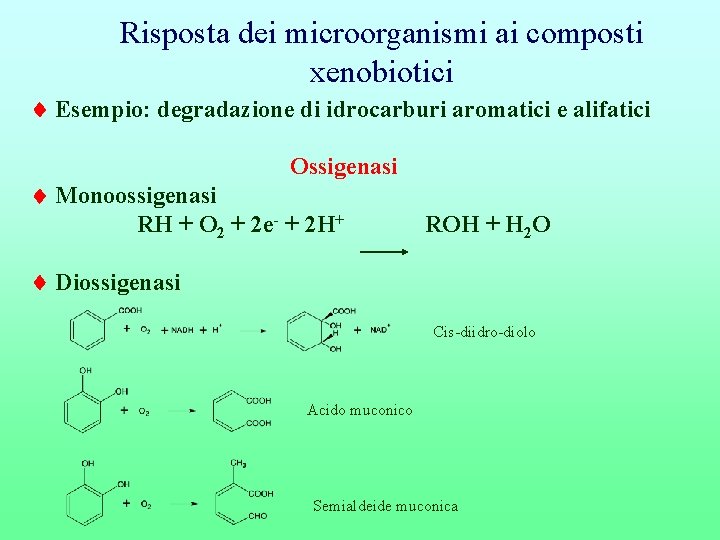
Risposta dei microorganismi ai composti xenobiotici Esempio: degradazione di idrocarburi aromatici e alifatici Ossigenasi Monoossigenasi RH + O 2 + 2 e- + 2 H+ ROH + H 2 O Diossigenasi Cis-diidro-diolo Acido muconico Semialdeide muconica

Monoossigenasi RH + O 2 + 2 e- + 2 H+ ROH + H 2 O Enzimi che catalizzano queste reazioni: 1) Metano monoossigenasi (MMO) 2 Fe 3+ non eme 2) 1 Cu-Cu + 1 Zn(Cu) 2) Citocromo P 450 1 Fe 3+ eme 3) Tirosinasi 2 Cu 2+ Per 1) e 2) lo stadio iniziale è la riduzione Fe 3+ + e. Fe 2+ lega O 2 per dare Fe 3+-O 2 - + e. Fe 3+-O 22 -

Monoossigenasi Le monoossigenasi catalizzano l’inserzione di un atomo di ossigeno nel substrato organico Il secondo atomo di ossigeno viene ridotto a H 2 O da un riducente esterno (monoossigenasi esterna) S + RH 2 + O 2 SO + H 2 O + R o dal substrato stesso (monoossigenasi interna) SH 2 + O 2 SO +H 2 O

Metano monoossigenasi Il metano viene prodotto nell’ambiente come prodotto finale del metabolismo anaerobico di batteri metanogenici Il metano viene utilizzato da batteri metanotrofici (Methylococcus capsulatus e Methylosinus trichosporium) che ossidano il metano come fonte di carbonio e di energia Parte del carbonio proveniente dal metano forma la biomassa dei batteri stessi, parte viene eliminato come CO 2. La reazione di ossidazionedel metano a metanolo necessita di catalizzatori perche’ CH 4 è inerte, con altqa energia di legame (C-H, 104 kcal/mol) Il passaggio iniziale dell’ossidazione di CH 4, in cui viene rotto il legame C-H, è catalizzato dall’enzima metano monoossigenasi (MMO). CH 4 + O 2 + NAD(P)H + H+ CH 3 OH + NAD(P) + H 2 O MMO catalizza l’ossidazione di altri idrocarburi saturi, insaturi, lineari, ramificati e ciclici fino a 8 atomi di C.
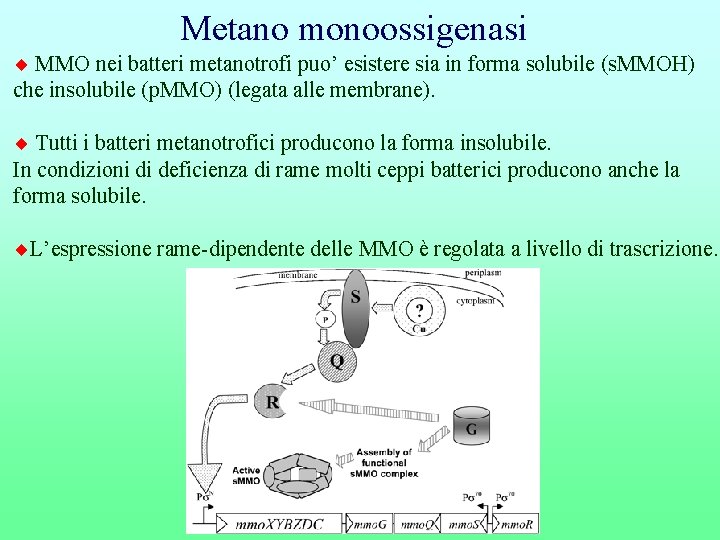
Metano monoossigenasi MMO nei batteri metanotrofi puo’ esistere sia in forma solubile (s. MMOH) che insolubile (p. MMO) (legata alle membrane). Tutti i batteri metanotrofici producono la forma insolubile. In condizioni di deficienza di rame molti ceppi batterici producono anche la forma solubile. L’espressione rame-dipendente delle MMO è regolata a livello di trascrizione.
- Slides: 16