Latomo e la sua struttura Particelle subatomiche Gli

L’atomo e la sua struttura

Particelle subatomiche • • Gli atomi sono formati da particelle: – Elettroni – Protoni – Neutroni Ogni atomo contiene un nucleo, cioè una zona piccola e densa in cui sono confinati protoni e neutroni.
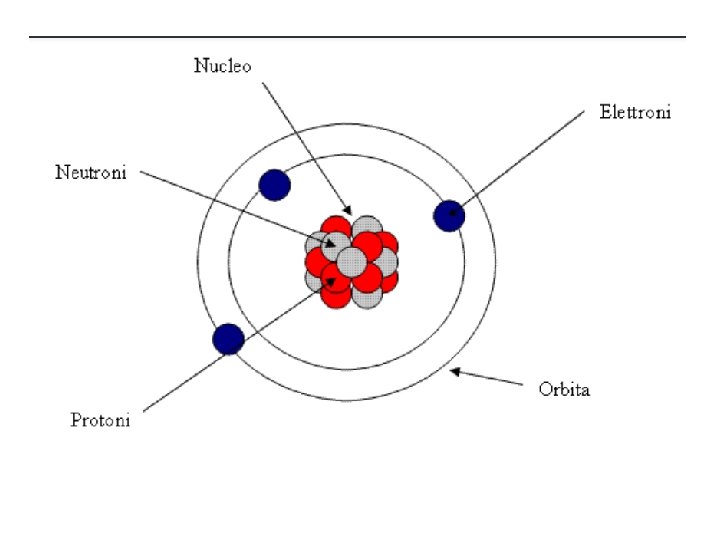
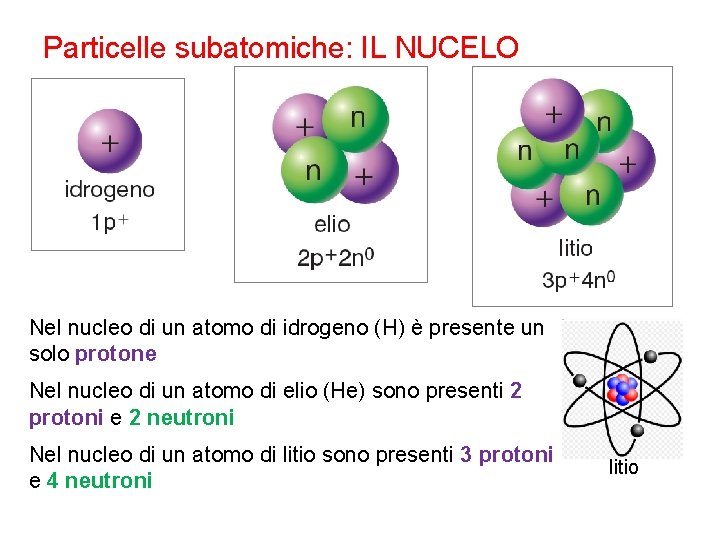
Particelle subatomiche: IL NUCELO Nel nucleo di un atomo di idrogeno (H) è presente un solo protone Nel nucleo di un atomo di elio (He) sono presenti 2 protoni e 2 neutroni Nel nucleo di un atomo di litio sono presenti 3 protoni e 4 neutroni litio
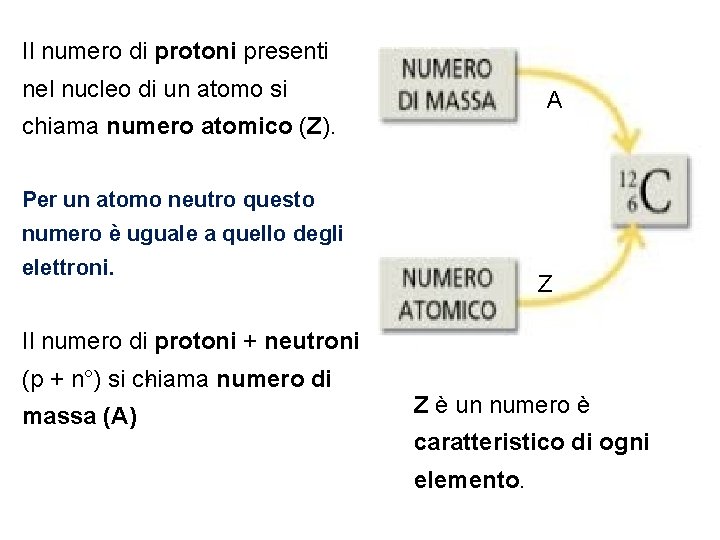
Il numero di protoni presenti nel nucleo di un atomo si A chiama numero atomico (Z). Per un atomo neutro questo numero è uguale a quello degli elettroni. Z Il numero di protoni + neutroni + (p + n°) si chiama numero di massa (A) Z è un numero è caratteristico di ogni elemento.
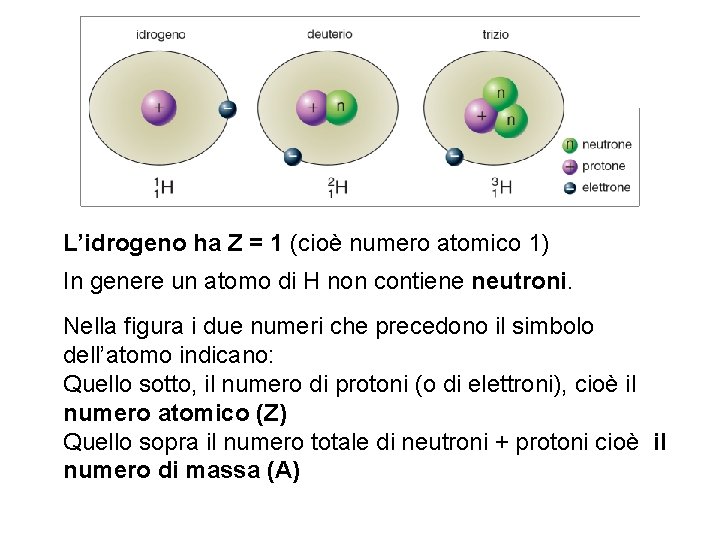
L’idrogeno ha Z = 1 (cioè numero atomico 1) In genere un atomo di H non contiene neutroni. Nella figura i due numeri che precedono il simbolo dell’atomo indicano: Quello sotto, il numero di protoni (o di elettroni), cioè il numero atomico (Z) Quello sopra il numero totale di neutroni + protoni cioè il numero di massa (A)
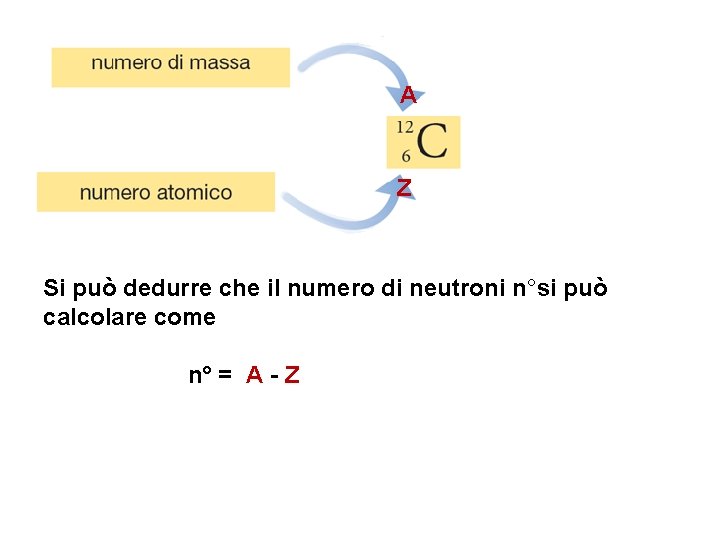
A Z Si può dedurre che il numero di neutroni n°si può calcolare come n° = A - Z
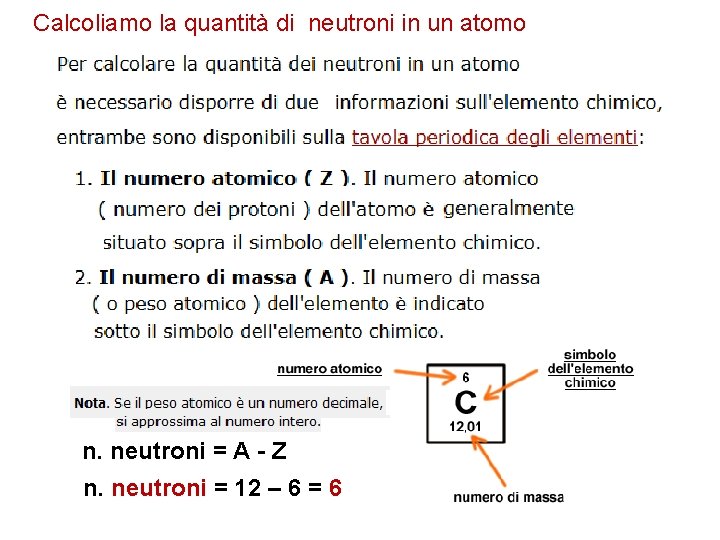
Calcoliamo la quantità di neutroni in un atomo n. neutroni = A - Z n. neutroni = 12 – 6 = 6

La regola dell’ottetto aiuta a capire perché si formano i legami
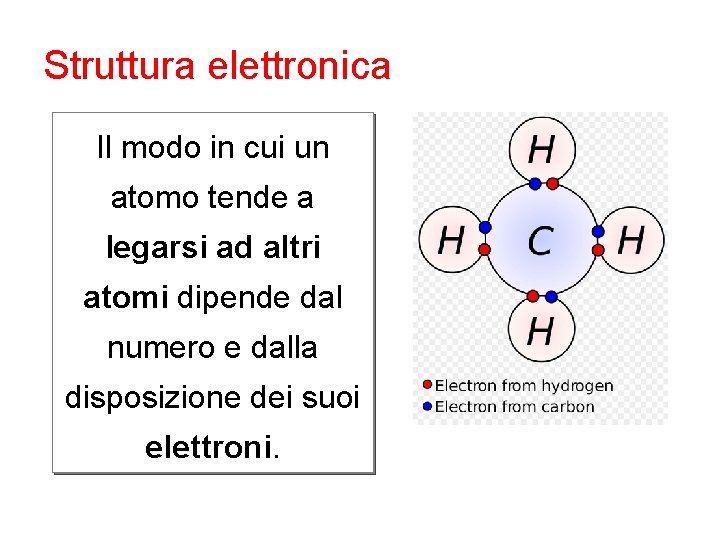
Struttura elettronica Il modo in cui un atomo tende a legarsi ad altri atomi dipende dal numero e dalla disposizione dei suoi elettroni.

Struttura elettronica • In un atomo solo alcuni valori di energia (livelli energetici) sono permessi per gli elettroni. • Quanto più è alta l’energia di un elettrone, tanto maggiore è la sua probabile distanza dal nucleo.
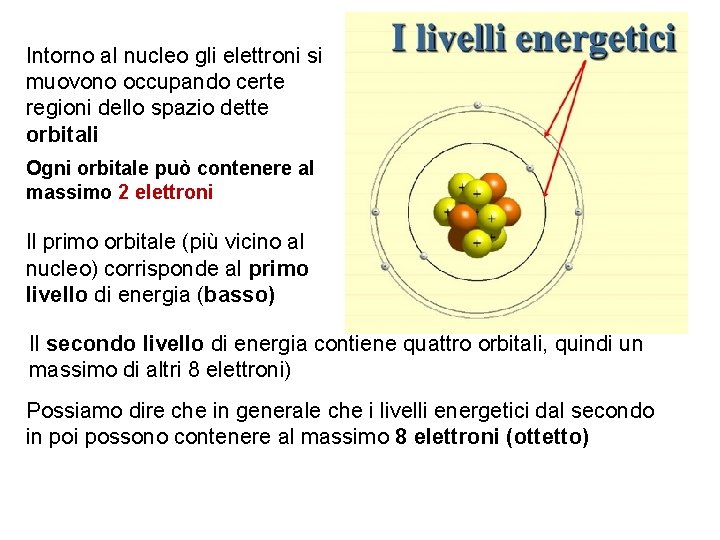
Intorno al nucleo gli elettroni si muovono occupando certe regioni dello spazio dette orbitali Ogni orbitale può contenere al massimo 2 elettroni Il primo orbitale (più vicino al nucleo) corrisponde al primo livello di energia (basso) Il secondo livello di energia contiene quattro orbitali, quindi un massimo di altri 8 elettroni) Possiamo dire che in generale che i livelli energetici dal secondo in poi possono contenere al massimo 8 elettroni (ottetto)
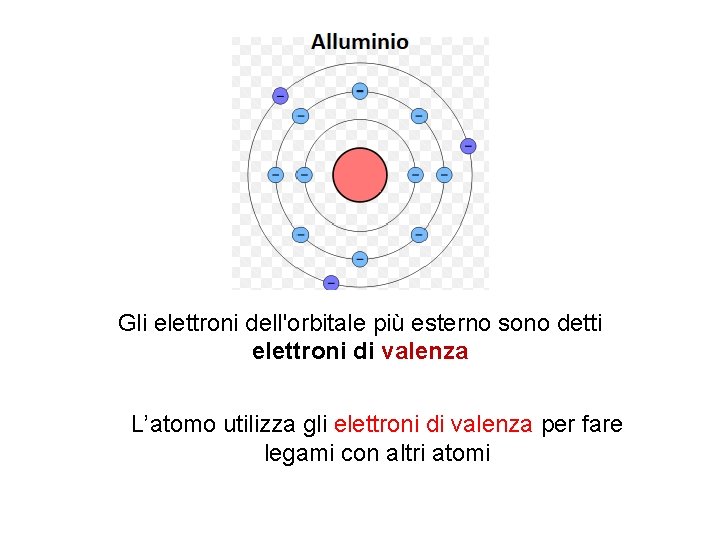
Gli elettroni dell'orbitale più esterno sono detti elettroni di valenza L’atomo utilizza gli elettroni di valenza per fare legami con altri atomi

Struttura elettronica Un atomo ha maggior stabilità quando i suoi elettroni si trovano nei livelli energetici più bassi. Perciò il primo livello è riempito prima del secondo, il secondo prima del terzo…

Struttura elettronica • Il primo livello può contenere al massimo due elettroni, il secondo e il terzo livello ne possono contenere otto ciascuno.

Struttura elettronica Regola dell’ottetto: Un atomo è particolarmente stabile quando ha otto elettroni nello strato di valenza.

I principali legami sono il covalente e lo ionico

Il legame chimico • Formando un legame chimico (covalente o ionico) gli atomi cercano di raggiungere la configurazione elettronica più stabile, mettendo in comune, cedendo o acquistando elettroni fino a completare un livello elettronico.

Il legame covalente • Il legame covalente si forma quando due atomi mettono in comune una coppia di elettroni. Ciascun elettrone proviene da uno dei due atomi. • Un insieme di atomi legati tra loro con legami covalenti è una molecola.
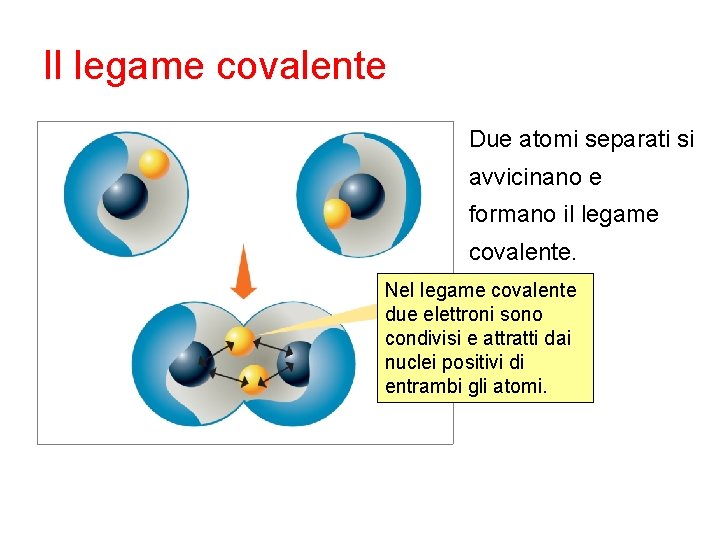
Il legame covalente Due atomi separati si avvicinano e formano il legame covalente. Nel legame covalente due elettroni sono condivisi e attratti dai nuclei positivi di entrambi gli atomi.
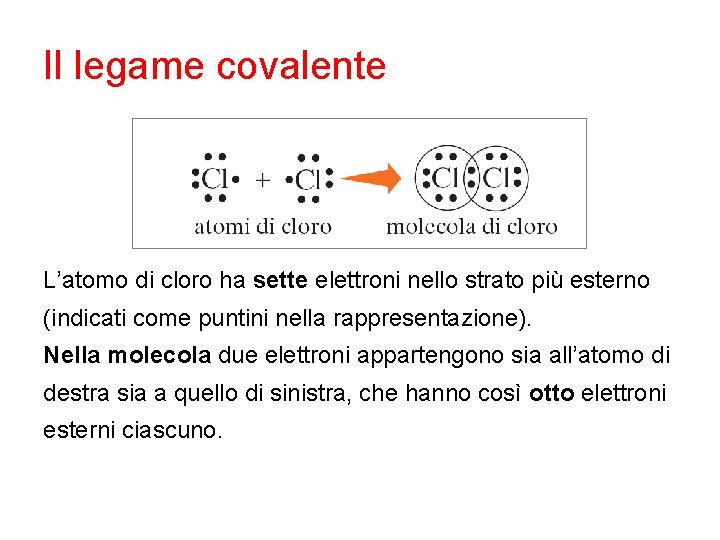
Il legame covalente L’atomo di cloro ha sette elettroni nello strato più esterno (indicati come puntini nella rappresentazione). Nella molecola due elettroni appartengono sia all’atomo di destra sia a quello di sinistra, che hanno così otto elettroni esterni ciascuno.

Il legame covalente • Se gli atomi appartengono allo stesso elemento o a elementi che hanno caratteristiche chimiche molto simili, gli elettroni sono condivisi in modo perfettamente equilibrato e si ha il legame covalente puro.
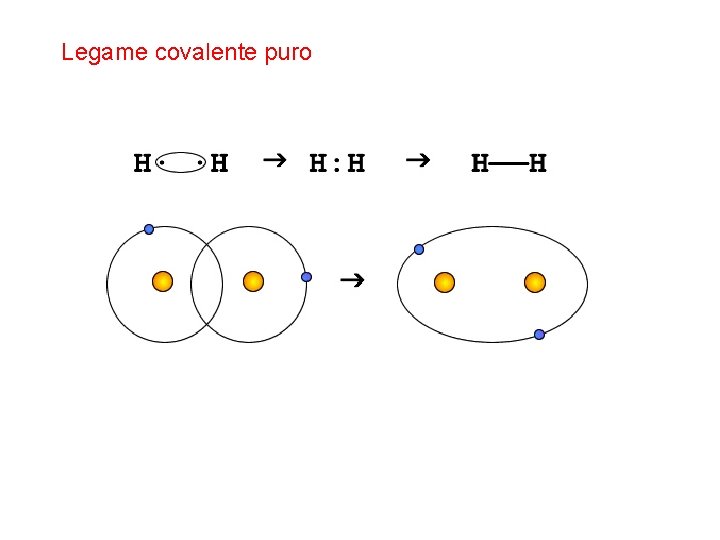
Legame covalente puro
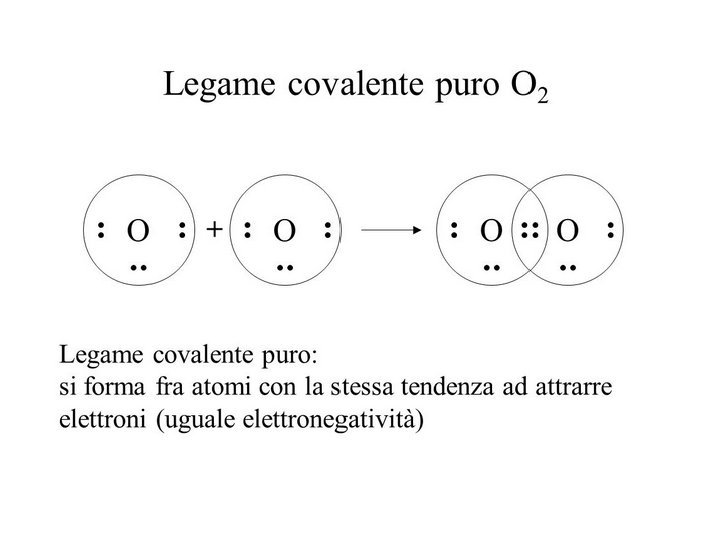

Il legame covalente • Se gli atomi appartengono a elementi differenti e con caratteristiche chimiche piuttosto diverse, gli elettroni sono più vicini all’atomo che li attrae con più forza. Si ha così il legame covalente polare.
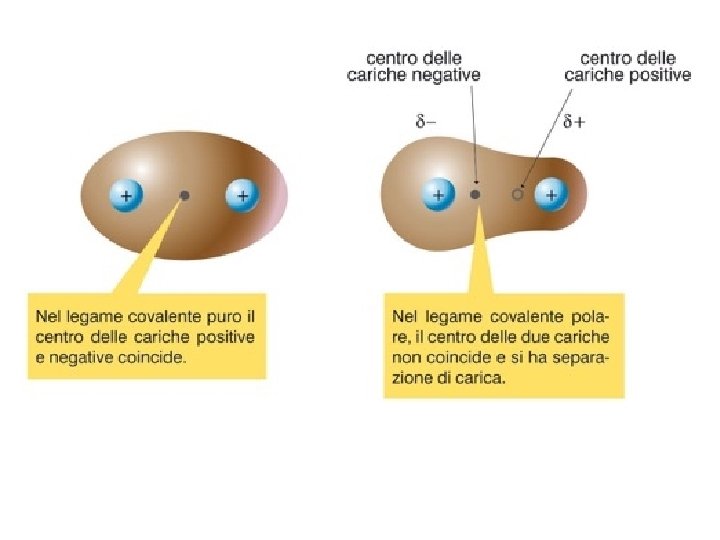
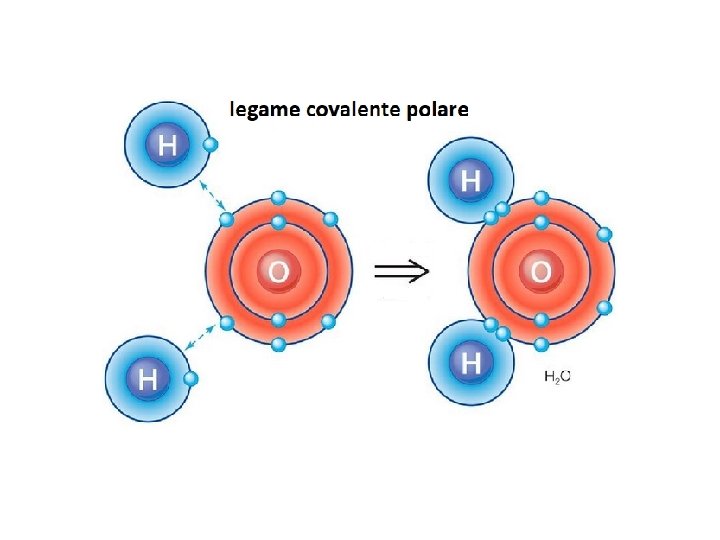

Il legame covalente
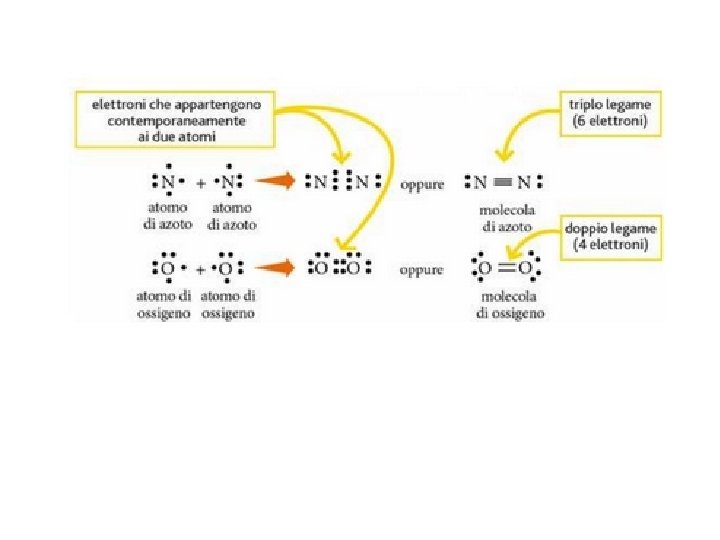

Il legame covalente I legami covalenti sono disegnati con trattini che collegano i simboli degli atomi coinvolti. Un trattino significa che c’è un solo legame (legame semplice), due trattini invece che vi è un doppio legame, tre che vi è un triplo legame.

Il legame ionico • Se gli atomi che si legano hanno caratteristiche nettamente diverse, con uno dei due che attrae gli elettroni molto più fortemente dell’altro, si avrà il completo trasferimeto di elettroni da un atomo all’altro.

Il legame ionico • L’atomo che perde gli elettroni di legame diventa ione positivo, quello che li acquista diventa ione negativo. • I due ioni sono legati da una intensa forza di attrazione elettrostatica, detta legame ionico.
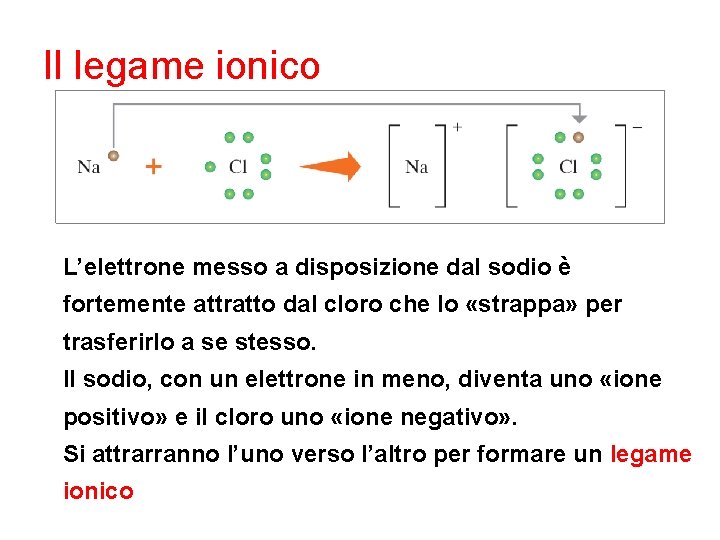
Il legame ionico L’elettrone messo a disposizione dal sodio è fortemente attratto dal cloro che lo «strappa» per trasferirlo a se stesso. Il sodio, con un elettrone in meno, diventa uno «ione positivo» e il cloro uno «ione negativo» . Si attrarranno l’uno verso l’altro per formare un legame ionico

FINE PRIMA PARTE
- Slides: 34