Las Lipasas Aplicaciones en Biotecnologa Definicin Una lipasa

Las Lipasas : Aplicaciones en Biotecnología

Definición : Una “lipasa verdadera” (EC 3. 1. 1. 3) se define como una carboxilesterasa capaz de catalizar la hidrólisis y la síntesis de acilgliceroles de cadena larga, teniendo como sustrato standard a la trioleina. Acilglicerolhidrolasas o triacilglicerolhidrolasas

Origen de las lipasas: • Las lipasas son enzimas ubicuas que pueden ser encontradas en: Microorganismos Plantas Animales • Comercialmente en su mayoría son de origen microbiano Hongos Bacterias Levaduras • Generalidades Peso molecular 20 -60 k. D Contienen 2 -15% de carbohidratos p. H óptimo = 8 -9 lipasas animales; 5. 5 -8. 5 microbianas Topt = 30 -60 o. C

Lipasas disponibles comercialmente
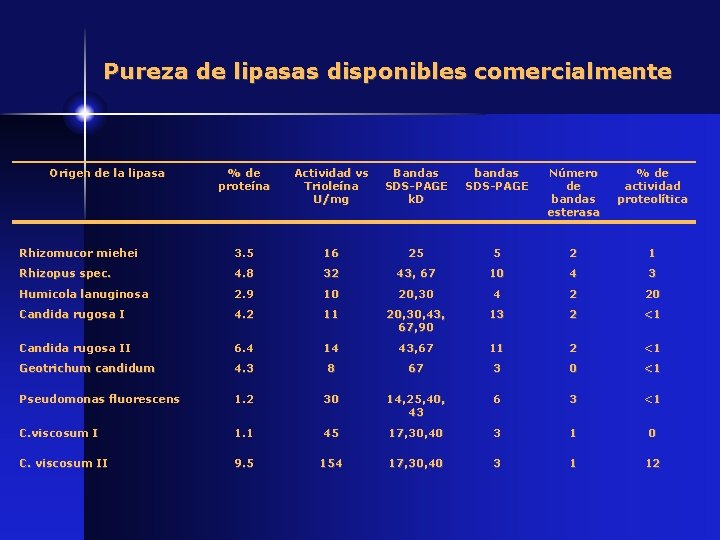
Pureza de lipasas disponibles comercialmente Origen de la lipasa % de proteína Actividad vs Trioleína U/mg Bandas SDS-PAGE k. D bandas SDS-PAGE Número de bandas esterasa % de actividad proteolítica Rhizomucor miehei 3. 5 16 25 5 2 1 Rhizopus spec. 4. 8 32 43, 67 10 4 3 Humicola lanuginosa 2. 9 10 20, 30 4 2 20 Candida rugosa I 4. 2 11 20, 30, 43, 67, 90 13 2 <1 Candida rugosa II 6. 4 14 43, 67 11 2 <1 Geotrichum candidum 4. 3 8 67 3 0 <1 Pseudomonas fluorescens 1. 2 30 14, 25, 40, 43 6 3 <1 C. viscosum I 1. 1 45 17, 30, 40 3 1 0 C. viscosum II 9. 5 154 17, 30, 40 3 1 12

Controversias en las propiedades de lipasas disponibles comercialmente Origen de la lipasa Observaciones Candida rugosa (CRL) Inicialmente clasificado como Candida cylindracea, clonación y purificación de la proteína revela al menos cinco isoformas. Geotrichum candidum (GCL) Contiene dos isoformas que se diferencían en la especificidad cis o trans en acidos grasos insaturados Rhizopus (RAL, ROL, RDL, RNL) En la literatura se reportan diferentes especificidades aunque la clonación reveló identidad casi total. Penicillium camembertii (Pe. CL) Clasificada como lipasa de P. cyclopium hasta 1990, recientemente se encontraron cuatro isoformas que difieren principalmente en el patrón de glicosilación Pseudomonas glumae (PGL) Clonación y secuenciación reveló alta identidad con la lipasa de Chromobacterium viscosum (CVL). Pseudomonas cepacia (PCL) Reclasificada en 1995 como Burkholderia cepacia. Clonación y secuenciación reveló identidad con la lipasa de Pseudomonas. sp. ATCC 21808 (PSL).
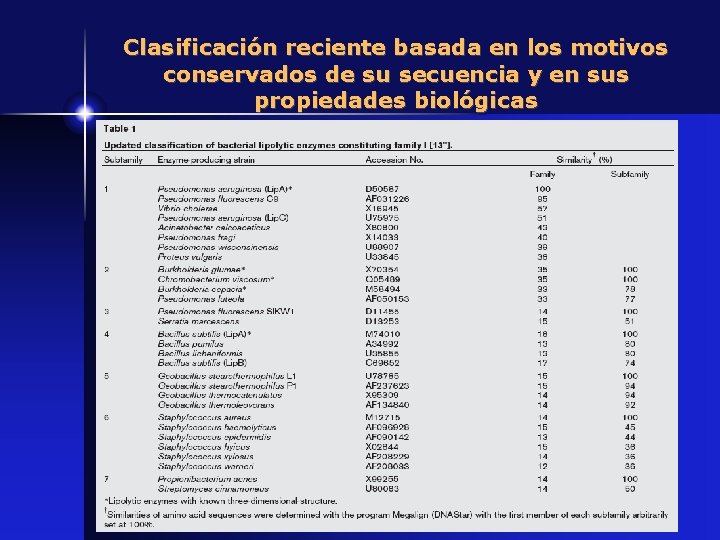
Clasificación reciente basada en los motivos conservados de su secuencia y en sus propiedades biológicas
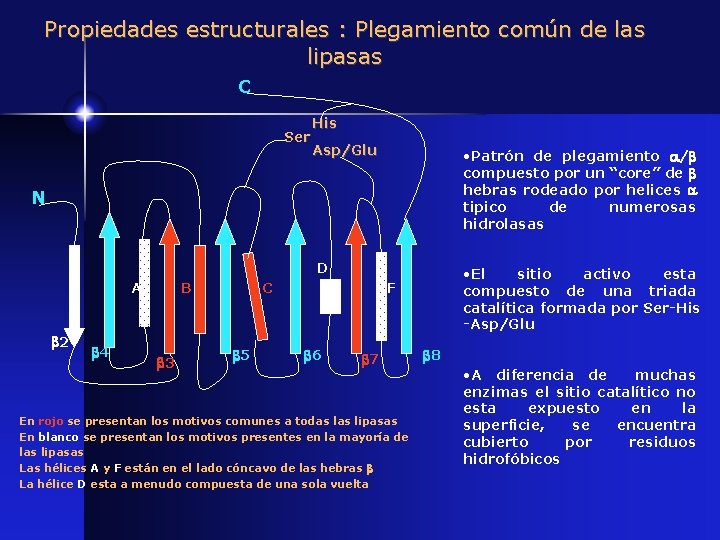
Propiedades estructurales : Plegamiento común de las lipasas C Ser His Asp/Glu • Patrón de plegamiento / compuesto por un “core” de hebras rodeado por helices tipico de numerosas hidrolasas N D A 2 4 B 3 C 5 • El sitio activo esta compuesto de una triada catalítica formada por Ser-His -Asp/Glu F 6 7 En rojo se presentan los motivos comunes a todas lipasas En blanco se presentan los motivos presentes en la mayoría de las lipasas Las hélices A y F están en el lado cóncavo de las hebras La hélice D esta a menudo compuesta de una sola vuelta 8 • A diferencia de muchas enzimas el sitio catalítico no esta expuesto en la superficie, se encuentra cubierto por residuos hidrofóbicos

Mecanismo de activación interfacial en las lipasas
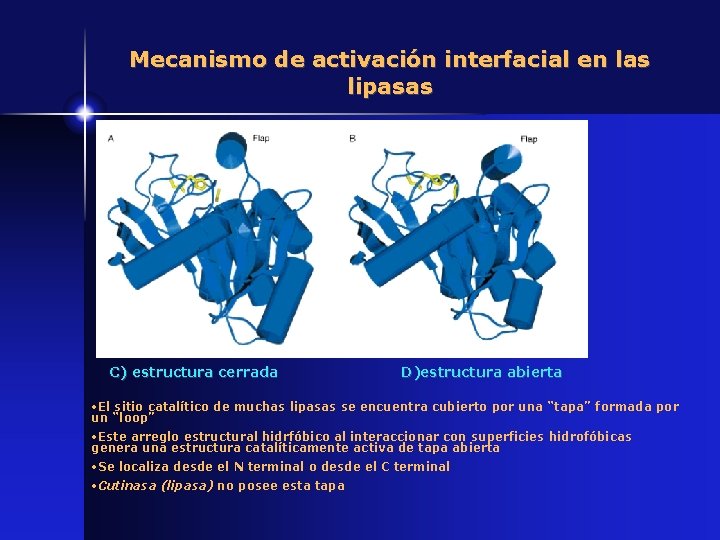
Mecanismo de activación interfacial en las lipasas C) estructura cerrada D)estructura abierta • El sitio catalítico de muchas lipasas se encuentra cubierto por una “tapa” formada por un “loop” • Este arreglo estructural hidrfóbico al interaccionar con superficies hidrofóbicas genera una estructura catalíticamente activa de tapa abierta • Se localiza desde el N terminal o desde el C terminal • Cutinasa (lipasa) no posee esta tapa

• La presencia de la tapa cubriendo el sitio activo de las lipasas y el fenómeno de activación interfacial no adecuado para distinguir lipasas de esterasas. • Varias enzimas tienen la tapa hidrofóbica pero no presentan activación interfacial • p. e. Pseudomonas glumae, Pseudomonas aeruginosa, C. antarctica B, y lipasa pancreática, lipasa

Acceso al sitio catalítico de las lipasas C) estructura cerrada D)estructura abierta • Vista de arriba de la lipas de Mucor miehei • En rojo zonas polares y en azul zonas hidrofóbicas • En amarillo sitio activo

Sitio activo y especificidad en lipasas Se han identificado cuatro sitios de reconocimiento del sustrato en el sitio activo : Un agujero oxianión y tres sitios de unión específica de los residuos acilo en los triglicéridos, sitios sn-1, sn-2, y sn-3 del glicerol sn 1 RO OR sn 2 sn 3 OR La diferencia de tamaño y del balance hidrofóbico/hidrofílico en estos sitios determina la especificidad de cada lipasa Especificidad por el tamaño de la cadena acilada Regioespecificidad sn-1, sn-2, y sn-3

Mecanismo catalítico
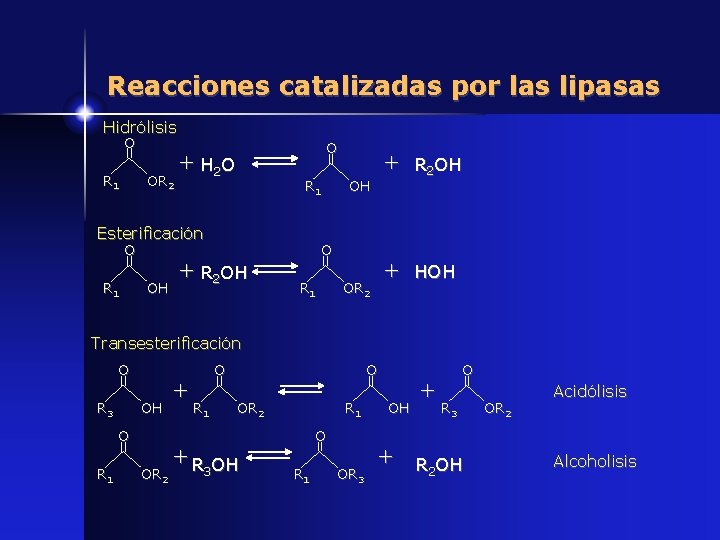
Reacciones catalizadas por las lipasas Hidrólisis O R 1 OR 2 O + H 2 O R 1 Esterificación O R 1 OH O + R 2 OH + HOH OH O R 1 + OR 2 Transesterificación O R 3 OH O R 1 OR 2 + O O R 1 OR 2 + R 3 OH O R 1 OR 3 OH + + O R 3 R 2 OH OR 2 Acidólisis Alcoholisis
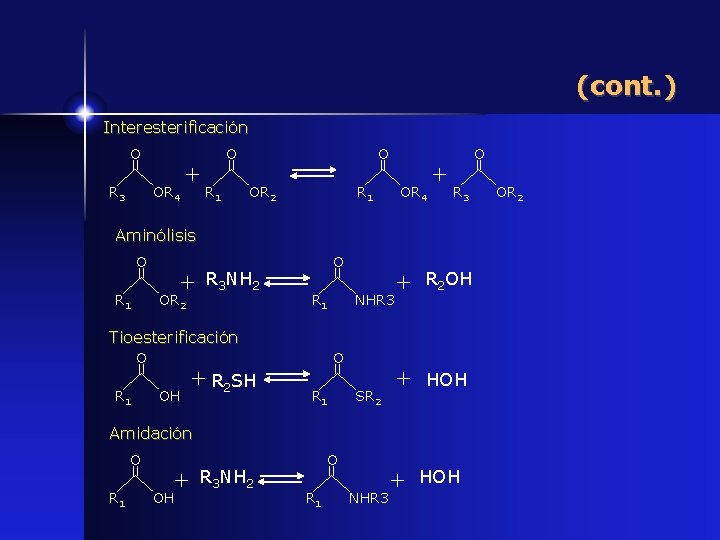
(cont. ) Interesterificación O R 3 + OR 4 O O R 1 OR 2 OR 4 + O R 3 Aminólisis O R 1 + OR 2 R 3 NH 2 O R 1 NHR 3 + R 2 OH + HOH Tioesterificación O R 1 OH + R 2 SH O R 1 SR 2 Amidación O R 1 OH + R 3 NH 2 O R 1 NHR 3 + HOH OR 2

Control del equilibrio termodinámico del proceso Control del grado de acilación de polioles Monoésteres, Diésteres, Triésteres……. . -Emulsificantes para especialidades farmacéuticas -Vehículos para medicamentos -Bloques de construcción en síntesis orgánica

Control de la posición del equilibrio termodinámico Actividad termodinámica: a = X = coeficiente de actividad X = fracción mol El coeficiente de actividad termodinámica función del número y tipo de interacciones soluto-solvente

Control de la posición del equilibrio termodinámico en reacciones laterales • Bloqueo de la síntesis de di- y triésteres por aumento de sus coeficientes de actividad • Favorecer la síntesis de monoésteres por disminución de sus coeficientes de actividad

• Coeficiente de actividad alto = baja interacción solutosolvente, baja concentración al equilibrio • Coeficiente de actividad bajo = alta interacción solutosolvente, alta concentración al equilibrio
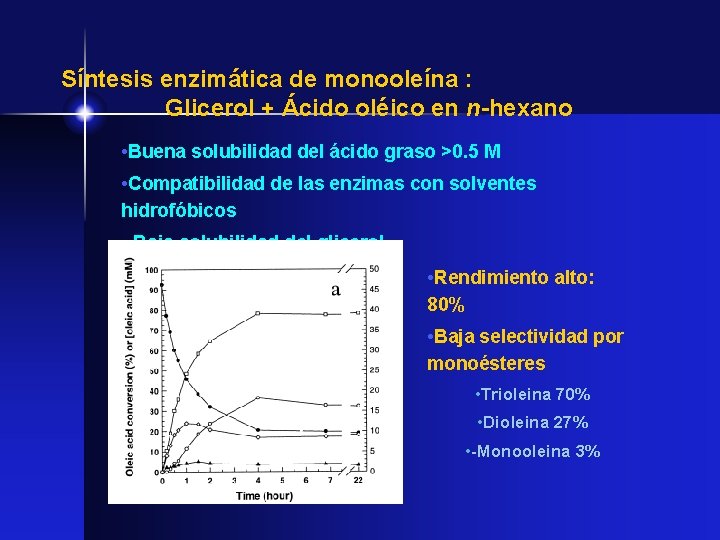
Síntesis enzimática de monooleína : Glicerol + Ácido oléico en n-hexano • Buena solubilidad del ácido graso >0. 5 M • Compatibilidad de las enzimas con solventes hidrofóbicos • Baja solubilidad del glicerol • Rendimiento alto: 80% trioleina dioleina monooleina • Baja selectividad por monoésteres • Trioleina 70% • Dioleina 27% • -Monooleina 3%

Síntesis selectiva de monoésteres de polioles
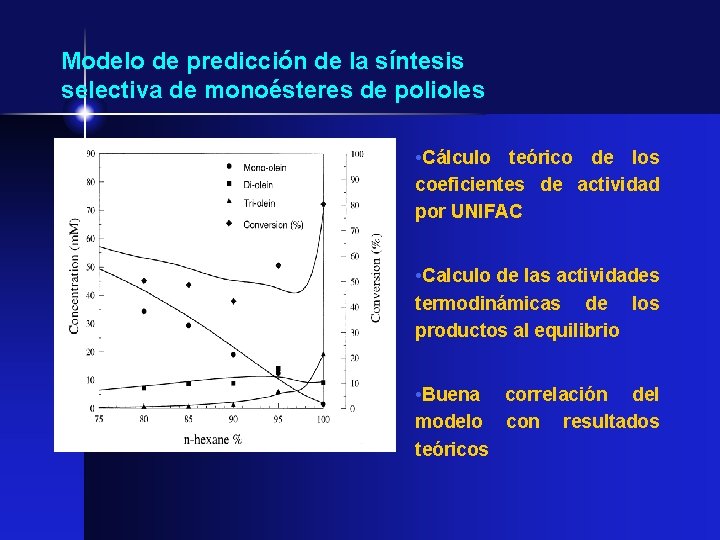
Modelo de predicción de la síntesis selectiva de monoésteres de polioles • Cálculo teórico de los coeficientes de actividad por UNIFAC • Calculo de las actividades termodinámicas de los productos al equilibrio • Buena correlación del modelo con resultados teóricos

Síntesis selectiva de monooleina por glicerólisis • Se pueden alcanzar concentraciones de producto entre 0. 5 -1 M • Proceso que se puede realizar en reactor contínuo

Síntesis selectiva de ésteres de xilitol

Síntesis selectiva de ésteres de xilitol

Coeficiente de actividad en función del parámetro de polaridad ET 30 • Predicción de la abundancia de los prooductos en función de la polaridad del medio de reacción • Evaluado para un gran número de mezclas de solventes (acetona, acetonitrilo, DMSO, hexano, 2 M 2 P, ……. . )

Control de la quimioselectividad del proceso 2 M 2 B Amida 95% Ester 52% Amida 54% Ester 95% n-hexane Baja actividad termodinámica de ésteres en nhexano Baja actividad termodinámica de amidas en 2 M 2 B

Resolución de mezclas racémicas quimioselectivamente

Síntesis de inductores selectivos de apoptosis en células cancerosas 3 -(4 -Hydroxy-3 -(S)-methoxy-phenyl)-N-[2 -(4 -hydroxy-phenyl)-2 -methoxyethyl]- acrylamide Síntesis preferencial de amidas en 2 M 2 B Reacción enantioselectiva
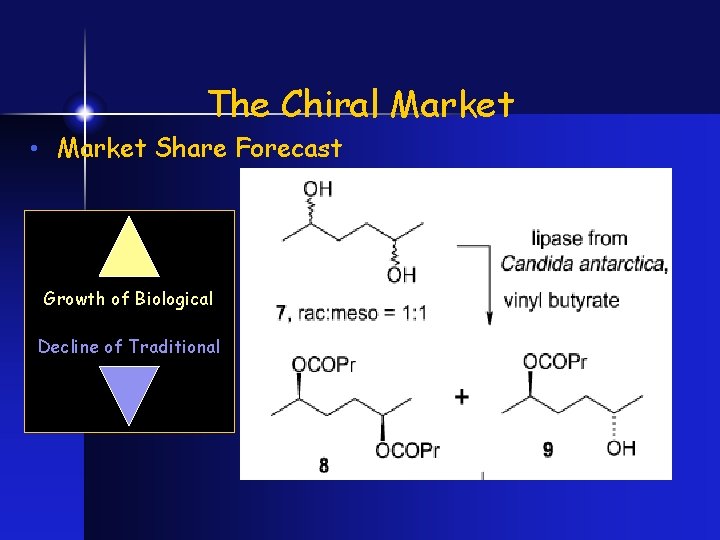
The Chiral Market • Market Share Forecast Growth of Biological Decline of Traditional
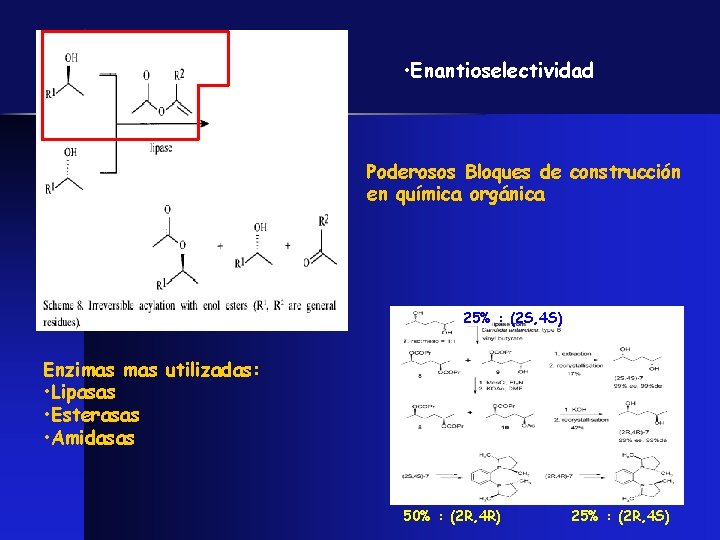
• Enantioselectividad Poderosos Bloques de construcción en química orgánica 25% : (2 S, 4 S) Enzimas utilizadas: • Lipasas • Esterasas • Amidasas 50% : (2 R, 4 R) 25% : (2 R, 4 S)

Resolución cinética con lipasas Evitar reversibilidad de la resolución

• Generación de centros quirales por acilación • Bloques de construcción en síntesis orgánica • Construcción de librerias • Resolución de centros quirales (en polioles) • Modelos moleculares para RMN

“Easy-On, Easy-Off Technology” Sintesis-hidrólisis de amidas “Imposible” la hidrólisis de amidas con lipasas Proceso altamente enantioselectivo

Sistemas de reacción para las lipasas SOLVENT SYSTEMS AND PROCESSES 1. Aqueous Reaction Media : Hidrolysis 2. Water: Water-Miscible Systems : Hydrolysis or Synthesis 3. Water: Water-Immiscible Systems : Hydrolysis or Synthesis 4. Nonaqueous Reaction Media : Synthesis 5. Anhydrous Reaction Media : Synthesis 6. Supercritical Fluids : Synthesis 7. Reverse Micellar Systems : Synthesis 8. Solvent-Free Systems : Synthesis 9. Gas-Phase Catalysis : Synthesis 10. Ionic Liquids : Synthesis Sistemas con bajo contenido de agua

PREPARATION OF MODIFIED LIPASES A. Immobilization • • • Adsorption onto solid supports such as silica gel Covalent attachment to solid supports Entrapment in organic polymers or microemulsions. B. Chemical Modification 1. Cross-Linking : • Use of glutaraldehyde to prepare insoluble cross-linked enzyme crystal (CLEC) • P. cepacia and C. antarctica lipases for CLEC-catalyzed resolution of phenyl acetate (ALTUS-Biotech)

2. Modification with Polyethylene Glycol, Polymers and Surfactants • Enhanced stability of C. rugosa lipase in isooctane by treating the enzyme with p- nitrophenyl chloroformate and cyanuric acid chloride activated PEG. • Alternative to PEG is to use the nonionic amphiphilic polyoxyethylene lauryl ether (Brij 35) as a covalent modifier • Hydrophobic polymers such as polystyrene and polymethyl methacrylate or amphiphilic polymers such as poly N-vinylpyrrolidone • Nonionic synthetic dialkyl amphiphiles or sorbitan monostearate (Span 60)

Aplicaciones industriales de las lipasas • Aplicaciones en oleoquímica : Hidrólisis de triglicéridos • Disponibilidad de materia prima, 60 millones de tons de aceites y grasas por año. • Cinco millones de toneladas para uso no alimentario • La principal aplicación es la obtención de jabones, proceso químico • El uso alternativo de las lipasas (hidrólisis de grasas y aceites) permite condiciones mas suaves, mejor calidad del producto y mejor rendimiento de glicerol como subproducto • Miyoshi Yushi, en Nagoya, Japón, la única empresa en el mundo que usa esta tecnología con Candida rugosa lipase. • Proceso en lote a 40 o. C, durante 48 horas

• Síntesis de metil- o etil- ésteres de ácidos grasos por alcoholisis : Biodiesel • An alternative source of energy for public transport is the so-called biodiesel, reduces sulfur oxide production. • METHYL ESTERS OF FATTY ACIDS • Produced chemically using oil from various plants (e. g. rapeseed). • Alcohoysis catalyzed by KOH • Can be catalysed in a single transesterification reaction using lipases in organic solvents. • At an industrial scale failed so far because of the high cost of the appropriate biocatalyst. • Two strategies were recently presented : • Immobilisation of P. fluorescens lipase increased its stability even upon repeated use • Cytoplasmic overexpression of Rhizopus oryzae lipase in Saccharomyces cerevisiae with subsequent freeze-thawing and air drying resulted in a whole-cell biocatalyst
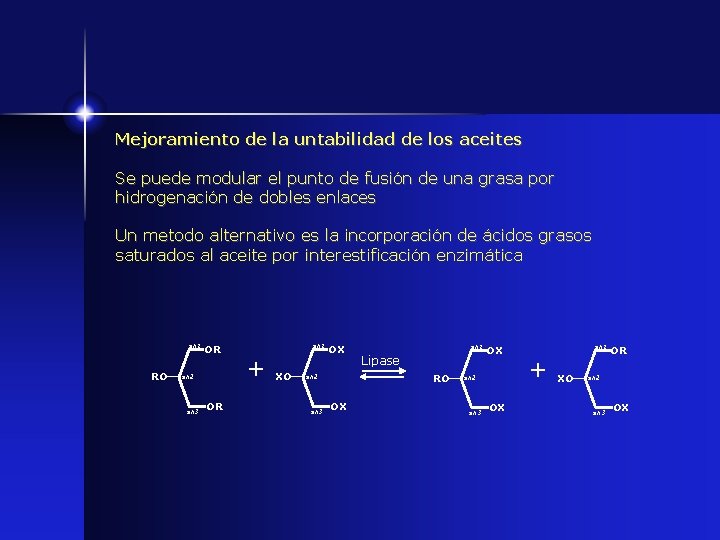
Mejoramiento de la untabilidad de los aceites Se puede modular el punto de fusión de una grasa por hidrogenación de dobles enlaces Un metodo alternativo es la incorporación de ácidos grasos saturados al aceite por interestificación enzimática sn 1 RO OR sn 2 sn 3 OR sn 1 + XO OX Lipase RO sn 2 sn 3 sn 1 OX OX sn 2 sn 3 OX sn 1 + XO OR sn 2 sn 3 OX

Síntesis de sustitutos de grasa de cacao • En 1995 100, 000 toneladas de grasa de cacao fueron exportadas por Kenia y Malasia • Grasa con demanda en alimentos y farmacia (Pf = 37 o. C) sn 1 XO OR Para X = oléico, Y = esteárico y R = palmítico sn 2 sn 3 OY Grasa de cacao compuesta de SOS o SOP primordialmente • Interesterificación enzimática del aceite de palma (POP) o de girasol (OOO) con ácido esteárico o triesterarina (SSS). • Uso de lipasas 1, 3 específicas en proceso limpio • Unichema (ICI) produce varios cientos de toneladas y Fuji Oil varios miles de toneladas utilizando lipasas de Rhizopus.

Grasas de alta digestibilidad • Mejoramiento en la absorción de triglicéridos • Triglicéridos con palmítico en posición sn-2 mejor absorción sn 1 XO OR Para X = palmítico sn 2 sn 3 OY Grasas de alta digestibilidad, p. e. leche materna • Unichema produce OPO en dietas para niños prematuros por interestirificación de tripalmitina y ácido oléico • Otro tipo de grasas de facil digestión son MLM (M=medium, L=long refiriendose al tamaño de cadena acilada) • “Caprenin” (C 6, C 22: 0, C 8) producido por Procter&Gamble mediante síntesis química

Síntesis de emulsificantes • Monoglicéridos emulsificantes mas utilizados en la industria de alimentos • 150, 000 ton preparadas por glicerólisis química a partir de triglicéridos • Los métodos enzimáticos incluyen : Esterificación y glicerólisis • Bajos rendimientos y proceso económicamente desfavorable • Necesidad de abaratar el costo del biocatalizador y aumentar su estabilidad operacional

Aplicaciones diversas (Hidrólisis) • Detergentes: Remoción de productos lipídicos • Productos comerciales : Lipolasa de Novo-Nordisk, Lipomax de Gist-Brocades y Lumafast de Genencor. • Industria papelera : Eliminación de triglicéridos de pulpa de celulosa o eliminación de tintas a base de lípidos en papel reciclado por Nihon Seishi Co. , • Industria de lacteos : mejorar la calidad de cuajadas, generación de aromas y sabores en quesos o preparación de aditivos a partir de productos lacteos
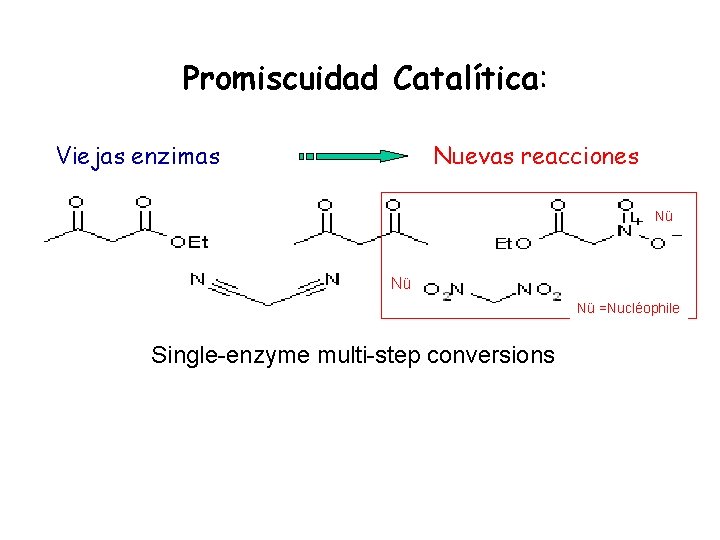
Promiscuidad Catalítica: Viejas enzimas Nuevas reacciones Nü Nü Nü =Nucléophile Single-enzyme multi-step conversions

“Catalytic promiscuity in enzymes is the ability of enzyme active sites to catalyze more than one chemical transformation” • Posibilidad de las enzimas para reaccionar sobre: • Diferentes grupos funcionales • Diferentes tipos de enlace • Diferente mecanismo de reacción Angew. Chem. Int Ed. 2004, 43, 6032 -6040 47
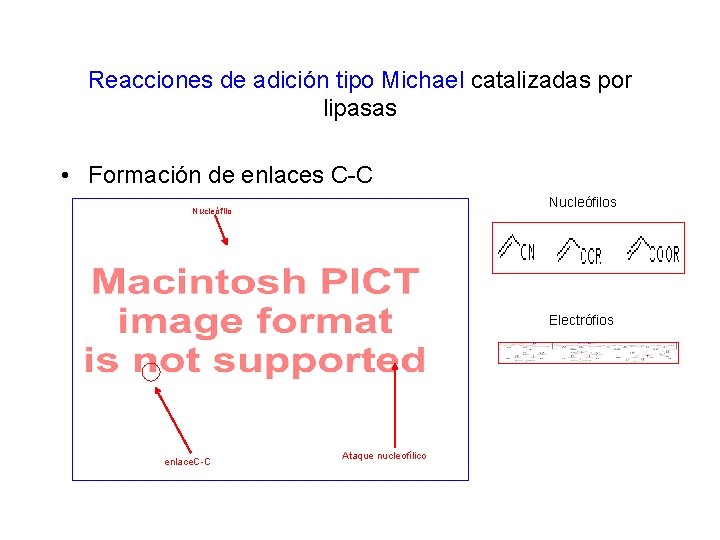
Reacciones de adición tipo Michael catalizadas por lipasas • Formación de enlaces C-C Nucleófilos Nucleófilo Electrófios enlace. C-C Ataque nucleofílico 48

50°C Solvant organique a) Torre, O. ; Alfonso, I. ; Gotor, V. ; Chem. Commun. 2004, 1724; 14; b) Cai, Y. ; Wu, Q. ; Xiao, Y. M. ; Lv, D. S. ; Lin, X. F. J. of Biotech. , 2006. 49
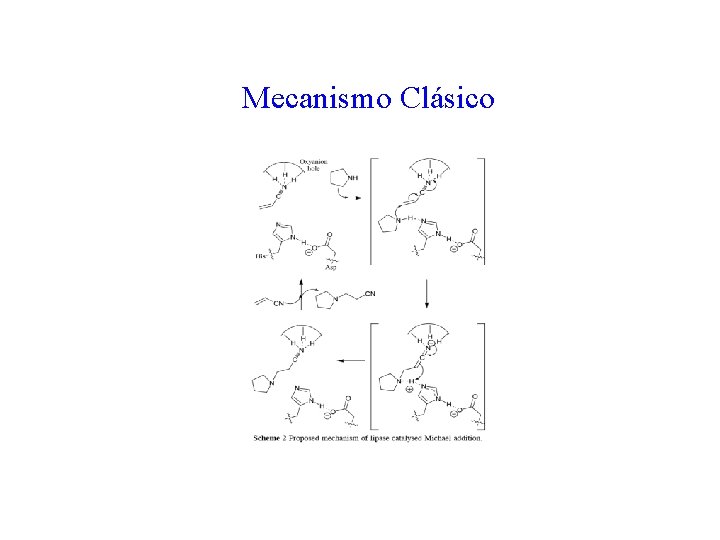
Mecanismo Clásico 50

Mecanismo propuesto para Ser-Hidrolasas Acido de Lewis Transferencia de protón Acido-Base Desplazamiento catalítico 51

But : Preparación de intermediarios de la síntesis de b-aminoácidos con estereo quuimica específica 52

Esters a, b insaturés Amines primaires Ammonium Benzylamine (R) and (S) phenylethylamine 53

Figure 1. Hypothetical catalytic addition of benzylamine to methyl crotonate in the active site of Ca. L-B. The carbonyl oxygen of the , -unsaturated is bound to the oxyanion hole and the nucleophile is activated by His. 54

Posibles reacciones Adición 1, 4 Adición 1, 2 Doble Adición 1, 4 Se ha reportado la formación preferencial de amidas : • Solventes no polares • Bajas concentraciones de sustrato (Metil acrilato) • Temperaturas ≈ 45 ºC 55
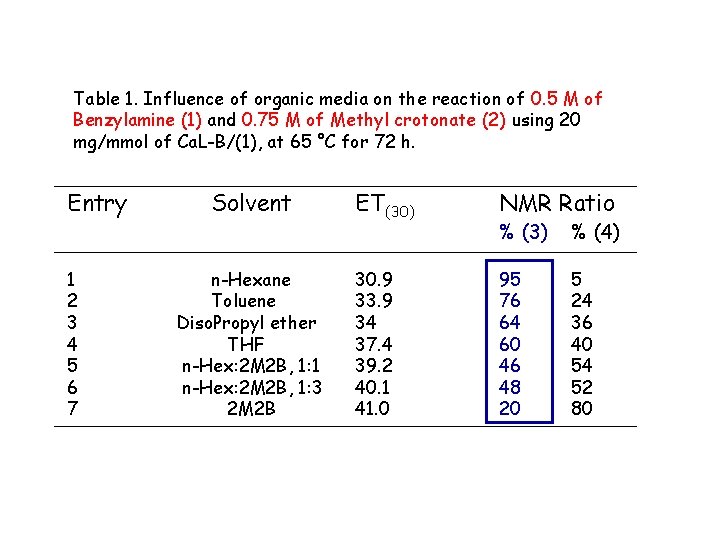
Table 1. Influence of organic media on the reaction of 0. 5 M of Benzylamine (1) and 0. 75 M of Methyl crotonate (2) using 20 mg/mmol of Ca. L-B/(1), at 65 °C for 72 h. Entry 1 2 3 4 5 6 7 Solvent n-Hexane Toluene Diso. Propyl ether THF n-Hex: 2 M 2 B, 1: 1 n-Hex: 2 M 2 B, 1: 3 2 M 2 B ET(30) NMR Ratio % (3) % (4) 30. 9 33. 9 34 37. 4 39. 2 40. 1 41. 0 95 76 64 60 46 48 20 5 24 36 40 54 52 80 56

Changes in polarity of reaction media describing the profile of (A) Michael adduct (3) and (B) aminolysis product (4) as a function of empirical polarity parameters ET(30). 57
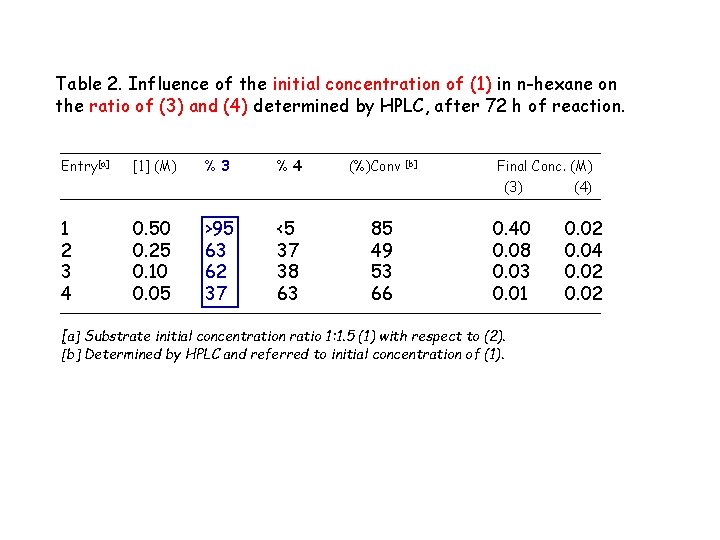
Table 2. Influence of the initial concentration of (1) in n-hexane on the ratio of (3) and (4) determined by HPLC, after 72 h of reaction. Entry[a] [1] (M) %3 %4 1 2 3 4 0. 50 0. 25 0. 10 0. 05 >95 63 62 37 <5 37 38 63 (%)Conv 85 49 53 66 [b] Final Conc. (M) (3) (4) 0. 40 0. 08 0. 03 0. 01 0. 02 0. 04 0. 02 [a] Substrate initial concentration ratio 1: 1. 5 (1) with respect to (2). [b] Determined by HPLC and referred to initial concentration of (1). 58
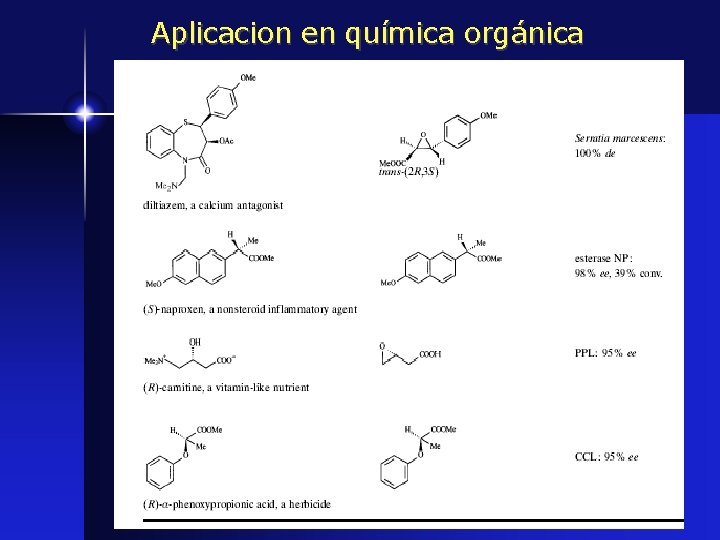
Aplicacion en química orgánica
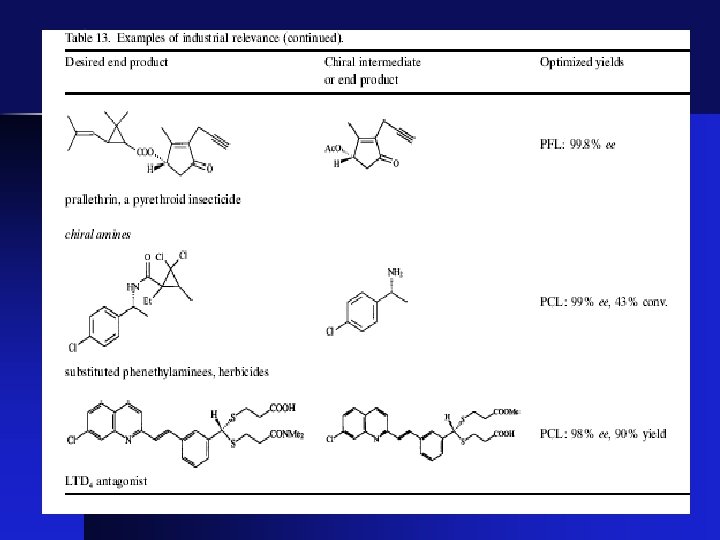


Las Lipasas : Aplicaciones en Biotecnología
- Slides: 62