Las columnas verticales reciben el nombre de GRUPOS


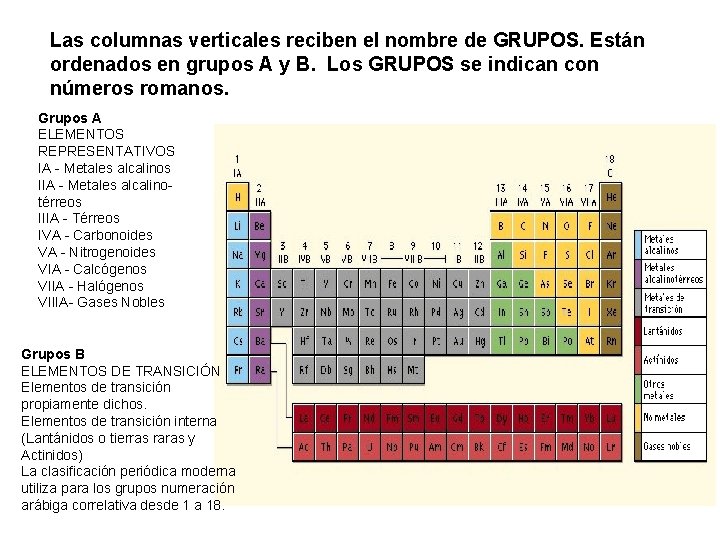
Las columnas verticales reciben el nombre de GRUPOS. Están ordenados en grupos A y B. Los GRUPOS se indican con números romanos. Grupos A ELEMENTOS REPRESENTATIVOS IA - Metales alcalinos IIA - Metales alcalinotérreos IIIA - Térreos IVA - Carbonoides VA - Nitrogenoides VIA - Calcógenos VIIA - Halógenos VIIIA- Gases Nobles Grupos B ELEMENTOS DE TRANSICIÓN Elementos de transición propiamente dichos. Elementos de transición interna (Lantánidos o tierras raras y Actinidos) La clasificación periódica moderna utiliza para los grupos numeración arábiga correlativa desde 1 a 18.

GRUPOS (o FAMILIAS) FAMILIAS Los elementos de un mismo grupo, tienen propiedades químicas semejantes, ya que tienen el mismo número de electrones en su capa de valencia (última capa electrónica) y están distribuidos en orbitales del mismo tipo Por ejemplo, los elementos del grupo 17: Configuración electrónica Elemento Flúor Cloro Bromo Yodo Configuración más externa 1 s 2 2 p 5 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 5 ns 2 np 5 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 5 s 2 5 p 5 Estos hechos sugieren que las propiedades químicas de un elemento están relacionadas con la configuración electrónica de su capa de valencia

3. - Metales de transición Están situados en la parte central del sistema periódico, son los elementos de los grupos B, cuya principal característica es que tienen el subnivel d parcialmente ocupado. Presentan una configuración electrónica externa ns (n-1)d. Ejemplo: Sc; Z=21 = [ Ar] 4 s 2 3 d 1 4. - Metales de transición interna (Lantánidos y Actínidos Estos elementos presentan el subnivel f parcialmente ocupado y su configuración electrónica externa es del tipo ns (n-2)f. Lantánidos (números atómicos desde 58 al 71), se está ocupando el subnivel 4 f. Actínidos (números atómicos desde 90 al 103) se está ocupando el subnivel 5 f.


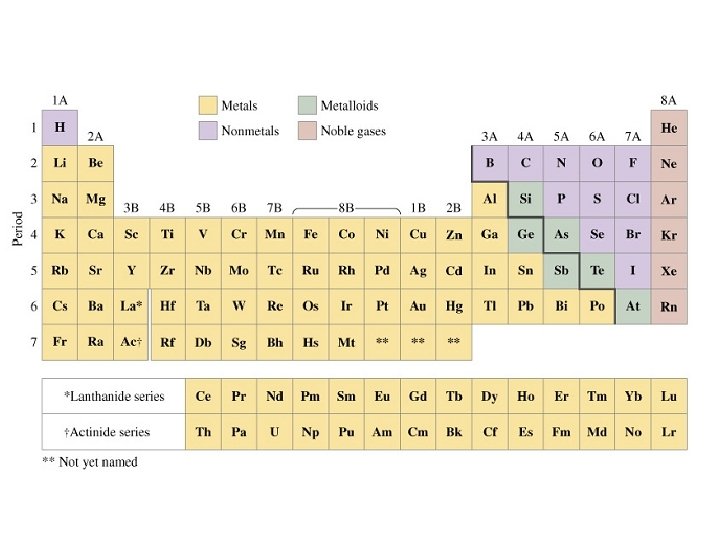


TENDENCIAS PERIÓDICAS
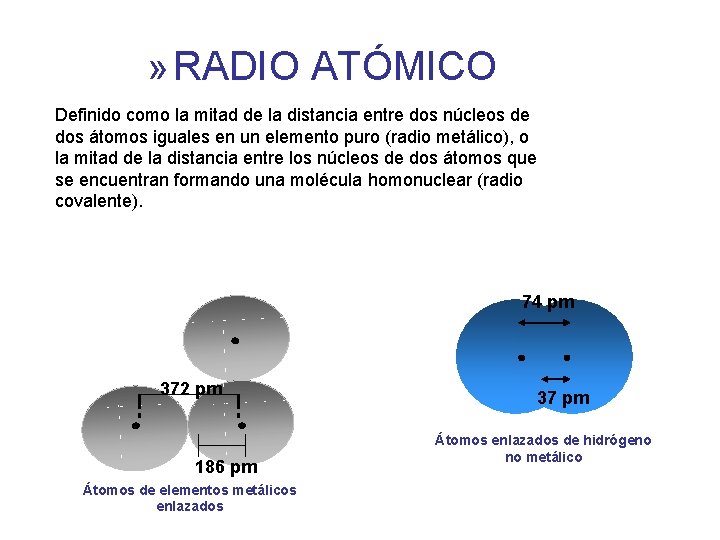
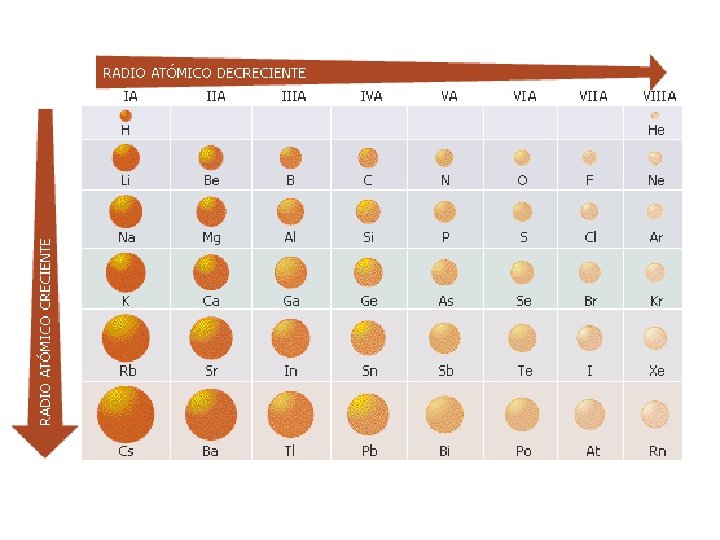
» RADIO ATÓMICO Definido como la mitad de la distancia entre dos núcleos de dos átomos iguales en un elemento puro (radio metálico), o la mitad de la distancia entre los núcleos de dos átomos que se encuentran formando una molécula homonuclear (radio covalente). 74 pm 372 pm 186 pm Átomos de elementos metálicos enlazados 37 pm Átomos enlazados de hidrógeno no metálico
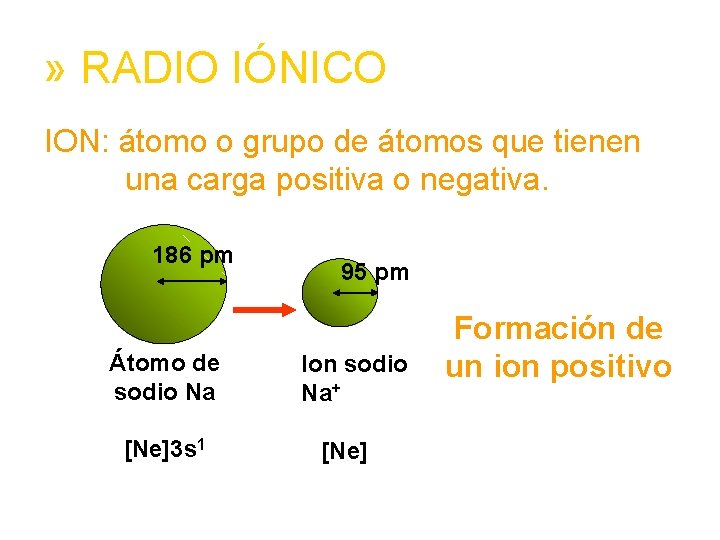
» RADIO IÓNICO ION: átomo o grupo de átomos que tienen una carga positiva o negativa. 186 pm Átomo de sodio Na [Ne]3 s 1 95 pm Ion sodio Na+ [Ne] Formación de un ion positivo
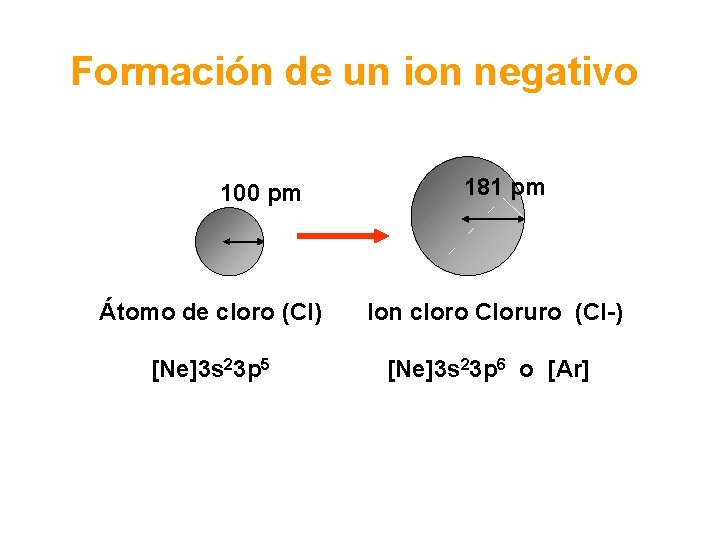
Formación de un ion negativo 100 pm 181 pm Átomo de cloro (Cl) Ion cloro Cloruro (Cl-) [Ne]3 s 23 p 5 [Ne]3 s 23 p 6 o [Ar]
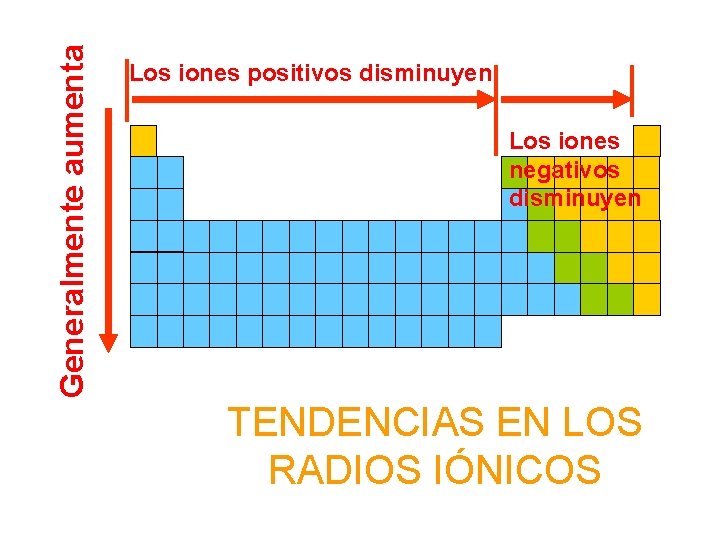
Generalmente aumenta Los iones positivos disminuyen Los iones negativos disminuyen TENDENCIAS EN LOS RADIOS IÓNICOS

» ENERGÍA DE IONIZACIÓN « § Es la energía necesaria para remover un electrón de un átomo gaseoso. § La energía necesaria para remover el primer electrón de un átomo se denomina primera energía de ionización, la energía necesaria para remover el segundo electrón del un átomo es la segunda energía de ionización y así sucesivamente.
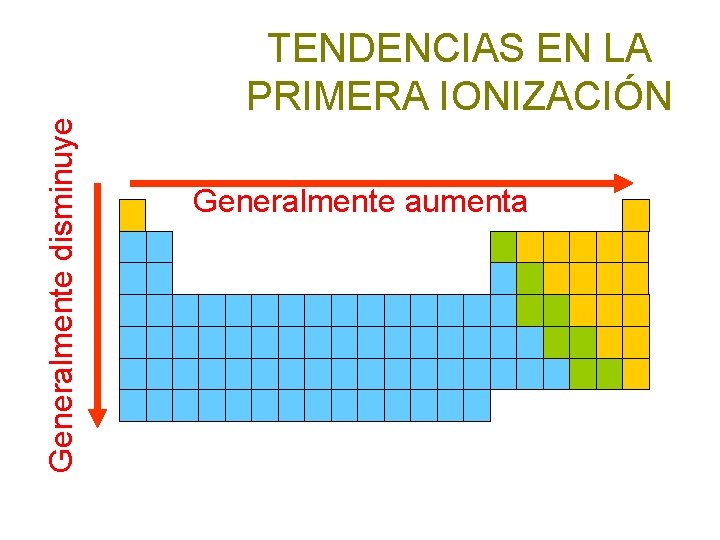
Generalmente disminuye TENDENCIAS EN LA PRIMERA IONIZACIÓN Generalmente aumenta

§ REGLA DEL OCTETO § Los átomos tienden a perder, ganar o compartir electrones para adquirir un juego de ocho electrones de valencia. Orbitales s y p llenos= ESTABILIDAD Los elementos del primer periodo son la excepción a la regla.

» ELECTRONEGATIVIDAD « § Capacidad relativa de los átomos de un elemento de atraer electrones a un enlace químico. § Las unidades de electronegatividad se denominan Paulings. § El Fluor es el elemento más electronegativo, con un valor de 3. 98. El cesio y el francio son los elementos menos electronegativos, son valores de 0. 79 y 0. 70 respectivamente
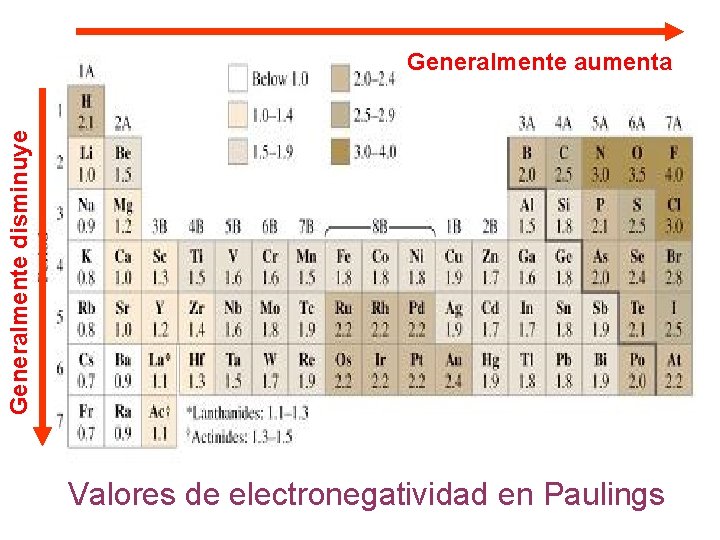
Generalmente disminuye Generalmente aumenta Valores de electronegatividad en Paulings
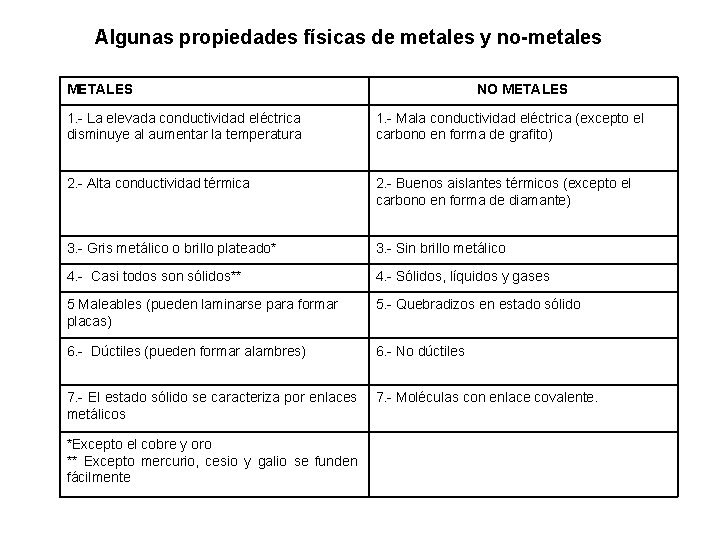
Algunas propiedades físicas de metales y no-metales METALES NO METALES 1. - La elevada conductividad eléctrica disminuye al aumentar la temperatura 1. - Mala conductividad eléctrica (excepto el carbono en forma de grafito) 2. - Alta conductividad térmica 2. - Buenos aislantes térmicos (excepto el carbono en forma de diamante) 3. - Gris metálico o brillo plateado* 3. - Sin brillo metálico 4. - Casi todos son sólidos** 4. - Sólidos, líquidos y gases 5 Maleables (pueden laminarse para formar placas) 5. - Quebradizos en estado sólido 6. - Dúctiles (pueden formar alambres) 6. - No dúctiles 7. - El estado sólido se caracteriza por enlaces metálicos 7. - Moléculas con enlace covalente. *Excepto el cobre y oro ** Excepto mercurio, cesio y galio se funden fácilmente
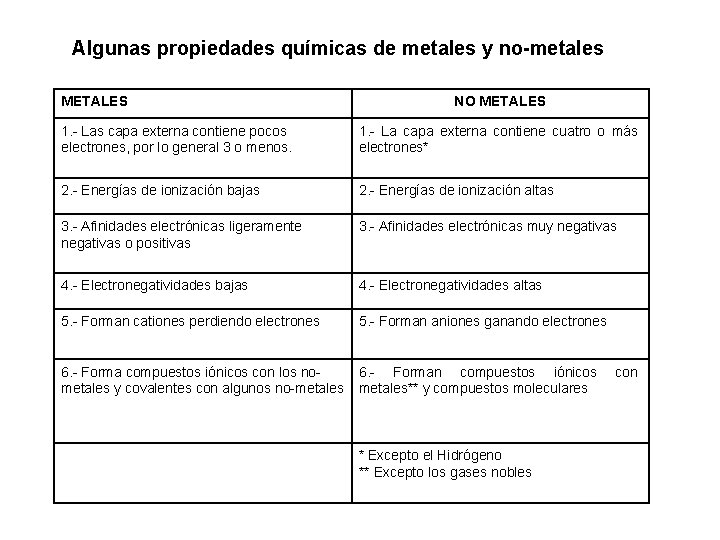
Algunas propiedades químicas de metales y no-metales METALES NO METALES 1. - Las capa externa contiene pocos electrones, por lo general 3 o menos. 1. - La capa externa contiene cuatro o más electrones* 2. - Energías de ionización bajas 2. - Energías de ionización altas 3. - Afinidades electrónicas ligeramente negativas o positivas 3. - Afinidades electrónicas muy negativas 4. - Electronegatividades bajas 4. - Electronegatividades altas 5. - Forman cationes perdiendo electrones 5. - Forman aniones ganando electrones 6. - Forma compuestos iónicos con los nometales y covalentes con algunos no-metales 6. - Forman compuestos iónicos metales** y compuestos moleculares * Excepto el Hidrógeno ** Excepto los gases nobles con
- Slides: 22