LARUTAN 10262020 Solution Process Solute intermolecular forces Combine

LARUTAN 10/26/2020
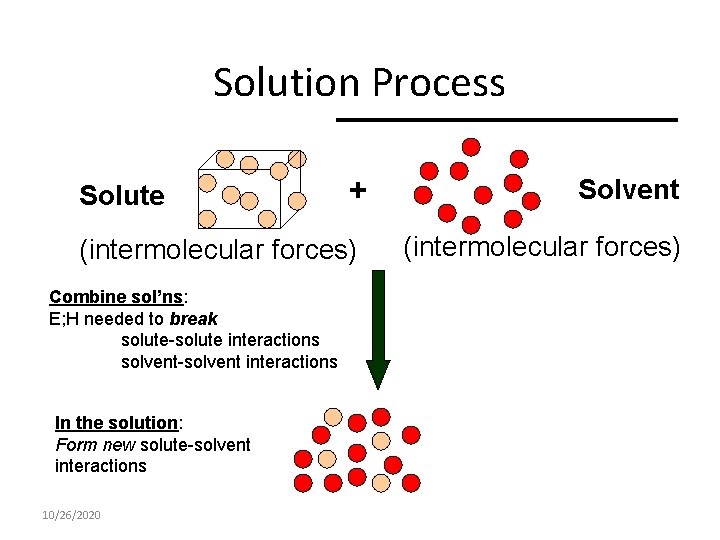
Solution Process Solute + (intermolecular forces) Combine sol’ns: E; H needed to break solute-solute interactions solvent-solvent interactions In the solution: Form new solute-solvent interactions 10/26/2020 Solvent (intermolecular forces)
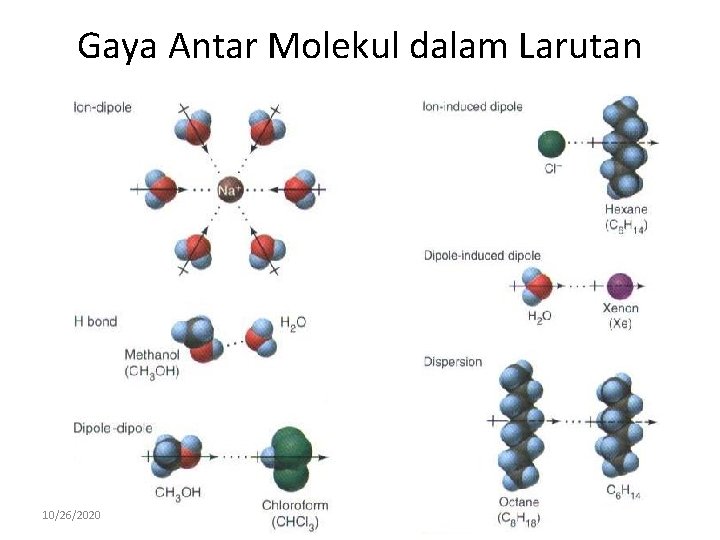
Gaya Antar Molekul dalam Larutan 10/26/2020
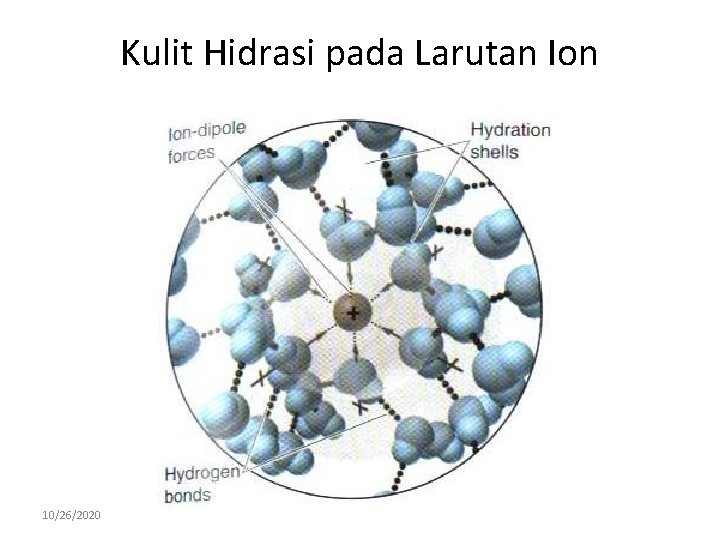
Kulit Hidrasi pada Larutan Ion 10/26/2020

Perubahan Energi dalam Proses Pelarutan • Agar suatu zat dapat larut ada 3 tahapan: 1. Partikel solut harus terpisah satu sama lain 2. Beberapa partikel solven harus terpisah untuk memberi ruang bagi partikel solut 3. Partikel solut dan solven harus bercampur menjadi satu • • Energi akan diserap saat terjadi pemisahan partikel sebaliknya energi akan dilepas ketika partikel bergabung dan tertarik satu sama lain Kesimpulannya pelarutan akan disertai perubahan entalpi 10/26/2020

Concentration = the quantity or amount of solute in a standard quantity of solution. Eg. Units: mol/L We also use the relative terms : dilute and concentrated A solution is dilute, when the solute concentration is low A solution is concentrated when the solute concentration is high. 10/26/2020

Concentration Units Molarity (M) : moles solute per L solution Molality (m) : moles solute per Kg solvent Mole fxn (X): mole “part” per mole “whole” Bagian per massa : jumlah massa solut per jumlah massa larutan Bagian per volume : volume solut per volume larutan Dll… 10/26/2020

Example of Molality (m) Find the molality of a solution prepared by adding 20 g of Na. Cl to 750 m. L of water? Molality = moles solute / kg Solvent (always just find these two numbers, and divide) Moles solute = 20 g Na. Cl x (1 mol/58 g) = 0. 3 mol Na. Cl Kg solv= 750 ml H 2 O (1. 0 g H 2 O/1. 0 m. L H 2 O) 1 kg/1000 g = 0. 75 kg H 2 O Molality = 0. 3 mol / 0. 75 kg = 0. 4 m 10/26/2020

Example of mol fxn (C) What is the mole fraction of Na. Cl in a sol’n prepared by adding 20 g of Na. Cl to 750 m. L of water? C= mol “part” / mol “whole” ‘part’ = Na. Cl 20 g Na. Cl x (1 mol/58 g) = 0. 3 mol Na. Cl 750 ml H 2 O (1. 0 g H 2 O/1. 0 m. L H 2 O) (1 mol H 2 O/18 g H 2 O) = 41. 7 mol CNa. Cl = (0. 3 mol Na. Cl/ 0. 3 mol Na. Cl + 41. 7 mol H 2 O) = (0. 3 mol /42 mol) = 0. 007 CH 2 O = (41. 7 mol H 2 O / 0. 3 mol Na. Cl + 41. 7 mol H 2 O) = (0. 3 mol /42 mol) = 0. 993 10/26/2020

Another Example The mol fxn all components in sol’n must sum to 1. 0. A solution of Na. Cl, KCl, and H 2 O is 0. 4 KCl and 0. 1 Na. Cl, and is 100 g of water. What is the mass of KCl and Na. Cl? XH 2 O + XNa. Cl + XKCl = 1. 0 XH 2 O = 0. 5 100 g H 2 O x 1 mol/18 g = 5. 6 mol H 2 O XH 2 O = 0. 5 = 5. 6 mol/z and z = 11. 2 mol total 11. 2 moltotal - 5. 6 mol H 2 O = 5. 6 mol salts KCl and Na. Cl if : 10/26/2020 x = mol Na. Cl then KCl = 4 x and 5 x = 5. 6 mol

Exercise Calculating molarity from mass and volume. 1. A student prepared a solution by dissolving 1. 345 g of potassium nitrate (KNO 3) in enough water to prepare 25. 00 m. L of solution. What is the molarity (concentration) of the solution? 2. Larutan yang dibuat dengan mencampur 1 g etanol dengan 100 g air membentuk larutan dengan volume 101 m. L. Tentukan molaritas, molalitas, fraksi mol dan % massa dari etanol! 10/26/2020

Example Or the other way around!! Calculate the mass of potassium permanganate needed to prepare 250 m. L of 0. 0380 M KMn. O 4 (aq) solution. 10/26/2020

Dilution It is often necessary to reduce the concentration of a solution - that is to dilute it. This can be accomplished by taking a certain volume of the more concentrated solution and then diluting it with additional solvent. NB - during dilution the number of moles of solute remains constant. 10/26/2020

The Dilution Equation For initial solution : M 1 x V 1 = n 1 For final solution : M 2 x V 2 = n 2 However n 1 = n 2 therefore : M 1 x V 1 = M 2 x V 2 or : 10/26/2020 M 1 V 1 = M 2 V 2

Example Diluting a solution Calculate the volume of 0. 0155 M HCl that we should use to prepare 100 m. L of a 5. 23 x 10 -4 M HCl solution. M 1 = 0. 0155 M V 1 = ? M 2 = 5. 23 x 10 -4 M V 2 = 100 m. L 10/26/2020

Volumetric Analysis A titration is a procedure for determining the amount of substance A by adding a carefully measured volume of a solution with a known concentration of B until the reaction of A and B is just complete. A 10/26/2020 B A+B

Example Calculating the Quantity of a Substance in a Titrated Solution A dilute solution of hydrogen peroxide is sold in pharmacies as a mild antiseptic. A typical solution was analyzed for the percentage of hydrogen peroxide by titrating it with potassium permanganate. 5 H 2 O 2 + 2 KMn. O 4 + 6 H+ 8 H 2 O + 5 O 2 + 2 K+ + Mn 2+ What is the mass percentage of H 2 O 2 in a solution if 57. 5 g of peroxide solution required 38. 9 m. L of 0. 534 M KMn. O 4? 10/26/2020

Soal Latihan • Berapa molalitas larutan yang dibuat dengan melarutkan 32 g Ca. Cl 2 dalam 271 g air? • Berapa gram glukosa (C 6 H 12 O 6) yang harus dilarutkan dalam 563 g etanol (C 2 H 5 OH) untuk membuat larutan dengan konsentrasi 2, 40 x 10 -2 m? • Hitung ppm (massa) kalsium dalam 3, 50 g pil yang mengandung 40, 5 mg Ca! • Hidrogen peroksida adalah zat pengoksidasi yang berguna dalam pemutih, bahan bakar roket dll. Larutan encer H 2 O 2 30% (m/m) memiliki densitas 1, 11 g/m. L hitung (a) molalitas (b) fraksi mol H 2 O 2 (c) molaritas

Sifat Koligatif Larutan • Ada 4 sifat larutan yang sangat dipengaruhi oleh kuantitas solut dalam larutan 4 sifat koligatif (kolektif) • Sifat itu adalah penurunan tekanan uap, kenaikan titik didih, penurunan titik beku dan tekanan osmotik • Awal mulanya sifat koligatif digunakan untuk melihat pengaruh solut elektrolit dan non elektrolit terhadap sifat larutan

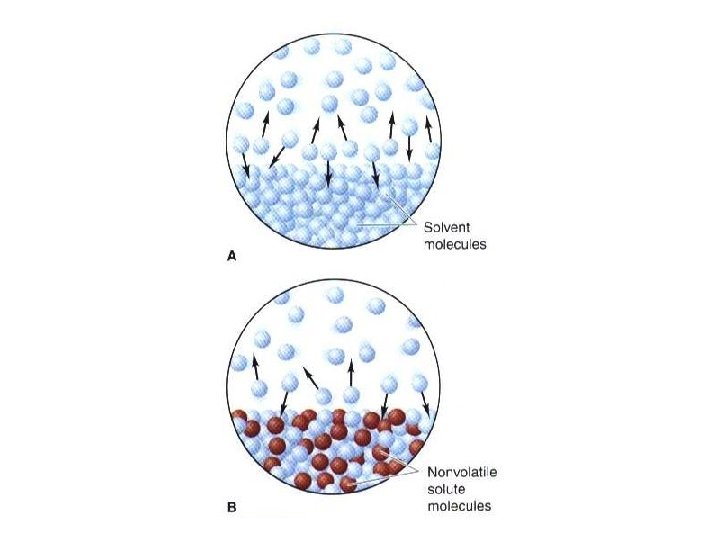
Penurunan Tekanan Uap • Untuk solut dengan karakter non volatil dan non elektrolit seperti gula, solut ini tidak terdisosiasi dan tidak menguap • Tekanan uap pelarut murni lebih besar dari larutan karena pada yang murni kecenderungan uap memicu entropi besar • Sedangkan pada larutan dengan solut entropi besar sudah ada dalam larutan sehingga penguapan menjadi berkurang • Hukum Raoult: Psolven = Xsolven × P 0 solven Xsolven + Xsolut = 1 atau Xsolven = 1 - Xsolut

Kenaikan Titik Didih • Karena tekanan uap larutan lebih rendah (turun) dibanding pelarut murni, maka konsekuensinya larutan juga akan mendidih pada suhu yang lebih tinggi • Titik didih larutan adalah suhu dimana tekanan uap sama dengan tekanan eksternal (1 atm) ΔTb ∞ m atau ΔTb = Kb × m • Dimana m molalitas larutan dan Kb adalah konstanta kenaikan titik didih molal ΔTb = Tb(larutan) – Tb(solven)
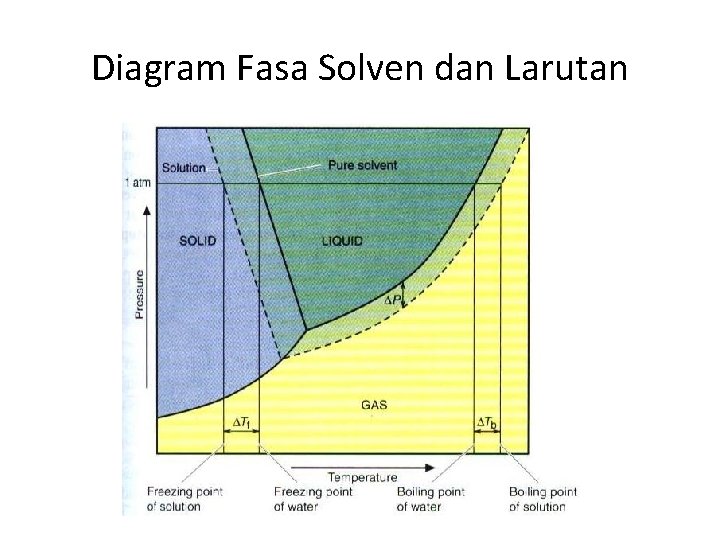
Diagram Fasa Solven dan Larutan
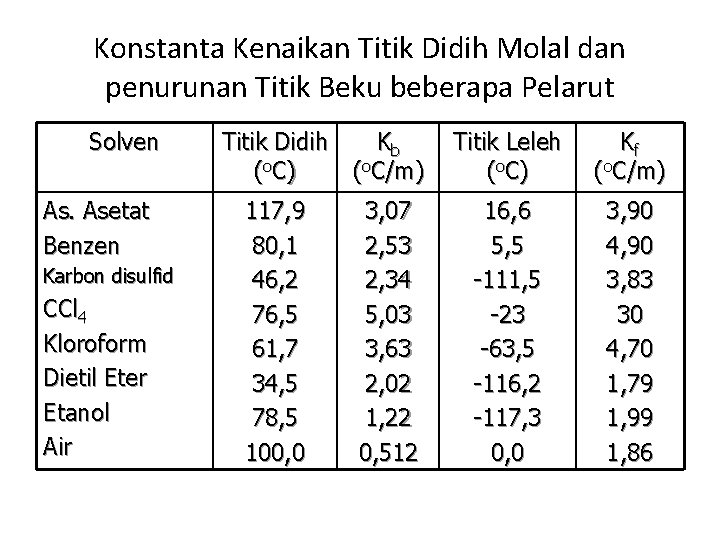
Konstanta Kenaikan Titik Didih Molal dan penurunan Titik Beku beberapa Pelarut Solven As. Asetat Benzen Karbon disulfid CCl 4 Kloroform Dietil Eter Etanol Air Titik Didih Kb (o. C) (o. C/m) 117, 9 80, 1 46, 2 76, 5 61, 7 34, 5 78, 5 100, 0 3, 07 2, 53 2, 34 5, 03 3, 63 2, 02 1, 22 0, 512 Titik Leleh (o. C) Kf (o. C/m) 16, 6 5, 5 -111, 5 -23 -63, 5 -116, 2 -117, 3 0, 0 3, 90 4, 90 3, 83 30 4, 70 1, 79 1, 99 1, 86

Penurunan Titik Beku • Seperti halnya dalam penguapan hanya solven yang menguap, dalam pembekuan juga hanya senyawa solven yang membeku • Titik beku larutan adalah suhu dimana tekanan uap larutan sama dengan tekanan pelarut murni • Pada suhu ini solven beku dan larutan yang masih mencair berada dalam kesetimbangan ΔTf ∞ m atau ΔTf = Kf × m ΔTf = Tf (solven) – Tf (larutan)
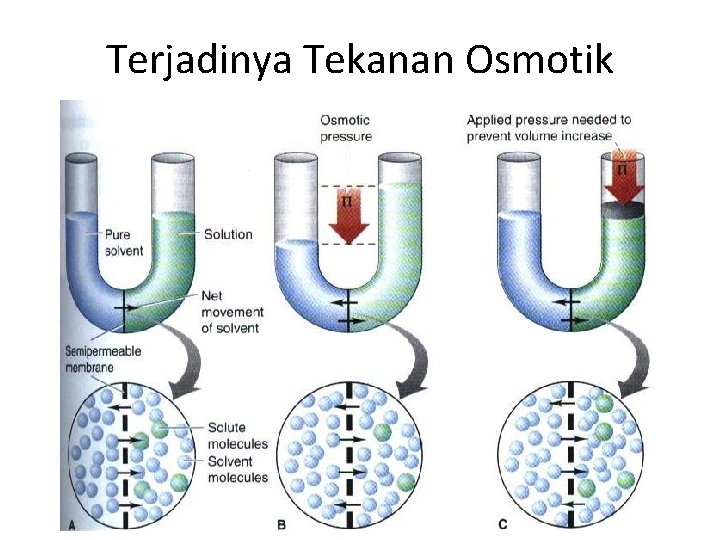
Terjadinya Tekanan Osmotik

Tekanan Osmotik • Tekanan osmotik didefinisikan sebagai tekanan yang harus diberikan untuk mencegah pergerakan air dari solven ke larutan seperti pada gambar sebelum ini • Tekanan ini berbanding lurus dengan jumlah solut dalam volume larutan Π ∞ nsolut/Vlarutan atau Π ∞ M Π = (nsolut/Vlarutan) RT = MRT

Latihan • Hitung penurunan tekanan uap ΔP saat 10 m. L gliserol (C 3 H 8 O 3) ditambahkan ke 500 m. L air pada 50 o. C. Pada suhu ini tekanan uap air murni 92, 5 torr berat jenis 0, 988 g/m. L dan berat jenis gliserol 1, 26 g/m. L • Hitung penurunan tekanan uap larutan 2 g aspirin (Mr: 180, 15 g/mol) dalam 50 g metanol pada 21, 2 o. C. Metanol murni memiliki tekanan uap 101 torr pada suhu ini. • Larutan yang disiapkan dengan melarutkan 18 g glukosa dalam 150 ml air. Larutan tersebut mempunyai titik didih 100. 34 o. C. Hitung berat molekul glukosa tersebut

Latihan • Jika anda menambahkan 1 kg senyawa antibeku etilen glikol (C 2 H 6 O 2) ke dalam radiator mobil yang berisi 4450 g air. Berapa titik didih dan titik beku air radiator? • Larutan 0, 30 M sukrosa pada 37 o. C memiliki tekanan osmotik hampir sama dengan tekanan darah, hitung tekanan osmotik sukrosa tsb! 10/26/2020







- Slides: 44