Laccrditation des laboratoires de biologie mdicale en France

L’accréditation des laboratoires de biologie médicale en France Présenté par Hélène MEHAY, Responsable de la Section Santé Humaine du Cofrac Page 1

L’accréditation Attestation délivrée par un organisme faisant autorité, ayant rapport à un organisme d’évaluation de la conformité (LBM), constituant une reconnaissance formelle de la compétence dernier à réaliser des activités spécifiques d’évaluation de la conformité (examens de biologie médicale, …) (NF EN ISO/CEI 17011 mai 2005) Page 2

Les garanties de l’accréditation §Les résultats sont obtenus selon des méthodes validées et des procédures conformes à des référentiels définis, § Les personnes sont compétentes pour réaliser les examens, § Les moyens (équipements raccordés, locaux …) sont adaptés aux examens réalisés, § L’organisation du laboratoire est conforme à un modèle de management de la qualité décrit dans une norme comme la norme NF EN ISO 15189…(maîtrise de la documentation, revue de contrats, maîtrise des non conformités, traitement des réclamations, processus d’amélioration continue…). Page 3

Le Cofrac § instance nationale d’accréditation (décret du 19/12/08) § dispositions prises en application du Règlement CE 765/2008 du 9 juillet 2008 fixant les prescriptions relatives à l'accréditation et à la surveillance du marché pour la commercialisation des produits § l’accréditation assimilée à une activité de puissance publique § l’instance nationale d’accréditation doit exercer ses fonctions sans but lucratif § l’instance nationale d’accréditation doit garantir la participation effective et équilibrée de toutes les parties intéressées § les exigences applicables à l’instance nationale d’accréditation en matière d’indépendance / impartialité, confidentialité, transparence notamment financière, organisation, compétence des personnels…(en phase avec la norme ISO/CEI 17011 applicable aux accréditeurs) § les instances nationales d’accréditation ayant fait l’objet avec succès de l’évaluation par les pairs (mis en place par EA) sont réputées conformes Page 4

La mission du Cofrac § Évaluer suivant des référentiels internationaux des OEC en vue d’attester leur compétence dans les domaines volontaire et réglementaire pour : § les étalonnages, les essais et analyses § l’inspection § la certification (de produits, de personnes, de systèmes de management) § Obtenir au niveau international l’acceptation de leurs prestations et la reconnaissance de leurs compétences grâce aux accords de reconnaissance multilatéraux (MLA) signés dans les cadres : - d’European Cooperation for Accreditation (EA), - d’International Laboratory Accreditation Cooperation (ILAC) ou d’International Accreditation Forum (IAF). Page 5
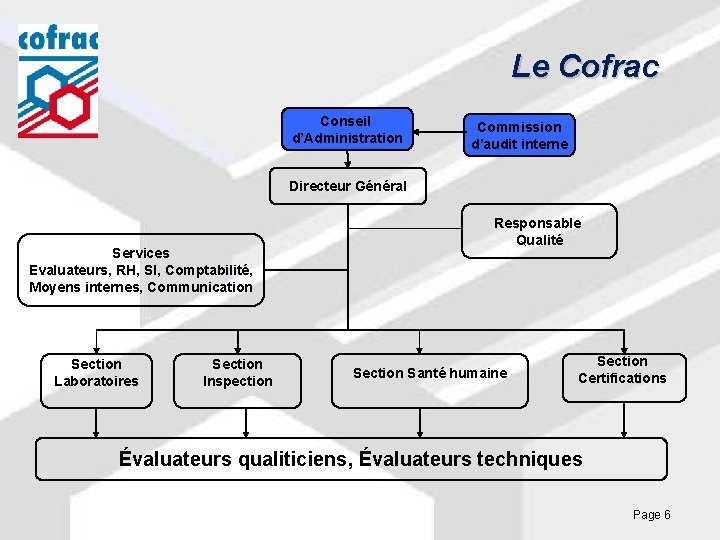
Le Cofrac Conseil d’Administration Commission d’audit interne Directeur Général Services Evaluateurs, RH, SI, Comptabilité, Moyens internes, Communication Section Laboratoires Section Inspection Responsable Qualité Section Santé humaine Section Certifications Évaluateurs qualiticiens, Évaluateurs techniques Page 6

Structures concernées par la section SH § les laboratoires de biologie médicale tels que définis par le code de la santé publique; § toute autre structure réalisant des examens portant sur des personnes ou des substances d’origine humaine qui visent à apporter des informations utiles au diagnostic, à la prévention ou au traitement des maladies ou à l’évaluation de l’état de santé d’êtres humains (les plateaux de qualification du don, les structures qui réalisent les actes d’anatomie et de cytologie pathologiques (ACP), les structures qui réalisent des activités biologiques d’assistance médicale à la procréation (AMP), …); § les laboratoires de biologie médico-légale. Page 7

3 domaines d’activité § Biologie médicale § Anatomie et cytologie pathologiques (ACP) § Biologie médico-légale Page 8

Domaine biologie médicale Sous-domaine : Biochimie Familles : Biochimie générale et spécialisée Pharmacologie – Toxicologie Radiotoxicologie Sous-domaine : Hématologie Familles : Hématocytologie Hémostase Immunohématologie Sous-domaine : Immunologie Familles : Auto-immunité Allergie Immunologie cellulaire spécialisée et histocompatibilité Page 9

Domaine biologie médicale Sous-domaine : Microbiologie Familles : Sérologie infectieuse Bactériologie Virologie Parasitologie – Mycologie Agents transmissibles non conventionnels Sous-domaine : Génétique Familles : Génétique somatique Génétique constitutionnelle Sous-domaine : Biologie de la reproduction (AMP) Familles : Spermiologie Embryologie clinique Page 10

Les instances de la section SH § le comité de section (CS) contribue à élaborer la stratégie de l’accréditation ainsi que les documents utiles à l’évaluation et à l’accréditation ; § la commission technique d’accréditation (CTA) étudie les rapports d’évaluation et examine les candidatures d’évaluateurs / experts techniques ; § le CS et la CTA comprennent des représentants de la DGS, des ARS, de l’HAS, des professionnels biologistes et des “clients” (patients ou prescripteurs) des LBM. Page 11

Les évaluateurs des LBM § l’accréditation repose sur des évaluations réalisées par des pairs ; § les évaluateurs techniques sont des biologistes médicaux exerçant dans un LBM accrédité ou inscrit dans la démarche d’accréditation, disposant d’une bonne expérience en qualité et si possible d’audit ; § les évaluateurs qualiticiens et techniques sont missionnés par le Cofrac ; ils remplissent une déclaration de confidentialité et de “conflits d’intérêts” ; ils peuvent être récusés par le LBM § ils bénéficient d’une formation initiale et leurs pratiques d’évaluation font l’objet d’une harmonisation. Page 12

Contexte réglementaire Ordonnance n° 2010 -49 du 13 janvier 2010 relative à la biologie médicale §Accréditation obligatoire §Application des normes NF EN ISO 15189 et NF EN ISO 22870 ainsi que de dispositions législatives et réglementaires du CSP §Pour la totalité de l’activité du LBM §Examens de biologie médicale, de la phase pré-analytique à la phase post-analytique §Les activités biologiques d’assistance médicale à la procréation (AMP) §Les examens d’anatomie et de cytologie pathologiques effectués à l’aide de techniques relevant de la biologie médicale Page 13

Contexte réglementaire §Médicalisation (adaptation de la prescription par le biologiste médical et interprétation des résultats) §Réglementation identique ville-hôpital §Réorganisation territoriale de l’offre de biologie médicale (LBM multi-sites, un LBM par établissement de santé) §Phase pré-analytique réalisée en dehors du LBM, sous la responsabilité du biologiste médical (convention) §Modalités de transmission des résultats Page 14

Recueil des exigences spécifiques (SH REF 02) Document de référence rassemblant les exigences de l’accréditation et les exigences réglementaires § Les exigences des normes NF EN ISO 15189 et NF EN ISO 22870 explicitées (en accord avec les positions d’EA notamment) § Les dispositions législatives et réglementaires relatives à la qualité des pratiques § Des notes et recommandations Page 15

Recueil des exigences spécifiques (SH REF 02) § Ecart “d’accréditation” : écart aux exigences normatives, aux exigences du Cofrac (en accord avec les positions EA/ILAC) et aux dispositions législatives et réglementaires précisées dans le document SH REF 02 (ainsi qu’aux dispositions que le LBM s’est lui-même fixé) § Signalement (fait par le Cofrac à l’ARS) : tout manquement grave ou évident dans le respect d’exigences réglementaires Information de la HAS, de l’AFSSAPS, de l’ABM et des ARS des décisions d’accréditation Page 16

Une accréditation en portée flexible Phase pré-analytique : Portée par nature flexible, LBM autorisé à adopter, adapter voire à développer les méthodes de prélèvement par famille Phase analytique : 2 types de portée Extrait SH INF 50 génétique. doc Portée flexible standard (A) : LBM autorisé à utiliser les révisions successives de méthodes reconnues (méthodes fournisseurs DM-DIV marqués CE) et à adopter des méthodes reconnues reposant sur les mêmes compétences techniques Vérification de méthode Portée flexible étendue (B) : LBM autorisé en plus à adapter ou à développer des méthodes Validation de méthode Page 17
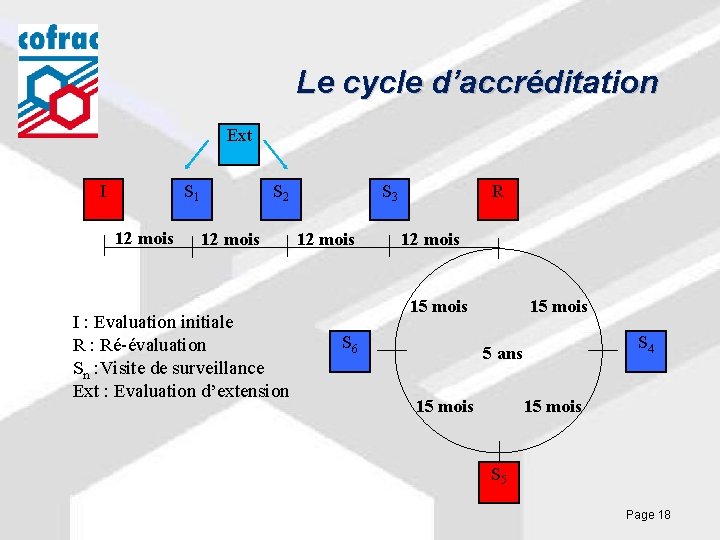
Le cycle d’accréditation Ext I S 1 12 mois S 2 12 mois I : Evaluation initiale R : Ré-évaluation Sn : Visite de surveillance Ext : Evaluation d’extension S 3 12 mois R 12 mois 15 mois S 6 15 mois S 4 5 ans 15 mois S 5 Page 18

Le processus d’accréditation Les 3 phases du processus d’accréditation : § Analyser et formaliser la demande du LBM (instruction) Questionnaire de renseignements (SH FORM 05) / Formulaire d’auto-évaluation (SH FORM 03) Ä un seul dossier d’accréditation (un seul numéro d’accréditation) Ä un système de management de la qualité unique Ä une organisation tenant compte d’une activité répartie sur plusieurs sites, dont certains pouvant ne pas réaliser de phase analytique § Évaluer de manière documentaire (expertise) et sur site (évaluation) les compétences du LBM § Décider (examen du rapport d’évaluation) Page 19

L’évaluation Les points clés de l’évaluation : § Examen de la pertinence et de l’adéquation des dispositions documentées, d’ordre organisationnel et technique ; § Vérification de la bonne application des dispositions (examen de traçabilité) ; § Evaluation de la maîtrise technique (interview, observation d’activité) et de la qualité des résultats (EEQ, CIQ). Le comportement des évaluateurs s’inscrit dans une démarche de progrès pour le laboratoire. Page 20

L’évaluation sur site § Impressions générales en vue de conclure sur la confiance dans la qualité des examens (Points forts / Axes d’amélioration) § Eventuels écarts (critiques/non critiques) Ø Présentation de l’intégralité des conclusions et des écarts relevés lors de la réunion de clôture Ø Le LBM peut accepter / refuser l’écart signalé par l’évaluateur Ø Pour chaque écart, il est demandé au LBM de fournir un plan d’actions. Page 21

Le processus de décision § les dossiers d’évaluation sont examinés de façon collégiale par des commissions d’accréditation ; Un avis favorable ne peut être proposé que si la preuve de la maîtrise des écarts critiques relevés a pu être apportée. §Evaluation initiale / d’extension (LBM déjà ouvert) §Evaluation de surveillance / Réévaluation (LBM déjà accrédité) § la décision d’accréditation est prise par le DG du Cofrac ; § les décisions peuvent être contestées via une procédure d’appel. Page 22

Documents utiles à l’accréditation §Documents contractuels (opposables) : GEN REF XX, SH REF XX, … § Outils d’aide à l’accréditation (non opposables) : SH GTA XX, documents des sociétés savantes (SFBC, …) § Formulaires (FORM) et des documents d’information (INF) – modalités de candidature à l’accréditation détaillées dans le document SH INF 20 Documents du Cofrac disponibles sur www. cofrac. fr/centre de documentation Page 23

Documents utiles à l’accréditation § SH REF 08 - Expression et évaluation des portées d’accréditation § SH INF 50 - Portées-types d’accréditation § SH GTA 04 - Guide technique d’accréditation de vérification (portée A) et de validation (portée B) des méthodes de biologie médicale § SH FORM 43 - FICHE TYPE QUANTITATIF - Vérification (portée A) / Validation (portée B) d'une méthode de biologie médicale § SH FORM 44 - FICHE TYPE QUALITATIF - Vérification (portée A) / Validation (portée B) d'une méthode de biologie médicale § SH GTA 01 - Guide technique d’accréditation en biologie médicale § SH GTA 14 – Guide technique d’accréditation pour l’évaluation des incertitudes en biologie médicale Page 24

Documents utiles à l’accréditation Travaux en cours : § SH GTA 06 – Guide technique d’accréditation relatif aux contrôles de la qualité en biologie médicale (publication prévue pour la fin de l’année 2011) § Biologie de la reproduction (AMP) § Anatomie et cytologie pathologiques (ACP) § Informatique (LAB GTA 09 : Guide Technique d'Accréditation Dématérialisation des données dans les laboratoires) Page 25
- Slides: 25