Laboratorio del bicarbonato de sosa Estequiometra Llave Propsitos

Laboratorio del bicarbonato de sosa Estequiometría Llave

Propósitos: 1. Calcular la masa teórica del Na. Cl basada en una masa sabida de Na. HCO 3. 2. Determinar experimental la masa real del Na. Cl producida. 3. Calcular el por ciento rinden para su experimento. Ecuación de la reacción: Na. HCO 3(s) + ácido clorhídrico (aq) Na. Cl + CO 2( Materiales: bicarbonato de sosa de las gafas de seguridad (Na. HCO 3) ácido el soporte del anillo de la cápsula de evaporación con el anillo bunsen la horn pinzas de la gasa del alambre del vidrio de reloj

Procedimiento 1. Encontrar la masa de la cápsula de evaporación y del vidrio de reloj. Registrar esta masa en la tabla de los datos. 2. Agregar 1/3 de una cucharilla de bicarbonato de sosa a la cápsula de evaporación, y registrar la masa total en la tabla de los datos. 3. Cubrir la cápsula de evaporación con el vidrio de reloj de modo que solamente el c de la cápsula de evaporación se expone. • Utilizar el cuentagotas para gotear el ácido clorhídrico abajo del canalón y en el pla 2. Agregar el ácido clorhídrico hasta que el fizzing cese. 3. Dejando el vidrio de reloj en el lugar, hervir del líquido hasta solamente la sal de ta 4. restos en el plato. • Dejar el plato fresco por cinco minutos, después pesarlo otra vez y registrar la mas 3. en la tabla de los datos. 4. 7. Limpiar aclarando su equipo con agua y limpiándolo seco con una toalla de pape
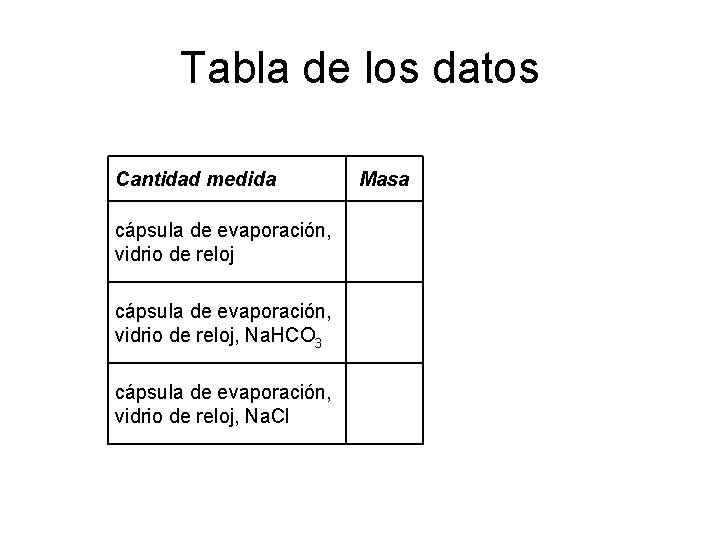
Tabla de los datos Cantidad medida cápsula de evaporación, vidrio de reloj, Na. HCO 3 cápsula de evaporación, vidrio de reloj, Na. Cl Masa

Cálculos 1. Encontrar la masa teórica del Na. Cl que sería producida si su experimento era perfecto. 2. Encontrar la masa real del Na. Cl que usted obtuvo. 3. Encontrar que el por ciento rinde para su experimento. Si el su por cien es mayor de 100%, proporciona por lo menos una fuente de error posib eso pudo haber hechole conseguir la producción más del de 100%.
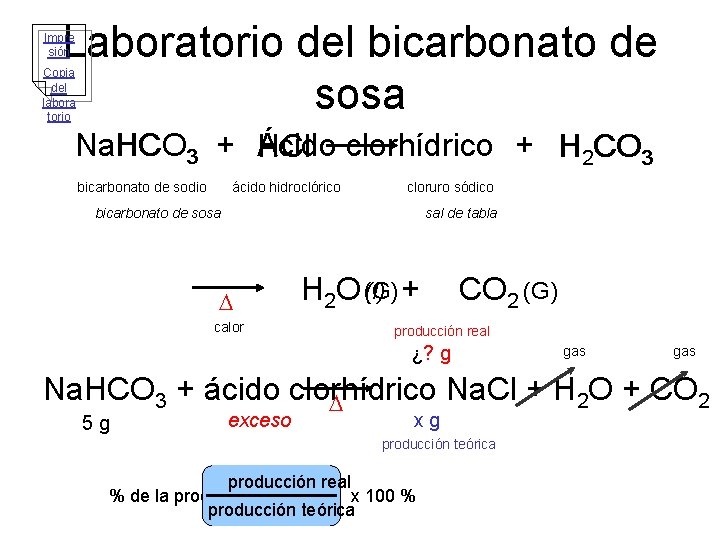
Laboratorio del bicarbonato de sosa Impre sión Copia del labora torio Na Na. HCO Ácido clorhídrico + H 2 CO 3 HCO 3 + H Cl bicarbonato de sodio ácido hidroclórico cloruro sódico bicarbonato de sosa sal de tabla D calor (l) + H 2 O (G) CO 2 (G) producción real ¿? g gas Na. HCO 3 + ácido clorhídrico Na. Cl + H 2 O + CO 2 D 5 g exceso x g producción teórica producción real % de la producción = x 100 % producción teórica
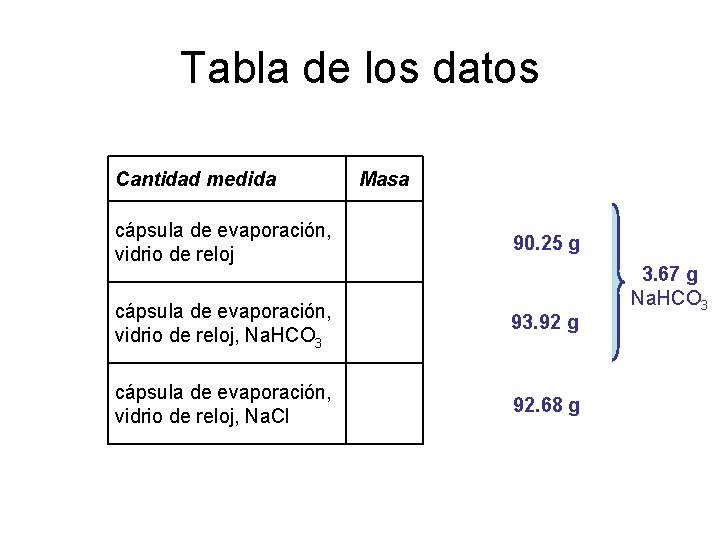
Tabla de los datos Cantidad medida Masa cápsula de evaporación, vidrio de reloj 90. 25 g cápsula de evaporación, vidrio de reloj, Na. HCO 3 93. 92 g cápsula de evaporación, vidrio de reloj, Na. Cl 92. 68 g 3. 67 g Na. HCO 3

Cálculos x g Na. Cl = 3. 67 g Na. HCO 3 1 mol de Na. Cl de 58. 5 g de = Na. Cl 2. 56 g 84 g Na. HCO 3 1 mol de Na. HCO 31 mol de Na. Cl 1. Encontrar la masa teórica del Na. Cl que sería producida si su experimento era perfecto. 2. Encontrar la masa real del Na. Cl que usted obtuvo. Cantidad medida Masa cápsula de evaporación, vidrio de reloj 3. 3. Encontrar que el por ciento rinde para su experimento. Si el su por c 90. 25 g 92. 68 g - 90. 25 g de = Na. Cl 2. 43 g cápsula de evaporación, vidrio de reloj, Na. HCO 93. 92 g es mayor de 100%, proporciona por lo menos una fuente de error posib (producción rea cápsula de evaporación, vidrio de reloj, Na. Cl 92. 68 g eso pudo haber hechole conseguir la producción más del de 100%. 3 producción real % de la producción = x 100 % producción teórica Na. Cl de 2. 43 g x 100 % = producción del 95% Na. Cl de 2. 56 g
- Slides: 8