laboration de biomatriaux partir de polysaccharides naturels Prsente

Élaboration de biomatériaux à partir de polysaccharides naturels Présentée par: V. GADENNE Laboratoire Polymères, Biopolymères, Surfaces

Introduction La contamination bactérienne entraînant la formation de biofilms qui sont directement responsables de près de 60% des infections nosocomiales. La formation d’un biofilm débute par une phase d’adhésion des bactéries sur la surface. Résistance de ces biofilms aux traitements antibiotiques Nécessité de concevoir des biomatériaux capables d’inhiber l’adhésion bactérienne 2
Introduction Surfaces anti-bactériennes Surfaces bioactives Immobilisation ou imprégnation de composés biocides. - Antibiotiques - Peptides - Argent, Cuivre… Surfaces passives - Rugosité - Énergie de surface - Immobilisation de composés anti-adhésifs (PEG, polysaccharides…) 3

Polysaccharides sulfatés: Ulvanes Avantages: • Issue de ressources renouvelables • Valorisation des algues vertes • Nombreuses activités biologiques A 3 s O H O 2 C HO B 3 s OH O O O H C O 3 OH H O 2 C O O OH n b -D -1, 4 -glucuronic acid a-L-1, 4 -rhamnose 3 -sulfate O O X + -O 3 S O X + -O 3 S O O H 3 C OH OH a-L-1, 4 -iduronic acid n a-L-1, 4 -rhamnose 3 -sulfate Inconvénients: Structure dépendante de l’espèce 4

Polysaccharides sulfatés: Ulvanes U. rotundata: Ur U. compressa: Uc Objectifs: Fonctionnalisation des surfaces de Ti. O 2 par des polysaccharides Évaluer les propriétés anti-adhésives de ces surfaces 5
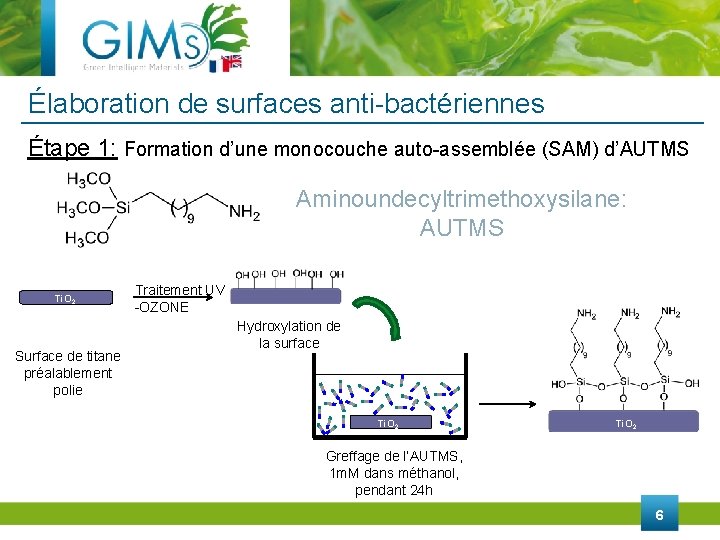
Élaboration de surfaces anti-bactériennes Étape 1: Formation d’une monocouche auto-assemblée (SAM) d’AUTMS Aminoundecyltrimethoxysilane: AUTMS Ti. O 2 Surface de titane préalablement polie Traitement UV -OZONE Ti. O 2 Hydroxylation de la surface Ti. O 2 Greffage de l’AUTMS, 1 m. M dans méthanol, pendant 24 h 6
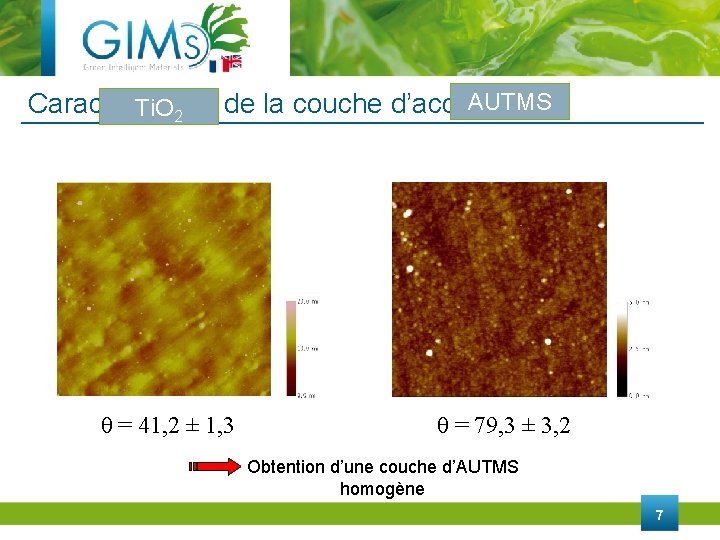
AUTMS Caractérisation de la couche d’accroche Ti. O 2 θ = 41, 2 ± 1, 3 θ = 79, 3 ± 3, 2 Obtention d’une couche d’AUTMS homogène 7
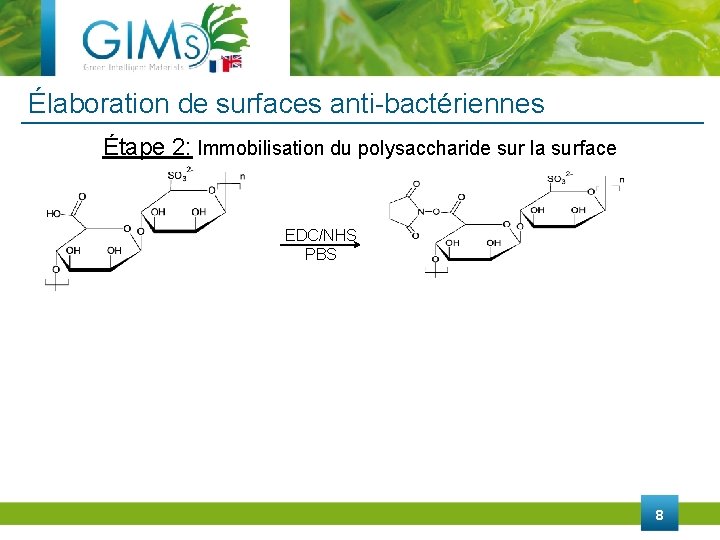
Élaboration de surfaces anti-bactériennes Étape 2: Immobilisation du polysaccharide sur la surface EDC/NHS PBS 8
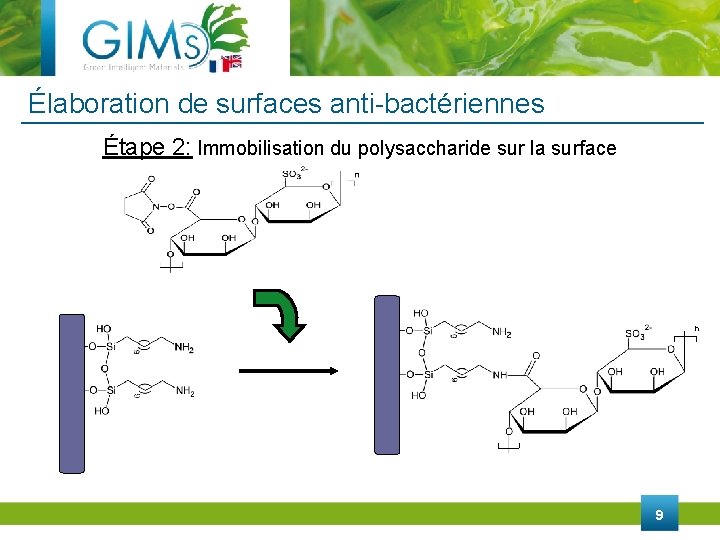
Élaboration de surfaces anti-bactériennes Étape 2: Immobilisation du polysaccharide sur la surface n 9
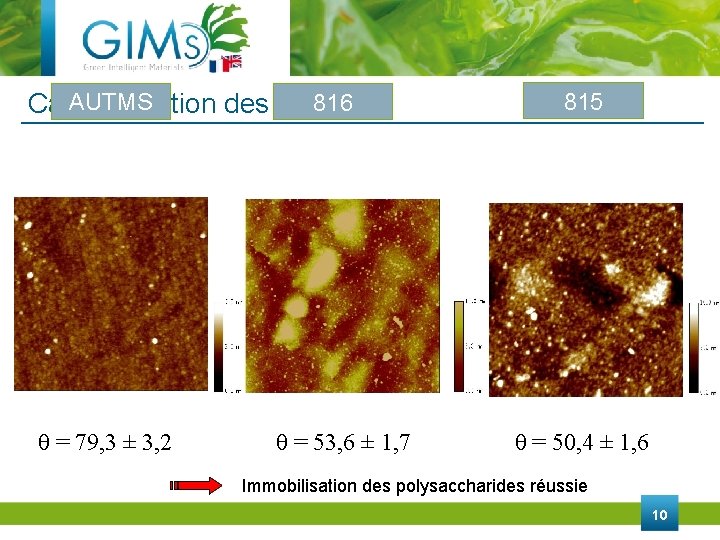
AUTMS 816 Caractérisation des surfaces θ = 79, 3 ± 3, 2 θ = 53, 6 ± 1, 7 815 θ = 50, 4 ± 1, 6 Immobilisation des polysaccharides réussie 10
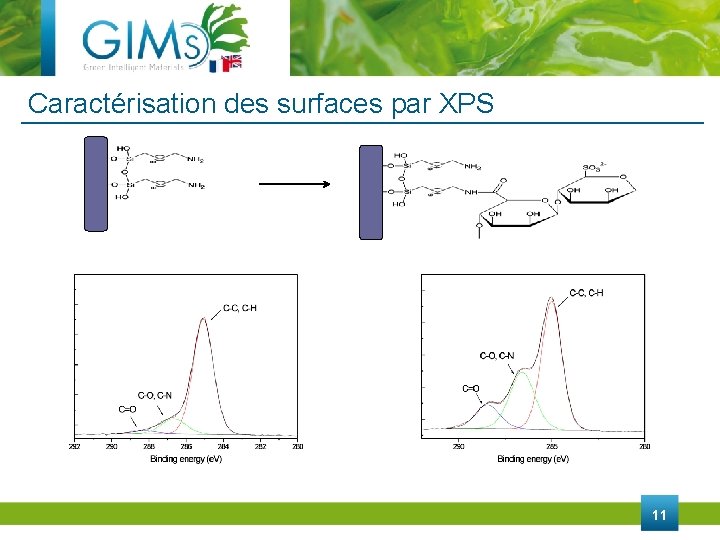
Caractérisation des surfaces par XPS 11
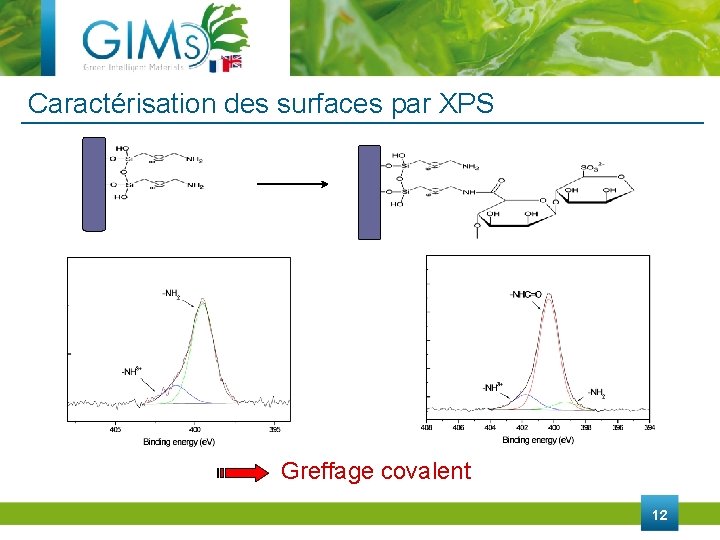
Caractérisation des surfaces par XPS Greffage covalent 12
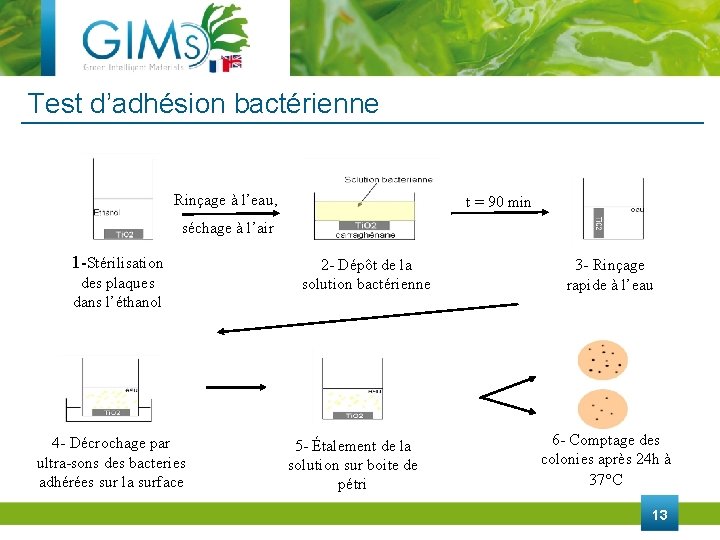
Test d’adhésion bactérienne Rinçage à l’eau, t = 90 min séchage à l’air 1 -Stérilisation des plaques dans l’éthanol 4 - Décrochage par ultra-sons des bacteries adhérées sur la surface 2 - Dépôt de la solution bactérienne 5 - Étalement de la solution sur boite de pétri 3 - Rinçage rapide à l’eau 6 - Comptage des colonies après 24 h à 37°C 13

Résultats des tests d’adhésion Pseudomonas. aeruginosa Hydrophobe % d’inhibition AUTMS 815 816 X 64 % 71 % Surface hydrophobe = adhésion favorisée Surface hydrophile = adhésion limitée 14

Résultats des tests d’adhésion Staphylococcus. epidermidis Hydrophile % d’inhibition AUTMS 815 816 80 % 94 % 97 % Effet anti-adhésifs indépendant de la nature de la bactérie 15

Conclusion • Élaboration de nouvelles surfaces à base de polysaccharides • Sur la monocouche d’ AUTMS, l’adhésion bactérienne dépend des interactions d’hydrophobicité. • Avec les ulvanes: Obtention d’une surface anti-adhésive indépendante de l’hydrophobicité des bactéries. Effet des groupements sulfatés ? ? ? Tests sur des Ulvanes non-sulfatés 16

Remerciements Partenaires: Université de Portsmouth INSA Université de Rouen Société biofilm control CNRS 17
- Slides: 17