LAB ALIMENTOS Valor calrico Quantas calorias por grama

LAB ALIMENTOS Valor calórico: Quantas calorias por grama de alimento
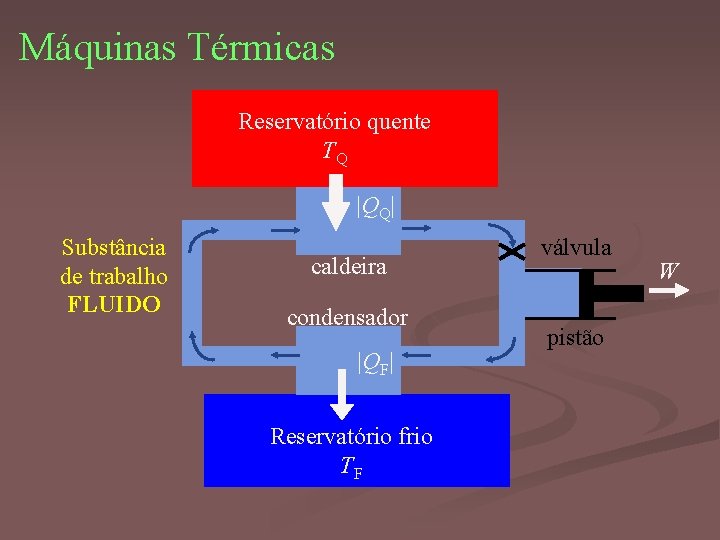
Máquinas Térmicas Reservatório quente TQ |QQ| Substância de trabalho FLUIDO caldeira condensador |QF| Reservatório frio TF válvula pistão W
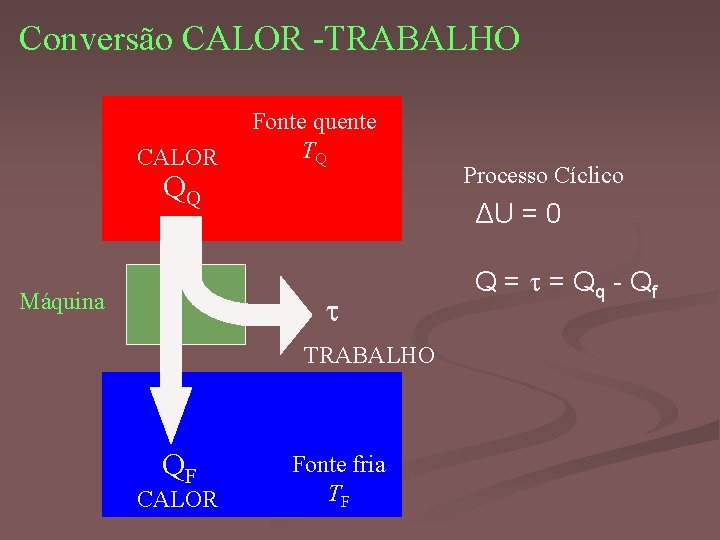
Conversão CALOR -TRABALHO CALOR Fonte quente TQ QQ Máquina ΔU = 0 TRABALHO QF CALOR Processo Cíclico Fonte fria TF Q = = Q q - Qf
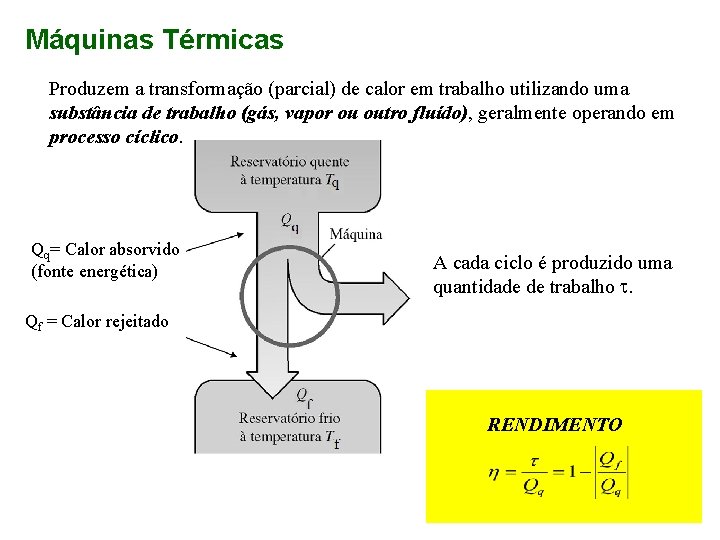
Máquinas Térmicas Produzem a transformação (parcial) de calor em trabalho utilizando uma substância de trabalho (gás, vapor ou outro fluído), geralmente operando em processo cíclico. Qq= Calor absorvido (fonte energética) A cada ciclo é produzido uma quantidade de trabalho . Qf = Calor rejeitado RENDIMENTO
Qq Qf

Ciclo de Carnot Ciclo de processos reversíveis para máquinas térmicas e refrigeradores ideais Máquinas Reais Processos Irreversíveis • Atrito • Perdas de calor durante as transferências de calor entre corpos com temperaturas diferentes
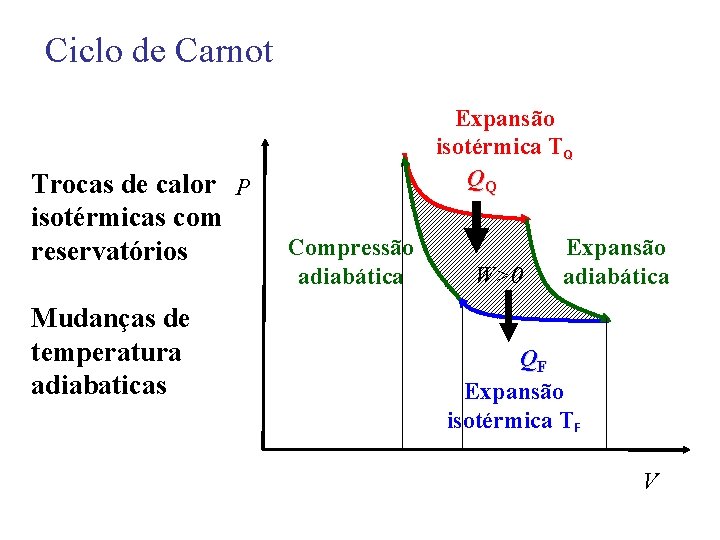
Ciclo de Carnot Trocas de calor P isotérmicas com reservatórios Mudanças de temperatura adiabaticas Expansão isotérmica TQ QQ Compressão adiabática W>0 Expansão adiabática QF Expansão isotérmica TF V

Rendimento num ciclo de Carnot

Segunda Lei Termodinâmica É impossível construir uma máquina térmica com eficiência 100%. Nenhuma máquina térmica operando em ciclos pode retirar calor de uma fonte e transformá-lo integralmente em trabalho. Formulação de Kelvin-Planck
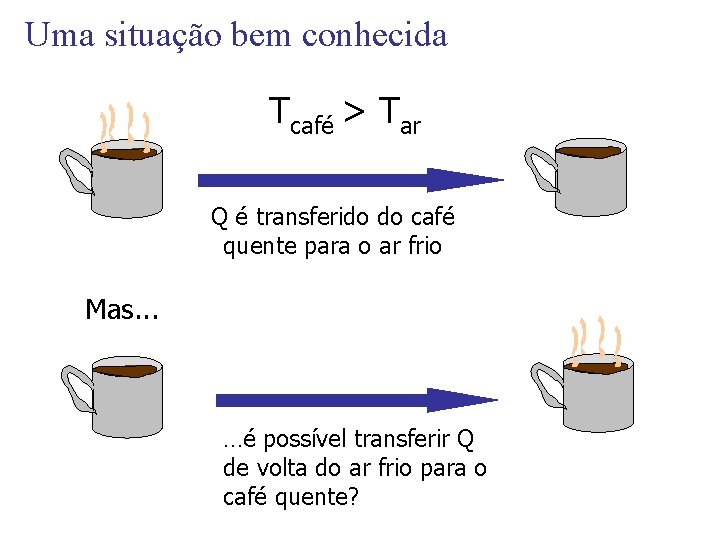
Uma situação bem conhecida Tcafé > Tar Q é transferido do café quente para o ar frio Mas. . . …é possível transferir Q de volta do ar frio para o café quente?

Em todos os casos • A energia é conservada. • Porque estes eventos não são observados? • Irreversibilidade : a seta do tempo. 2º. Lei da Termodinâmica Entropia

FÍSICA - 2º ano do Ensino Médio Segunda lei da termodinâmica Em geral, os fenômenos que observamos, espontâneos ou naturais, são irreversíveis. Em um fenômeno irreverversível, é possível distinguir entre o antes e o depois.

Segunda Lei Termodinâmica Formulação de Clausius É impossível existir transferência espontânea de calor de uma fonte fria para outra quente. É impossível realizar um processo cujo único efeito seja transferir calor de um corpo mais frio para um corpo mais quente.
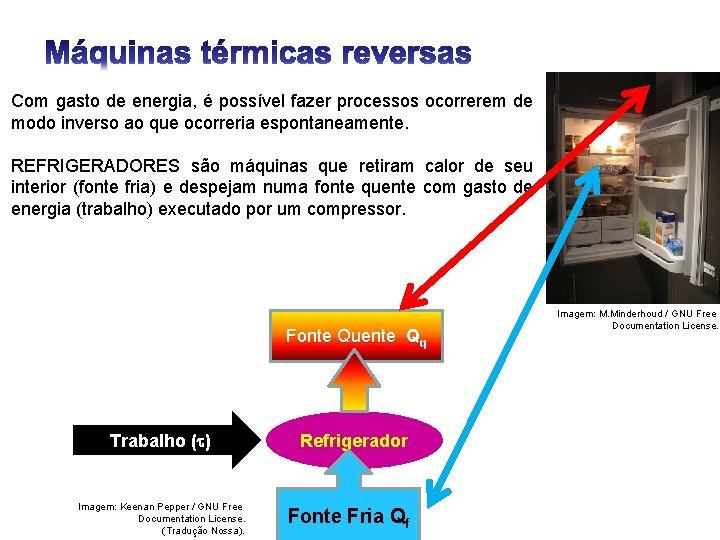
Com gasto de energia, é possível fazer processos ocorrerem de modo inverso ao que ocorreria espontaneamente. REFRIGERADORES são máquinas que retiram calor de seu interior (fonte fria) e despejam numa fonte quente com gasto de energia (trabalho) executado por um compressor. Fonte Quente Qq Trabalho ( ) Imagem: Keenan Pepper / GNU Free Documentation License. (Tradução Nossa). Refrigerador Fonte Fria Qf Imagem: M. Minderhoud / GNU Free Documentation License.
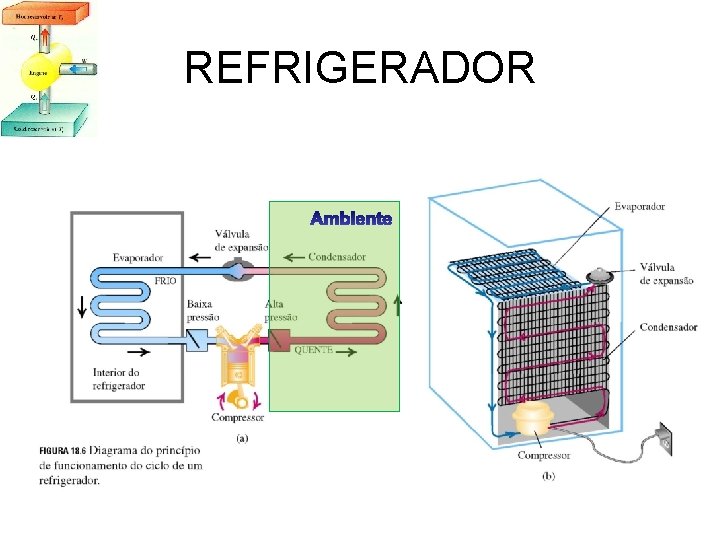
REFRIGERADOR
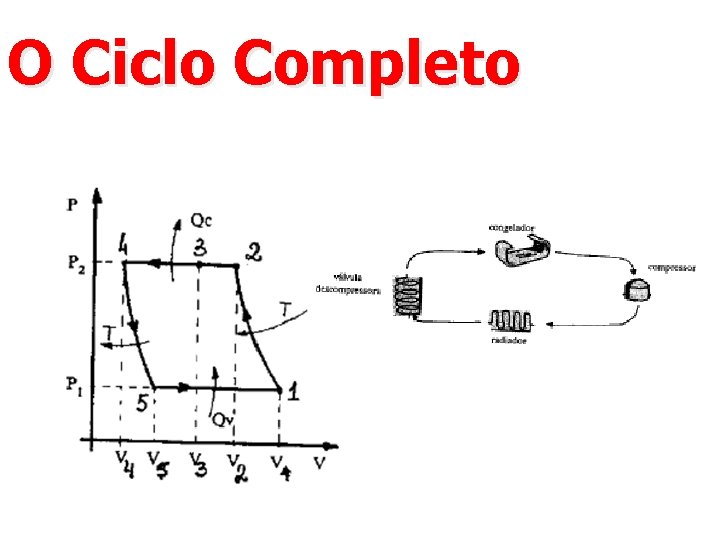
O Ciclo Completo
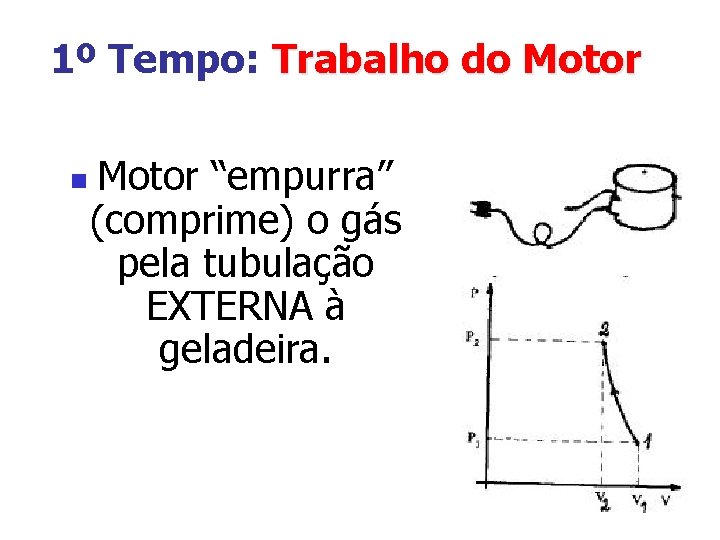
1º Tempo: Trabalho do Motor n Motor “empurra” (comprime) o gás pela tubulação EXTERNA à geladeira.

2º Tempo: Esfriando no Radiador n n Ao percorrer o radiador (serpentina), o gás vai perdendo calor para o ambiente, resfriando-se; como a serpentina é um tubo único, sem obstáculos, a pressão em todo o trajeto é constante (processo isobárico) (2 4).

3º Tempo: Soprando de “biquinho” n Válvula Descompressora: esta descompressão (expansão) pode ser considerada adiabática devido à rapidez com que ocorre. A pressão diminui e o volume aumenta (4 5).
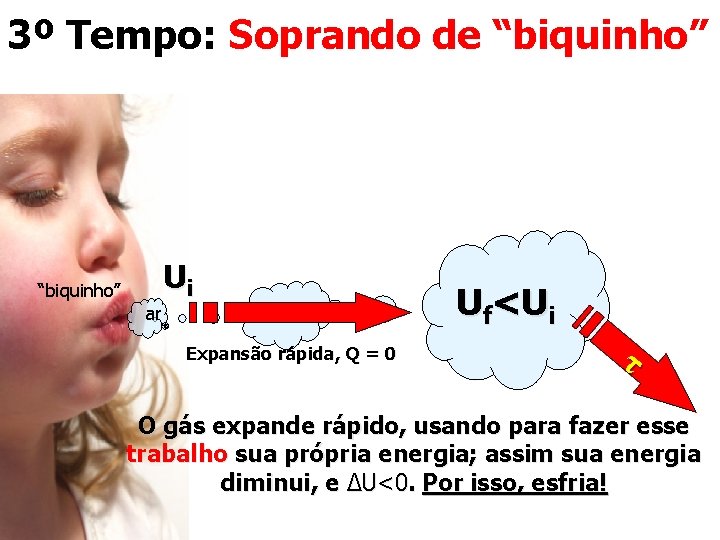
3º Tempo: Soprando de “biquinho” Ui “biquinho” ar Expansão rápida, Q = 0 Uf<Ui τ O gás expande rápido, usando para fazer esse trabalho sua própria energia; assim sua energia diminui, e ΔU<0. Por isso, esfria!
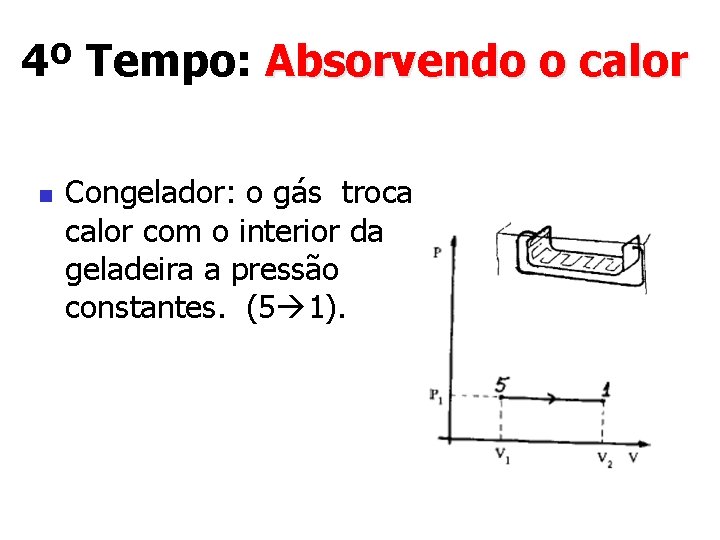
4º Tempo: Absorvendo o calor n Congelador: o gás troca calor com o interior da geladeira a pressão constantes. (5 1).
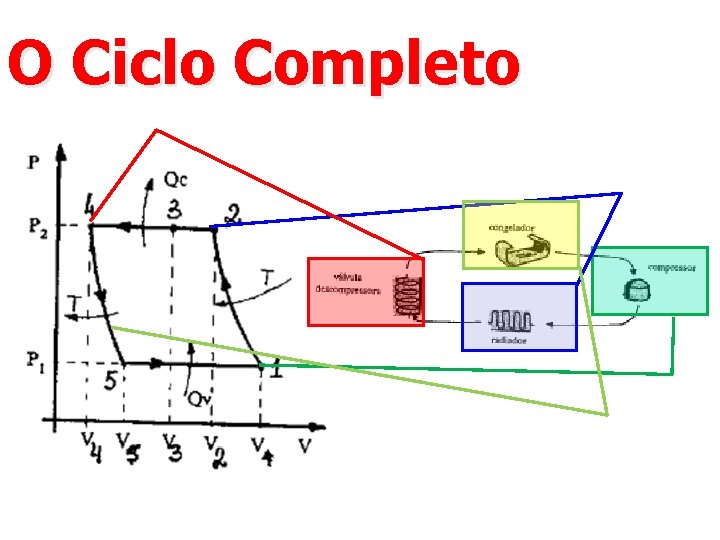
O Ciclo Completo

EFICIÊNCIA (e) Onde Qf => Quantidade de calor retirada da fonte fria. Qq => Quantidade de calor cedida à fonte quente.

EXERCÍCIOS

Entropia • O que é entropia?
ENTROPIA MEDE A A tendência à desordem pode ser medida pela Entropia. DESORGANIZAÇÃO Logo, quanto maior a desordem num. UM sistema termodinâmico, DE SISTEMA maior sua Entropia. Determina o CAOS.

Em qualquer sistema físico, a tendência natural é o aumento da desordem; o restabelecimento da ordem só é possível mediante o dispêndio (gasto) de energia. Em todo processo natural espontâneo, entropia do Universo sempre aumenta. a

ENTROPIA Numa transformação espontânea (ou irreversível). . . a ENTROPIA sempre AUMENTA

A segunda lei da termodinâmica Se um processo ocorre num sistema fechado, a entropia do sistema aumenta para processos irreversíveis e permanece constante para processos reversíveis. A entropia nunca diminui.

Transformação irreversível (queima de papel) Aumento da entropia, aumento da desordem

Processos irreversíveis • A reversibilidade não viola o princípio de conservação da energia. • A Entropia, S, é uma propriedade nova que determina se algum processo é reversível ou não. • S não obedece uma lei de conservação. Postulado da Entropia Se um processo irreversível ocorre em um sistema fechado, a entropia S do sistema sempre aumenta
EXISTEM PROCESSOS IRREVERSÍVEIS TEMPO

https: //www. youtube. com/watch? v=q. XC 4 f 1 -48 v. Y https: //www. youtube. com/watch? v=FHMN_QSRe. Hg

Princípio da mínima ação princípio de D’Alembert ou princípio da mínima ação: • Os sistemas físicos evoluem, espontaneamente, pelo caminho que consome menos energia.
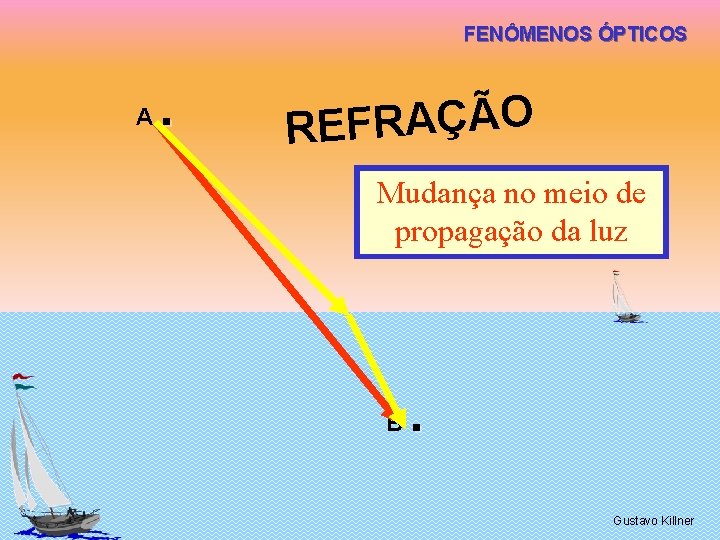
FENÔMENOS ÓPTICOS A . O Ã Ç A R F E R Mudança no meio de propagação da luz B . Gustavo Killner
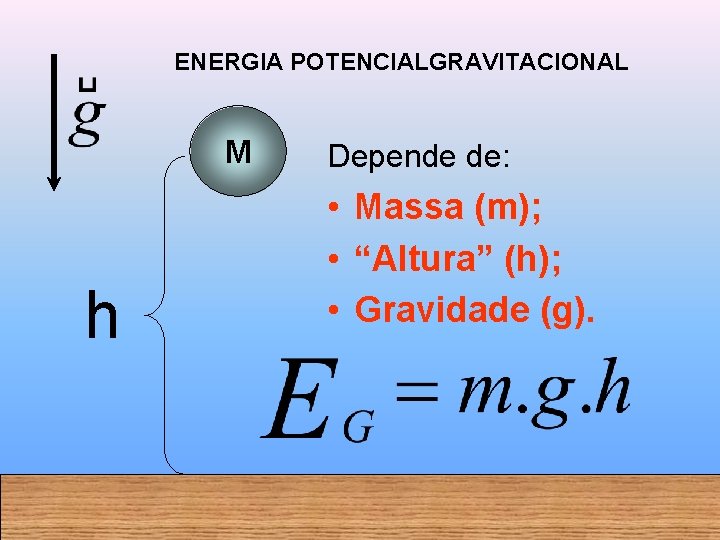
ENERGIA POTENCIALGRAVITACIONAL M h Depende de: • Massa (m); • “Altura” (h); • Gravidade (g).


Lição para 1ª aula de setembro Livro – Óptica geométrica Ler e resumir pg. 345 a 349 Avaliando a aprendizagem: 4 e 5
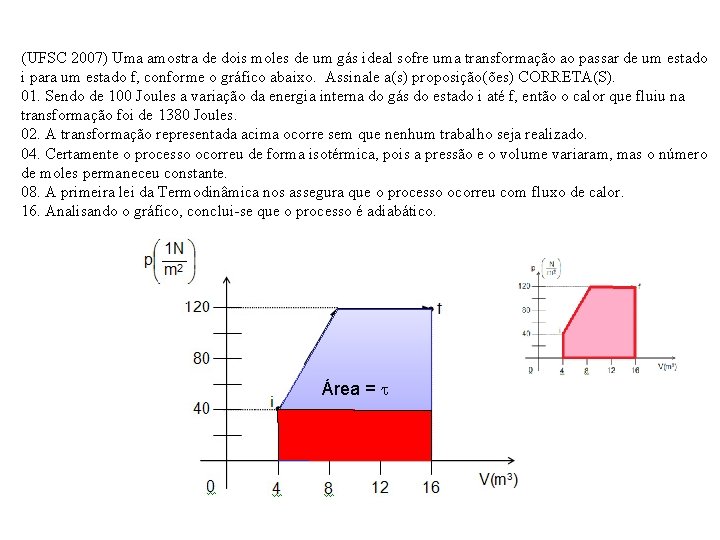
(UFSC 2007) Uma amostra de dois moles de um gás ideal sofre uma transformação ao passar de um estado i para um estado f, conforme o gráfico abaixo. Assinale a(s) proposição(ões) CORRETA(S). 01. Sendo de 100 Joules a variação da energia interna do gás do estado i até f, então o calor que fluiu na transformação foi de 1380 Joules. 02. A transformação representada acima ocorre sem que nenhum trabalho seja realizado. 04. Certamente o processo ocorreu de forma isotérmica, pois a pressão e o volume variaram, mas o número de moles permaneceu constante. 08. A primeira lei da Termodinâmica nos assegura que o processo ocorreu com fluxo de calor. 16. Analisando o gráfico, conclui-se que o processo é adiabático. Área =
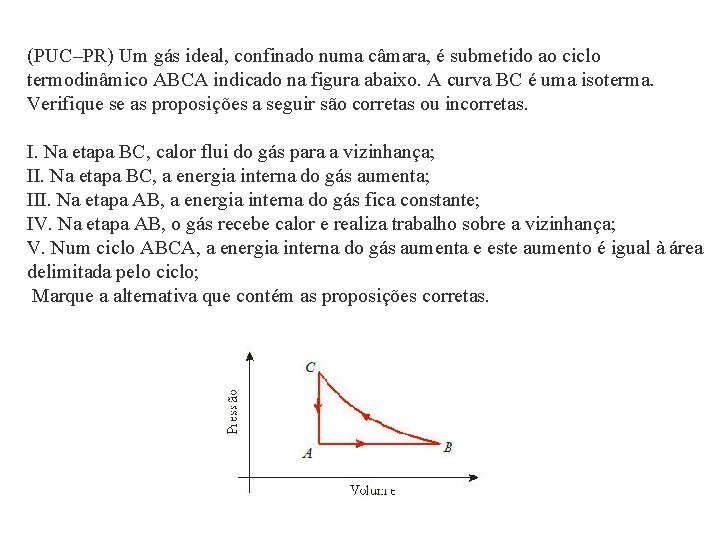
(PUC–PR) Um gás ideal, confinado numa câmara, é submetido ao ciclo termodinâmico ABCA indicado na figura abaixo. A curva BC é uma isoterma. Verifique se as proposições a seguir são corretas ou incorretas. I. Na etapa BC, calor flui do gás para a vizinhança; II. Na etapa BC, a energia interna do gás aumenta; III. Na etapa AB, a energia interna do gás fica constante; IV. Na etapa AB, o gás recebe calor e realiza trabalho sobre a vizinhança; V. Num ciclo ABCA, a energia interna do gás aumenta e este aumento é igual à área delimitada pelo ciclo; Marque a alternativa que contém as proposições corretas.

Uma central de energia utilizada por uma equipe móvel de TV desenvolve 1, 8. 107 joules de energia elétrica enquanto seu motor a gasolina consome 2, 5 litros de combustível, cujo poder calorífico é de 3, 6. 107 joules/litro. O rendimento da central é de: a) 10%; b) 20%; c) 40%; d) 50%; e) 100%. Um refrigerador de uso doméstico é uma máquina térmica invertida: o calor é retirado do congelador à temperatura de -23°C, enquanto a temperatura do ambiente em que ele se encontra é de 27°C. O coeficiente de desempenho do refrigerador de Carnot, operando em ciclos entre essas temperaturas, é a) 0, 20 b) 0, 80 c) 2, 0 d) 4, 0 e) 5, 0
- Slides: 42