La variabilidad interindividual Origen e importancia en la

La variabilidad interindividual. Origen e importancia en la utilización clínica de los medicamentos PROF. A. DOMÍNGUEZ-GIL HURLÉ SERVICIO DE FARMACIA HOSPITAL UNIVERSITARIO DE SALAMANCA Oviedo, 30 de Septiembre de 2005

“. . . si no fuera por la gran variabilidad entre los pacientes la medicina podría ser considerada como una ciencia y no un arte” “The Principles and Practice of Medicine” William Osler, 1892
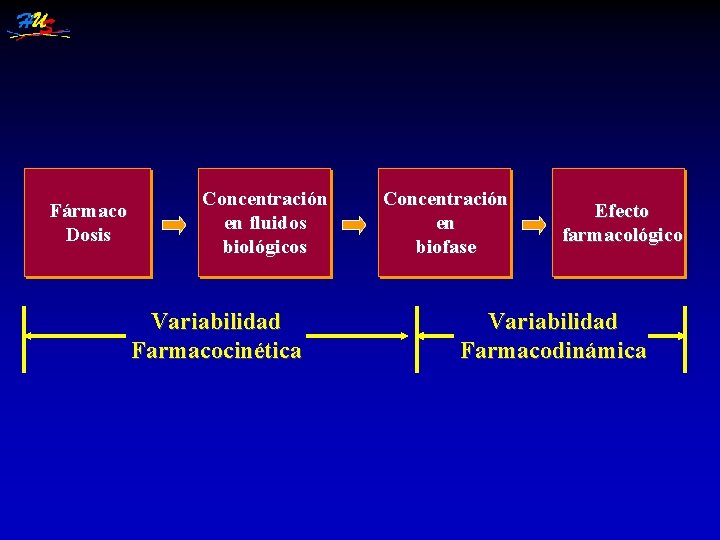
Fármaco Dosis Concentración en fluidos biológicos Variabilidad Farmacocinética Concentración en biofase Efecto farmacológico Variabilidad Farmacodinámica
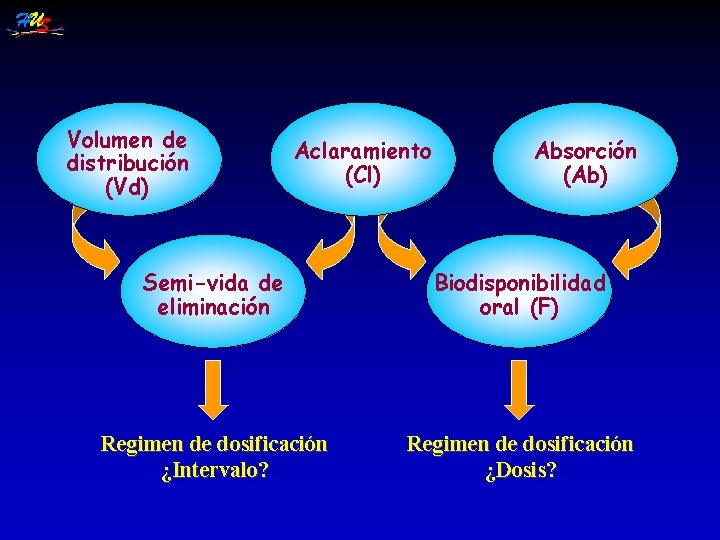
Volumen de distribución (Vd) Aclaramiento (Cl) Absorción (Ab) Semi-vida de eliminación Biodisponibilidad oral (F) Regimen de dosificación ¿Intervalo? Regimen de dosificación ¿Dosis?
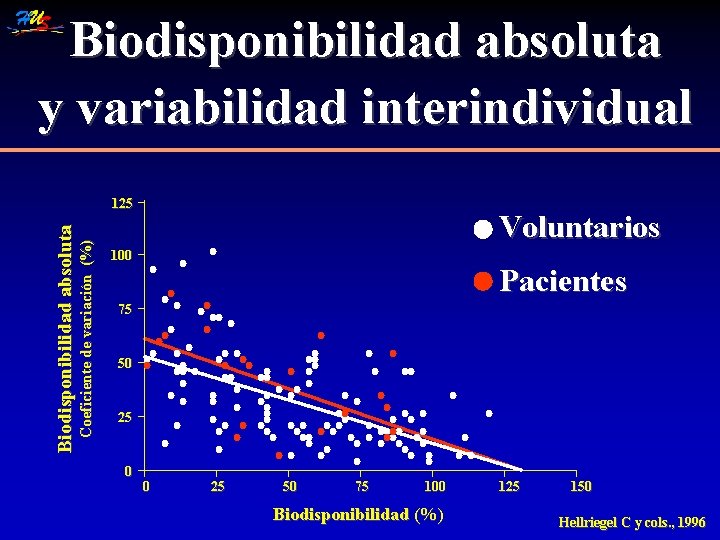
Biodisponibilidad absoluta y variabilidad interindividual Coeficiente de variación (%) Biodisponibilidad absoluta 125 Voluntarios 100 Pacientes 75 50 25 0 0 25 50 75 100 Biodisponibilidad (%) 125 150 Hellriegel C y cols. , 1996
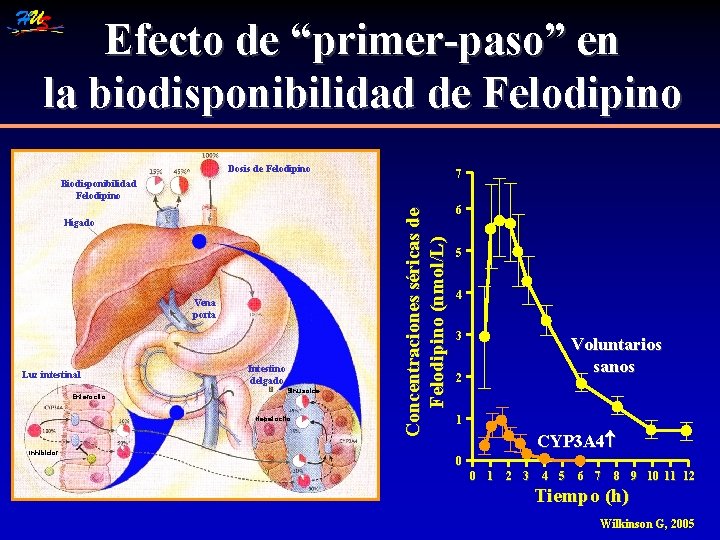
Efecto de “primer-paso” en la biodisponibilidad de Felodipino Dosis de Felodipino 7 Hígado Vena porta Luz intestinal Enterocito Intestino delgado Sinusoide Hepatocito Inhibidor Concentraciones séricas de Felodipino (nmol/L) Biodisponibilidad Felodipino 6 5 4 3 2 1 0 Voluntarios sanos CYP 3 A 4 0 1 2 3 4 5 6 7 8 9 10 11 12 Tiempo (h) Wilkinson G, 2005
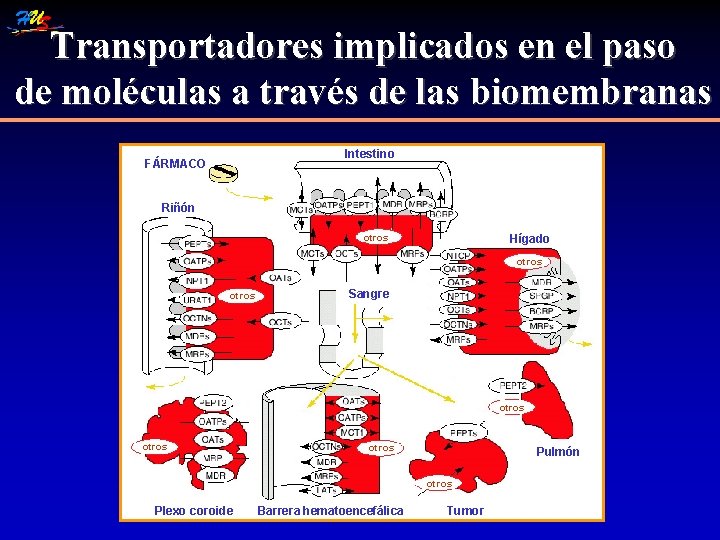
Transportadores implicados en el paso de moléculas a través de las biomembranas Intestino FÁRMACO Riñón otros Hígado otros Sangre otros Pulmón otros Plexo coroide Barrera hematoencefálica Tumor
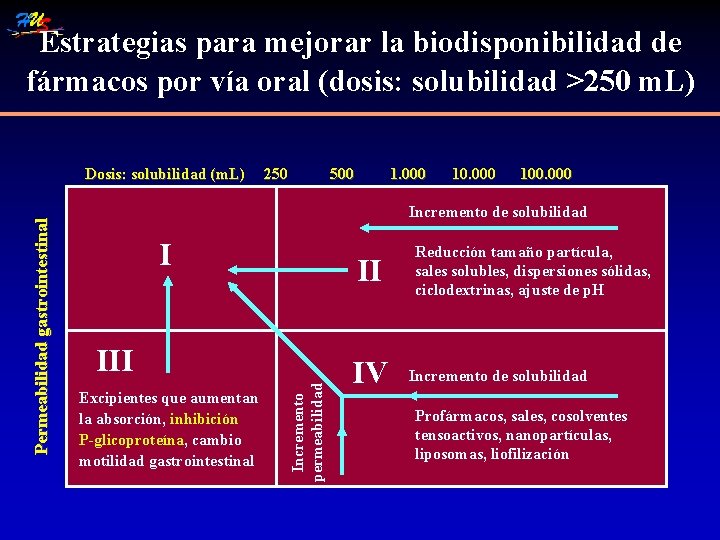
Estrategias para mejorar la biodisponibilidad de fármacos por vía oral (dosis: solubilidad >250 m. L) 250 500 1. 000 100. 000 Incremento de solubilidad I II III Excipientes que aumentan la absorción, inhibición P-glicoproteína, cambio motilidad gastrointestinal Incremento permeabilidad Permeabilidad gastrointestinal Dosis: solubilidad (m. L) IV Reducción tamaño partícula, sales solubles, dispersiones sólidas, ciclodextrinas, ajuste de p. H Incremento de solubilidad Profármacos, sales, cosolventes tensoactivos, nanopartículas, liposomas, liofilización
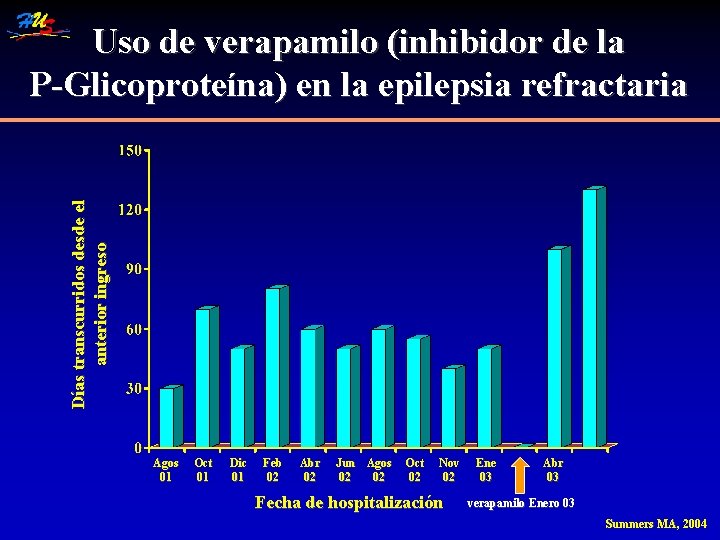
Días transcurridos desde el anterior ingreso Uso de verapamilo (inhibidor de la P-Glicoproteína) en la epilepsia refractaria Agos 01 Oct 01 Dic 01 Feb 02 Abr 02 Jun Agos 02 02 Oct 02 Nov 02 Fecha de hospitalización Ene 03 Abr 03 verapamilo Enero 03 Summers MA, 2004

Variabilidad en el volumen de distribución D C INCREMENTO DE VOLUMEN D Vd = C 1000 mg Vd = = 20 L 50 mg/L Vd (L/Kg) 0, 1 0, 2 0, 3 0, 4 0, 5 0, 6 C (mg/L) 70 50 35 28 23 140 DESCENSO CONCENTRACIONES

Variabilidad en el aclaramiento Farmacocinética Farmacodinámica CLp = 50 L/h Cp Efecto (%) 80 Dosis CLp = 100 L/h Cp 0 AUC/CMI Dosis Aclaramiento Exposición sistémica (p. K) Respuesta clínica (p. D)
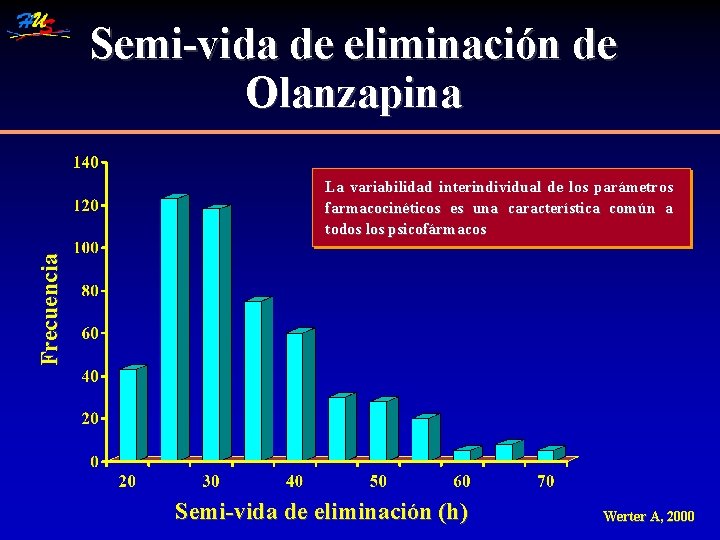
Semi-vida de eliminación de Olanzapina Frecuencia La variabilidad interindividual de los parámetros farmacocinéticos es una característica común a todos los psicofármacos Semi-vida de eliminación (h) Werter A, 2000
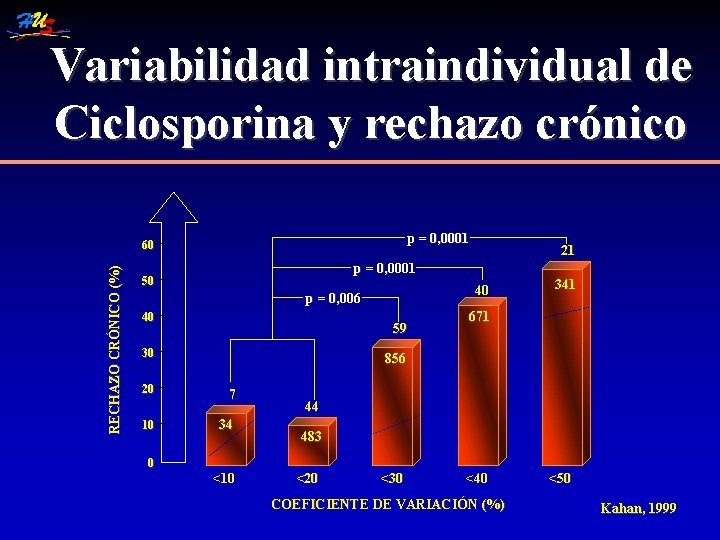
Variabilidad intraindividual de Ciclosporina y rechazo crónico p = 0, 0001 RECHAZO CRÓNICO (%) 60 p = 0, 0001 50 40 p = 0, 006 40 59 30 20 10 21 341 671 856 7 34 44 483 0 <10 <20 <30 <40 COEFICIENTE DE VARIACIÓN (%) <50 Kahan, 1999

Consecuencias derivadas de las interacciones farmacológicas RIESGO DE INTOXICACIONES: por asociación con fármacos que son metabolizados por el CYP 3 A 4 en los que se produce por antagonismo competitivo, un descenso en su aclaramiento. Ej. benzodiazepinas, estatinas, antihistamínicos, inmunosupresores, antiasmáticos, opioides, anticonvulsivantes, anticoagulantes, calcioantagonistas. RIESGO DE FRACASOS TERAPÉUTICOS: por asociación con fármacos inductores del CYP 3 A 4 como carbamazepina, fenobarbital, fenitoina y rifampicin
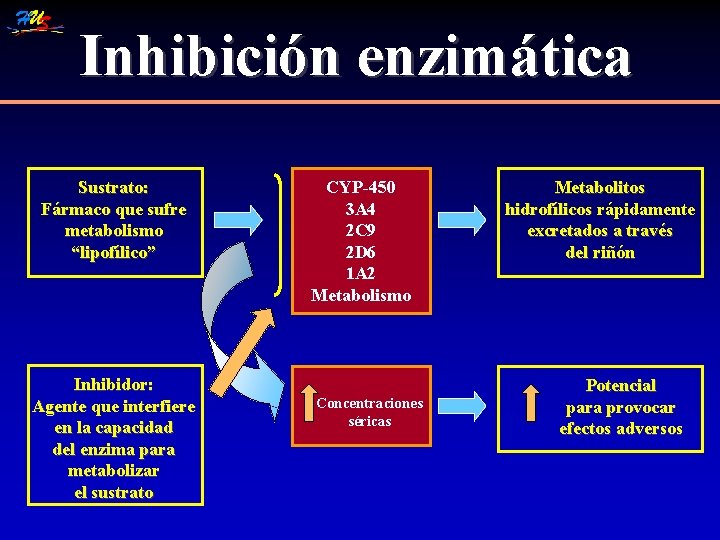
Inhibición enzimática Sustrato: Fármaco que sufre metabolismo “lipofílico” Inhibidor: Agente que interfiere en la capacidad del enzima para metabolizar el sustrato CYP-450 3 A 4 2 C 9 2 D 6 1 A 2 Metabolismo Concentraciones séricas Metabolitos hidrofílicos rápidamente excretados a través del riñón Potencial para provocar efectos adversos
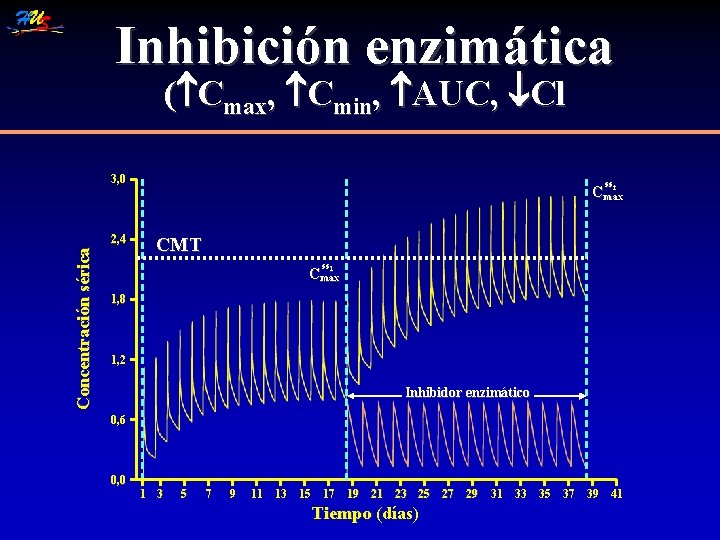
Inhibición enzimática ( Cmax, Cmin, AUC, Cl 3, 0 Concentración sérica 2, 4 ss 2 Cmax CMT ss 1 Cmax 1, 8 1, 2 Inhibidor enzimático 0, 6 0, 0 1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 Tiempo (días) 31 33 35 37 39 41
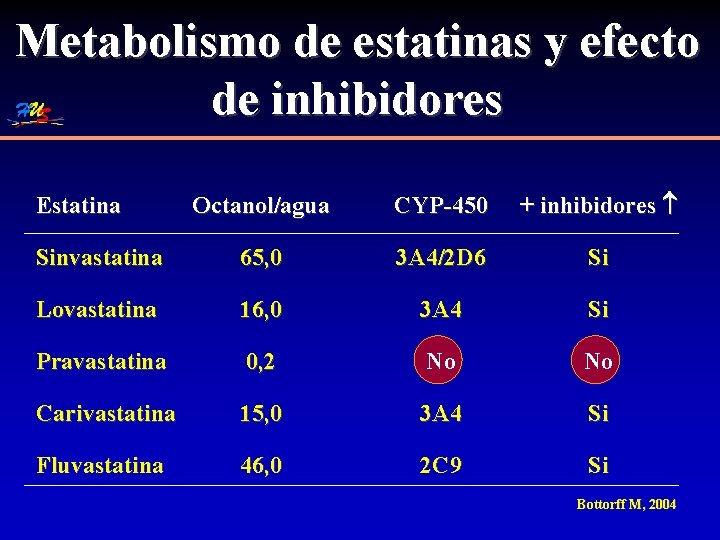
Metabolismo de estatinas y efecto de inhibidores Octanol/agua CYP-450 + inhibidores Sinvastatina 65, 0 3 A 4/2 D 6 Si Lovastatina 16, 0 3 A 4 Si Pravastatina 0, 2 No No Carivastatina 15, 0 3 A 4 Si Fluvastatina 46, 0 2 C 9 Si Estatina Bottorff M, 2004

Propuesta de la FDA para los estudios de interacciones

Variabilidad en la respuesta EFICACIA TOXICIDAD CONCENTRACIÓN “La excesiva complejidad de los procesos fisiológicos y de los organismos en los que son observados impone respeto por el dicho de que no hay dos pacientes iguales” C. Bernard 1895
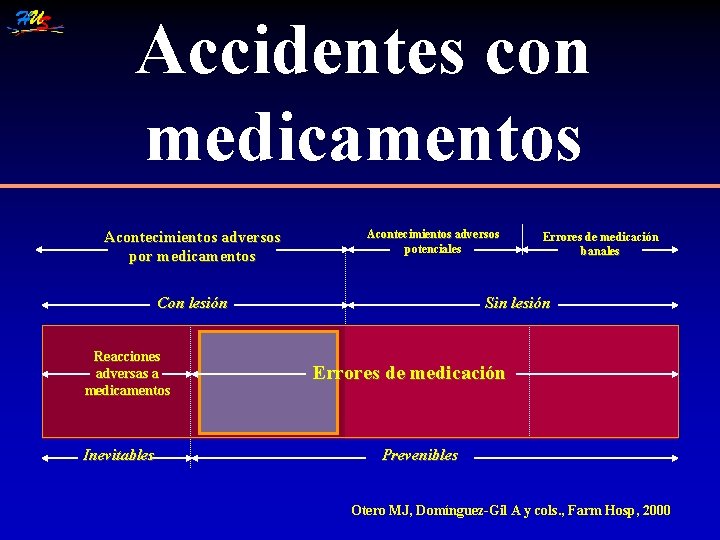
Accidentes con medicamentos Acontecimientos adversos por medicamentos Acontecimientos adversos potenciales Con lesión Reacciones adversas a medicamentos Inevitables Errores de medicación banales Sin lesión Errores de medicación Prevenibles Otero MJ, Domínguez-Gil A y cols. , Farm Hosp, 2000
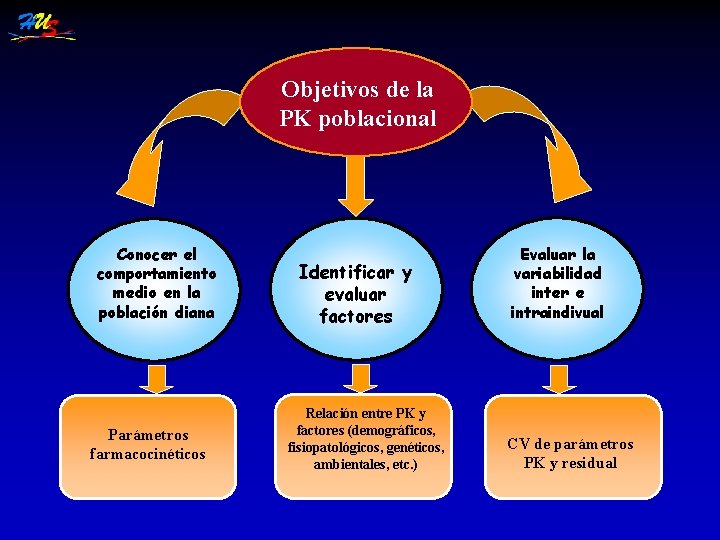
Objetivos de la PK poblacional Conocer el comportamiento medio en la población diana Parámetros farmacocinéticos Identificar y evaluar factores Relación entre PK y factores (demográficos, fisiopatológicos, genéticos, ambientales, etc. ) Evaluar la variabilidad inter e intraindivual CV de parámetros PK y residual
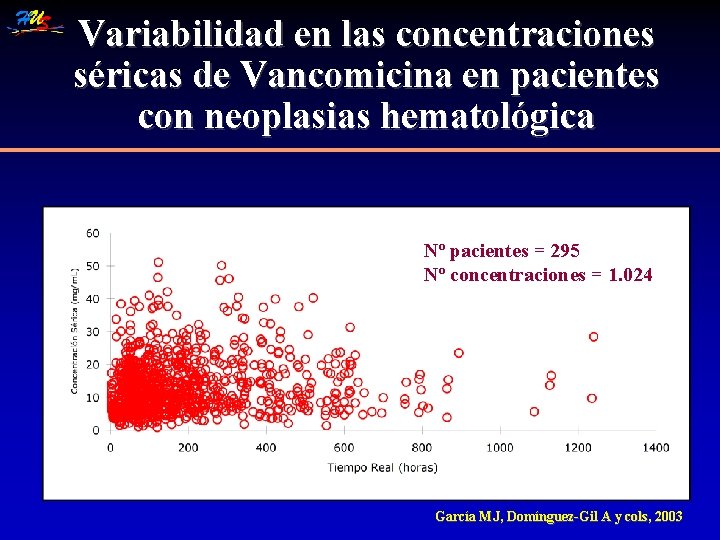
Variabilidad en las concentraciones séricas de Vancomicina en pacientes con neoplasias hematológica Nº pacientes = 295 Nº concentraciones = 1. 024 García MJ, Domínguez-Gil A y cols, 2003
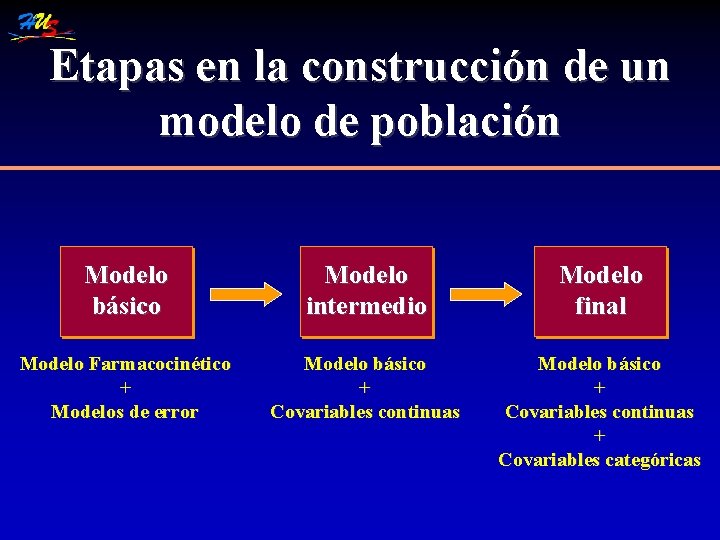
Etapas en la construcción de un modelo de población Modelo básico Modelo intermedio Modelo final Modelo Farmacocinético + Modelos de error Modelo básico + Covariables continuas + Covariables categóricas

Farmacocinética poblacional de amikacina en pacientes con neoplasias hematológicas (n=207) Modelos Ecuaciones Función Objetivo Básico Cl = 5, 04 Vd = 30, 1 2249, 23 Intermedio Cl = 1, 15 Clcr Vd = 0, 42 PCT 1933, 36 Final Cl = 1, 11 Clcr (1+0, 20 LMA) Vd = 0, 37 PCT (1+0, 30 H) 1916, 44 Covariables continuas: edad, peso, Clcr, semanas postquimioterapia, ECOG. Covariables categóricas: diagnostico, nutrición parenteral, medicación asociada, neutropenia, hipoalbuminemia, sobrehidratación Lanao JM, Domínguez-Gil A y cols, 1999


Bridging Study – ICH E 5 – A supplemental study performed in the new region to provide pharmacodynamic or clinical data on efficacy, safety, dosage and dose regimen in the new region that will allow extrapolation of the foreign clinical data package to the new region. Such studies could include further pharmacokinetic information. Definition of not only p. K but also p. D and doseresponse early in the development program may facilitate the determination of the need for, and nature of, any requisite bridging data. Tanigawara Y, 2002
Corrección de dosis de Docetaxel 60 mg/m 2 100 mg/m 2 p. K/p. D poblacional Datos clínicos p. K/p. D Perfil de eficacia y seguridad
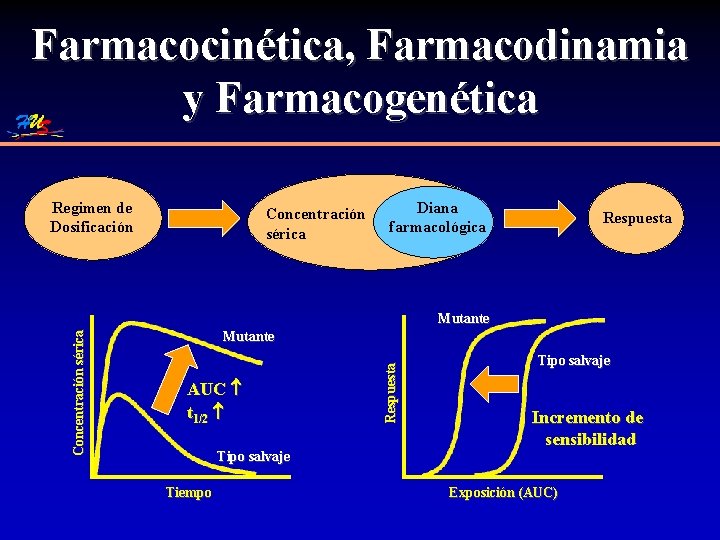
Farmacocinética, Farmacodinamia y Farmacogenética Regimen de Dosificación Concentración sérica Diana farmacológica Respuesta Mutante AUC t 1/2 Tipo salvaje Tiempo Respuesta Concentración sérica Mutante Tipo salvaje Incremento de sensibilidad Exposición (AUC)

Aplicaciones de la Farmacogenética Investigación y desarrollo de medicamentos Ø Selección de posibles candidatos Ø Mejorar criterios de inclusión / exclusión Ø Mejorar la eficiencia de los ensayos clínicos Ø Evergreening Utilización clínica Ø Identificar grupos de riesgo y/o de eficacia Ø Terapéutica más efectiva e individualizada
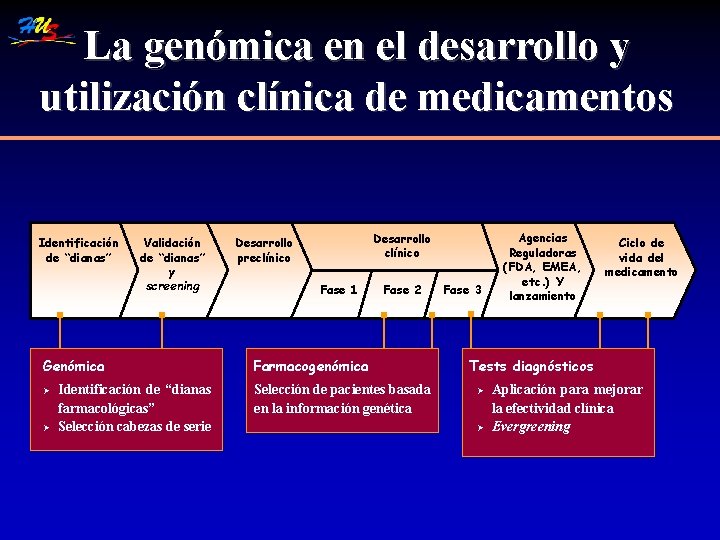
La genómica en el desarrollo y utilización clínica de medicamentos Identificación de “dianas” Validación de “dianas” y screening Genómica Ø Ø Identificación de “dianas farmacológicas” Selección cabezas de serie Desarrollo clínico Desarrollo preclínico Fase 1 Fase 2 Farmacogenómica Selección de pacientes basada en la información genética Fase 3 Agencias Reguladoras (FDA, EMEA, etc. ) Y lanzamiento Ciclo de vida del medicamento Tests diagnósticos Ø Ø Aplicación para mejorar la efectividad clínica Evergreening

22 Marzo de 2005
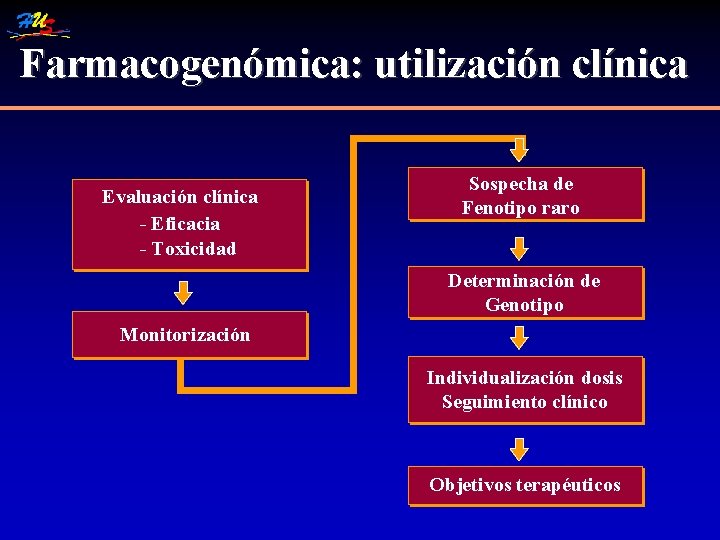
Farmacogenómica: utilización clínica Evaluación clínica - Eficacia - Toxicidad Sospecha de Fenotipo raro Determinación de Genotipo Monitorización Individualización dosis Seguimiento clínico Objetivos terapéuticos

“When the defined metabolic ratio ranges as used, as rule of thumb in clinical practice, aberrant genotypes can be more easily detected” Jan van der Weide, 2005

Integrando la farmacogenética en el “Pharma Pipeline” “If the drug company is able to include the use of the test on the label for therapy then it has achieved a powerful tool in its ability to extend the patent life of the drug. As long as the test is kept proprietary it will be impossible for a generic manufacturar to launch a drug into the market” www. currentdrugdiscovery. com, October 2004
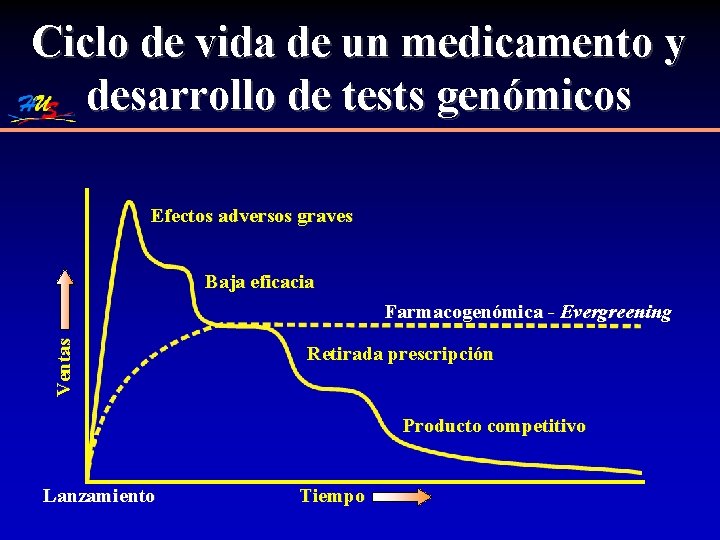
Ciclo de vida de un medicamento y desarrollo de tests genómicos Efectos adversos graves Baja eficacia Ventas Farmacogenómica - Evergreening Retirada prescripción Producto competitivo Lanzamiento Tiempo

“The Right Dose of The Right Drug for The Right Indication for The Right Patient at The Right Time”
- Slides: 36