La toxicocintique dans lvaluation des risques Alain BousquetMlou

La toxicocinétique dans l’évaluation des risques Alain Bousquet-Mélou UMR 1331 TOXALIM Laboratoire de Physiologie-Pharmacologie-Thérapeutique Ecole Nationale Vétérinaire de Toulouse Avril 2016 1
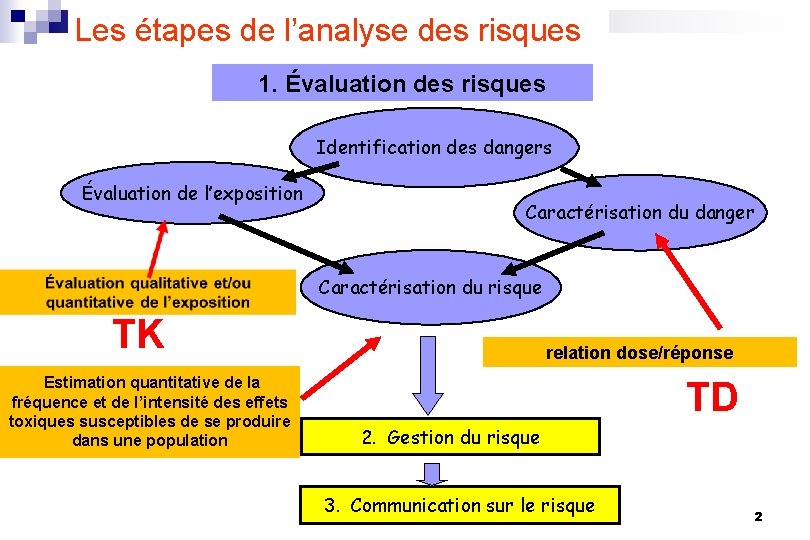
Les étapes de l’analyse des risques 1. Évaluation des risques Identification des dangers Évaluation de l’exposition Caractérisation du danger Caractérisation du risque TK Estimation quantitative de la fréquence et de l’intensité des effets toxiques susceptibles de se produire dans une population relation dose/réponse TD 2. Gestion du risque 3. Communication sur le risque 2
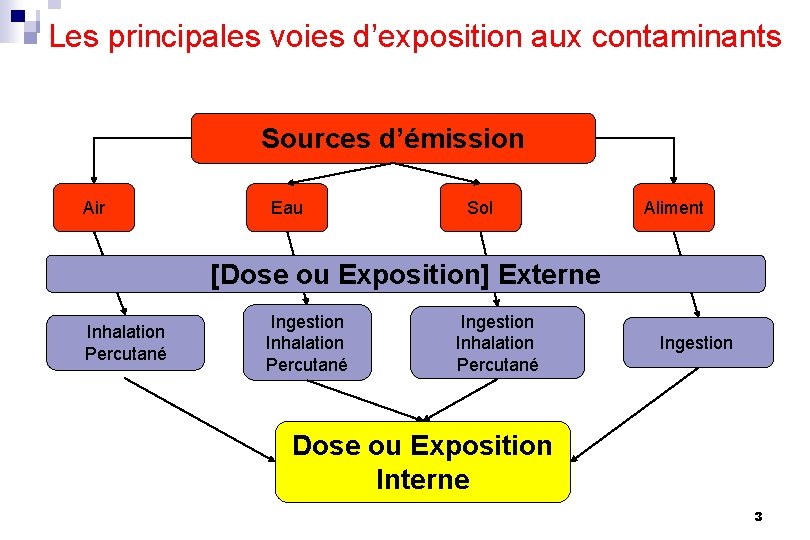
Les principales voies d’exposition aux contaminants Sources d’émission Air Eau Sol Aliment [Dose ou Exposition] Externe Inhalation Percutané Ingestion Dose ou Exposition Interne 3

La (pharmaco)toxicologie Toxicodynamie Toxicocinétique Action du toxique sur l’organisme Action de l’organisme sur le toxique 4
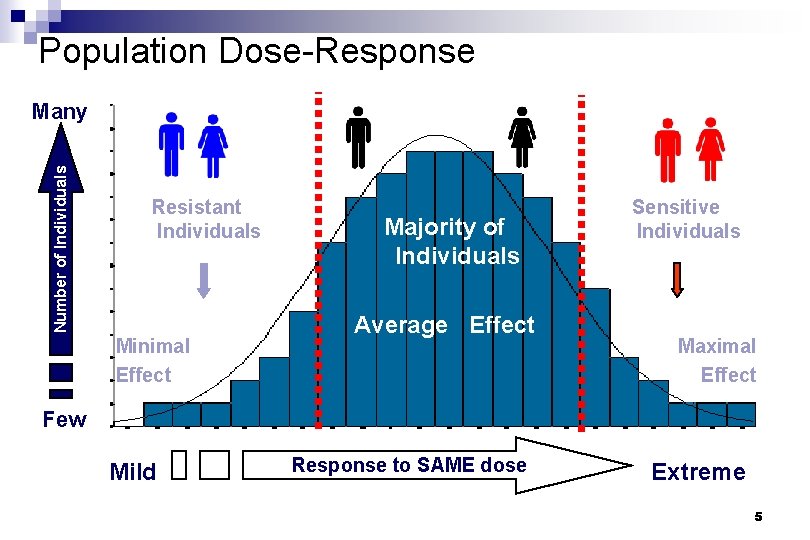
Population Dose-Response Number of Individuals Many Resistant Individuals Minimal Effect Majority of Individuals Average Effect Sensitive Individuals Maximal Effect Few Mild Response to SAME dose Extreme 5
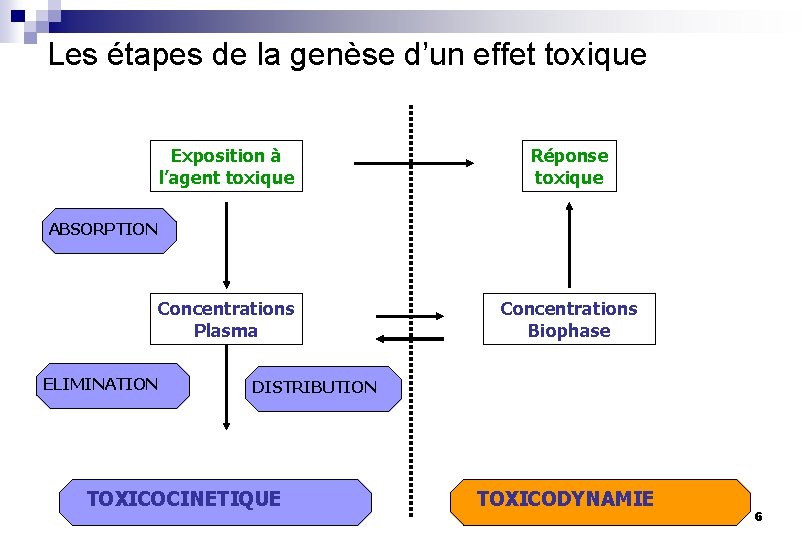
Les étapes de la genèse d’un effet toxique Exposition à l’agent toxique Réponse toxique Concentrations Plasma Concentrations Biophase ABSORPTION ELIMINATION DISTRIBUTION TOXICOCINETIQUE TOXICODYNAMIE 6
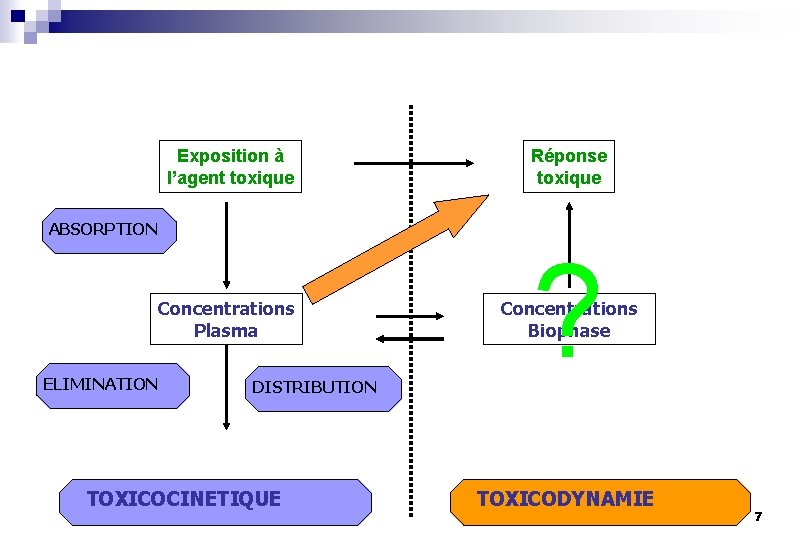
Exposition à l’agent toxique Réponse toxique Concentrations Plasma Concentrations Biophase ABSORPTION ELIMINATION DISTRIBUTION TOXICOCINETIQUE ? TOXICODYNAMIE 7
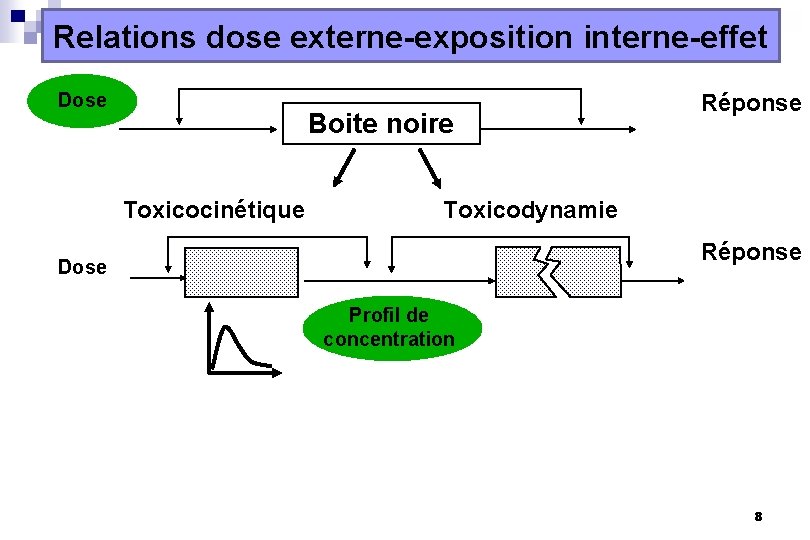
Relations dose externe-exposition interne-effet Dose Boite noire Toxicocinétique Réponse Toxicodynamie Réponse Dose Profil de concentration 8

Relations dose externe-exposition interne-effet Dose Boite noire Toxicocinétique Réponse Toxicodynamie Réponse Dose Profil de concentration Variabilité toxicocinétique / Variabilité toxicodynamique A mesurer et à prendre en compte pour la gestion du risque 9
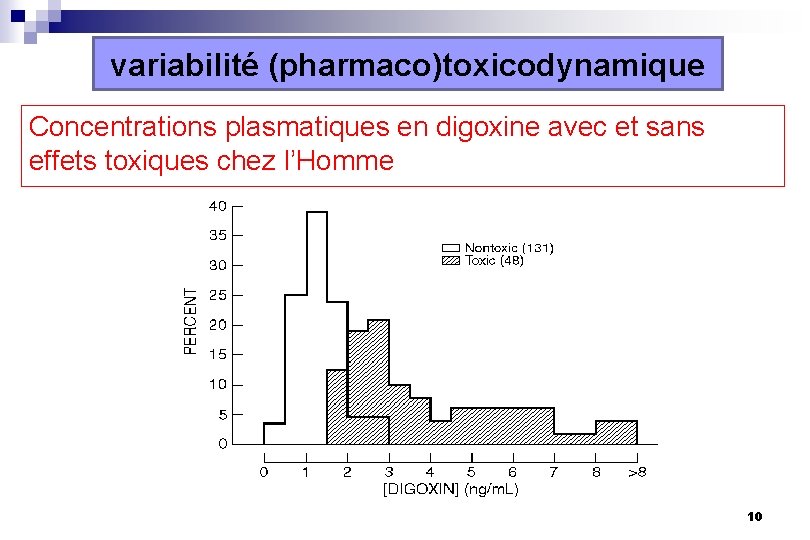
variabilité (pharmaco)toxicodynamique Concentrations plasmatiques en digoxine avec et sans effets toxiques chez l’Homme 10

variabilité (pharmaco)toxicocinétique Concentrations plasmatiques en phénytoïne chez l’Homme Concentrations moyennes après une dose identique de 300 mg 11
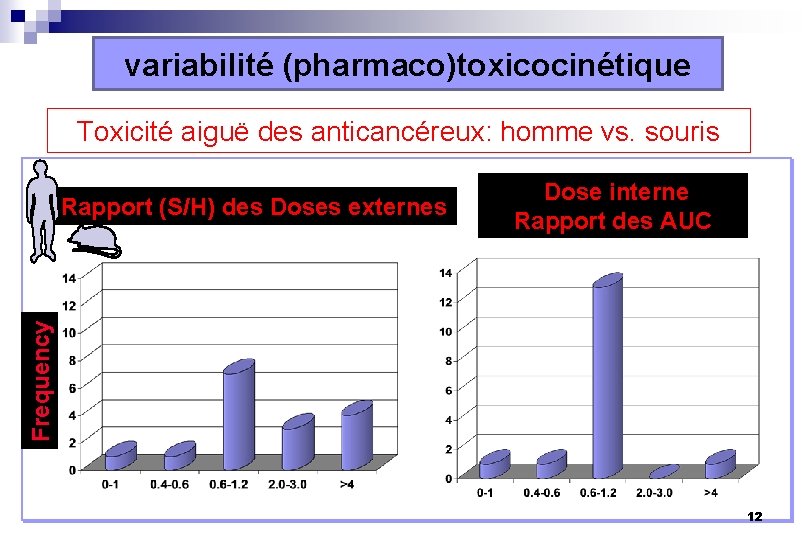
variabilité (pharmaco)toxicocinétique Toxicité aiguë des anticancéreux: homme vs. souris Frequency Rapport (S/H) des Doses externes Dose interne Rapport des AUC 12

Toxicocinétique Les étapes du devenir d’un toxique 13

Les étapes pharmaco(toxico)cinétiques n Absorption Etapes du devenir qui conduisent le produit administré de son site d’administration jusqu’à la circulation générale n Distribution Répartition du produit administré dans l’organisme à partir de la circulation générale 14

Les étapes pharmaco(toxico)cinétiques n Métabolisme Ensemble des processus qui modifient les structures chimiques des composés administrés - Essentiellement : biotransformations hépatiques n Elimination Ensemble des processus qui permettent aux composés administrés de quitter l’organisme. - Excrétion : urinaire, biliaire, salivaire, dans le lait etc… - Métabolisation 15
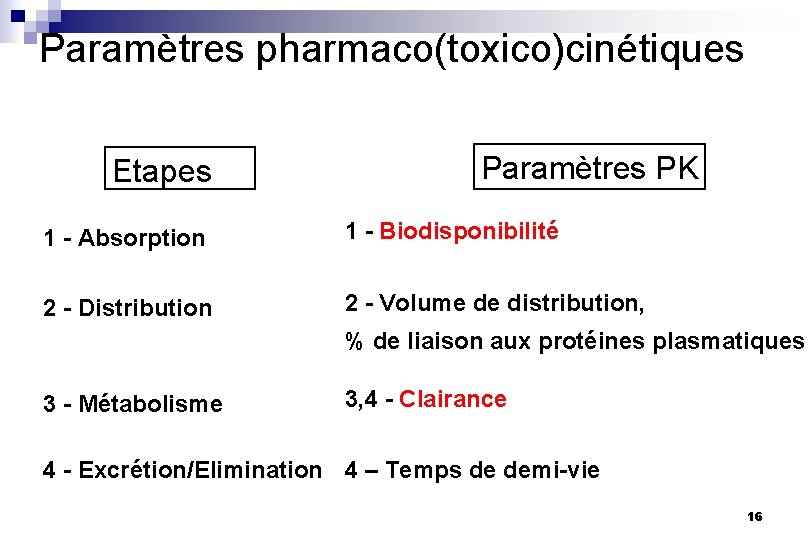
Paramètres pharmaco(toxico)cinétiques Etapes Paramètres PK 1 - Absorption 1 - Biodisponibilité 2 - Distribution 2 - Volume de distribution, % de liaison aux protéines plasmatiques 3 - Métabolisme 3, 4 - Clairance 4 - Excrétion/Elimination 4 – Temps de demi-vie 16

L’élimination 17
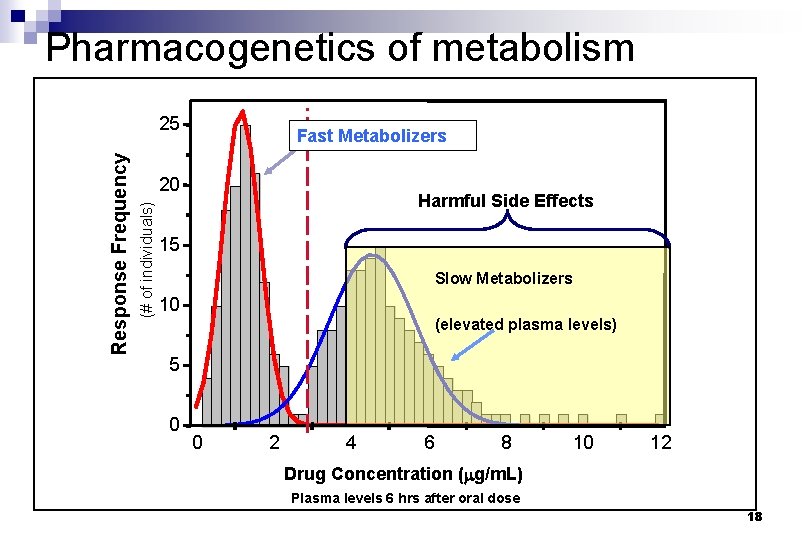
Pharmacogenetics of metabolism Fast Metabolizers 20 (# of individuals) Response Frequency 25 Harmful Side Effects 15 Slow Metabolizers 10 (elevated plasma levels) 5 0 0 2 4 6 8 10 12 Drug Concentration ( g/m. L) Plasma levels 6 hrs after oral dose 18
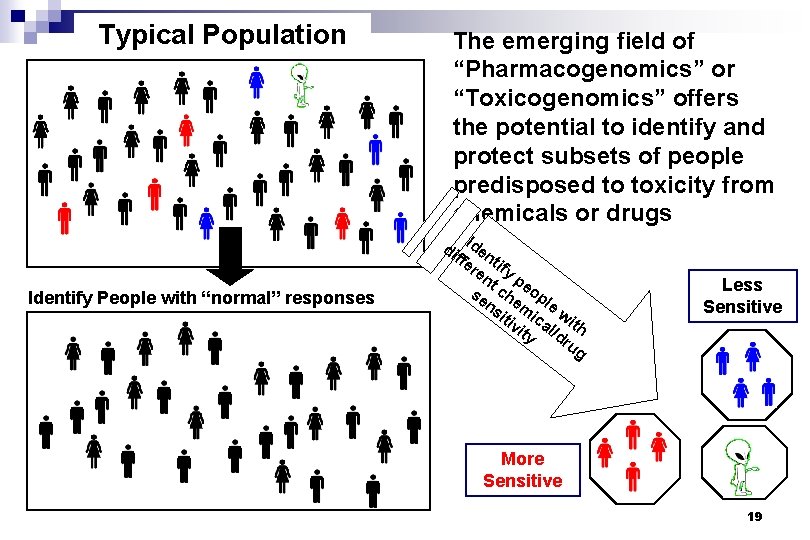
Typical Population Identify People with “normal” responses The emerging field of “Pharmacogenomics” or “Toxicogenomics” offers the potential to identify and protect subsets of people predisposed to toxicity from chemicals or drugs di Iden ffe t re ify nt pe se ch op ns em le iti ic wit vi al/ h ty d ru g Less Sensitive More Sensitive 19

La biodisponibilité 20

La biodisponibilité n La biodisponibilité décrit comment un principe actif devient disponible pour produire son action biologique ¨ Quantité disponible n Exprimée en pourcentage de la dose administrée ¨ Vitesse du processus 21
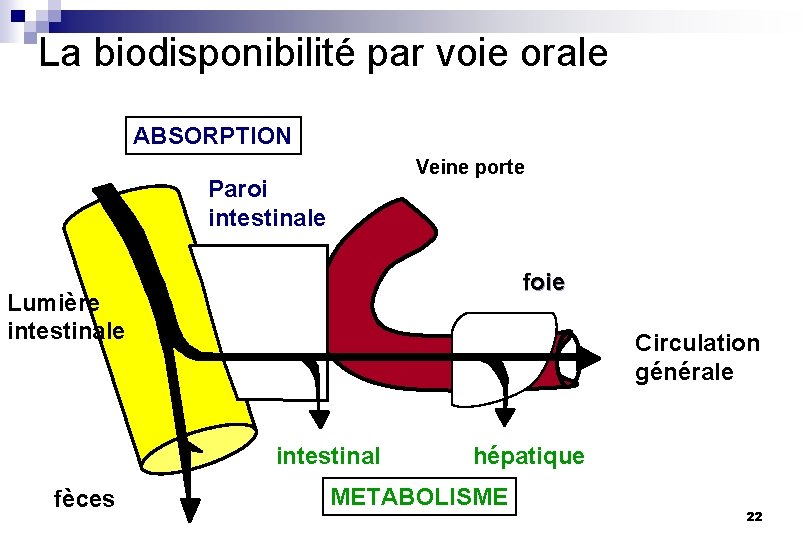
La biodisponibilité par voie orale ABSORPTION Veine porte Paroi intestinale foie Lumière intestinale Circulation générale intestinal fèces hépatique METABOLISME 22

Toxicocinétique La relation entre doses externes et expositions internes 23

La relation qui lie toxicocinétique et toxicodynamie Dose = Clairance Biodisponibilité X Exposition interne X AUC 24

La relation qui lie toxicococinétique et toxicodynamie Dose par unité de temps = Clairance Biodisponibilité Propriétés toxicocinétiques X Concentration moyenne Propriétés toxicodynamiques 25

La relation issue de l’approche TK/TD : de l’exposition interne à la dose externe TD Dose = Clairance plasmatique x concentration de référence Biodisponibilité TK Dose de référence (BMD) Dose journalière admissible Dose journalière tolérable Dose sans effet observé Dose sans effet nocif observé (NOAEL) 26
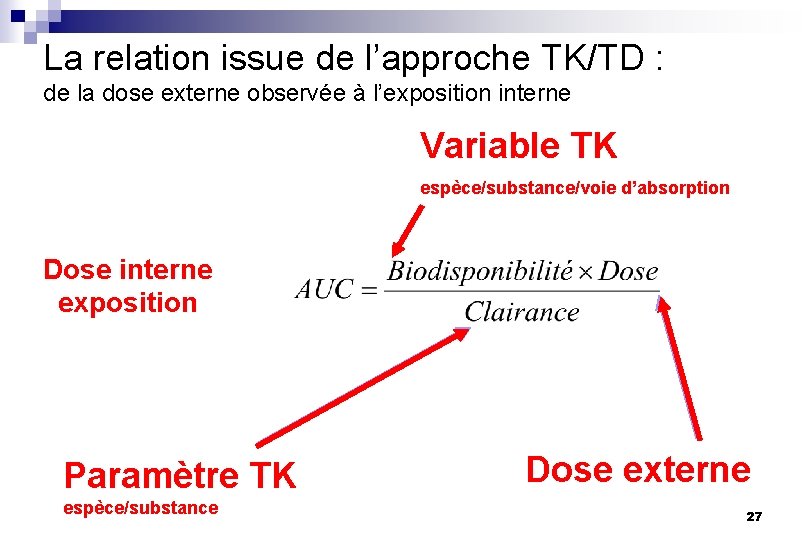
La relation issue de l’approche TK/TD : de la dose externe observée à l’exposition interne Variable TK espèce/substance/voie d’absorption Dose interne exposition Paramètre TK espèce/substance Dose externe 27

Toxicocinétique Quantification des facteurs d’incertitude 28
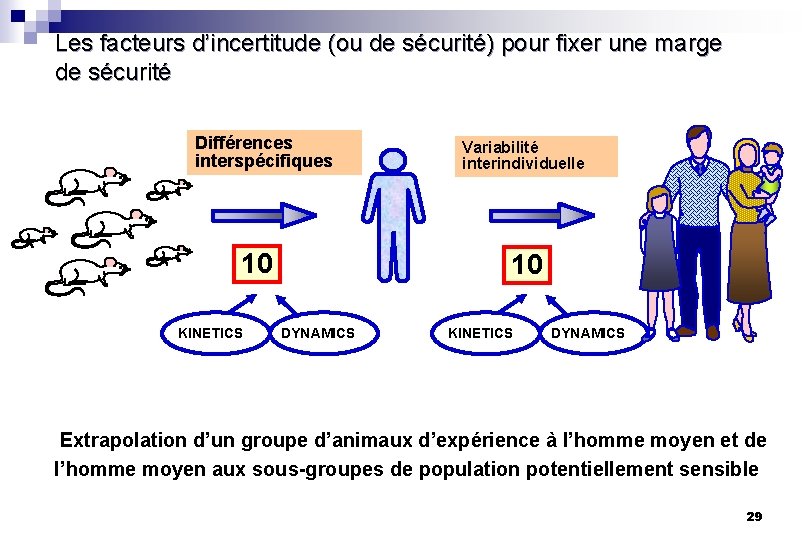
Les facteurs d’incertitude (ou de sécurité) pour fixer une marge de sécurité Différences interspécifiques 10 KINETICS Variabilité interindividuelle 10 DYNAMICS KINETICS DYNAMICS Extrapolation d’un groupe d’animaux d’expérience à l’homme moyen et de l’homme moyen aux sous-groupes de population potentiellement sensible 29
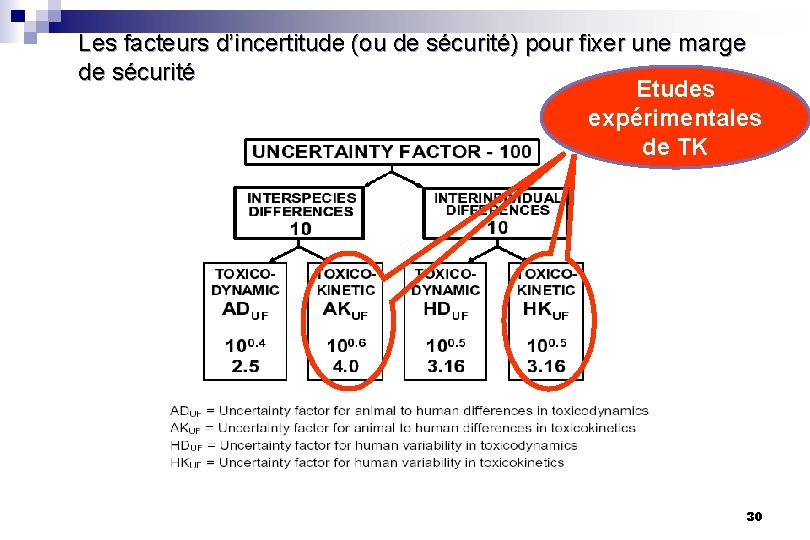
Les facteurs d’incertitude (ou de sécurité) pour fixer une marge de sécurité Etudes expérimentales de TK 30

Prediction de la variabilité TK ou TK/TD au sein de la population humaine avec des simulations Monte Carlo

Modèles probabilistes (stochastiques) • Prise en compte des différentes sources de variabilité et d’incertitude dans l’estimation de l’exposition
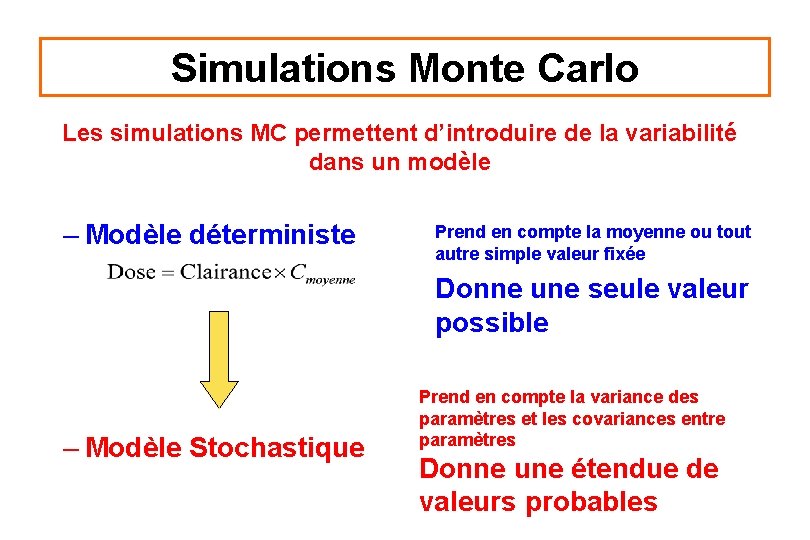
Simulations Monte Carlo Les simulations MC permettent d’introduire de la variabilité dans un modèle – Modèle déterministe Prend en compte la moyenne ou tout autre simple valeur fixée Donne une seule valeur possible – Modèle Stochastique Prend en compte la variance des paramètres et les covariances entre paramètres Donne une étendue de valeurs probables
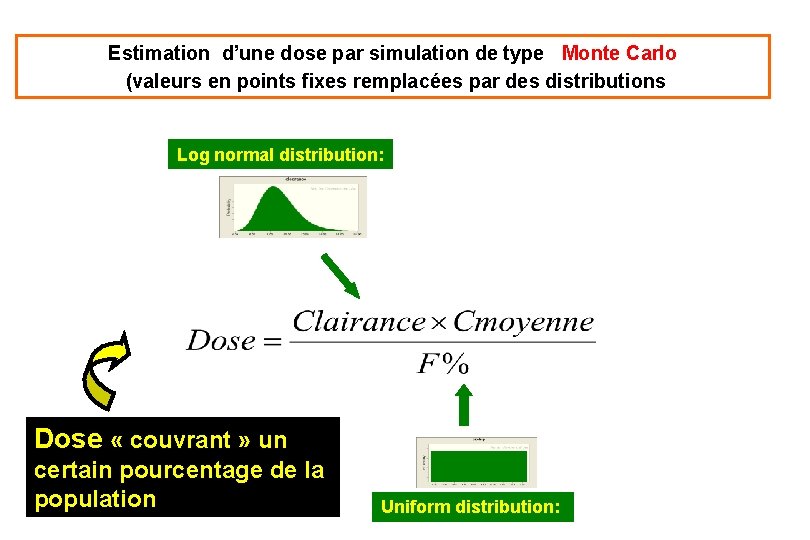
Estimation d’une dose par simulation de type Monte Carlo (valeurs en points fixes remplacées par des distributions Log normal distribution: Dose « couvrant » un certain pourcentage de la population Uniform distribution:
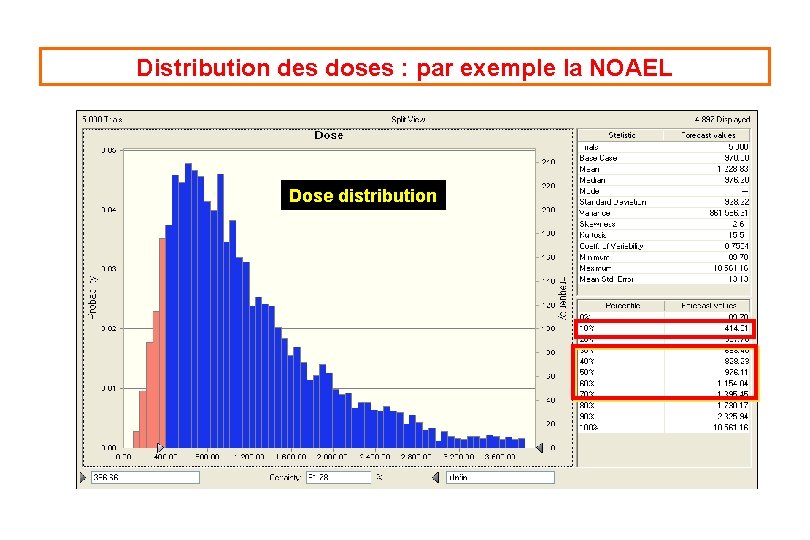
Distribution des doses : par exemple la NOAEL Dose distribution

Monte Carlo - Home Page Mc. Namara et al. Design, development and validation of software for modelling dietary exposure to food chemicals and nutrients Food additives and contaminants 2003 vol 20 pp. S 8 -S 26
- Slides: 37