La Tabla Peridica Qumica Miss Romina Vergara C

La Tabla Periódica Química Miss Romina Vergara C 2020

Unidad 2: Tabla Periódica Objetivos • Conocer la Tabla Periódica de los elementos químicos. • Identificar la estructura y organización de la Tabla Periódica.

¿Qué es la Tabla Periódica? Es la herramienta gráfica donde se representan a todos los elementos organizados según el orden creciente de sus números atómicos.

Historia de la Tabla Periódica Durante el siglo XIX, se descubrieron nuevas sustancias, las que fueron identificadas como elementos químicos. Los investigadores al disponer de más elementos y conocer sus características, observaron que las propiedades de algunos eran muy similares , así nace la idea de clasificarlos.

Historia de la Tabla Periódica Johann Dobereiner En 1829, clasificó algunos elementos en grupos de tres, que denominó triadas. Los elementos de cada triada tenían propiedades químicas similares, así como propiedades físicas crecientes. (Modelo de las Triadas 1780 - 1849)

Historia de la Tabla Periódica John Newlands En 1863 propuso que los elementos se ordenaban en “octavas”, ya que observó, tras ordenar los elementos según el aumento de la masa atómica, que ciertas propiedades se repetían cada 8 elementos. Ley de las Octavas 1838 - 1898

John Newland: “Ley delas Octavas” La propuesta de Newland fue ridiculizada en su momento por la comunidad científica. Cuando intentó publicar su trabajo en la Sociedad de Química, se le rechazó, aduciendo a que dicha propuesta era tan arbitraria como el haber sugerido un orden alfabético de los elementos (además a partir del K esta regla dejaba de cumplirse)

Mendeleiev y Meyer En 1869 publican por separado, una clasificación para los elementos químicos. Ambos los ordenaron de acuerdo al incremento de la masa atómica, observando propiedades similares a intervalos regulares. Dimitri Mendeleiev Lothar Meyer

Mendeleiev La ley periódica propuesta por Mendeleiev indicaba: “Las propiedades de los elementos químicos no son arbitrarias, si no que varían con la masa atómica de manera periódica” Gracias a esta ley periódica se puso , predecir la existencia de otros elementos, no descubiertos, así como sus propiedades. Debido a esto Mendeleiev dejo espacios vacios, para aquellos elementos faltantes.
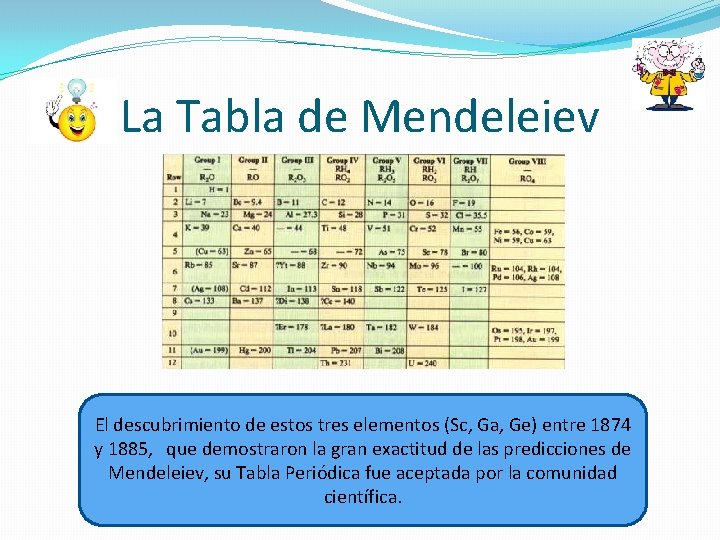
La Tabla de Mendeleiev El descubrimiento de estos tres elementos (Sc, Ga, Ge) entre 1874 y 1885, que demostraron la gran exactitud de las predicciones de Mendeleiev, su Tabla Periódica fue aceptada por la comunidad científica.

Tabla Periódica Actual En 1912 Henry Moseley, ordeno los elementos de la tabla periódica usando como criterio de clasificación el número atómico (Z), ya que el valor es el mismo para todos los átomos de un mismo elemento tenga o no isótopos (diferente número de neutrones)

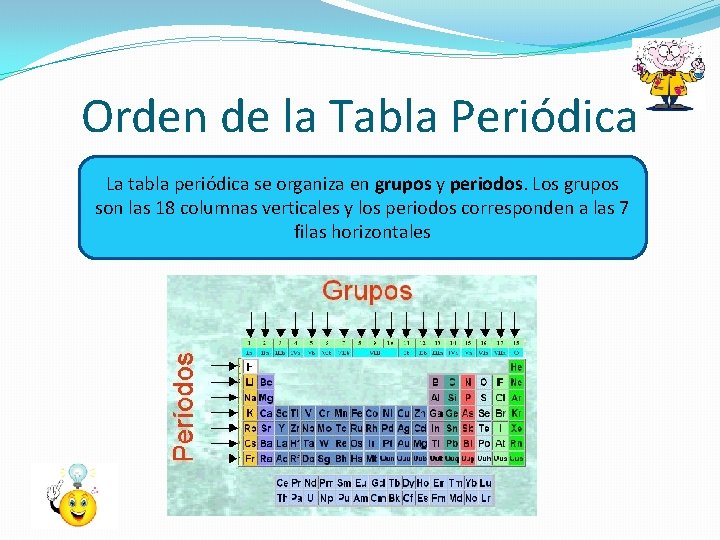
Orden de la Tabla Periódica La tabla periódica se organiza en grupos y periodos. Los grupos son las 18 columnas verticales y los periodos corresponden a las 7 filas horizontales
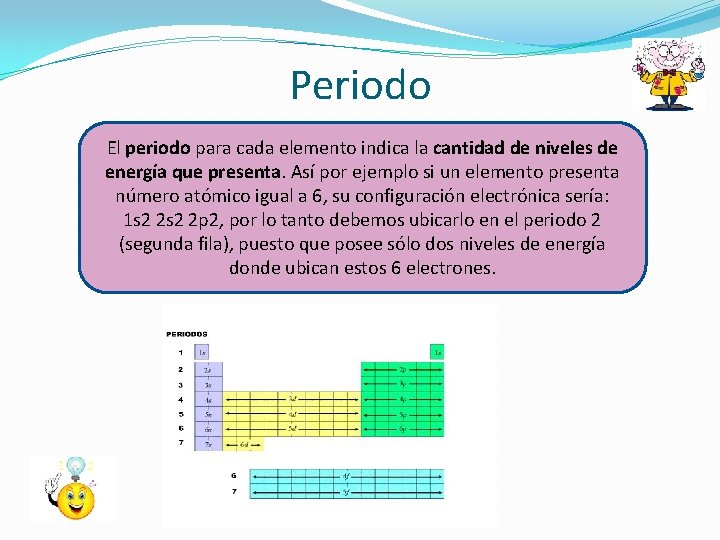
Periodo El periodo para cada elemento indica la cantidad de niveles de energía que presenta. Así por ejemplo si un elemento presenta número atómico igual a 6, su configuración electrónica sería: 1 s 2 2 p 2, por lo tanto debemos ubicarlo en el periodo 2 (segunda fila), puesto que posee sólo dos niveles de energía donde ubican estos 6 electrones.
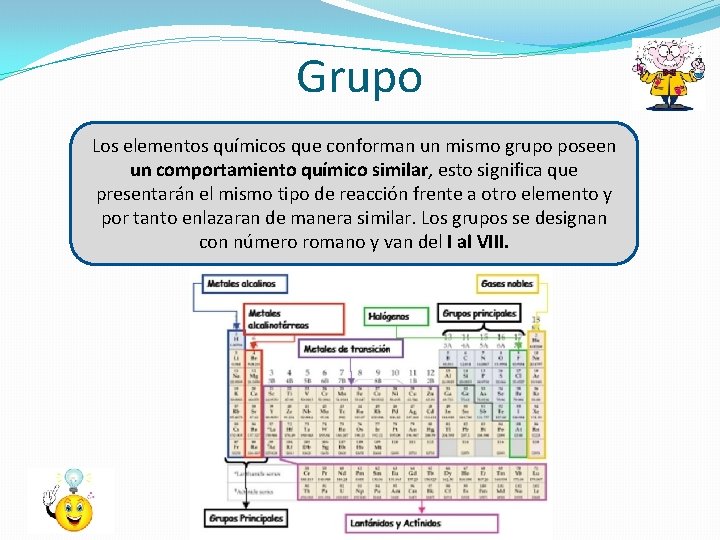
Grupo Los elementos químicos que conforman un mismo grupo poseen un comportamiento químico similar, esto significa que presentarán el mismo tipo de reacción frente a otro elemento y por tanto enlazaran de manera similar. Los grupos se designan con número romano y van del I al VIII.
- Slides: 15