La stratgie actuelle du traitement du diabte de

La stratégie actuelle du traitement du diabète de type 2. A partir d’un cas clinique Pr Denis Raccah Hôpital Sainte Marguerite CHU Marseille 1

• Homme de 51 ans • ATCD de diabète de type 2 chez sa mère et son frère • 87 kg pour 1, 78 m soit IMC= 27, 4 kg/m² • Tour de taille= 103 cm • Examen clinique sans anomalie • FDR : HTA traitée par IEC : PA= 130/75 mm. Hg Tabagisme sevré il y a 1 ans EAL : LDL= 1, 25 g/l – HDL= 0, 39 g/l – Triglycérides= 2, 15 g/l • Fonction rénale et bilan hépatique sans anomalie • GAJ mesurée à 1, 41 g/l et 1, 67 g/l à une semaine d’intervalle Etape 1 Quelle prise en charge thérapeutique proposer ?

Recommandations HAS novembre 2006 : Prise en charge précoce et stricte de l’hyperglycémie et des FDR associés au diabète La prévention et le traitement de la microangiopathie et de la macro-angiopathie diabétiques reposent sur : • Mesures hygiéno-diététiques, exercice physique, perte de poids • Recherche de la normalisation glycémique • Pression artérielle : contrôle strict < 130/80 mm. Hg • Lipides : cibles pour le LDL cholestérol graduées selon un niveau de risque CV croissant • Arrêt du tabac
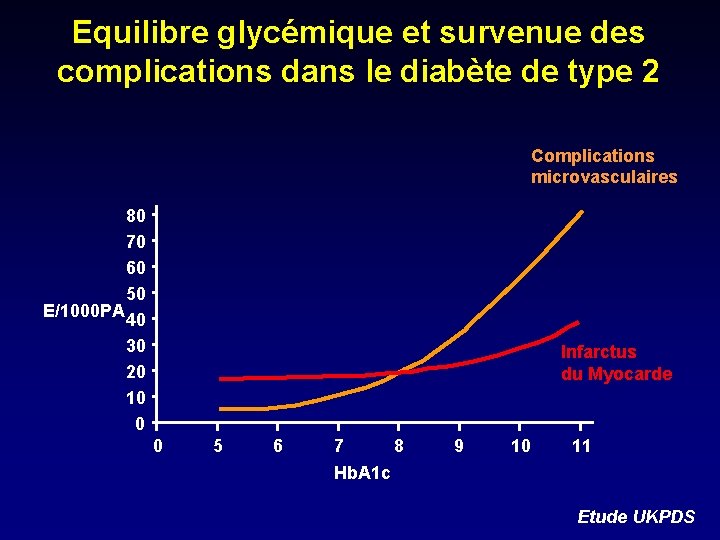
Equilibre glycémique et survenue des complications dans le diabète de type 2 Complications microvasculaires 80 70 60 50 E/1000 PA 40 30 20 10 0 Infarctus du Myocarde 0 5 6 7 8 Hb. A 1 c 9 10 11 Etude UKPDS
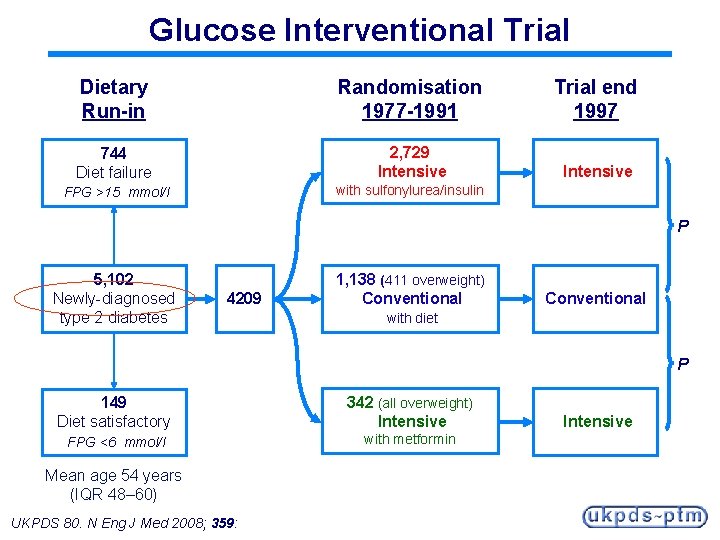
Glucose Interventional Trial Dietary Run-in Randomisation 1977 -1991 Trial end 1997 744 Diet failure 2, 729 Intensive FPG >15 mmol/l with sulfonylurea/insulin P 5, 102 Newly-diagnosed type 2 diabetes 4209 1, 138 (411 overweight) Conventional with diet P 149 Diet satisfactory 342 (all overweight) Intensive FPG <6 mmol/l with metformin Mean age 54 years (IQR 48– 60) UKPDS 80. N Eng J Med 2008; 359: Intensive
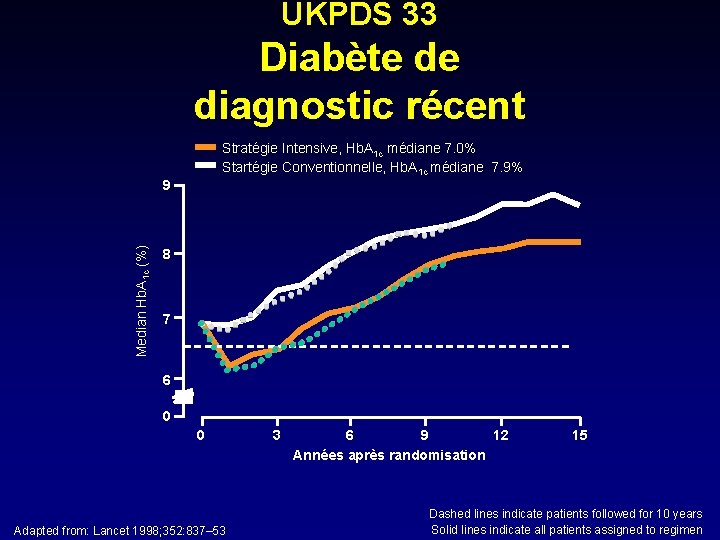
UKPDS 33 Diabète de diagnostic récent Stratégie Intensive, Hb. A 1 c médiane 7. 0% Startégie Conventionnelle, Hb. A 1 c médiane 7. 9% Median Hb. A 1 c (%) 9 8 7 6 0 0 Adapted from: Lancet 1998; 352: 837– 53 3 6 9 12 Années après randomisation 15 Dashed lines indicate patients followed for 10 years Solid lines indicate all patients assigned to regimen
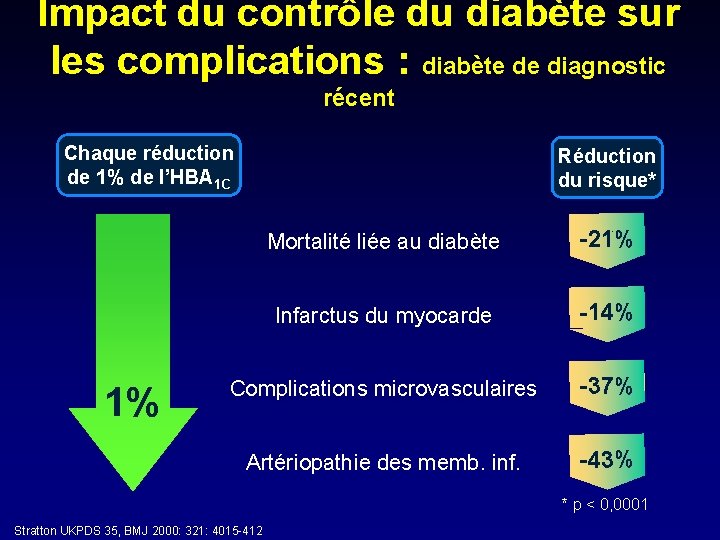
Impact du contrôle du diabète sur les complications : diabète de diagnostic récent Chaque réduction de 1% de l’HBA 1 C 1% Réduction du risque* Mortalité liée au diabète - 21% Infarctus du myocarde - 14% Complications microvasculaires - 37% Artériopathie des memb. inf. - 43% * p < 0, 0001 Stratton UKPDS 35, BMJ 2000: 321: 4015 -412
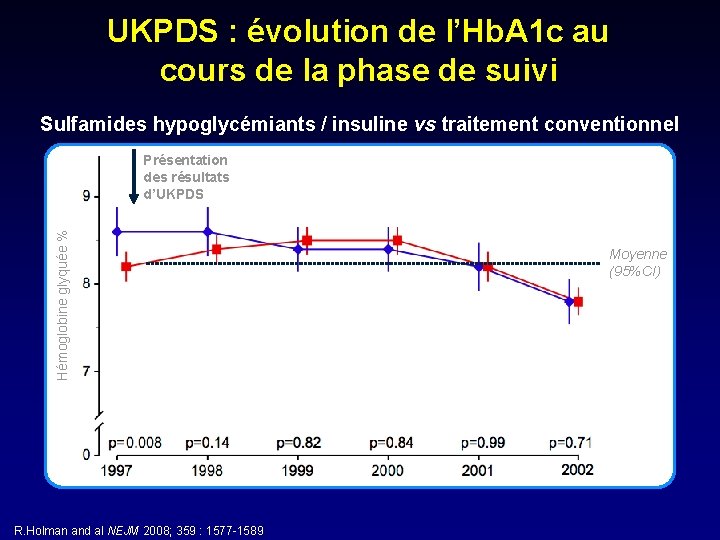
UKPDS : évolution de l’Hb. A 1 c au cours de la phase de suivi Sulfamides hypoglycémiants / insuline vs traitement conventionnel Hémoglobine glyquée % Présentation des résultats d’UKPDS R. Holman and al NEJM 2008; 359 : 1577 -1589 Moyenne (95%CI)
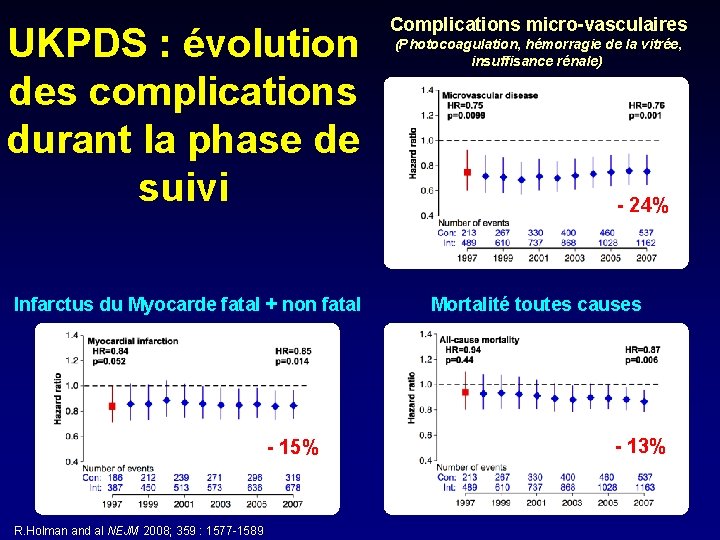
UKPDS : évolution des complications durant la phase de suivi Complications micro-vasculaires Infarctus du Myocarde fatal + non fatal Mortalité toutes causes - 15% R. Holman and al NEJM 2008; 359 : 1577 -1589 (Photocoagulation, hémorragie de la vitrée, insuffisance rénale) - 24% - 13%

Objectifs glycémiques chez le diabétique de type 2 Il faut être exigeant d’emblée ! Objectif d’Hb. A 1 c < 6, 5% Notion de mémoire glycémique

Etape 2 Après 6 mois de mesures hygiéno-diététiques respectées : - IMC= 27 kg/m², Tour de taille= 97 cm - GAJ= 1, 24 g/l et Hb. A 1 c= 6, 9 % - Fonction rénale et bilan hépatique sans anomalie Quel est votre attitude thérapeutique?

Traitement du diabète de type 2 : une attitude consensuelle Prescription de METFORMINE en première intention en dehors des situation de contre-indications ou d’intolérance • Recommandations internationales (EASD-ADA) : dès le diagnostic en association aux mesures hygiéno-diététiques • Recommandations HAS 2006 : dès que l’Hb. A 1 c dépasse 6% malgré les mesures hygiéno-diététiques

Etape 3 Vous le revoyez 2 ans plus tard : - Metformine 1000 mg 2 cp/j depuis 6 mois - IMC= 27, 8 kg/m², Tour de taille= 100 cm - Hb. A 1 c= 7, 4% Quelle attitude thérapeutique?
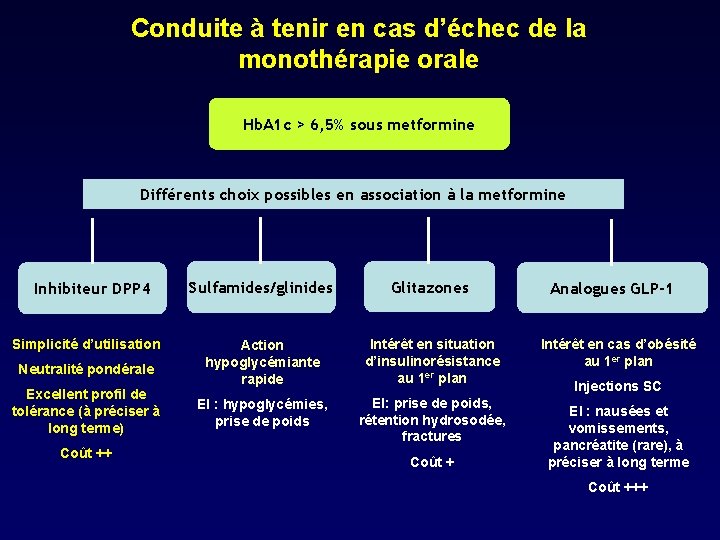
Conduite à tenir en cas d’échec de la monothérapie orale Hb. A 1 c > 6, 5% sous metformine Différents choix possibles en association à la metformine Inhibiteur DPP 4 Simplicité d’utilisation Neutralité pondérale Excellent profil de tolérance (à préciser à long terme) Coût ++ Sulfamides/glinides Glitazones Action hypoglycémiante rapide Intérêt en situation d’insulinorésistance au 1 er plan EI : hypoglycémies, prise de poids EI: prise de poids, rétention hydrosodée, fractures Coût + Analogues GLP-1 Intérêt en cas d’obésité au 1 er plan Injections SC EI : nausées et vomissements, pancréatite (rare), à préciser à long terme Coût +++

Régulation de l’homéostasie du glucose par les incrétines (GLP-1 et GIP) effets sur la fonction des cellules des îlots de Langherans Ingestion d’aliment Insuline éGlucose dépendante par les cellules β (GLP-1 et GIP) Tube digestif Libération des incrétines par le TD captation et stockage de Glucose dans le muscle et le tissu adipeux Pancréas Beta cells Alpha cells Contrôle du glucose plus stable GLP-1 et GIP activés äGlucagon Glucose dépendante par les cellules (GLP-1) libération de Glucose dans le sang par le foie Brubaker PL, Drucker DJ. Endocrinology. 2004; 145: 2653– 2659; Zander M et al. Lancet. 2002; 359: 824– 830; Ahrén B. Curr Diab Rep. 2003; 3: 365– 372; Holst JJ. Diabetes Metab Res Rev. 2002; 18: 430– 441; Holz GG, Chepurny OG. Curr Med Chem. 2003; 10: 2471– 2483; Creutzfeldt WOC et al. Diabetes Care. 1996; 19: 580– 586; Drucker DJ. Diabetes Care. 2003; 26: 2929– 2940.

Le GLP-1 est très rapidement dégradé par la DPP 4 GLP-1 Repas T½= 1 à 2 min S° intestinale De GLP-1 (7 -36) actif DPP -4 GLP-1 (9 -36) inactif (>80% du pool) GLP-1 = glucagon-like peptide– 1; DPP-4 = dipeptidyl-peptidase Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126 -1131. – 4
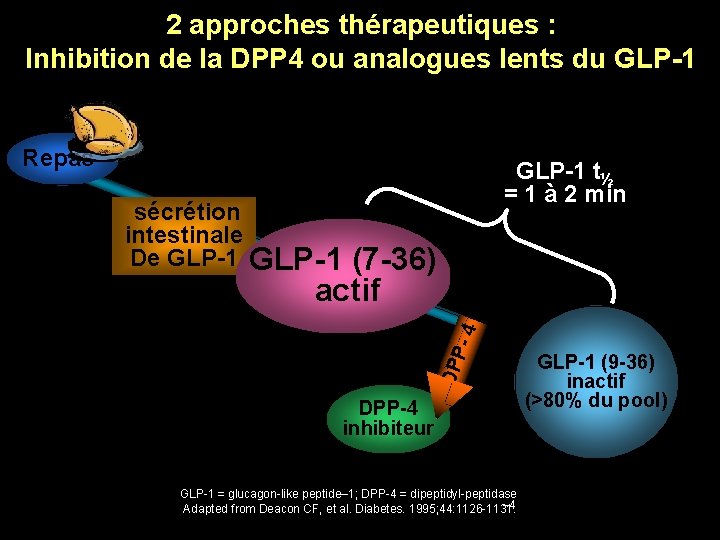
2 approches thérapeutiques : Inhibition de la DPP 4 ou analogues lents du GLP-1 Repas GLP-1 t½ = 1 à 2 min DPP -4 sécrétion intestinale De GLP-1 (7 -36) actif DPP-4 inhibiteur GLP-1 = glucagon-like peptide– 1; DPP-4 = dipeptidyl-peptidase – 4 Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126 -1131. GLP-1 (9 -36) inactif (>80% du du pool) (>80% pool)
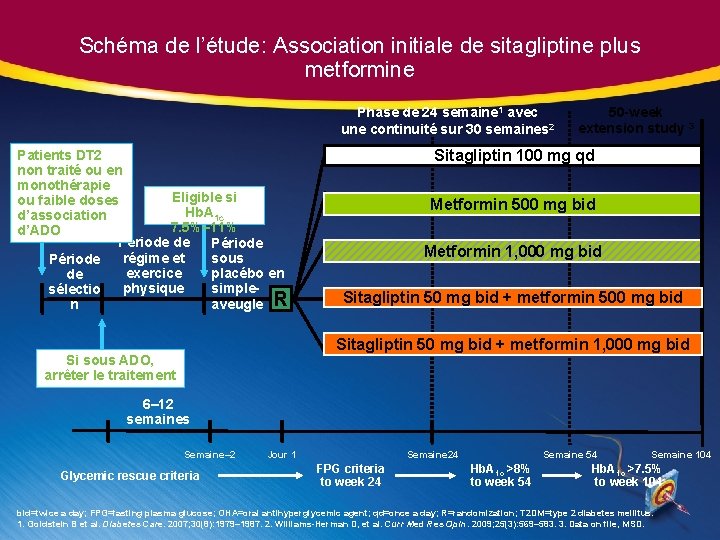
Schéma de l’étude: Association initiale de sitagliptine plus metformine Phase de 24 semaine 1 avec une continuité sur 30 semaines 2 Patients DT 2 non traité ou en monothérapie Eligible si ou faible doses Hb. A 1 c d’association 7. 5%– 11% d’ADO Période de Période régime et sous Période exercice placébo en de physique simplesélectio aveugle R n 50 -week extension study 3 Sitagliptin 100 mg qd Metformin 500 mg bid Metformin 1, 000 mg bid Sitagliptin 50 mg bid + metformin 500 mg bid Sitagliptin 50 mg bid + metformin 1, 000 mg bid Si sous ADO, arrêter le traitement 6– 12 semaines Semaine– 2 Glycemic rescue criteria Jour 1 Semaine 24 FPG criteria to week 24 Semaine 54 Hb. A 1 c >8% to week 54 Semaine 104 Hb. A 1 c >7. 5% to week 104 bid=twice a day; FPG=fasting plasma glucose; OHA=oral antihyperglycemic agent; qd=once a day; R=randomization; T 2 DM=type 2 diabetes mellitus. 1. Goldstein B et al. Diabetes Care. 2007; 30(8): 1979– 1987. 2. Williams-Herman D, et al. Curr Med Res Opin. 2009; 25(3): 569– 583. 3. Data on file, MSD.
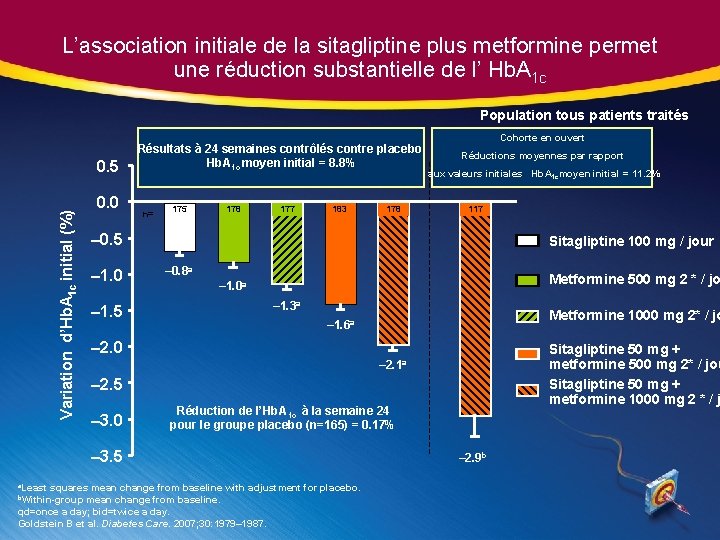
L’association initiale de la sitagliptine plus metformine permet une réduction substantielle de l’ Hb. A 1 c Population tous patients traités Variation d’Hb. A 1 c initial (%) 0. 5 0. 0 Résultats à 24 semaines contrôlés contre placebo Hb. A 1 c moyen initial = 8. 8% n= 175 178 177 183 aux valeurs initiales Hb. A 1 cmoyen initial = 11. 2% 117 – 1. 0 – 1. 5 Sitagliptine 100 mg / jour – 0. 8 a Metformine 500 mg 2 * / jo – 1. 0 a – 1. 3 a Metformine 1000 mg 2* / jo – 1. 6 a – 2. 0 Sitagliptine 50 mg + metformine 500 mg 2* / jou Sitagliptine 50 mg + metformine 1000 mg 2 * / j – 2. 1 a – 2. 5 – 3. 0 Réduction de l’Hb. A 1 c à la semaine 24 pour le groupe placebo (n=165) = 0. 17% squares mean change from baseline with adjustment for placebo. mean change from baseline. qd=once a day; bid=twice a day. Goldstein B et al. Diabetes Care. 2007; 30: 1979– 1987. b. Within-group Réductions moyennes par rapport – 0. 5 – 3. 5 a. Least 178 Cohorte en ouvert – 2. 9 b
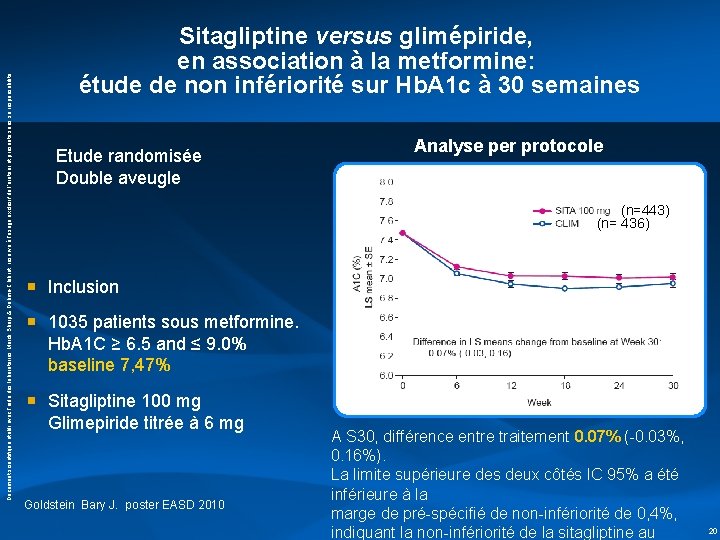
Document scientifique établi avec l’aide des laboratoires Merck Sharp & Dohme-Chibret, réservé à l’usage exclusif de l’orateur et présenté sous sa responsabilité Sitagliptine versus glimépiride, en association à la metformine: étude de non infériorité sur Hb. A 1 c à 30 semaines Etude randomisée Double aveugle Analyse per protocole (n=443) (n= 436) ■ Inclusion ■ 1035 patients sous metformine. Hb. A 1 C ≥ 6. 5 and ≤ 9. 0% baseline 7, 47% ■ Sitagliptine 100 mg Glimepiride titrée à 6 mg Goldstein Bary J. poster EASD 2010 A S 30, différence entre traitement 0. 07% (-0. 03%, 0. 16%). La limite supérieure des deux côtés IC 95% a été inférieure à la marge de pré-spécifié de non-infériorité de 0, 4%, indiquant la non-infériorité de la sitagliptine au 20
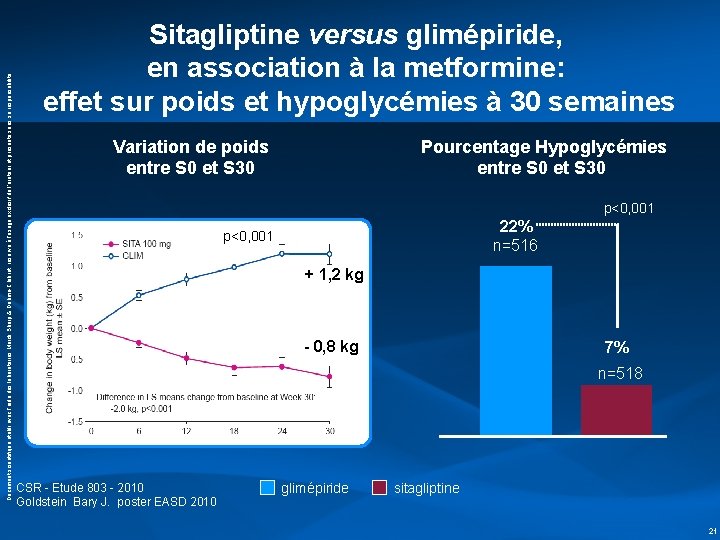
Document scientifique établi avec l’aide des laboratoires Merck Sharp & Dohme-Chibret, réservé à l’usage exclusif de l’orateur et présenté sous sa responsabilité Sitagliptine versus glimépiride, en association à la metformine: effet sur poids et hypoglycémies à 30 semaines Variation de poids entre S 0 et S 30 Pourcentage Hypoglycémies entre S 0 et S 30 p<0, 001 22% n=516 p<0, 001 + 1, 2 kg - 0, 8 kg 7% n=518 CSR - Etude 803 - 2010 Goldstein Bary J. poster EASD 2010 glimépiride sitagliptine 21
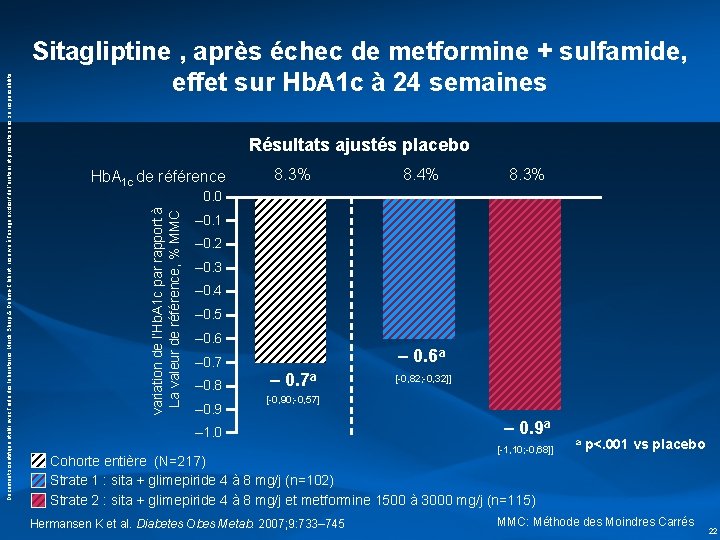
Résultats ajustés placebo Hb. A 1 c de référence 8. 3% 8. 4% 8. 3% 0. 0 variation de l’Hb. A 1 c par rapport à La valeur de référence, % MMC Document scientifique établi avec l’aide des laboratoires Merck Sharp & Dohme-Chibret, réservé à l’usage exclusif de l’orateur et présenté sous sa responsabilité Sitagliptine , après échec de metformine + sulfamide, effet sur Hb. A 1 c à 24 semaines – 0. 1 – 0. 2 – 0. 3 – 0. 4 – 0. 5 – 0. 6 a – 0. 7 – 0. 8 – 0. 9 – 0. 7 a [-0, 82; -0, 32]] [-0, 90; -0, 57] – 1. 0 – 0. 9 a [-1, 10; -0, 68]] a p<. 001 vs placebo Cohorte entière (N=217) Strate 1 : sita + glimepiride 4 à 8 mg/j (n=102) Strate 2 : sita + glimepiride 4 à 8 mg/j et metformine 1500 à 3000 mg/j (n=115) Hermansen K et al. Diabetes Obes Metab. 2007; 9: 733– 745 MMC: Méthode des Moindres Carrés 22

Conclusion La prise en charge précoce du patient diabétique de type 2 1) Metformine 2) Associée précocément aux Inhibiteurs de la DPP-4 (Sitagliptine Januvia) car même efficacité à ce stade que les sulfamides hypoglycémiants mais sans risque d’hypoglycémies +++ et moindre prise de poids Réévaluation régulière de l’option thérapeutique choisie sur la base de : 1) des bénéfices escomptés (Hb. A 1 c, poids…) 2) la réponse thérapeutique obtenue 3) du profil de tolérance observé (hypoglycémies, effets digestifs)

Back up slides
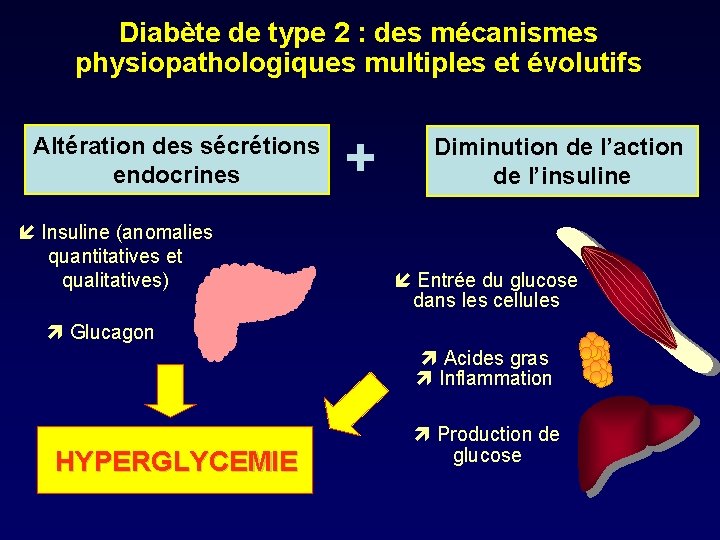
Diabète de type 2 : des mécanismes physiopathologiques multiples et évolutifs Altération des sécrétions endocrines Insuline (anomalies quantitatives et qualitatives) + Diminution de l’action de l’insuline Entrée du glucose dans les cellules Glucagon Acides gras Inflammation HYPERGLYCEMIE Production de glucose

Diabète de type 2 : Insulinorésistance + anomalie de l’insulinosécrétion Temps Insulinorésistance Insulinosécrétion Glycémie Pas de diabète PréDiabète de type 2
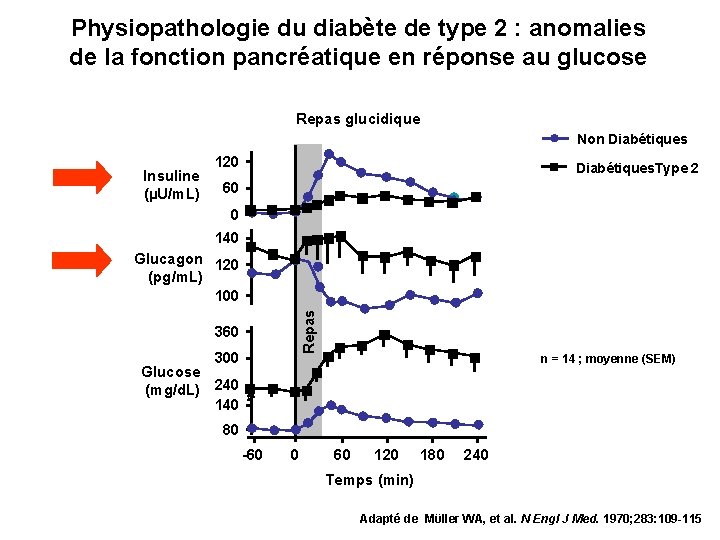
Physiopathologie du diabète de type 2 : anomalies de la fonction pancréatique en réponse au glucose Repas glucidique Non Diabétiques Insuline (µU/m. L) 120 Diabétiques. Type 2 60 0 140 Repas Glucagon 120 (pg/m. L) 100 360 300 n = 14 ; moyenne (SEM) Glucose (mg/d. L) 240 140 80 -60 0 60 120 180 240 Temps (min) Adapté de Mϋller WA, et al. N Engl J Med. 1970; 283: 109 -115
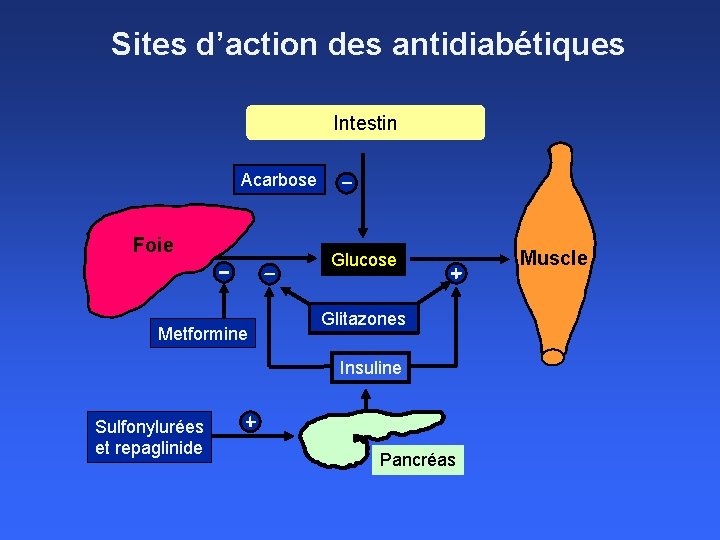
Sites d’action des antidiabétiques Intestin Acarbose Foie Metformine Glucose Glitazones Insuline Sulfonylurées et repaglinide Pancréas Muscle
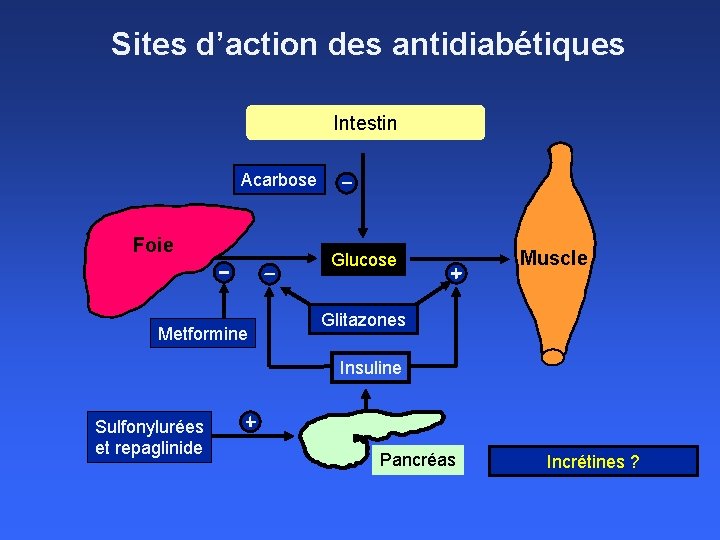
Sites d’action des antidiabétiques Intestin Acarbose Foie Metformine Glucose Muscle Glitazones Insuline Sulfonylurées et repaglinide Pancréas Incrétines ?

Régulation de l’homéostasie du glucose par les incrétines (GLP-1 et GIP) effets sur la fonction des cellules des îlots de Langherans Ingestion d’aliment Insuline éGlucose dépendante par les cellules β (GLP-1 et GIP) Tube digestif Libération des incrétines par le TD captation et stockage de Glucose dans le muscle et le tissu adipeux Pancréas Beta cells Alpha cells Contrôle du glucose plus stable GLP-1 et GIP activés äGlucagon Glucose dépendante par les cellules (GLP-1) libération de Glucose dans le sang par le foie Brubaker PL, Drucker DJ. Endocrinology. 2004; 145: 2653– 2659; Zander M et al. Lancet. 2002; 359: 824– 830; Ahrén B. Curr Diab Rep. 2003; 3: 365– 372; Holst JJ. Diabetes Metab Res Rev. 2002; 18: 430– 441; Holz GG, Chepurny OG. Curr Med Chem. 2003; 10: 2471– 2483; Creutzfeldt WOC et al. Diabetes Care. 1996; 19: 580– 586; Drucker DJ. Diabetes Care. 2003; 26: 2929– 2940.

Le GLP-1 est très rapidement dégradé par la DPP 4 GLP-1 Repas T½= 1 à 2 min S° intestinale De GLP-1 (7 -36) actif DPP -4 GLP-1 (9 -36) inactif (>80% du pool) GLP-1 = glucagon-like peptide– 1; DPP-4 = dipeptidyl-peptidase Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126 -1131. – 4
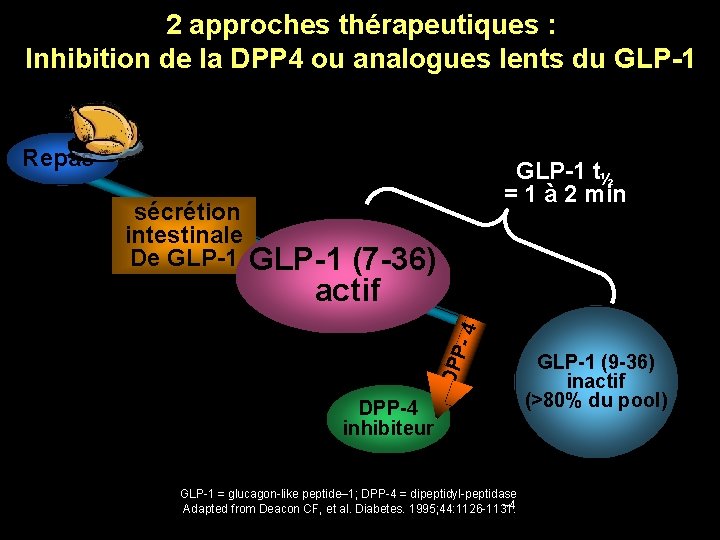
2 approches thérapeutiques : Inhibition de la DPP 4 ou analogues lents du GLP-1 Repas GLP-1 t½ = 1 à 2 min DPP -4 sécrétion intestinale De GLP-1 (7 -36) actif DPP-4 inhibiteur GLP-1 = glucagon-like peptide– 1; DPP-4 = dipeptidyl-peptidase – 4 Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126 -1131. GLP-1 (9 -36) inactif (>80% du du pool) (>80% pool)

Diabète de type 2 : stratégie thérapeutique • Améliorer l’action de l’insuline – Améliorer l'équilibre alimentaire, réduire le surpoids – activité physique – Comprimés : biguanides, glitazones • Corriger le manque d’insuline – Comprimés : sulfamides hypoglycémiants / glinides – Insuline • Diminuer l’absorption digestive des glucides – Eviter les sucres rapides – Comprimés : inhibiteurs des -glucosidases • Améliorer la balance insuline/glucagon, et plus… – inhibiteurs de DPP 4 – incrétino-mimétiques et analogues du GLP-1

Mise en place de mesures hygiénodiététiques adaptées dès le stade d’anomalies modérées de la glycémie

Conditions de prise en charge des dispositifs d’autosurveillance glycémique (JO 12 janvier 2010)

Etape 4 Vous le revoyez 1 an plus tard : - Metformine 1000 mg 3 cp/j et glimépiride 4 mg/j depuis 4 mois - IMC= 28, 0 kg/m², Tour de taille= 102 cm - Hb. A 1 c= 7, 9% - Bilan de retentissement négatif Quelle attitude thérapeutique?
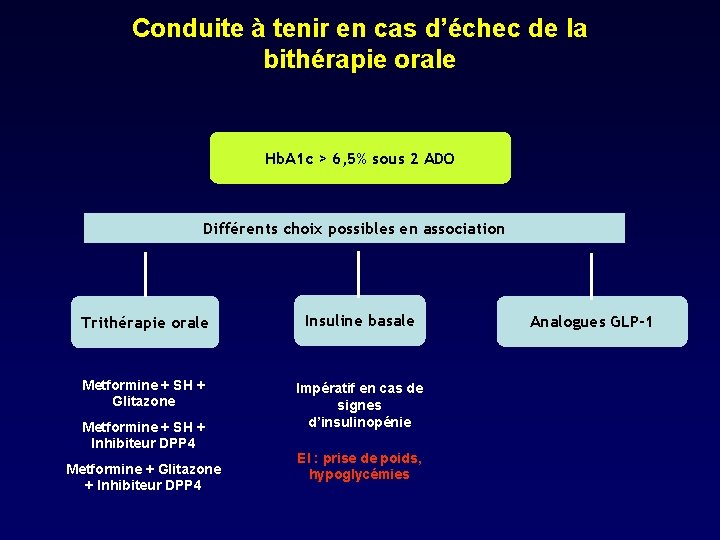
Conduite à tenir en cas d’échec de la bithérapie orale Hb. A 1 c > 6, 5% sous 2 ADO Différents choix possibles en association Trithérapie orale Insuline basale Metformine + SH + Glitazone Impératif en cas de signes d’insulinopénie Metformine + SH + Inhibiteur DPP 4 Metformine + Glitazone + Inhibiteur DPP 4 EI : prise de poids, hypoglycémies Analogues GLP-1
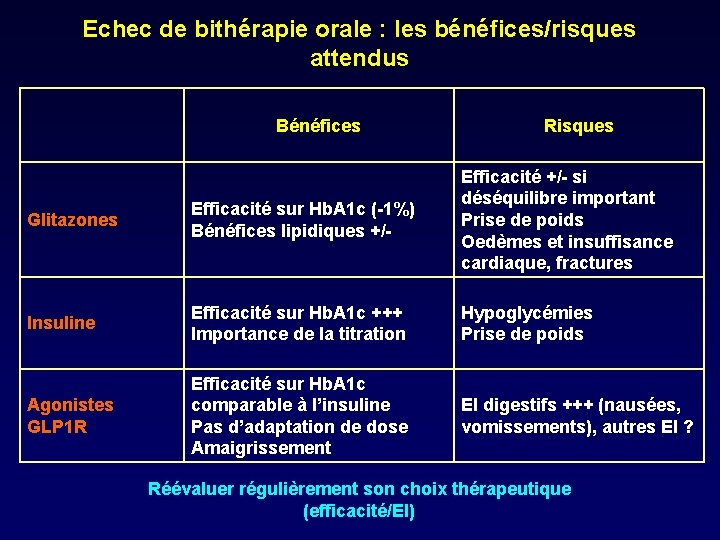
Echec de bithérapie orale : les bénéfices/risques attendus Bénéfices Risques Glitazones Efficacité sur Hb. A 1 c (-1%) Bénéfices lipidiques +/- Efficacité +/- si déséquilibre important Prise de poids Oedèmes et insuffisance cardiaque, fractures Insuline Efficacité sur Hb. A 1 c +++ Importance de la titration Hypoglycémies Prise de poids Agonistes GLP 1 R Efficacité sur Hb. A 1 c comparable à l’insuline Pas d’adaptation de dose Amaigrissement EI digestifs +++ (nausées, vomissements), autres EI ? Réévaluer régulièrement son choix thérapeutique (efficacité/EI)
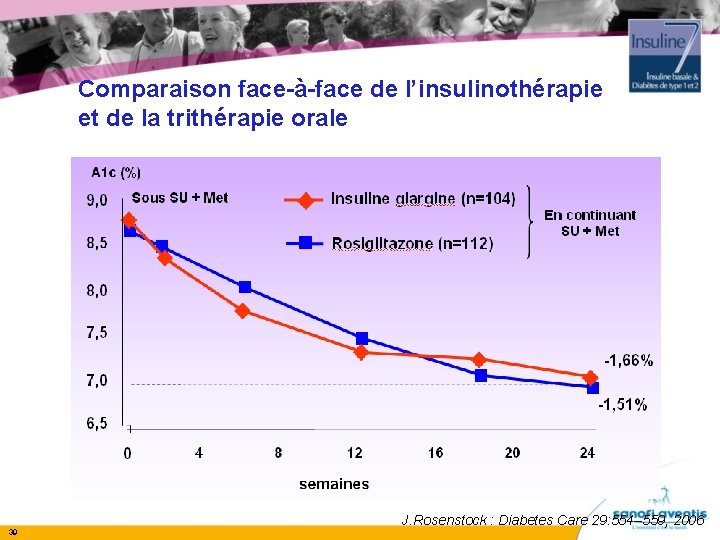
Comparaison face-à-face de l’insulinothérapie et de la trithérapie orale 39 J. Rosenstock : Diabetes Care 29: 554– 559, 2006
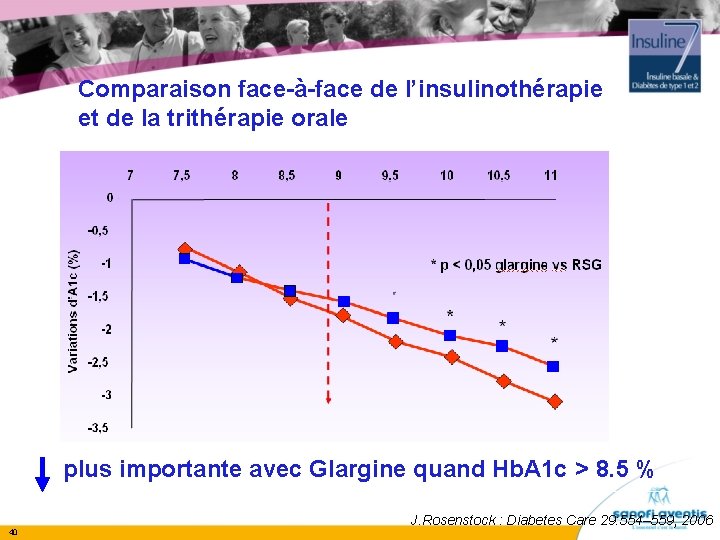
Comparaison face-à-face de l’insulinothérapie et de la trithérapie orale plus importante avec Glargine quand Hb. A 1 c > 8. 5 % 40 J. Rosenstock : Diabetes Care 29: 554– 559, 2006
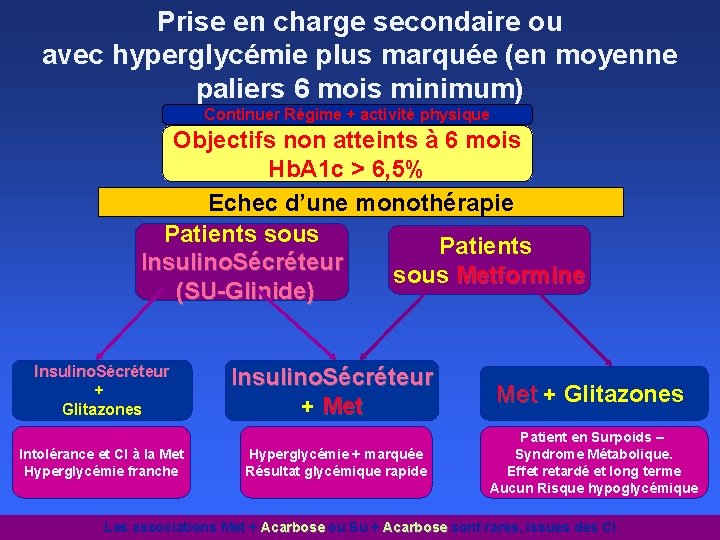
Prise en charge secondaire ou avec hyperglycémie plus marquée (en moyenne paliers 6 mois minimum) Continuer Régime + activité physique Objectifs non atteints à 6 mois Hb. A 1 c > 6, 5% Echec d’une monothérapie Patients sous Patients Insulino. Sécréteur sous Metformine (SU-Glinide) Insulino. Sécréteur + Glitazones Intolérance et CI à la Met Hyperglycémie franche Insulino. Sécréteur + Met + Glitazones Hyperglycémie + marquée Résultat glycémique rapide Patient en Surpoids – Syndrome Métabolique. Effet retardé et long terme Aucun Risque hypoglycémique Les associations Met + Acarbose ou Su + Acarbose sont rares, issues des CI
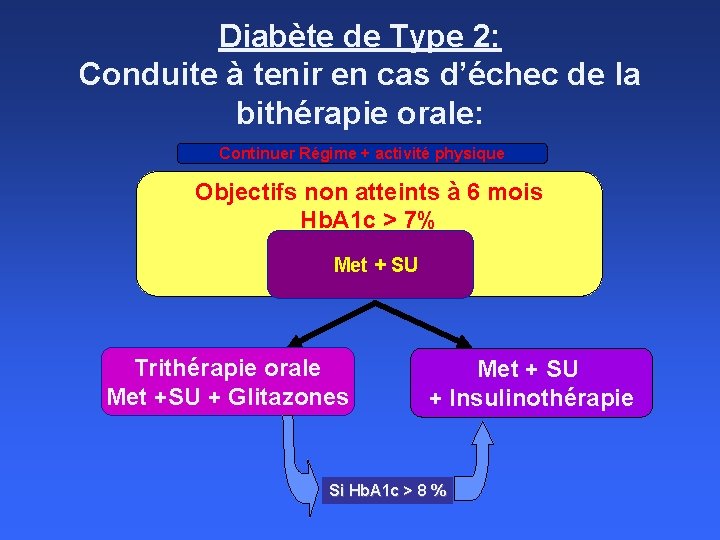
Diabète de Type 2: Conduite à tenir en cas d’échec de la bithérapie orale: Continuer Régime + activité physique Objectifs non atteints à 6 mois Hb. A 1 c > 7% Met + SU Trithérapie orale Met +SU + Glitazones Met + SU + Insulinothérapie Si Hb. A 1 c > 8 %

Les nouvelles molécules La voie des incrétines… 43

• Les incrétines ont une influence bénéfique sur la glucorégulation à la fois par le biais de l’insuline et par le biais du glucagon
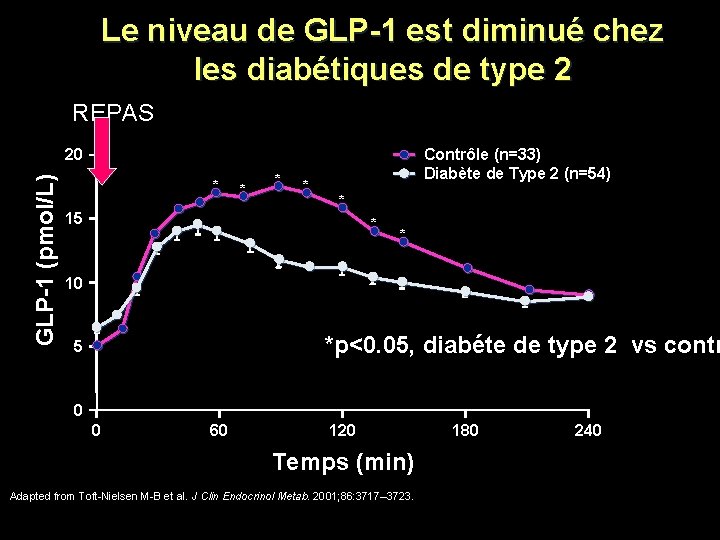
Le niveau de GLP-1 est diminué chez les diabétiques de type 2 REPAS Contrôle (n=33) Diabète de Type 2 (n=54) GLP-1 (pmol/L) 20 * 15 * * * 10 *p<0. 05, diabéte de type 2 vs contr 5 0 0 60 120 Temps (min) Adapted from Toft-Nielsen M-B et al. J Clin Endocrinol Metab. 2001; 86: 3717– 3723. 180 240
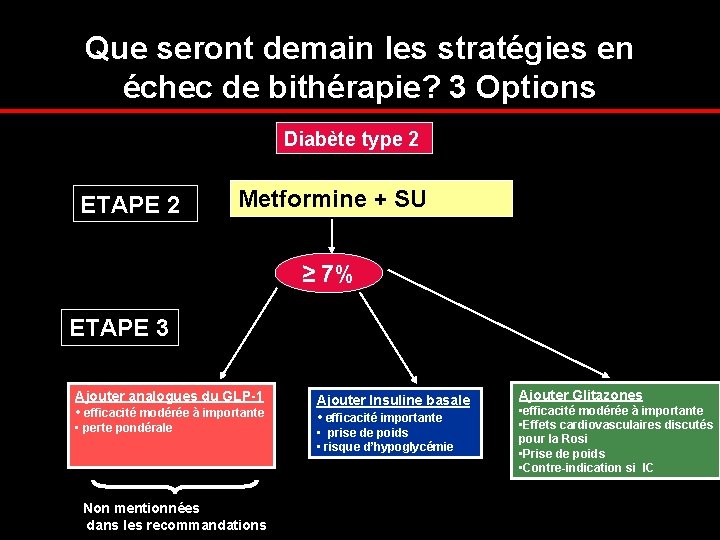
Que seront demain les stratégies en échec de bithérapie? 3 Options Diabète type 2 ETAPE 2 Metformine + SU ≥ 7% ETAPE 3 Ajouter analogues du GLP-1 • efficacité modérée à importante • perte pondérale Non mentionnées dans les recommandations Ajouter Insuline basale • efficacité importante • prise de poids • risque d’hypoglycémie Ajouter Glitazones • efficacité modérée à importante • Effets cardiovasculaires discutés pour la Rosi • Prise de poids • Contre-indication si IC
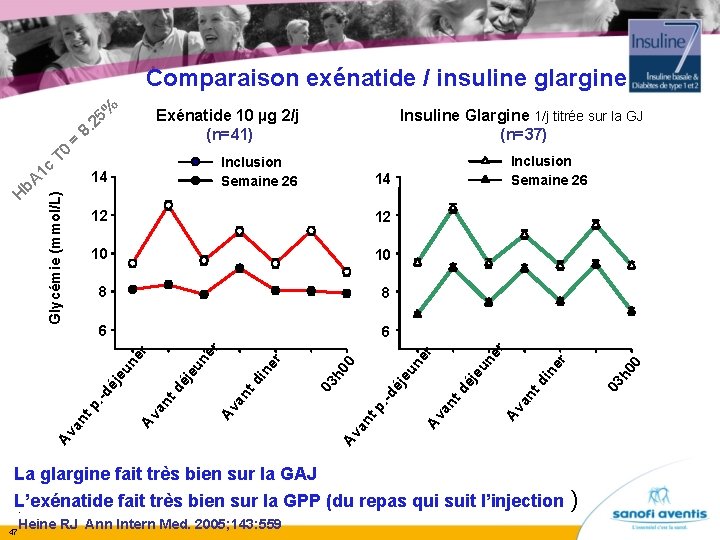
Comparaison exénatide / insuline glargine Insuline Glargine 1/j titrée sur la GJ (n=37) 14 8 6 6 r eu ne éj eu ne td an Av an tp. -d éj h 0 in Av an td éj an td Av 0 er r ne eu eu ne éj an tp. -d Av 0 8 h 0 10 er 10 nt di n 12 r 12 Av a 14 Inclusion Semaine 26 03 = r b. A H Glycémie (mmol/L) 1 c T 0 Exénatide 10 µg 2/j (n=41) 8. Av % 5 2 La glargine fait très bien sur la GAJ L’exénatide fait très bien sur la GPP (du repas qui suit l’injection. Heine RJ Ann Intern Med. 2005; 143: 559 47 )
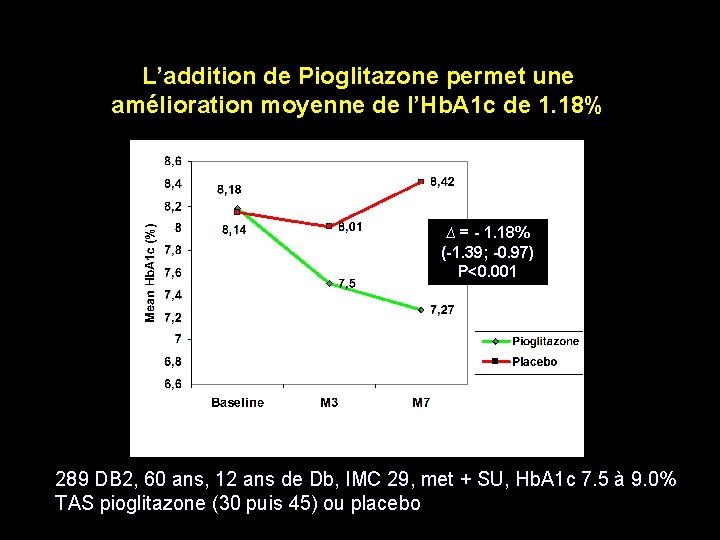
L’addition de Pioglitazone permet une amélioration moyenne de l’Hb. A 1 c de 1. 18% ∆ = - 1. 18% (-1. 39; -0. 97) P<0. 001 289 DB 2, 60 ans, 12 ans de Db, IMC 29, met + SU, Hb. A 1 c 7. 5 à 9. 0% TAS pioglitazone (30 puis 45) ou placebo
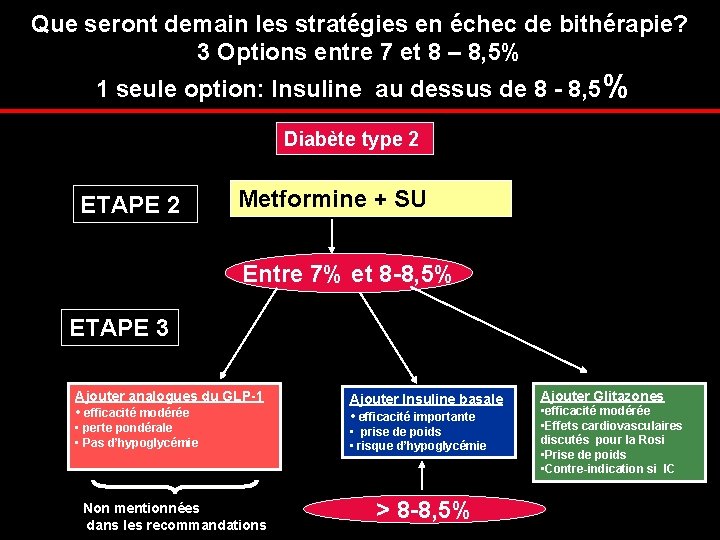
Que seront demain les stratégies en échec de bithérapie? 3 Options entre 7 et 8 – 8, 5% 1 seule option: Insuline au dessus de 8 - 8, 5% Diabète type 2 ETAPE 2 Metformine + SU Entre 7% et 8 -8, 5% ETAPE 3 Ajouter analogues du GLP-1 • efficacité modérée • perte pondérale • Pas d’hypoglycémie Non mentionnées dans les recommandations Ajouter Insuline basale • efficacité importante • prise de poids • risque d’hypoglycémie > 8 -8, 5% Ajouter Glitazones • efficacité modérée • Effets cardiovasculaires discutés pour la Rosi • Prise de poids • Contre-indication si IC

UKPDS Le suivi 10 ans après
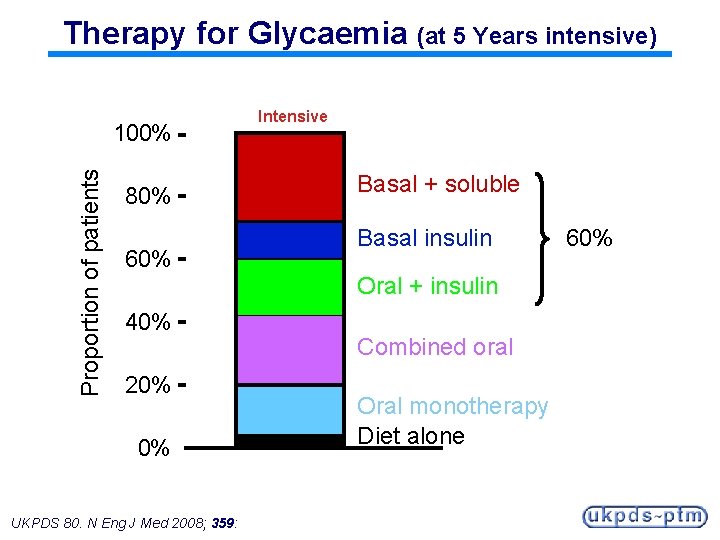
Therapy for Glycaemia (at 5 Years intensive) Proportion of patients 100% 80% 60% Intensive Basal + soluble Basal insulin Oral + insulin 40% 20% 0% UKPDS 80. N Eng J Med 2008; 359: Combined oral Oral monotherapy Diet alone 60%
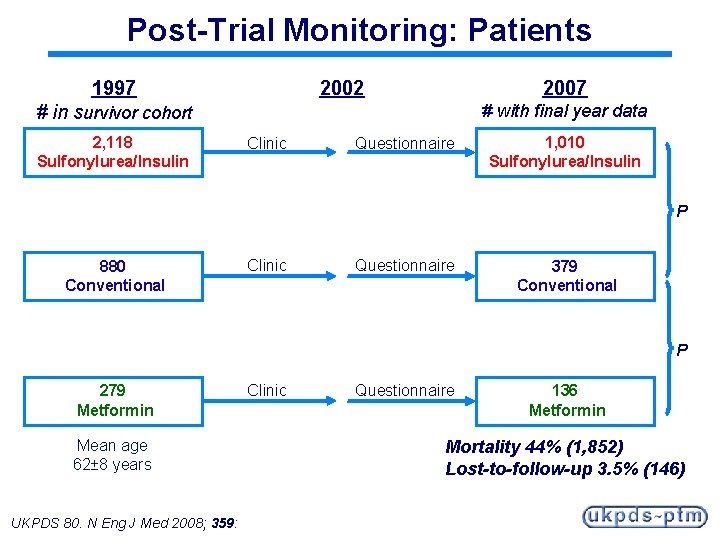
Post-Trial Monitoring: Patients 2002 1997 2007 # with final year data # in survivor cohort 2, 118 Sulfonylurea/Insulin Clinic Questionnaire 1, 010 Sulfonylurea/Insulin P 880 Conventional Clinic Questionnaire 379 Conventional P 279 Metformin Mean age 62± 8 years UKPDS 80. N Eng J Med 2008; 359: Clinic Questionnaire 136 Metformin Mortality 44% (1, 852) Lost-to-follow-up 3. 5% (146)
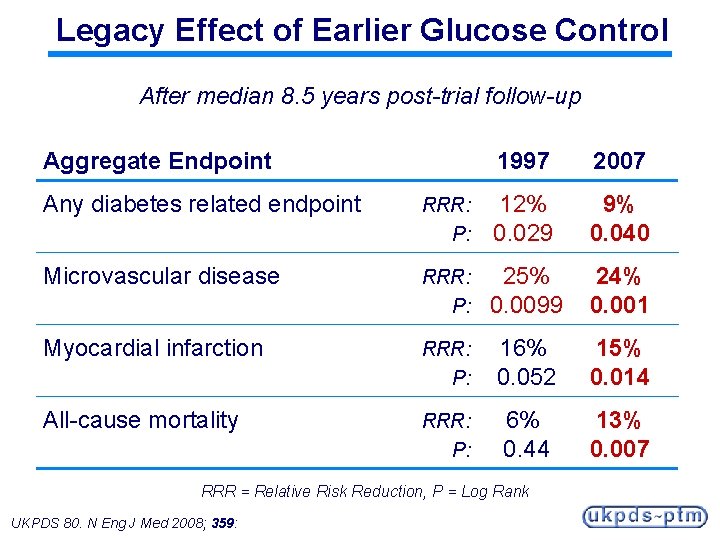
Legacy Effect of Earlier Glucose Control After median 8. 5 years post-trial follow-up Aggregate Endpoint 1997 2007 Any diabetes related endpoint RRR: P: 12% 0. 029 9% 0. 040 Microvascular disease RRR: P: 25% 0. 0099 24% 0. 001 Myocardial infarction RRR: P: 16% 0. 052 15% 0. 014 All-cause mortality RRR: P: 6% 0. 44 13% 0. 007 RRR = Relative Risk Reduction, P = Log Rank UKPDS 80. N Eng J Med 2008; 359:
- Slides: 53