LA STRATEGIA STA Simplified Treatment Approaches UNA RISPOSTA

























- Slides: 58

LA STRATEGIA STA (Simplified Treatment Approaches) UNA “RISPOSTA COMPLESSIVA” PER GESTIRE UNA PATOLOGIA SUFFICIENTEMENTE DIFFUSA 12 Aprile 2013 Seminario annuale

Contenuto: Determinanti alternativi all’EBM (Evidence Based Medicine) classica: perché interessarsene? Simone Marcotullio, Nadir Onlus Considerazioni da alcuni osservatori: Adriana Ammassari, INMI Spallanzani Antonella Castagna, Ospedale San Raffaele Franco Maggiolo, Ospedali Riuniti di Bergamo

Determinanti alternativi all’EBM (Evidence Based Medicine) classica: perché interessarsene? Simone Marcotullio

Evidence Based Medicine (EBM) Che cosa significa basare le decisioni diagnostiche e terapeutiche sull’Evidence Based Medicine (EBM)? • Significa riferirsi, per esempio, nella stesura di Linee Guida diagnostiche e terapeutiche, alla valutazione critica dei risultati reperibili dalla letteratura scientifica. • Ciò che interessa specificatamente la EBM non è semplicemente ciò che deriva da ricerche, bensì prevalentemente da Studi clinici controllati. • I dati sono ottenuti mediante una valutazione critica degli studi clinici esistenti. Predilezione per studi randomizzati rispetto a quelli osservazionali, per quelli prospettici rispetto ai retrospettivi, etc….

Alcuni limiti intrinsechi dell’EBM • E’ possibile progettare ed eseguire tutti gli studi clinici di cui si avrebbe necessità per comprendere le aree grigie della gestione di una patologia? • Gli studi reperibili in letteratura sono progettati secondo un principio di oggettività o sovente sono obiettivo-dipendenti? • I criteri stabiliti nel disegno di uno studio clinico (es. : chi è eleggibile, che analisi statistica fare, ecc. ) possono essere influenzatori del risultato? • E’ costo-efficace ed etico (? ) che il quesito scientifico sia a servizio della metodologia (rischio) oppure è la metodologia che dovrebbe essere al servizio dell’interpretazione del quesito clinico e/o di ricerca? Come, però, non cadere nel tranello di farsi le regole “a piacere”?

EBM: riformulazione David Sackett (Canada), dopo l'incauta presentazione dell'EBM come "paradigma emergente per la pratica clinica", precisa che "la EBM costituisce un approccio alla pratica clinica dove le decisioni cliniche risultano dall'integrazione tra l'esperienza del medico e l'utilizzo coscienzioso, esplicito e giudizioso delle migliori evidenze scientifiche disponibili, mediate dalle preferenze del paziente”.

Il problema della metodologia • Attenzione: le Good Clinical Practice (GCP), obbligatorie per gli studi clinici, non devono essere facoltative per gli studi osservazionali, per quanto adattate alle caratteristiche dello studio. Spesso non è così e si rischia di ottenere risultati fuorvianti. • Inoltre, spunti interessanti di riflessione, che vengono dall’analisi di “ciò che è oltre” lo studio clinico classico, potrebbero trovare un’integrazione sistematica nel “giudizio finale” di Linea Guida?

Non rottamiamo nulla! • Basare le decisioni di politica sanitaria solo sull’EBM calvinista potrebbe essere limitativo nel soddisfare sia le esigenze dei pazienti sia quelle di patologia. Occorre rifletterci! (rif. alcuni atteggiamenti regionali: i decisori politici quando vedono un “II” fanno finta di nulla o ignorano…. Perchè? ). • L’approccio calvinista all’EBM è già superato e recepito, in qualche modo, nelle Linee Guida: l’importanza (pur a fatica!) che in questi documenti assumono gli studi di coorte è prova di questo. Ma è sufficiente per interpretare, ad esempio, le esigenze del paziente? • Inoltre, parliamo sempre di studi di coorte “su base clinica”. Si può andare oltre?

Come interpretare? • La difficoltà di interpretare altri dati, osservazioni, che ci derivano da “database” o metodologie di analisi differenti è ampia, anche perché siamo tutti abituati a ragionare secondo l’EBM. • E’ quindi naturale, logico, umano intrinsecamente essere critici sul diverso. Pensate, ad esempio, alle intuizioni di Copernico…

Medicina narrativa • Oggi, in un’epoca in cui la medicina ha raggiunto straordinari traguardi di sviluppo tecnologico e il concetto di medicina basata sulle evidenze è ormai molto familiare, si è sentita l’esigenza di recuperare il rapporto medicopaziente, dove la narrazione della patologia del paziente al medico è considerata al pari dei segni e dei sintomi clinici della malattia stessa. • Questa medicina narrativa (NBM, Narrative Based Medicine) si riferisce non solo al vissuto del paziente, ma anche ai vissuti del medico ed alla loro relazione. Oggi è possibile quantificare tutto ciò.

Database amministrativi • Sono certamente database interessanti che, se impostati ab initio correttamente, potrebbero dare spunti di riflessione importanti (si vedano esempi di altri paesi). Al momento “parlano poco tra loro”, ma in prospettiva potrebbero essere differenti e potrebbero essere una base interessante per il decisore politico. • Hanno il pregio di registrare dati di real life, hanno il difetto di essere dipendenti dalle regole ab initio e dal singolo compilatore. Ma su grandi numeri e con appropriati correttivi … possono aiutare!

Database amministrativi • Idealmente, avere a disposizione un database pluricentrico comprendente i dati di pazienti seguiti da medici differenti, dati adeguatamente pesati per numerosità e fattori confondenti, potrebbe rispondere al dato mancante (per altro sovente countrydipendent): potere confrontare/integrare ciò che ci deriva dall’EBM con ciò che si riscontra in questo contesto è una sfida. Al momento difficile ottenerlo. • Tentare di fare con alcuni centri un’esperienza senz’altro pilota, è un’operazione possibile.

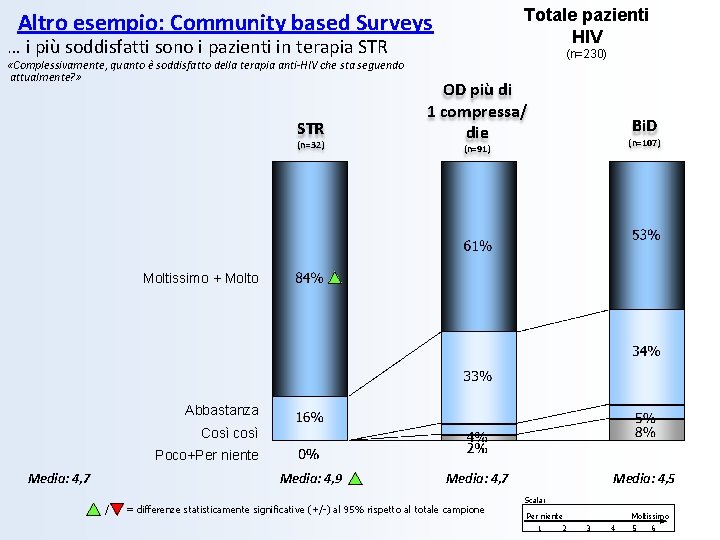
Totale pazienti HIV Altro esempio: Community based Surveys … i più soddisfatti sono i pazienti in terapia STR «Complessivamente, quanto è soddisfatto della terapia anti-HIV che sta seguendo attualmente? » STR (n=32) (n=230) OD più di 1 compressa/ die Bi. D (n=107) (n=91) Moltissimo + Molto Abbastanza Così così Poco+Per niente Media: 4, 7 Media: 4, 9 / Media: 4, 7 = differenze statisticamente significative (+/-) al 95% rispetto al totale campione Media: 4, 5 Scala: Per niente 1 2 Moltissimo 3 4 5 6

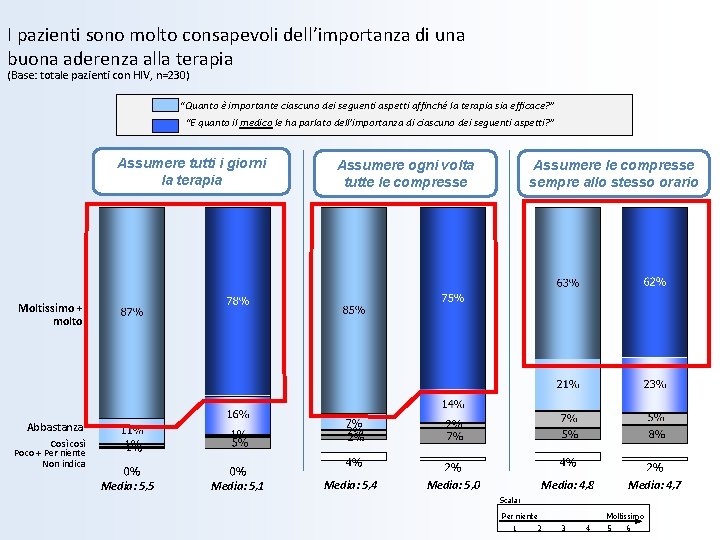
I pazienti sono molto consapevoli dell’importanza di una buona aderenza alla terapia (Base: totale pazienti con HIV, n=230) “Quanto è importante ciascuno dei seguenti aspetti affinché la terapia sia efficace? ” "E quanto il medico le ha parlato dell’importanza di ciascuno dei seguenti aspetti? ” Assumere tutti i giorni la terapia Assumere le compresse sempre allo stesso orario Assumere ogni volta tutte le compresse Moltissimo + molto Abbastanza Così così Poco + Per niente Non indica Media: 5, 5 Media: 5, 1 Media: 5, 4 Media: 5, 0 Media: 4, 8 Media: 4, 7 Scala: Per niente 1 2 Moltissimo 3 4 5 6

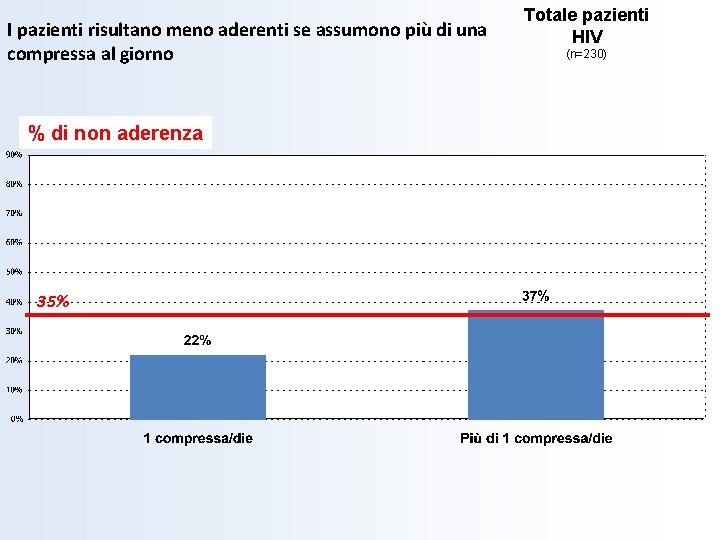
I pazienti risultano meno aderenti se assumono più di una compressa al giorno % di non aderenza 35% Totale pazienti HIV (n=230)

Quindi… • Gli studi clinici sono spesso disegnati con precise e limitate finalità e le popolazioni in essi arruolati non rispecchiano una popolazione di “pazienti reali” di un determinato paese. • Ecco perché impegnarsi a costruire un osservatorio complessivo alternativo, più rispondente alla realtà, che aiuti a pesare e valutare meglio i riscontri che ci provengono dagli studi clinici, aumentando la patient-perspective e le necessità della patologia.

Considerazioni da alcuni osservatori: Adriana Ammassari

• Con quale frequenza e a chi si prescrive STR (Single Tablet Regimen)? • Ci sono differenze tra STR e MTR (Multi Tablet Regimen) nel raggiungimento o nel mantenimento della risposta virologica? • Qual è l’aderenza ai regimi STR se paragonati agli altri e con quali conseguenze?

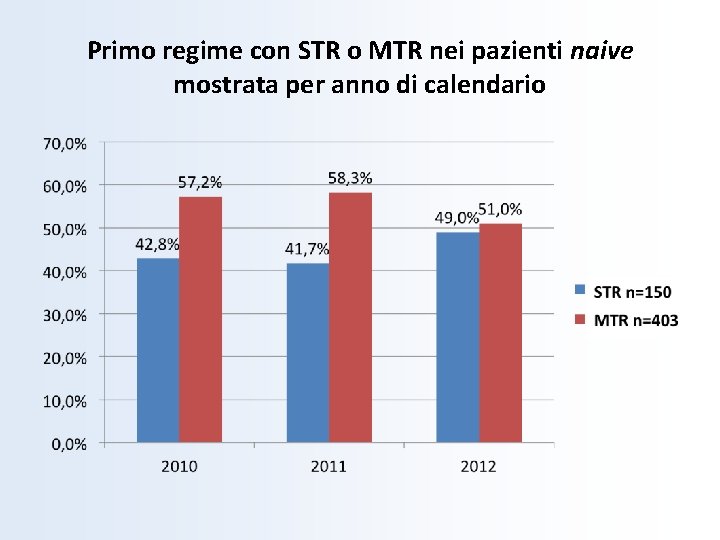
Primo regime con STR o MTR nei pazienti naive mostrata per anno di calendario

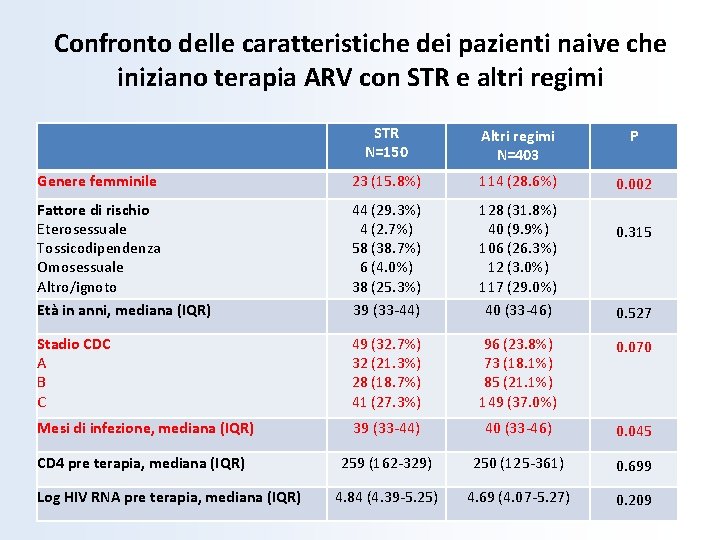
Confronto delle caratteristiche dei pazienti naive che iniziano terapia ARV con STR e altri regimi STR N=150 Altri regimi N=403 P Genere femminile 23 (15. 8%) 114 (28. 6%) 0. 002 Fattore di rischio Eterosessuale Tossicodipendenza Omosessuale Altro/ignoto Età in anni, mediana (IQR) 44 (29. 3%) 4 (2. 7%) 58 (38. 7%) 6 (4. 0%) 38 (25. 3%) 39 (33 -44) 128 (31. 8%) 40 (9. 9%) 106 (26. 3%) 12 (3. 0%) 117 (29. 0%) 40 (33 -46) Stadio CDC A B C 49 (32. 7%) 32 (21. 3%) 28 (18. 7%) 41 (27. 3%) 96 (23. 8%) 73 (18. 1%) 85 (21. 1%) 149 (37. 0%) 0. 070 Mesi di infezione, mediana (IQR) 39 (33 -44) 40 (33 -46) 0. 045 CD 4 pre terapia, mediana (IQR) 259 (162 -329) 250 (125 -361) 0. 699 4. 84 (4. 39 -5. 25) 4. 69 (4. 07 -5. 27) 0. 209 Log HIV RNA pre terapia, mediana (IQR) 0. 315 0. 527

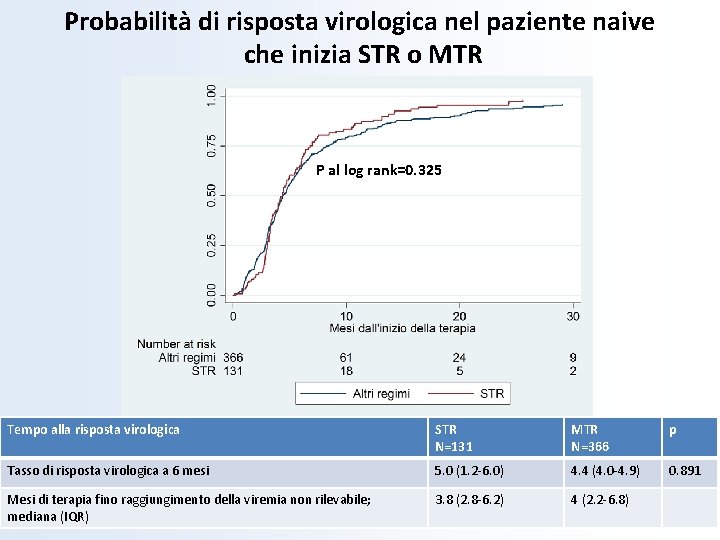
Probabilità di risposta virologica nel paziente naive che inizia STR o MTR P al log rank=0. 325 Tempo alla risposta virologica STR N=131 MTR N=366 p Tasso di risposta virologica a 6 mesi 5. 0 (1. 2 -6. 0) 4. 4 (4. 0 -4. 9) 0. 891 Mesi di terapia fino raggiungimento della viremia non rilevabile; mediana (IQR) 3. 8 (2. 8 -6. 2) 4 (2. 2 -6. 8)

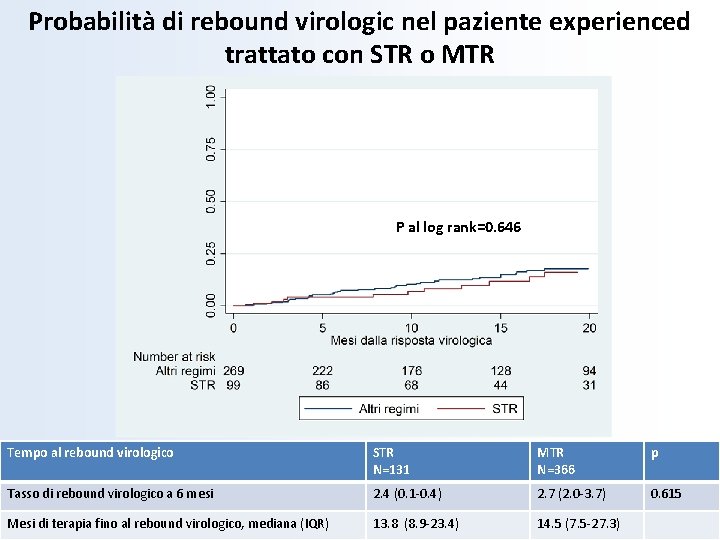
Probabilità di rebound virologic nel paziente experienced trattato con STR o MTR P al log rank=0. 646 Tempo al rebound virologico STR N=131 MTR N=366 p Tasso di rebound virologico a 6 mesi 2. 4 (0. 1 -0. 4) 2. 7 (2. 0 -3. 7) 0. 615 Mesi di terapia fino al rebound virologico, mediana (IQR) 13. 8 (8. 9 -23. 4) 14. 5 (7. 5 -27. 3)

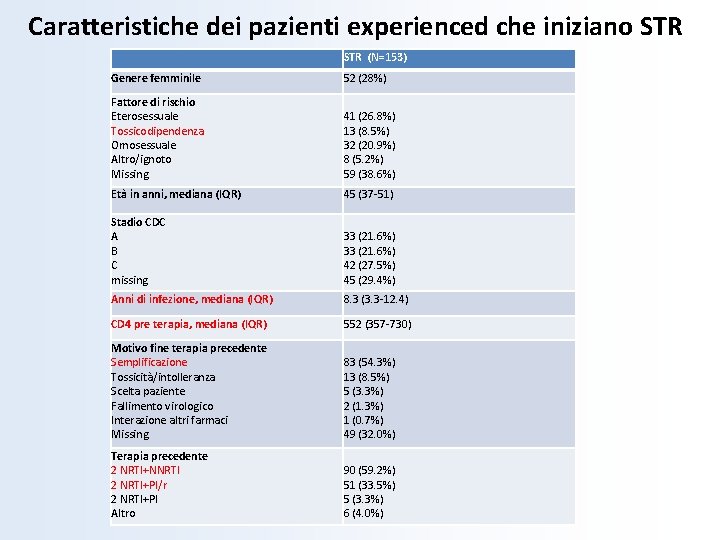
Caratteristiche dei pazienti experienced che iniziano STR (N=153) Genere femminile 52 (28%) Fattore di rischio Eterosessuale Tossicodipendenza Omosessuale Altro/ignoto Missing 41 (26. 8%) 13 (8. 5%) 32 (20. 9%) 8 (5. 2%) 59 (38. 6%) Età in anni, mediana (IQR) 45 (37 -51) Stadio CDC A B C missing 33 (21. 6%) 42 (27. 5%) 45 (29. 4%) Anni di infezione, mediana (IQR) 8. 3 (3. 3 -12. 4) CD 4 pre terapia, mediana (IQR) 552 (357 -730) Motivo fine terapia precedente Semplificazione Tossicità/intolleranza Scelta paziente Fallimento virologico Interazione altri farmaci Missing 83 (54. 3%) 13 (8. 5%) 5 (3. 3%) 2 (1. 3%) 1 (0. 7%) 49 (32. 0%) Terapia precedente 2 NRTI+NNRTI 2 NRTI+PI/r 2 NRTI+PI Altro 90 (59. 2%) 51 (33. 5%) 5 (3. 3%) 6 (4. 0%)

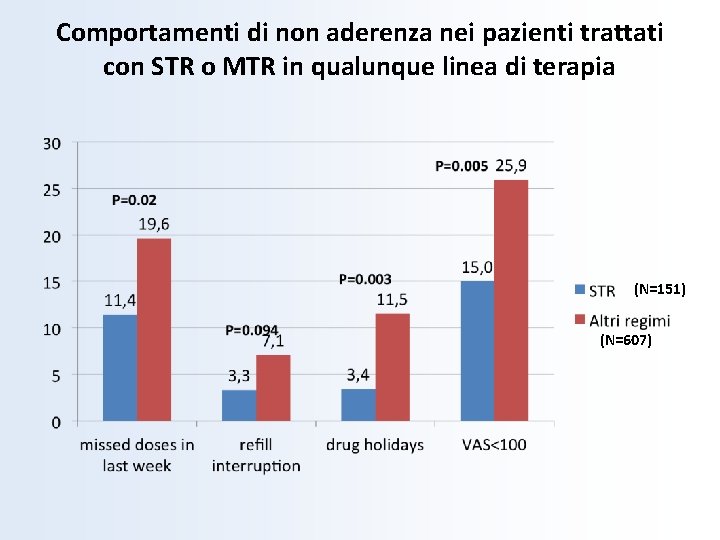
Comportamenti di non aderenza nei pazienti trattati con STR o MTR in qualunque linea di terapia (N=151) (N=607)

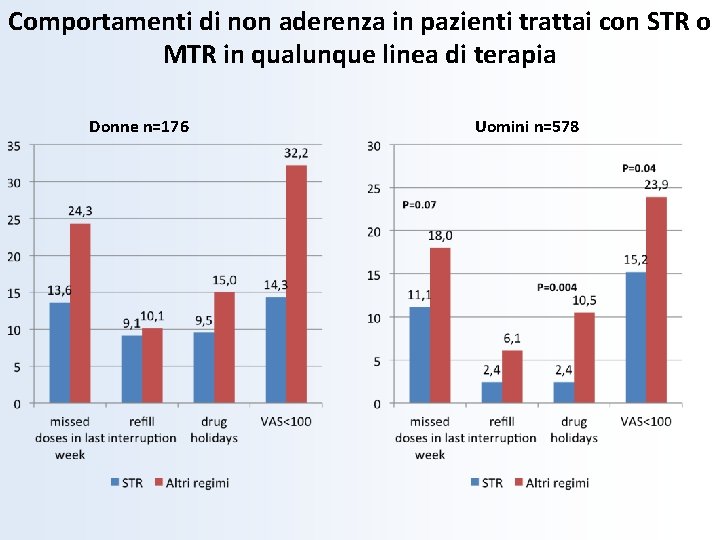
Comportamenti di non aderenza in pazienti trattai con STR o MTR in qualunque linea di terapia Donne n=176 Uomini n=578

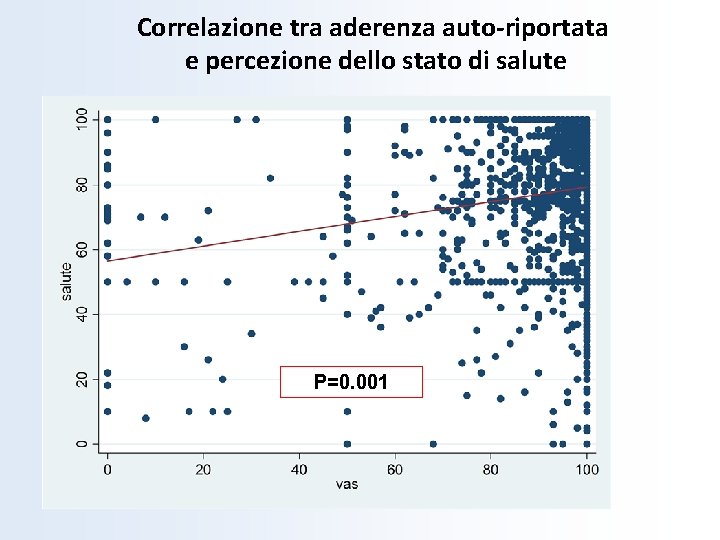
Correlazione tra aderenza auto-riportata e percezione dello stato di salute P=0. 001

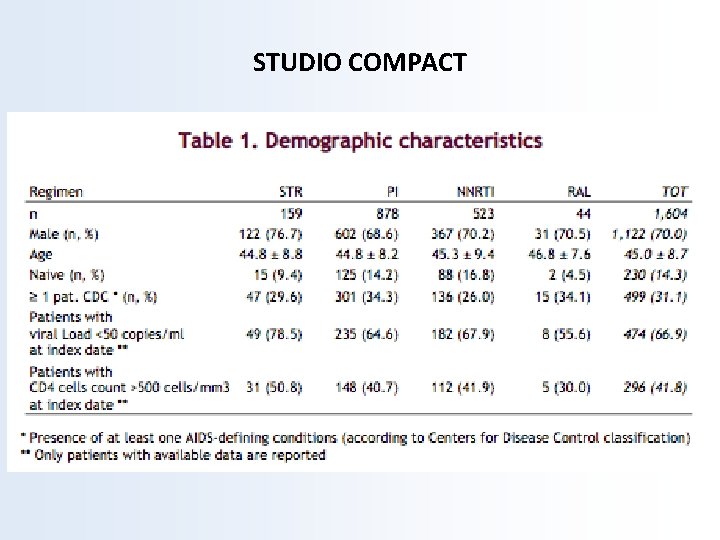
STUDIO COMPACT

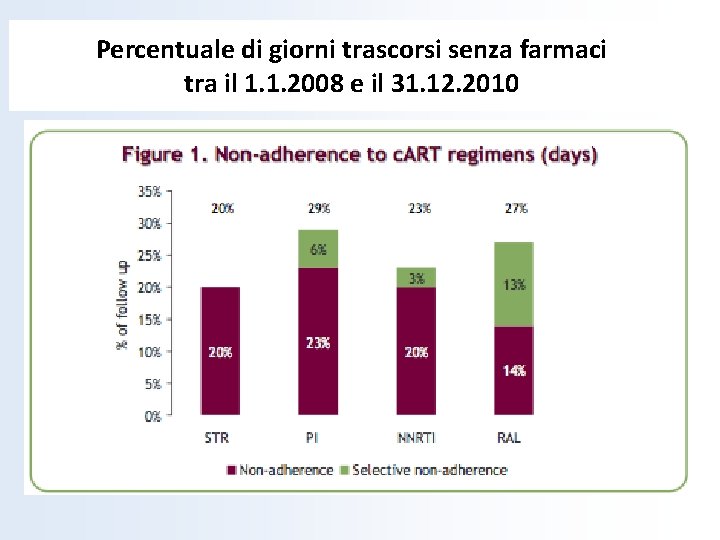
Percentuale di giorni trascorsi senza farmaci tra il 1. 1. 2008 e il 31. 12. 2010

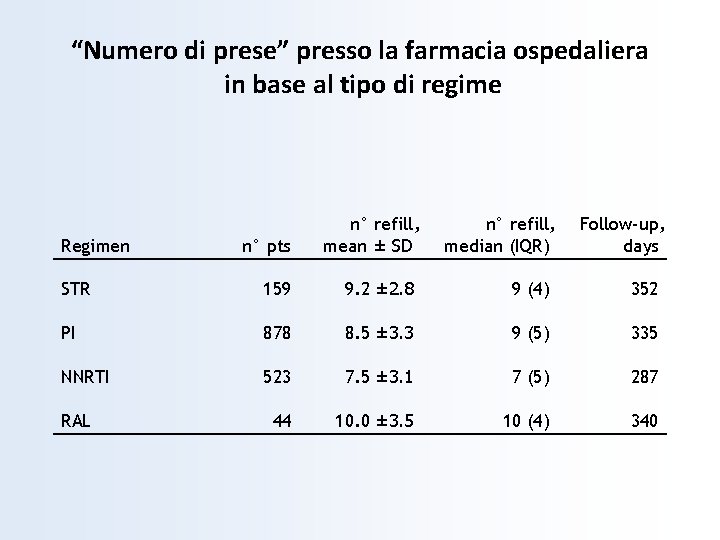
“Numero di prese” presso la farmacia ospedaliera in base al tipo di regime Regimen n° pts n° refill, mean ± SD n° refill, median (IQR) Follow-up, days STR 159 9. 2 ± 2. 8 9 (4) 352 PI 878 8. 5 ± 3. 3 9 (5) 335 NNRTI 523 7. 5 ± 3. 1 7 (5) 287 44 10. 0 ± 3. 5 10 (4) 340 RAL

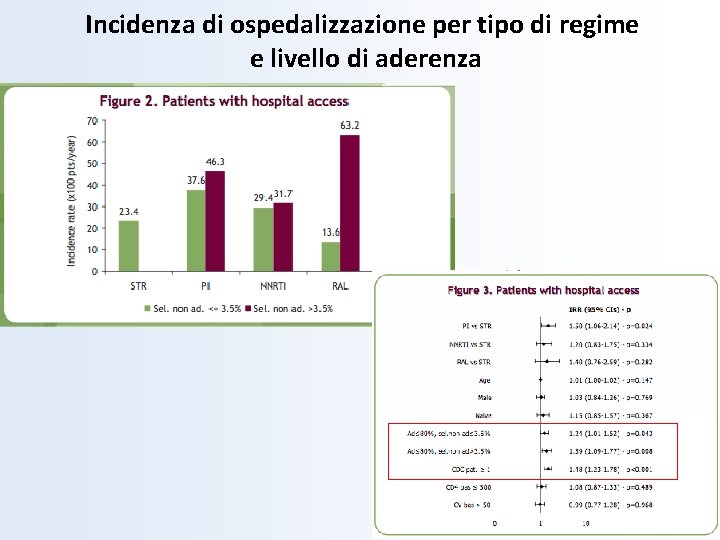
Incidenza di ospedalizzazione per tipo di regime e livello di aderenza

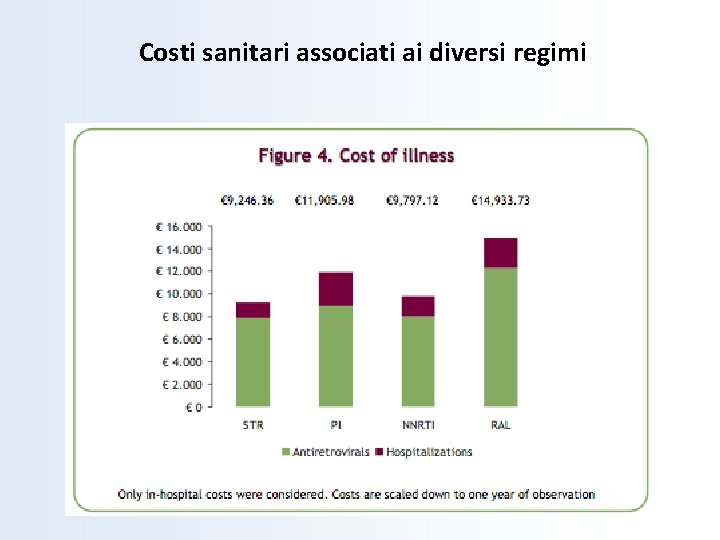
Costi sanitari associati ai diversi regimi

Considerazioni da alcuni osservatori: Antonella Castagna

Glasgow 2012 COST EFFECTIVENESS EVALUATION OF INITIAL HAART REGIMENS FOR MANAGING HIV INFECTED PATIENTS ACCORDINAG TO REAL CLINICAL PRACTICE Colombo G. L. , Castagna A. , …, Lazzarin A. We evaluated the single tablet regimen (STR) vs Multi -Pills Regimen (MPR) strategies through an incremental cost-effectiveness analysis in a large cohort of patients starting their first HAART.

METHODS Adult HIV-1 naive patients, followed at the S. Raffaele Scientific Institute, starting their first line regimen from June 2008 to April 2012 were included in the study. First line HAART regimens more frequently used (>10%) were grouped into two classes as follows: a) Single Tablet Regimen (STR) of TDF+FTC+EFV; b) Multi-Pills Regimen (MPR) including: TDF+FTC+EFV TDF+FTC+ATV/r TDF+FTC+DRV/r TDF+FTC+LPV/r

METHODS (2) As “persistent” we considered the patient doesn’t change the initially assigned therapy. Costs were considered independently from treatment change. The incremental cost-effectiveness analysis was carried out by means of a Markov model calculating Quality of Life and costs for each patient, according to the given regimen (including any subsequent switch if occurred), through 1 year cycles. The outcome measure was Quality Adjusted Life Years (QALY’s). Data were analyzed from the point of view of the Lombardy Regional Health Service (RHS): HAART, hospitalizations, visits, examinations and other concomitant non HAART drugs costs were evaluated, price variations included. At multivariable analysis, the generalized linear model was used to identify the predictive factors of the overall cost/effectiveness of the first line HAART regimens.

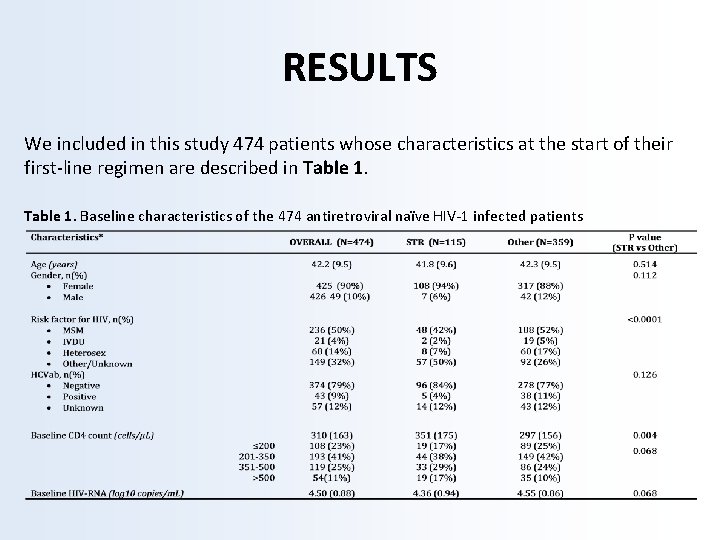
RESULTS We included in this study 474 patients whose characteristics at the start of their first-line regimen are described in Table 1. Baseline characteristics of the 474 antiretroviral naïve HIV-1 infected patients

DURABILITY

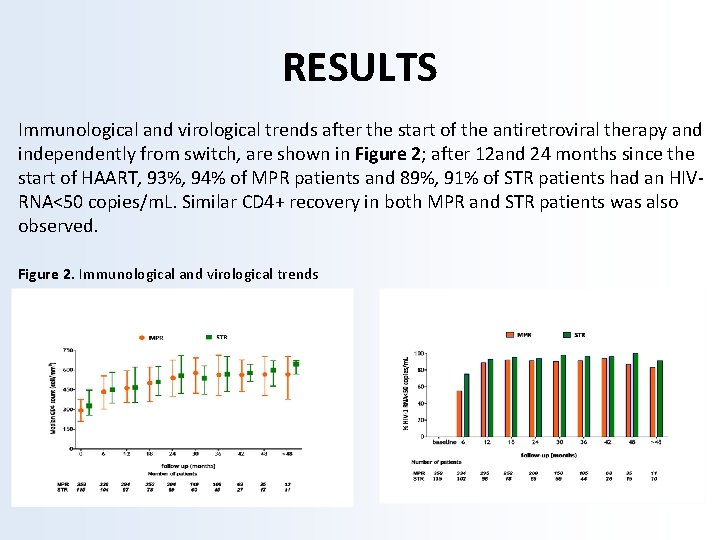
RESULTS Immunological and virological trends after the start of the antiretroviral therapy and independently from switch, are shown in Figure 2; after 12 and 24 months since the start of HAART, 93%, 94% of MPR patients and 89%, 91% of STR patients had an HIVRNA<50 copies/m. L. Similar CD 4+ recovery in both MPR and STR patients was also observed. Figure 2. Immunological and virological trends

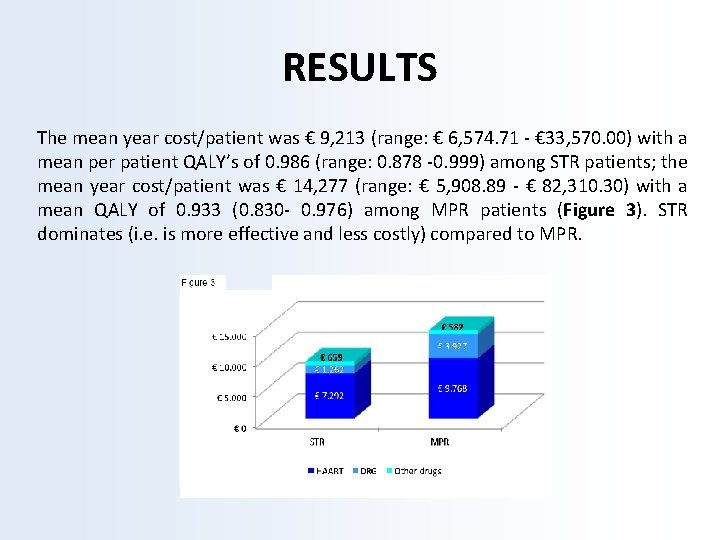
RESULTS The mean year cost/patient was € 9, 213 (range: € 6, 574. 71 - € 33, 570. 00) with a mean per patient QALY’s of 0. 986 (range: 0. 878 -0. 999) among STR patients; the mean year cost/patient was € 14, 277 (range: € 5, 908. 89 - € 82, 310. 30) with a mean QALY of 0. 933 (0. 830 - 0. 976) among MPR patients (Figure 3). STR dominates (i. e. is more effective and less costly) compared to MPR.

Multivariable analysis At multivariable analysis, after adjustment for age, gender, HCV-Ab status, HIV risk factor, baseline CD 4+ and HIV-RNA, the cost-effectiveness ratio was significantly lower among patients starting an STR treatment as compared to a MPR regimen [Adjusted mean: € 12, 096 vs. € 16, 106 P=0. 0001] (Table 2). Table 2. Factors associated with the overall cost/effectiveness (costs include antiretroviral regimens and hospitalizations and non-antiretroviral treatments)

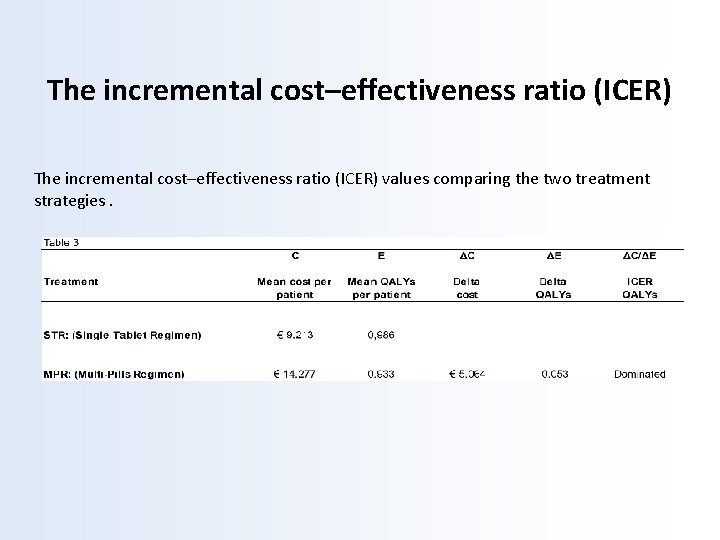
The incremental cost–effectiveness ratio (ICER) values comparing the two treatment strategies.

CONCLUSIONS Starting with a first line Single Tablet Regimen compared to Multi-Pills Regimen is associated with lower costs and better efficacy as measured by QALY’s.

Considerazioni da alcuni osservatori: Franco Maggiolo

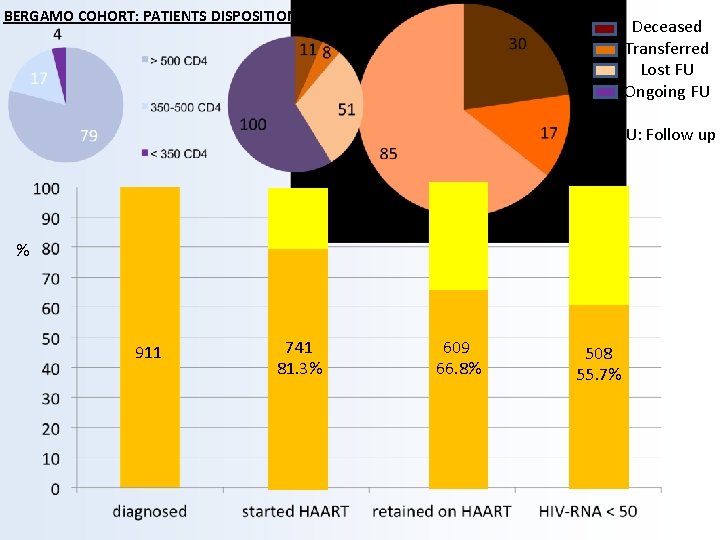
BERGAMO COHORT: PATIENTS DISPOSITION Deceased Transferred Lost FU Ongoing FU FU: Follow up % 911 741 81. 3% 609 66. 8% 508 55. 7%

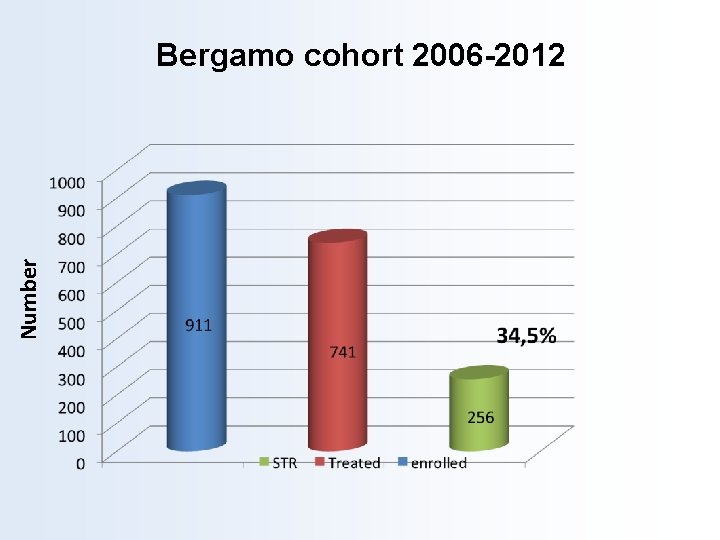
Number Bergamo cohort 2006 -2012

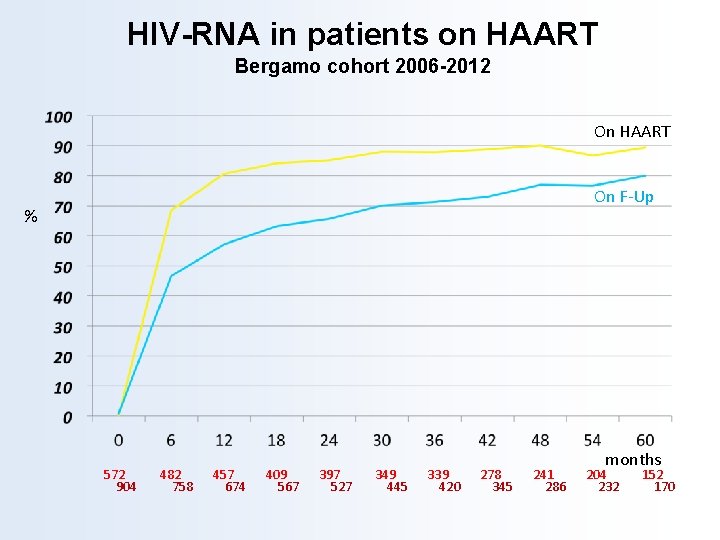
HIV-RNA in patients on HAART Bergamo cohort 2006 -2012 On HAART % On F-Up months 572 482 457 409 397 349 339 278 241 204 152 904 758 674 567 527 445 420 345 286 232 170

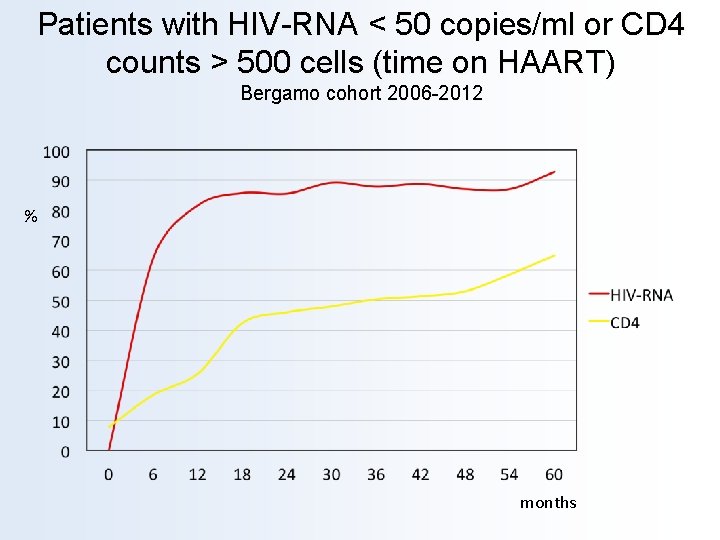
Patients with HIV-RNA < 50 copies/ml or CD 4 counts > 500 cells (time on HAART) Bergamo cohort 2006 -2012 % months

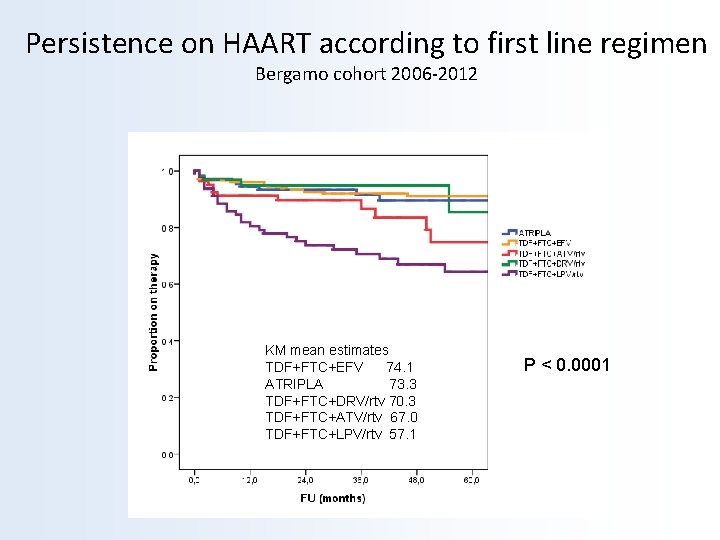
Persistence on HAART according to first line regimen Bergamo cohort 2006 -2012 KM mean estimates TDF+FTC+EFV 74. 1 ATRIPLA 73. 3 TDF+FTC+DRV/rtv 70. 3 TDF+FTC+ATV/rtv 67. 0 TDF+FTC+LPV/rtv 57. 1 P < 0. 0001

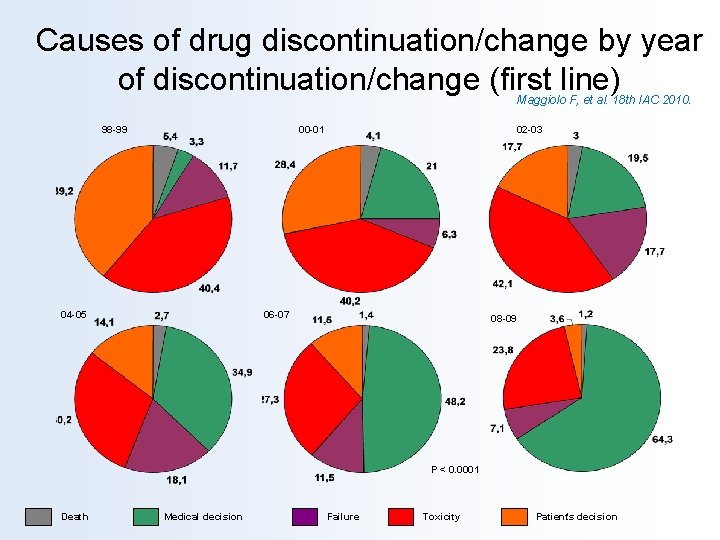
Causes of drug discontinuation/change by year of discontinuation/change (first line) Maggiolo F, et al. 18 th IAC 2010. 98 -99 00 -01 02 -03 06 -07 04 -05 08 -09 P < 0. 0001 Death Medical decision Failure Toxicity Patient’s decision

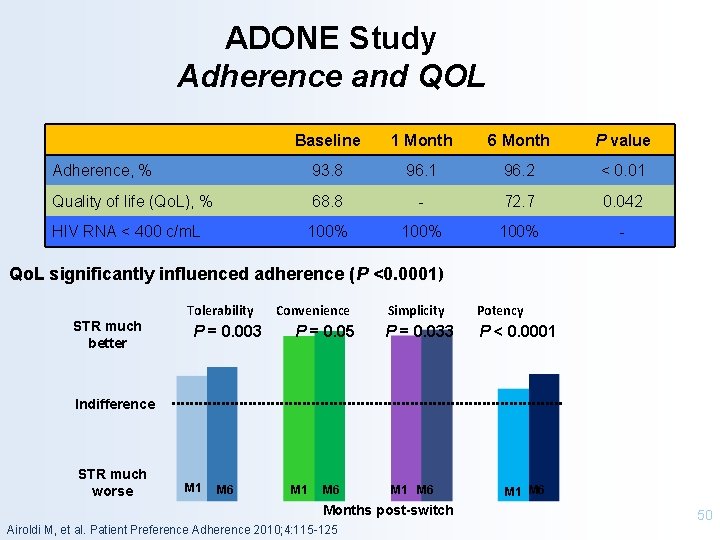
ADONE Study Adherence and QOL Baseline 1 Month 6 Month P value Adherence, % 93. 8 96. 1 96. 2 < 0. 01 Quality of life (Qo. L), % 68. 8 - 72. 7 0. 042 100% - HIV RNA < 400 c/m. L Qo. L significantly influenced adherence (P <0. 0001) STR much better Tolerability P = 0. 003 Convenience P = 0. 05 Simplicity Potency P = 0. 033 P < 0. 0001 Indifference STR much worse M 1 M 6 Months post-switch Airoldi M, et al. Patient Preference Adherence 2010; 4: 115 -125 M 1 M 6 50

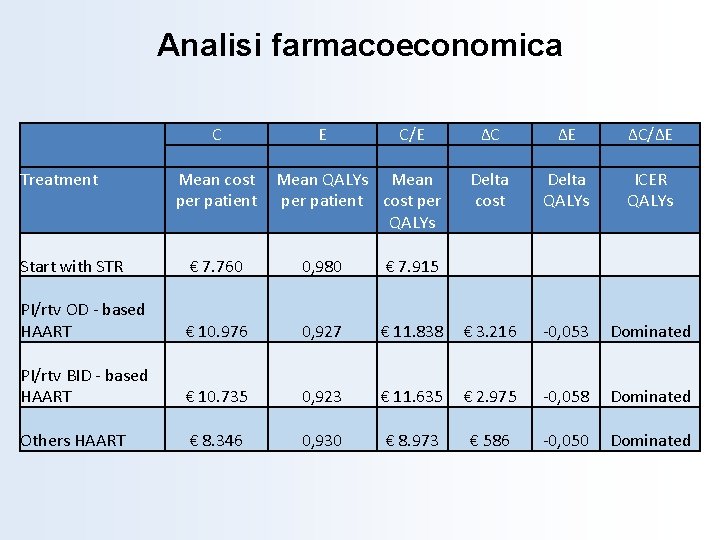
Analisi farmacoeconomica Treatment C E C/E Mean cost Mean QALYs Mean per patient cost per QALYs ΔC ΔE ΔC/ΔE Delta ICER cost QALYs Start with STR € 7. 760 0, 980 € 7. 915 PI/rtv OD - based HAART € 10. 976 0, 927 € 11. 838 € 3. 216 -0, 053 Dominated PI/rtv BID - based HAART € 10. 735 0, 923 € 11. 635 € 2. 975 -0, 058 Dominated Others HAART € 8. 346 0, 930 € 8. 973 € 586 -0, 050 Dominated

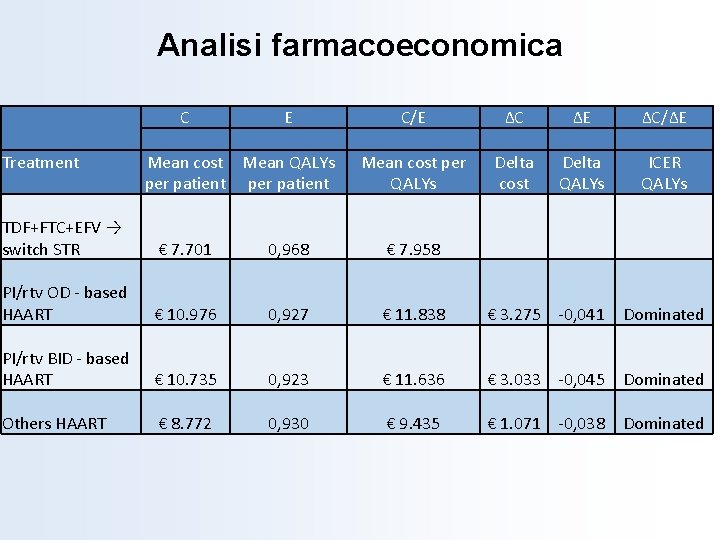
Analisi farmacoeconomica Treatment C E Mean cost Mean QALYs per patient C/E Mean cost per QALYs ΔC ΔE ΔC/ΔE Delta ICER cost QALYs TDF+FTC+EFV → switch STR € 7. 701 0, 968 € 7. 958 PI/rtv OD - based HAART € 10. 976 0, 927 € 11. 838 € 3. 275 -0, 041 Dominated PI/rtv BID - based HAART € 10. 735 0, 923 € 11. 636 € 3. 033 -0, 045 Dominated Others HAART € 8. 772 0, 930 € 9. 435 € 1. 071 -0, 038 Dominated

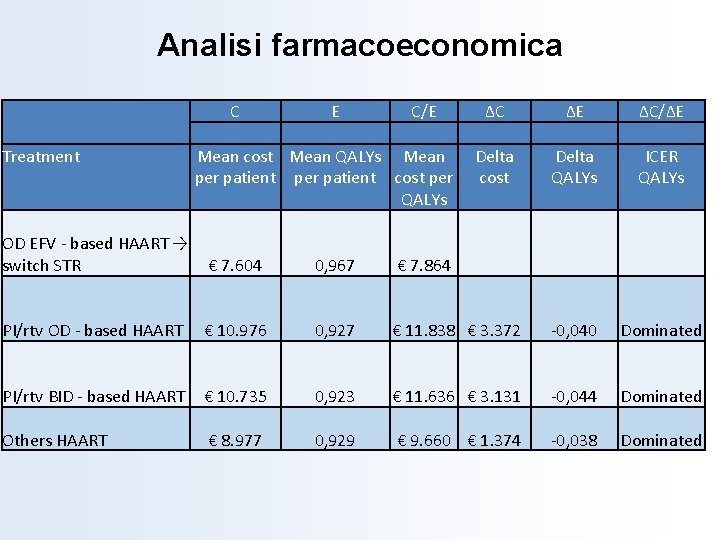
Analisi farmacoeconomica Treatment C E C/E ΔC ΔE ΔC/ΔE Mean cost Mean QALYs Mean Delta ICER per patient cost per cost QALYs OD EFV - based HAART → switch STR € 7. 604 0, 967 € 7. 864 PI/rtv OD - based HAART € 10. 976 0, 927 PI/rtv BID - based HAART € 10. 735 Others HAART € 8. 977 € 11. 838 € 3. 372 -0, 040 Dominated 0, 923 € 11. 636 € 3. 131 -0, 044 Dominated 0, 929 € 9. 660 € 1. 374 -0, 038 Dominated

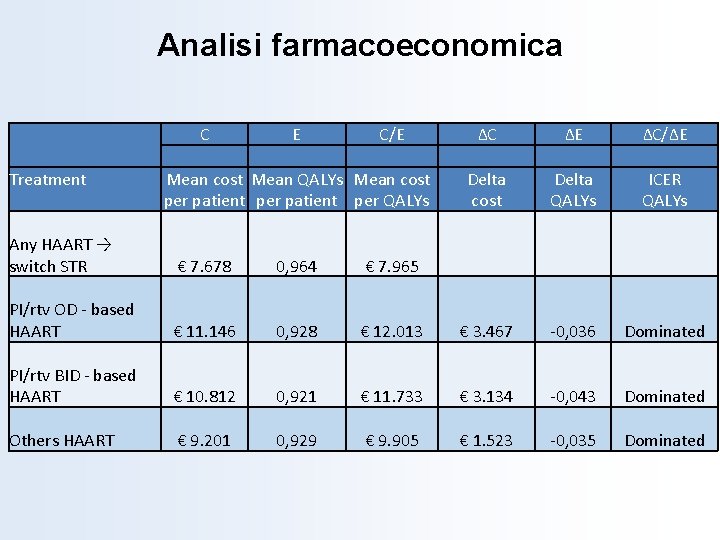
Analisi farmacoeconomica Treatment C E C/E Mean cost Mean QALYs Mean cost per patient per QALYs ΔC ΔE ΔC/ΔE Delta ICER cost QALYs Any HAART → switch STR € 7. 678 0, 964 € 7. 965 PI/rtv OD - based HAART € 11. 146 0, 928 € 12. 013 € 3. 467 -0, 036 Dominated PI/rtv BID - based HAART € 10. 812 0, 921 € 11. 733 € 3. 134 -0, 043 Dominated Others HAART € 9. 201 0, 929 € 9. 905 € 1. 523 -0, 035 Dominated

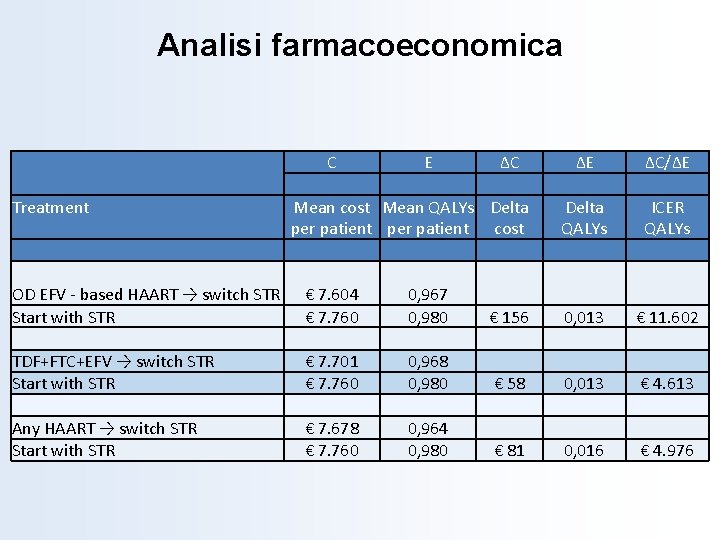
Analisi farmacoeconomica Treatment C E ΔC ΔE ΔC/ΔE Mean cost Mean QALYs Delta ICER per patient cost QALYs OD EFV - based HAART → switch STR Start with STR TDF+FTC+EFV → switch STR Start with STR Any HAART → switch STR Start with STR € 7. 604 € 7. 760 0, 967 0, 980 € 7. 701 € 7. 760 0, 968 0, 980 € 7. 678 € 7. 760 € 156 € 58 0, 964 0, 980 0, 013 € 81 € 11. 602 € 4. 613 0, 016 € 4. 976

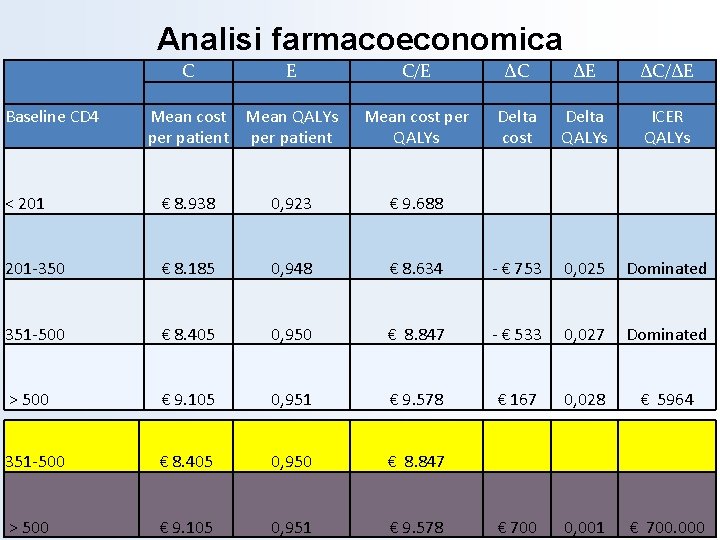
Analisi farmacoeconomica Baseline CD 4 C E Mean cost Mean QALYs per patient C/E Mean cost per QALYs ΔC ΔE ΔC/ΔE Delta ICER cost QALYs < 201 € 8. 938 0, 923 € 9. 688 201 -350 € 8. 185 0, 948 € 8. 634 - € 753 0, 025 Dominated 351 -500 € 8. 405 0, 950 € 8. 847 - € 533 0, 027 Dominated > 500 € 9. 105 0, 951 € 9. 578 € 167 0, 028 € 5964 351 -500 € 8. 405 0, 950 € 8. 847 > 500 € 9. 105 0, 951 € 9. 578 € 700 0, 001 € 700. 000

Osservazioni Finali Dai dati degli osservatori proposti, siano essi di natura osservazionale “più classica” (studi clinici), di natura più “pratica, di vita reale” (database amministrativi), oppure di natura paziente-centrata (survey sulle persone con HIV), la strategia STR tende ad essere quella più accettata, più duratura e costo-efficace.

Grazie al contributo di Gilead Sciences