LA PHARMACODYNAMIE DES ANTIBIOTIQUES 1 HODILLE ELISABETH BUFFAZ

LA PHARMACODYNAMIE DES ANTIBIOTIQUES 1 HODILLE ELISABETH BUFFAZ CAMILLE LE 12 MARS 2012 DES BACTÉRIOLOGIE : HIVER 2012 TUTEUR : PROFESSEUR GÉRARD LINA

PLAN 2 Définitions et intérêts en clinique Notions importantes de pharmacodynamie Bactéricidie CMI Paramètres p. K/p. D importants Les antibiotiques à bactéricidie temps-dépendante β-Lactamines Glycopeptides Les antibiotiques à bactéricidie concentration-dépendante Aminosides Fluoroquinolones Analyses pratiquées aux HCL
ABREVIATIONS ET ACRONYMES UTILISES 3 AUIC /ASIC: Aire sous la courbe/CMI ASC: Aire sous la courbe Cl: Clairance CMI : Concentration minimale inhibitrice Cmax: Concentration sérique maximale Cres : Concentration sérique résiduelle Css: Concentration sérique à l’équilibre EER : Epuration extra-rénale EPA : Effet post-antibiotique p. K: Pharmacocinétique p. D: Pharmacodynamie t ½: Demi-vie d’élimination Vd: Volume de distribution

DEFINITIONS 4 Pharmacodynamie (sens strict du terme): Étude des effets d’un principe actif sur l'organisme : étude de l'interaction substance active/récepteur Pharmacodynamie appliquée aux antibiotiques : concept de « p. K/p. D » Ensemble des propriétés pharmacocinétiques et antibactériennes (activité bactéricide) d’un antibiotique évaluation de son activité in vitro et in vivo In vivo : étude de la variation de l’effet bactéricide des antibiotiques aux sites infectieux en fonction du temps et de la concentration en antibiotique
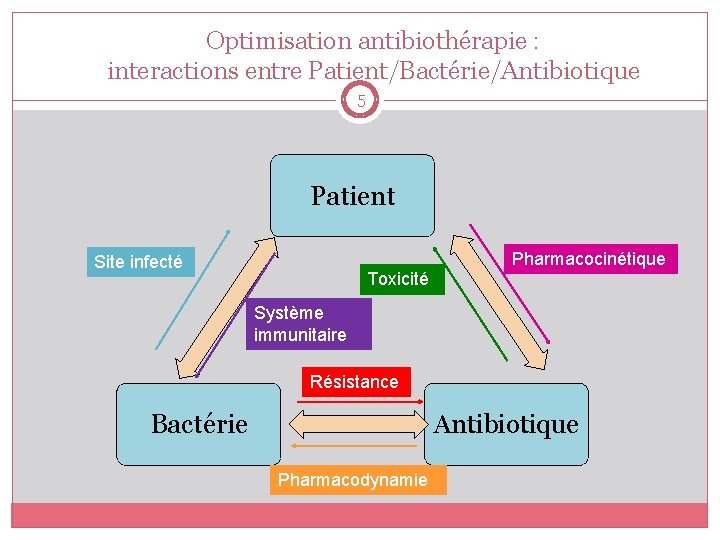
Optimisation antibiothérapie : interactions entre Patient/Bactérie/Antibiotique 5 Patient Site infecté Toxicité Pharmacocinétique Système immunitaire Résistance Bactérie Antibiotique Pharmacodynamie
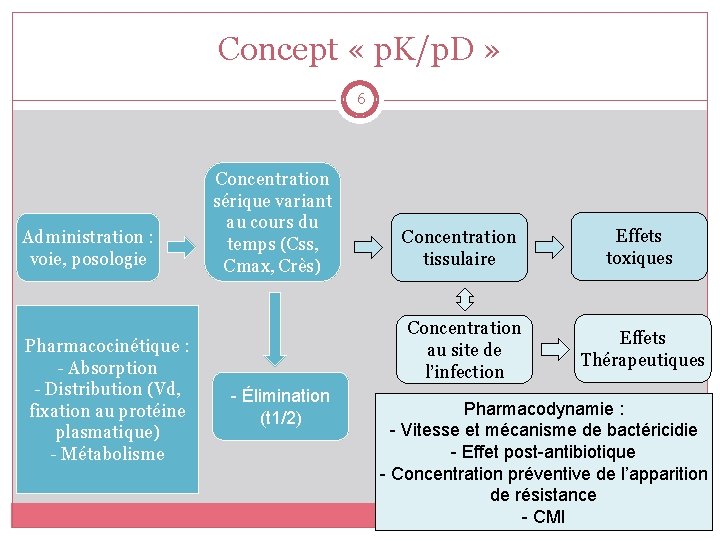
Concept « p. K/p. D » 6 Administration : voie, posologie Pharmacocinétique : - Absorption - Distribution (Vd, fixation au protéine plasmatique) - Métabolisme Concentration sérique variant au cours du temps (Css, Cmax, Crès) - Élimination (t 1/2) Concentration tissulaire Effets toxiques Concentration au site de l’infection Effets Thérapeutiques Pharmacodynamie : - Vitesse et mécanisme de bactéricidie - Effet post-antibiotique - Concentration préventive de l’apparition de résistance - CMI

INTERETS EN CLINIQUE Bon usage des antibiotiques 7 Obtenir une efficacité d’emblée du traitement Limiter la toxicité de l’antibiotique Aide à la prévention de mutants résistants Intérêt pharmaco-économique Aucun intérêt dans le cas d’infection simple à germe très sensible Critère de choix pour les infections nosocomiales +++ : Bactérie plus résistante (CMI plus élevée) Localisation de l’infection sur des sites difficiles d’accès pour les antibiotiques Patients sévères (réanimation, grand brûlés, néonat) modifications pharmacocinétiques Cas particulier des neutropéniques fébriles (Hématologie) Bactéricidie naturelle diminuée/Pas d’effet post antibiotique

EXEMPLE : Patients de réanimation 8 ↑ Vd (x 2 à 4) Utilisation d’agents vasoconstricteurs hypoperfusion tissulaire concentration tissulaire <<< concentration plasmatique (très variable) ↓ Cmax + ↓ C au site infectieux → Risque de sous dosage+++ ↓ Cl (t 1/2 x 2 à 3) ↑ Cres →Risque d’accumulation ↓ t 1/2 si EER donc ↑ Cl risque de sous-dosage Variabilité interindividuelle importante (CV de 40 à 60%) Mohr JF et al. 2004 Individualisation de la posologie propre aux patients et aux bactéries responsables de l’infection
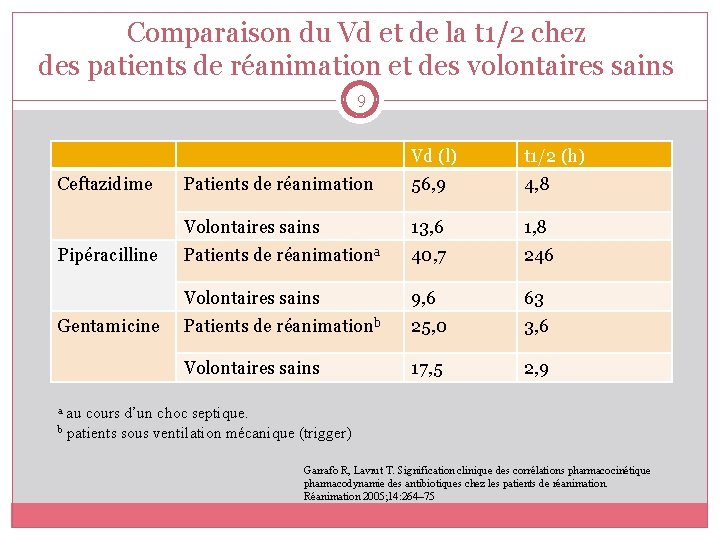
Comparaison du Vd et de la t 1/2 chez des patients de réanimation et des volontaires sains 9 Ceftazidime Pipéracilline Gentamicine Vd (l) t 1/2 (h) Patients de réanimation 56, 9 4, 8 Volontaires sains 13, 6 1, 8 Patients de réanimationa 40, 7 246 Volontaires sains 9, 6 63 Patients de réanimationb 25, 0 3, 6 Volontaires sains 17, 5 2, 9 a au cours d’un choc septique. b patients sous ventilation mécanique (trigger) Garrafo R, Lavrut T. Signification clinique des corrélations pharmacocinétique pharmacodynamie des antibiotiques chez les patients de réanimation. Réanimation 2005; 14: 264– 75
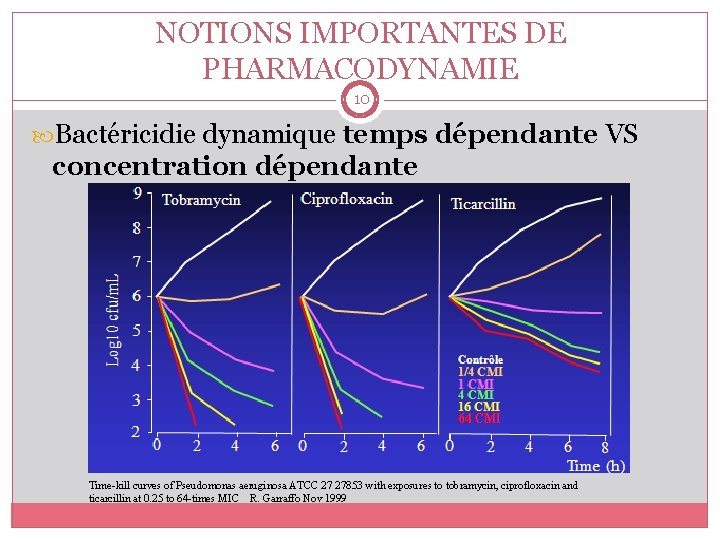
NOTIONS IMPORTANTES DE PHARMACODYNAMIE 10 Bactéricidie dynamique temps dépendante VS concentration dépendante Time-kill curves of Pseudomonas aeruginosa ATCC 27 27853 with exposures to tobramycin, ciprofloxacin and ticarcillin at 0. 25 to 64 -times MIC R. Garraffo Nov 1999

NOTIONS IMPORTANTES DE PHARMACODYNAMIE 11 Bactéricidie temps -dépendante ßlactamines, Glycopeptides, Clindamycine, Macrolides, Linezolide, Tetracyclines • Lente • Intensité liée au • Temps de contact • Concentration seuil • EPA faible ou nul Modèles animaux : T>CMI, prédictif du succès thérapeutique Relations concentration/effet varient selon le couple ATB/bactérie Bactéricidie concentrationdépendante Aminosides, Fluoroquinolones, Daptomycine, Métronidazole, Télithromycine • Rapide et intense • V augmente avec C • Prévention repousse • EPA variable A >>> FQ Modèles animaux : Cmax/CMI et AUC/CMI prédictifs du succès Relations concentration/effet varient selon le couple ATB/bactérie NB : Azithromycine et Linezolide possèdent un EPA modéré
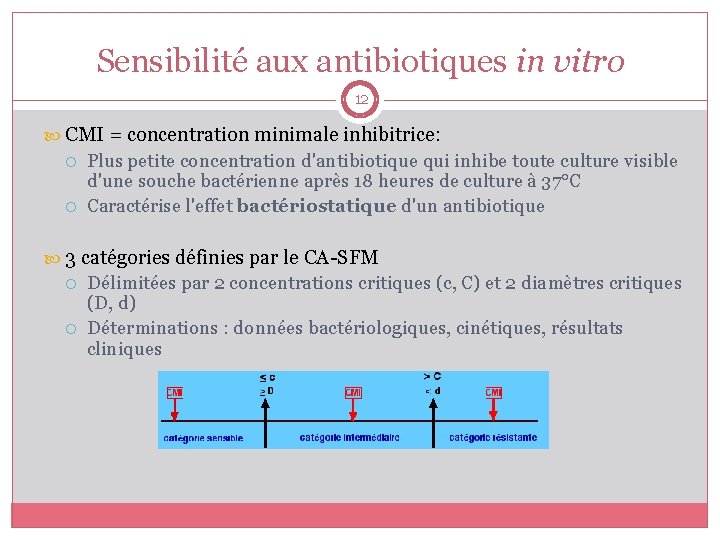
Sensibilité aux antibiotiques in vitro 12 CMI = concentration minimale inhibitrice: Plus petite concentration d'antibiotique qui inhibe toute culture visible d'une souche bactérienne après 18 heures de culture à 37°C Caractérise l'effet bactériostatique d'un antibiotique 3 catégories définies par le CA-SFM Délimitées par 2 concentrations critiques (c, C) et 2 diamètres critiques (D, d) Déterminations : données bactériologiques, cinétiques, résultats cliniques

PARAMETRES « PK/PD » IMPORTANTS : Relations entre paramètres pharmacocinétiques et CMI 13 T > CMI: Temps pendant lequel les concentrations sériques sont > CMI Intervalle de deux administrations Exprimé en % de cet intervalle Caractéristique des ATB temps dépendant ASIC (AUIC): ASC/CMI rapporté a 24 h Caractéristique des ATB temps ET concentration dépendant → paramètre universel Quotient inhibiteur (QI): Concentration /CMI: quotients inhibiteurs divers (max, min, sériques, tissulaires) suivant famille ATB
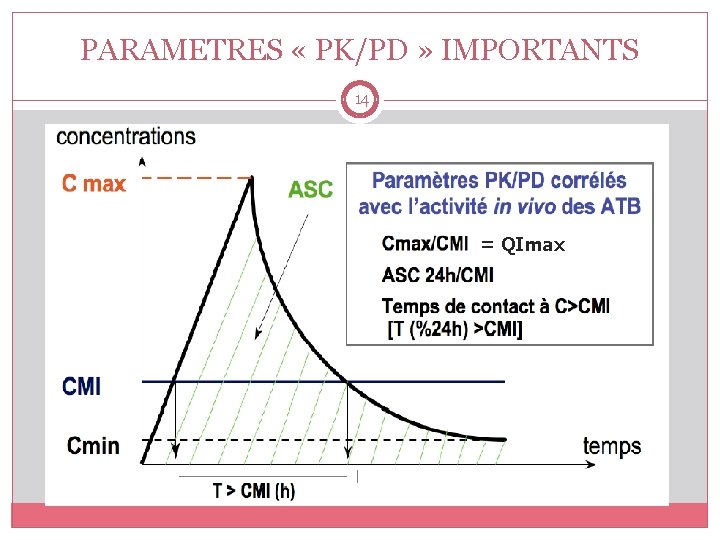
PARAMETRES « PK/PD » IMPORTANTS 14 = QImax

PARAMETRES « PK/PD » IMPORTANTS 15 CPM: Concentration de Prévention des Mutations = CMI de la sous population résistante FS: Fenêtre de sélection = Ensemble des C comprises entre CMI et CPM t. FS: Temps pendant lequel les C sériques sont dans la FS F Jehl et al. , RFL, 2011

CPM en routine? 16 = Concentration minimale d’antibiotique qui prévient la sélection de mutants résistants de premier niveau en présence d’un fort inoculum bactérien (109 -1010 UFC/m. L) ↔ En pratique = détermination de la CMI avec un inoculum de 109 -1010 au lieu de 105 UFC/m. L Concept non dynamique: calcul de CPM avec concentrations fixes En faveur de l’utilisation de doses fortes d’antibiotiques (>CPM), pas toujours atteignables en clinique (toxicité)
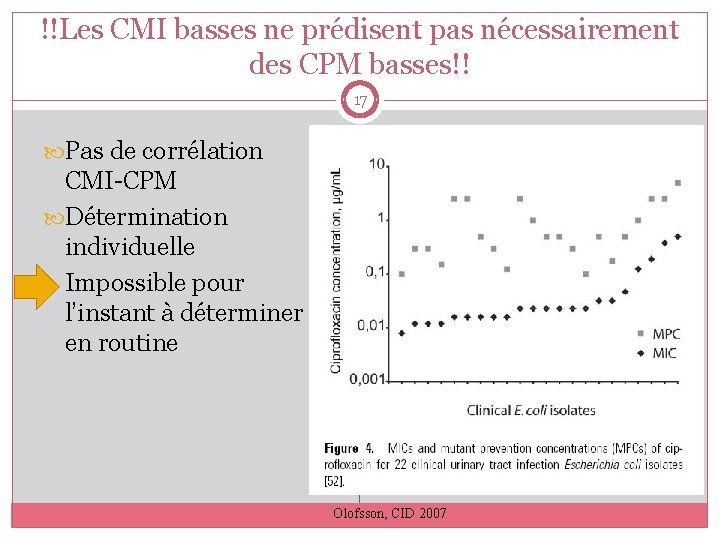
!!Les CMI basses ne prédisent pas nécessairement des CPM basses!! 17 Pas de corrélation CMI-CPM Détermination individuelle Impossible pour l’instant à déterminer en routine Olofsson, CID 2007

LES ANTIBIOTIQUES A BACTERICIDIE TEMPS DEPENDANT 18 Beta-Lactamines Glycopeptides

Effet inoculum 19 Baisse de l’activité ATB en présence d’un inoculum élevé: élévation de la CMI Observé à des concentrations de 5 x 107 UFC/m. L β-lactamines, Glycopeptides et Linezolide Justifie l’association avec les aminosides

LA PHARMACODYNAMIE DES BETA-LACTAMINES Pharmacocinétique 20 Absorption digestive médiocre (saturable): β-lactamines large spectre souvent disponibles que par voie IV Csérique et tissulaire per os<< Csérique et tissulaire IV Demi-vie d’élimination brève (1 à 2 h) Administration pluriquotidienne souvent nécessaire 2 à 6/j en IV directe Élimination rénale prédominante (adaptation posologie si IR) Diffusion tissulaire globalement satisfaisante Exception du LCR, œil, prostate et os Pour LCR varie d’une molécule à une autre Sauf Ceftriaxone
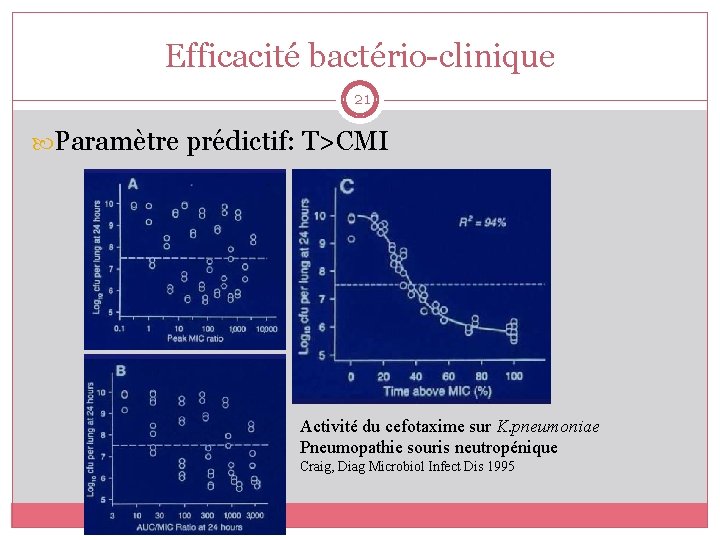
Efficacité bactério-clinique 21 Paramètre prédictif: T>CMI Activité du cefotaxime sur K. pneumoniae Pneumopathie souris neutropénique Craig, Diag Microbiol Infect Dis 1995

Efficacité bactério-clinique 22 Objectifs à atteindre: Infection modérée à peu sévère: T>CMI 40 à 70% F Jehl, D Leveque, Perfusion continue des bêtalactamines: intérêts, inconvénients, modalités pratiques Réanimation 2009
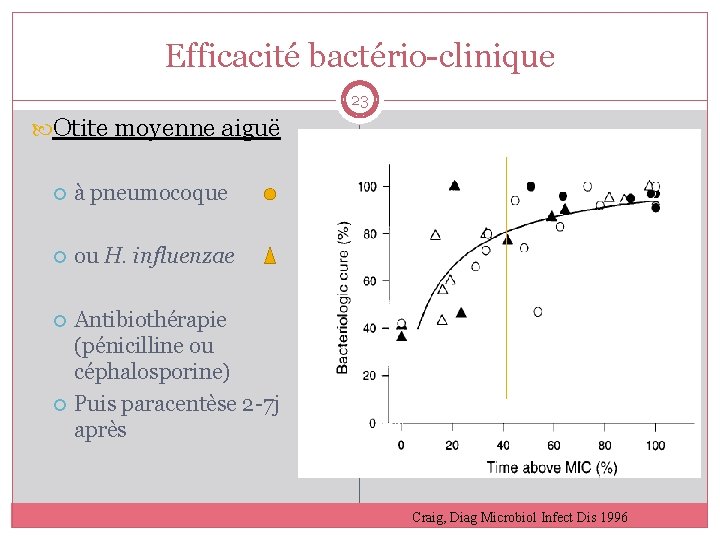
Efficacité bactério-clinique 23 Otite moyenne aiguë à pneumocoque ou H. influenzae Antibiothérapie (pénicilline ou céphalosporine) Puis paracentèse 2 -7 j après Craig, Diag Microbiol Infect Dis 1996

Efficacité bactério-clinique 24 Objectifs à atteindre: Contexte de réanimation: T> 4 -10 CMI = 100% → QI résiduel compris entre 4 et 10 Scaglione F, L. Paraboni / International Journal of Antimicrobial Agents 32 2008 Garraffo R, Lavrut T. Signification clinique des corrélations pharmacocinétique/pharmacodynamique des antibiotiques chez les patients de réanimation. Réanimation. 2005 F Jehl, D Leveque, Perfusion continue des bêtalactamines: intérêts, inconvenients, modalités pratiques Réanimation 2009 Neutropéniques traités par méropénème, bactériémies à Gram+ ou Gram-: T>CMI supérieur à 75%: 80% évolution favorable T>CMI inférieur à 50%: 36% évolution favorable (p = 0, 001) Ariano, Ann Pharmacother 2005
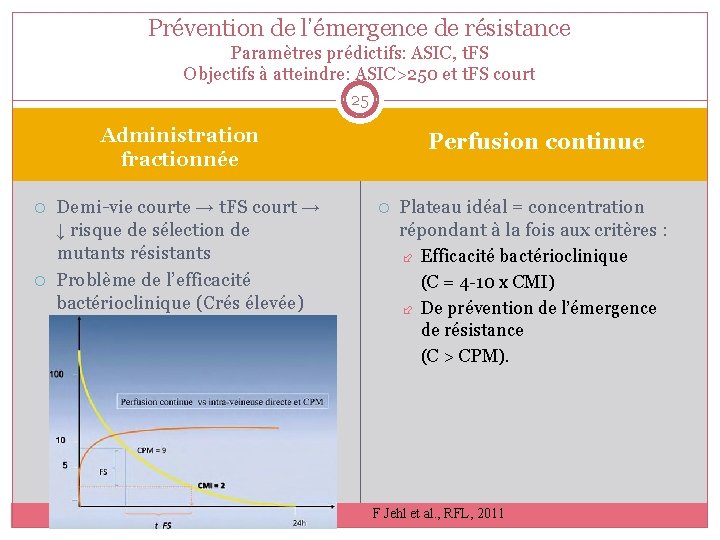
Prévention de l’émergence de résistance Paramètres prédictifs: ASIC, t. FS Objectifs à atteindre: ASIC>250 et t. FS court 25 Administration fractionnée Demi-vie courte → t. FS court → ↓ risque de sélection de mutants résistants Problème de l’efficacité bactérioclinique (Crés élevée) Perfusion continue Plateau idéal = concentration répondant à la fois aux critères : Efficacité bactérioclinique (C = 4 -10 x CMI) De prévention de l’émergence de résistance (C > CPM). F Jehl et al. , RFL, 2011
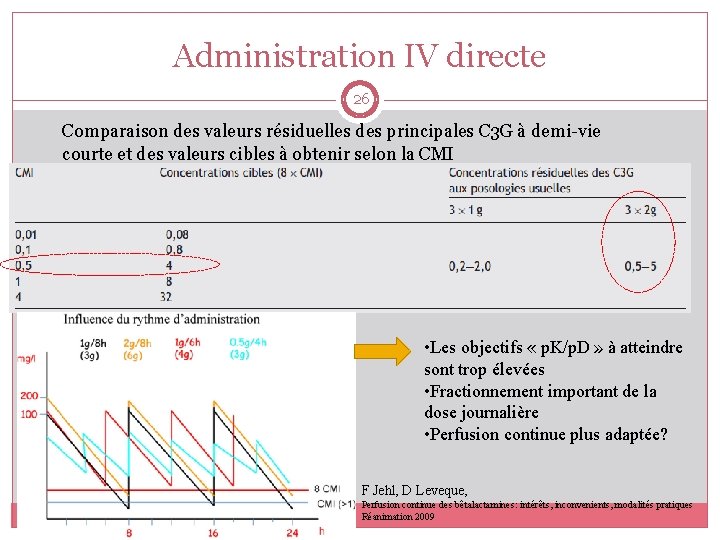
Administration IV directe 26 Comparaison des valeurs résiduelles des principales C 3 G à demi-vie courte et des valeurs cibles à obtenir selon la CMI • Les objectifs « p. K/p. D » à atteindre sont trop élevées • Fractionnement important de la dose journalière • Perfusion continue plus adaptée? F Jehl, D Leveque, Perfusion continue des bêtalactamines: intérêts, inconvenients, modalités pratiques Réanimation 2009

Perfusion continue plus adaptée? 27 Céfépime Mode d’administration Posologies(g/24 h) Concentrations (mg/L) Perfusion continue 4 28 (à l’équilibre) IV Directe 2 x 2 3. 2 (résiduelle) Bardin et al. , RICAI 1998 Dose à perfuser peu prévisible: Perfusion de 3 g/24 h de Ceftazidime → concentration à l’équilibre 10 -62 mg/L Benko AS et al. 1996
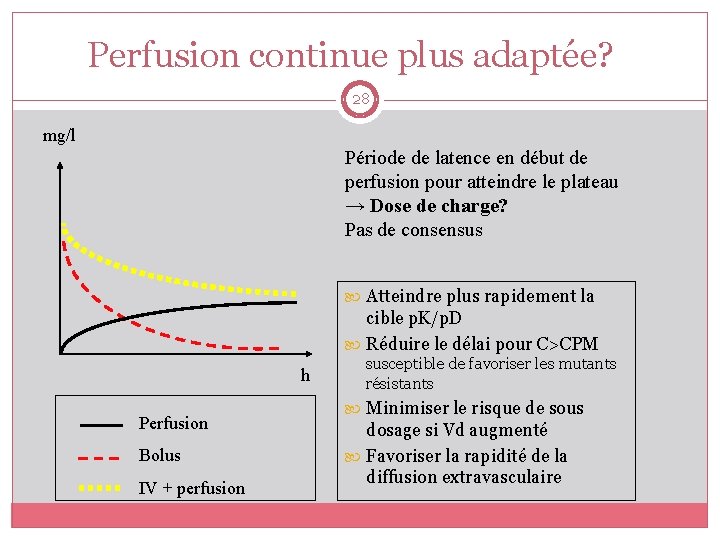
Perfusion continue plus adaptée? 28 mg/l Période de latence en début de perfusion pour atteindre le plateau → Dose de charge? Pas de consensus Atteindre plus rapidement la cible p. K/p. D Réduire le délai pour C>CPM h Perfusion Bolus IV + perfusion susceptible de favoriser les mutants résistants Minimiser le risque de sous dosage si Vd augmenté Favoriser la rapidité de la diffusion extravasculaire
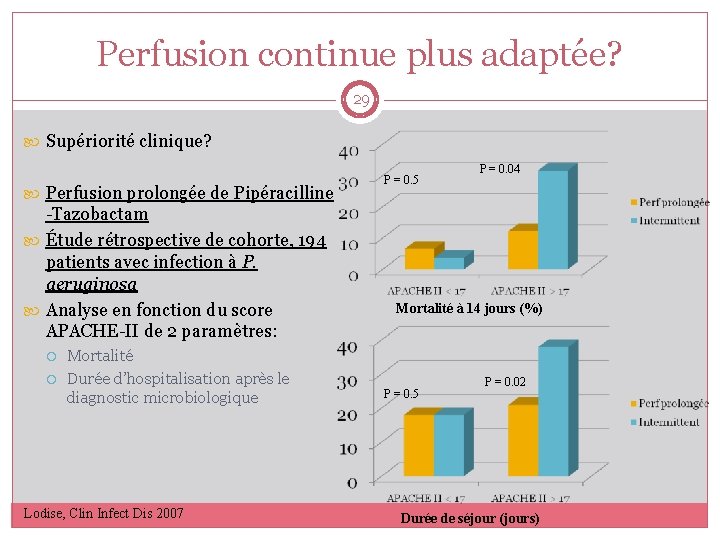
Perfusion continue plus adaptée? 29 Supériorité clinique? Perfusion prolongée de Pipéracilline -Tazobactam Étude rétrospective de cohorte, 194 patients avec infection à P. aeruginosa Analyse en fonction du score APACHE-II de 2 paramètres: Mortalité Durée d’hospitalisation après le diagnostic microbiologique Lodise, Clin Infect Dis 2007 P = 0. 5 P = 0. 04 Mortalité à 14 jours (%) P = 0. 5 P = 0. 02 Durée de séjour (jours)
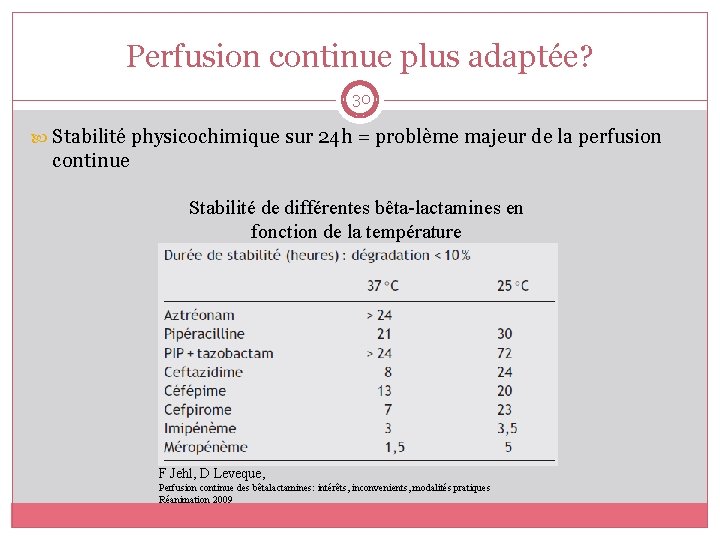
Perfusion continue plus adaptée? 30 Stabilité physicochimique sur 24 h = problème majeur de la perfusion continue Stabilité de différentes bêta-lactamines en fonction de la température F Jehl, D Leveque, Perfusion continue des bêtalactamines: intérêts, inconvenients, modalités pratiques Réanimation 2009

LA PHARMACODYNAMIE DES GLYCOPEPTIDES Pharmacocinétique 31 Pas d’absorption per os Diffusion tissulaire: Bonne dans les séreuses (plèvre, péricarde) Modérée dans l’os et le poumon (Teicoplanine +++) Nulle dans le LCR (faible et saturable dans la méningite) Elimination rénale sous forme inchangée Demi-vie : 6 -8 h Vancomycine 70 -100 h Teicoplanine
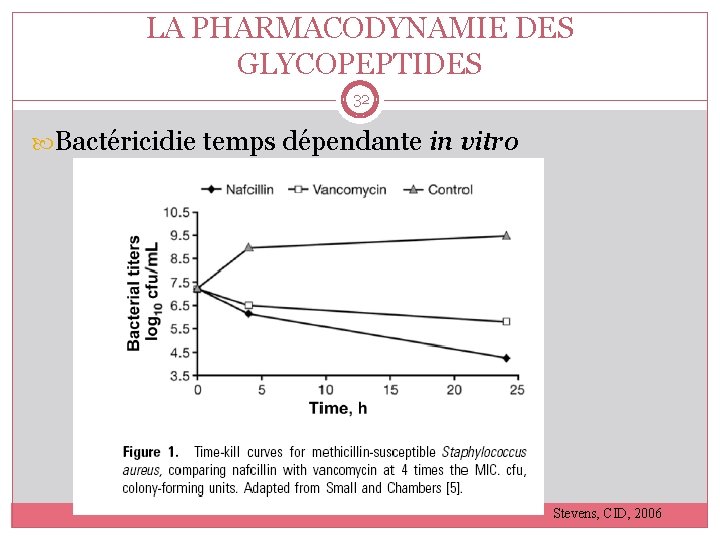
LA PHARMACODYNAMIE DES GLYCOPEPTIDES 32 Bactéricidie temps dépendante in vitro Stevens, CID, 2006

LA PHARMACODYNAMIE DES GLYCOPEPTIDES 33 Bactéricidie concentration dépendante in vivo Infection expérimentale de souris ( SASM) efficacité de la vancomycine ASIC > 300 Rybak, Clin Infect Dis 2006

LA PHARMACODYNAMIE DES GLYCOPEPTIDES 34 Infections à S. aureus incluant bactériémie et endocardite Pas de paramètre p. K/p. D identifié Pas de relation entre concentrations et efficacité bactérioclinique Rybak et al. , ICAAC 1997 Drew et al. , ICAAC 2004 Pneumonie à S. aureus meti R 102 patients; pas de relation entre ASC ou résiduelle et survie Jeffres et al, Chest, 2006 108 patients; relation ASIC> 400 et succès clinique Moise-Broder et al. , Clin Pharmacokinet 2004 35 patients; relation ASIC > 345 et succès clinique (76 vs 22%) Moise et al. , Am J Health Syst Pharm, 2000
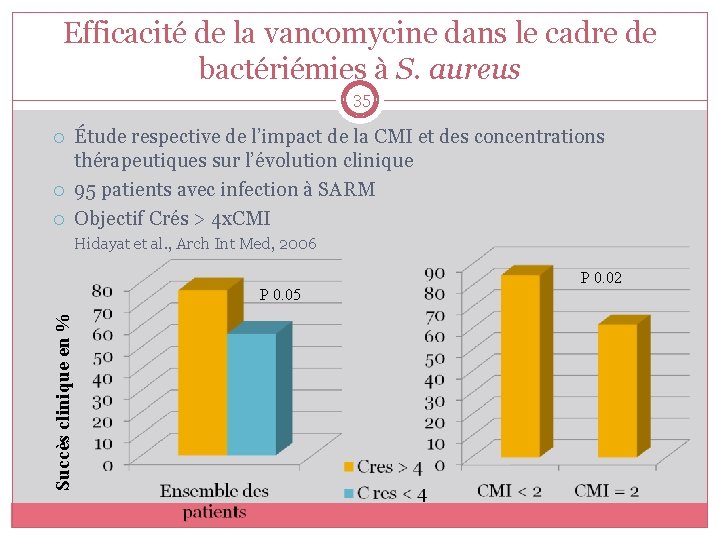
Efficacité de la vancomycine dans le cadre de bactériémies à S. aureus 35 Étude respective de l’impact de la CMI et des concentrations thérapeutiques sur l’évolution clinique 95 patients avec infection à SARM Objectif Crés > 4 x. CMI Hidayat et al. , Arch Int Med, 2006 Succès clinique en % P 0. 05 P 0. 02
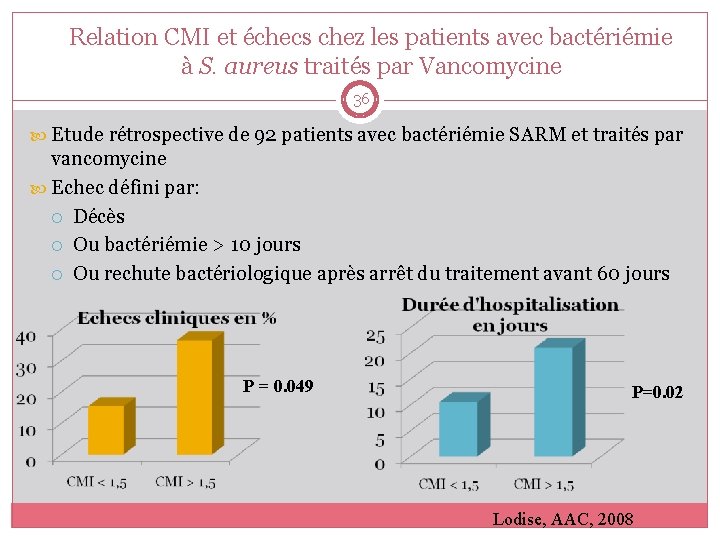
Relation CMI et échecs chez les patients avec bactériémie à S. aureus traités par Vancomycine 36 Etude rétrospective de 92 patients avec bactériémie SARM et traités par vancomycine Echec défini par: Décès Ou bactériémie > 10 jours Ou rechute bactériologique après arrêt du traitement avant 60 jours P = 0. 049 P=0. 02 Lodise, AAC, 2008

LA PHARMACODYNAMIE DES GLYCOPEPTIDES 37 Paramètres prédictifs et objectifs à atteindre: T>4 à 8 CMI= 100% ↔ QIres = 4 à 8 ASIC >250 -500 également retenue Non contradictoire avec une bactéricidie temps dépendant Ne préjuge pas du profil pharmacocinétique (t 1/2 élevée ou perfusion continue ↑ ASIC ) Prévention de l’émergence de résistance également corrélée F Jehl, C Koebel, Antibiotiques-bactéries: une relation (pharmaco)dynamique, RFL, 2011 Garrafo R, Lavrut T. Signification clinique des corrélations pharmacocinétique–pharmacodynamie des antibiotiques chez les patients de réanimation. Réanimation 2005
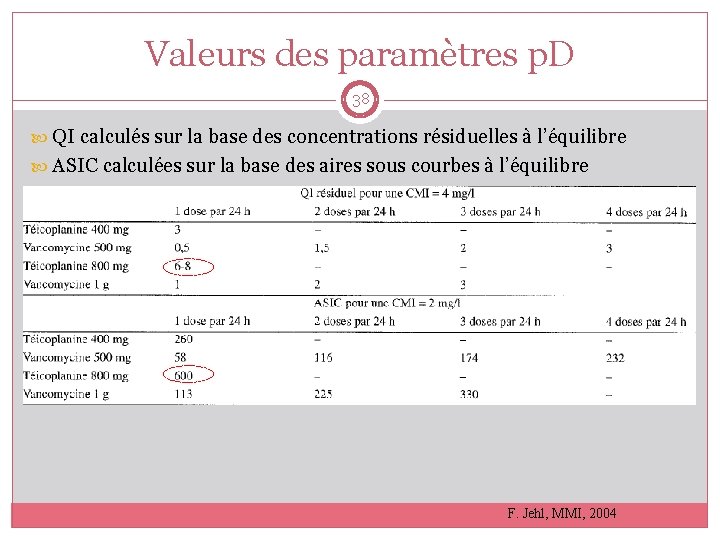
Valeurs des paramètres p. D 38 QI calculés sur la base des concentrations résiduelles à l’équilibre ASIC calculées sur la base des aires sous courbes à l’équilibre F. Jehl, MMI, 2004

LES ANTIBIOTIQUES À BACTÉRICIDIE CONCENTRATION-DÉPENDANTE 39 Aminosides Fluoroquinolones
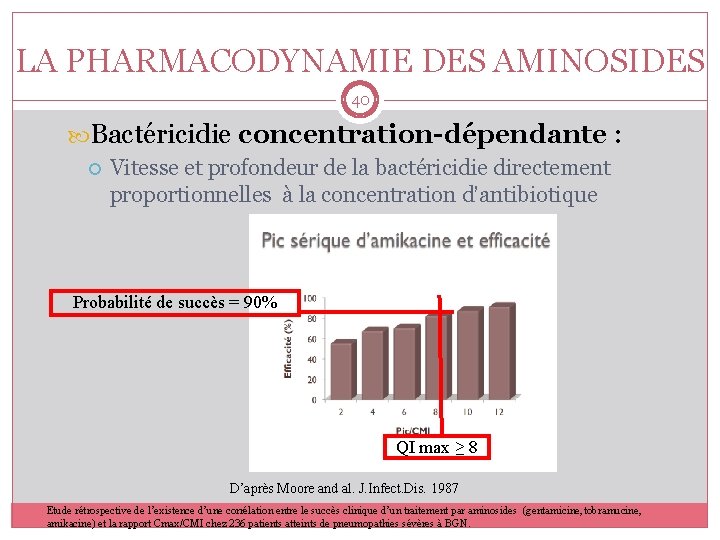
LA PHARMACODYNAMIE DES AMINOSIDES 40 Bactéricidie concentration-dépendante : Vitesse et profondeur de la bactéricidie directement proportionnelles à la concentration d’antibiotique Probabilité de succès = 90% QI max ≥ 8 D’après Moore and al. J. Infect. Dis. 1987 Etude rétrospective de l’existence d’une corrélation entre le succès clinique d’un traitement par aminosides (gentamicine, tobramucine, amikacine) et la rapport Cmax/CMI chez 236 patients atteints de pneumopathies sévères à BGN.

Pharmacocinétique des aminosides 41 Absorption : Molécule de petite taille et très hydrosoluble aucune absorption par voie orale Voie parentérale exclusive Distribution : Chez l’individu sain, Vd faible variant entre 0. 10 et 0. 20 L/Kg Distribution essentiellement plasmatique et interstitielle Vd variable chez les patients de réanimation : Le plus souvent Vd ↑ (X 2 -10) Fixation aux protéines plasmatiques faible < 10% Métabolisme : Très peu métabolisé Excrétion : Élimination sous forme active par voie rénale +++ avec réabsorption tubulaire concentration au niveau du cortex rénal Si IR accumulation +++ et risque de toxicité

Effet post-antibiotique des aminosides rémanence de l’effet bactéricide de l’antibiotique lorsque celui-ci a disparu In Vitro In Vivo • Correspond à l’intervalle de temps • Mesuré à partir du moment où la nécessaire aux bactéries pour recroître d’un log après le retrait de l’antibiotique concentration d’antibiotique au niveau du site infectieux tombent en dessous des valeurs de la CMI • Conséquence d’une altération profonde du métabolisme de la bactérie sur les systèmes respiratoires • Durée plus longue qu’in vitro • EPA leucocytes-dépendant : phagocytose • Variable en fonction de l’espèce + bactéricidie intracellulaire améliorées bactérienne (1 à 2 h pour S. aureus ; 2 à 8 h pendant EPA pour les BGN) Proportionnel à la concentration de l’antibiotique présente pendant la durée de contact et à la durée de contact •
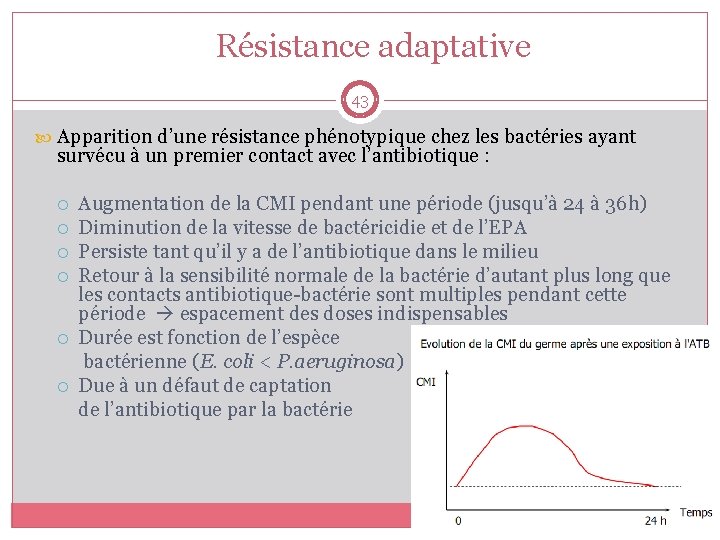
Résistance adaptative 43 Apparition d’une résistance phénotypique chez les bactéries ayant survécu à un premier contact avec l’antibiotique : Augmentation de la CMI pendant une période (jusqu’à 24 à 36 h) Diminution de la vitesse de bactéricidie et de l’EPA Persiste tant qu’il y a de l’antibiotique dans le milieu Retour à la sensibilité normale de la bactérie d’autant plus long que les contacts antibiotique-bactérie sont multiples pendant cette période espacement des doses indispensables Durée est fonction de l’espèce bactérienne (E. coli < P. aeruginosa) Due à un défaut de captation de l’antibiotique par la bactérie

Effet post-antibiotique ou résistance adaptative? 44 Paradoxe = un des 2 phénomènes l’emportent : Concentration initiale d’antibiotique suffisamment importante => peu de bactérie survivantes => EPA Concentration initiale d’antibiotique sub-optimale => plus de bactéries survivantes => résistance adaptative intérêt de la dose de charge +++
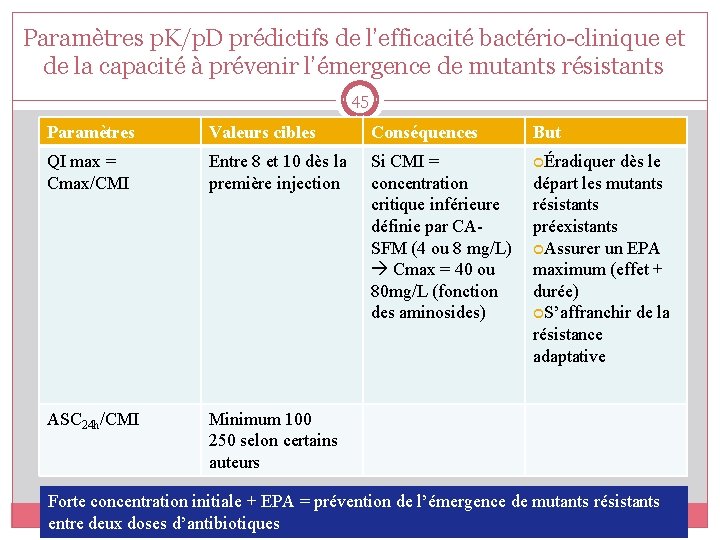
Paramètres p. K/p. D prédictifs de l’efficacité bactério-clinique et de la capacité à prévenir l’émergence de mutants résistants 45 Paramètres Valeurs cibles Conséquences But QI max = Cmax/CMI Entre 8 et 10 dès la première injection Si CMI = concentration critique inférieure définie par CASFM (4 ou 8 mg/L) Cmax = 40 ou 80 mg/L (fonction des aminosides) Éradiquer dès le ASC 24 h/CMI Minimum 100 250 selon certains auteurs départ les mutants résistants préexistants Assurer un EPA maximum (effet + durée) S’affranchir de la résistance adaptative Forte concentration initiale + EPA = prévention de l’émergence de mutants résistants entre deux doses d’antibiotiques

Conséquences sur le schéma posologique 46 Ancien schéma : dose totale journalière répartie en 2 ou 3 injections Pour obtenir les pics sériques adéquats efficaces dès la première injection Dose Unique Journalière = DUJ (administration de la dose totale journalière en une seule fois) Gentamicine/tobramycine/nétilmicine : 3 -4 à 8 mg/Kg/j Amikacine : 15 à 30 mg/Kg/j Administrer la dose suivante suffisamment loin de la précédente afin de minimiser l’impact de la résistance adaptative : Intervalle de dose : 24 h Dose de charge pour les patients de réanimation ayant un Vd très augmenté
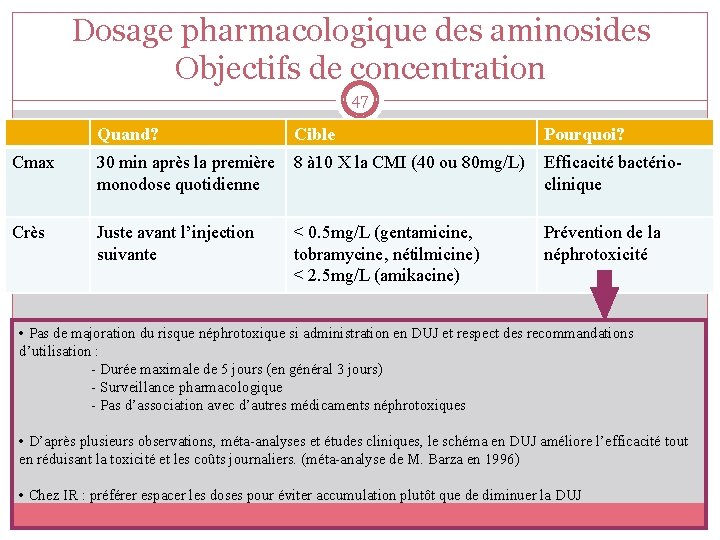
Dosage pharmacologique des aminosides Objectifs de concentration 47 Quand? Cible Pourquoi? Cmax 30 min après la première 8 à 10 X la CMI (40 ou 80 mg/L) monodose quotidienne Efficacité bactérioclinique Crès Juste avant l’injection suivante Prévention de la néphrotoxicité < 0. 5 mg/L (gentamicine, tobramycine, nétilmicine) < 2. 5 mg/L (amikacine) • Pas de majoration du risque néphrotoxique si administration en DUJ et respect des recommandations d’utilisation : - Durée maximale de 5 jours (en général 3 jours) - Surveillance pharmacologique - Pas d’association avec d’autres médicaments néphrotoxiques • D’après plusieurs observations, méta-analyses et études cliniques, le schéma en DUJ améliore l’efficacité tout en réduisant la toxicité et les coûts journaliers. (méta-analyse de M. Barza en 1996) • Chez IR : préférer espacer les doses pour éviter accumulation plutôt que de diminuer la DUJ
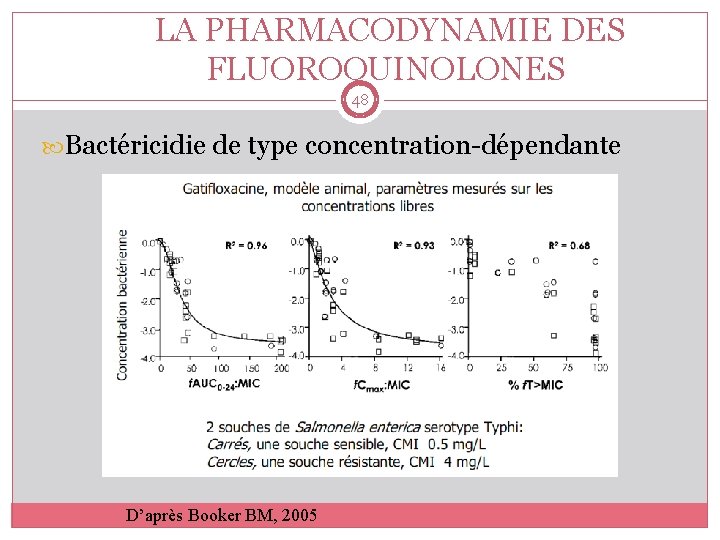
LA PHARMACODYNAMIE DES FLUOROQUINOLONES 48 Bactéricidie de type concentration-dépendante D’après Booker BM, 2005

Pharmacocinétique des FQ 49 Absorption : Excellente biodisponibilité par voie orale : 100% Chez les patients de réanimation, nombreuses variations donc utilisation de la voie parentérale +++ Distribution : Vd en moyenne important (1. 5 -3 L/Kg) Large diffusion tissulaire et intracellulaire Liaison aux protéines plasmatiques : 10 à 40% Métabolisme : hépatique par les cy. P 450 Très peu métabolisé : ofloxacine Plus métabolisé: péfloxacine attention aux IM Excrétion : Rénale sous forme inchangée pour l’ofloxacine Élimination rénale et hépatique : ciprofloxacine Adaptation posologique aléatoires si IH
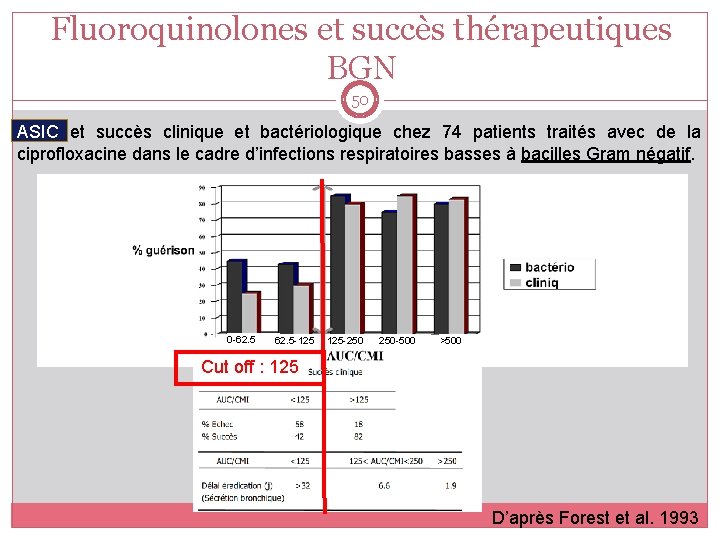
Fluoroquinolones et succès thérapeutiques BGN 50 ASIC et succès clinique et bactériologique chez 74 patients traités avec de la ciprofloxacine dans le cadre d’infections respiratoires basses à bacilles Gram négatif. 0 -62. 5 -125 125 -250 250 -500 >500 Cut off : 125 D’après Forest et al. 1993
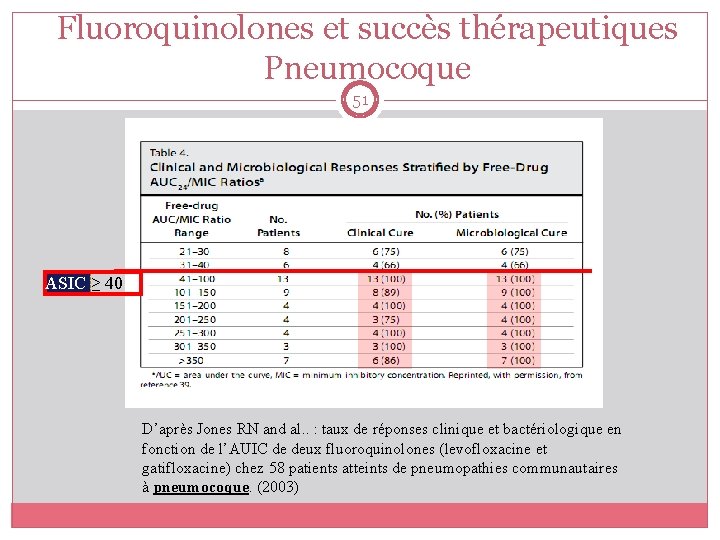
Fluoroquinolones et succès thérapeutiques Pneumocoque 51 ASIC ≥ 40 D’après Jones RN and al. . : taux de réponses clinique et bactériologique en fonction de l’AUIC de deux fluoroquinolones (levofloxacine et gatifloxacine) chez 58 patients atteints de pneumopathies communautaires à pneumocoque. (2003)
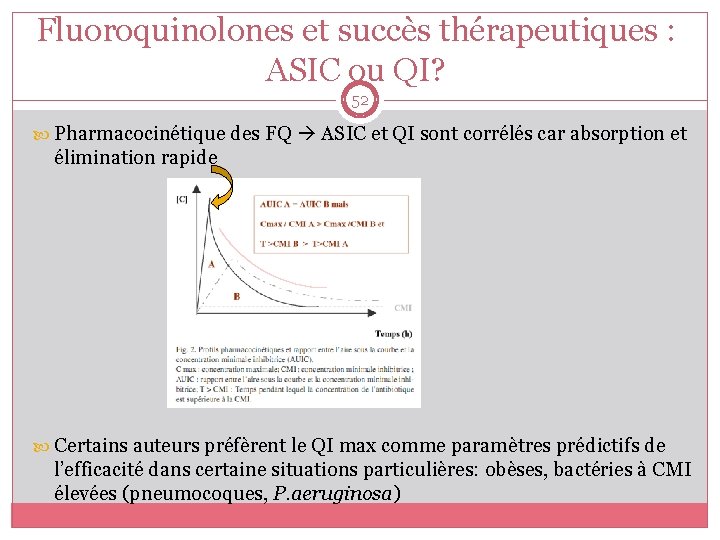
Fluoroquinolones et succès thérapeutiques : ASIC ou QI? 52 Pharmacocinétique des FQ ASIC et QI sont corrélés car absorption et élimination rapide Certains auteurs préfèrent le QI max comme paramètres prédictifs de l’efficacité dans certaine situations particulières: obèses, bactéries à CMI élevées (pneumocoques, P. aeruginosa)
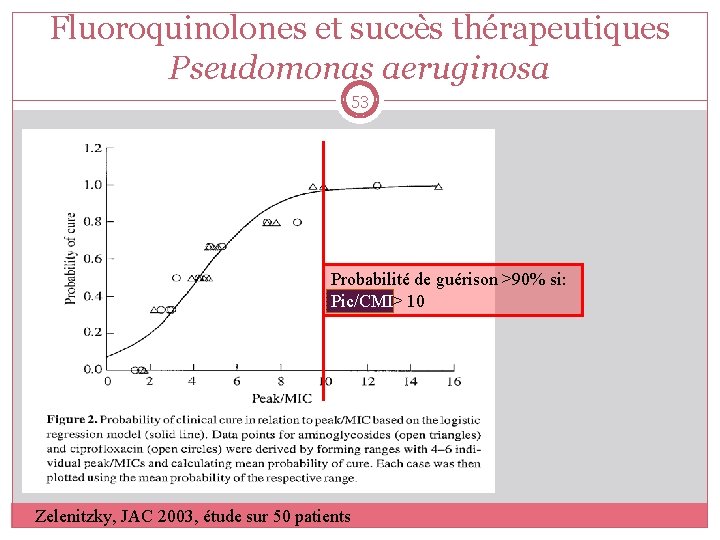
Fluoroquinolones et succès thérapeutiques Pseudomonas aeruginosa 53 Probabilité de guérison >90% si: Pic/CMI> 10 Zelenitzky, JAC 2003, étude sur 50 patients

Fluoroquinolones et résistance Faible barrière génétique : Importance d’atteindre la CPM 54 Mécanismes responsables de résistance de haut niveau : Mutation des cibles : ADN gyrase et topoisomérase de type IV (nécessité de 2 mutations successives sur l’ADN gyrase et sur la topoisomérase IV qui s’additionnent) Mécanismes responsables de résistance de bas niveau, facilitant l’apparition de résistances de haut niveau par augmentation de la CPM : Imperméabilité touchant les porines Pompes à efflux expulsant l’antibiotique après sa pénétration Synthèse d’une protéine qnr protégeant les topoisomérases Enzyme d’inactivation des FQ (1 seule mutation sur l’ADN gyrase ou la topoisomérase IV entraîne une résistance de haut niveau)
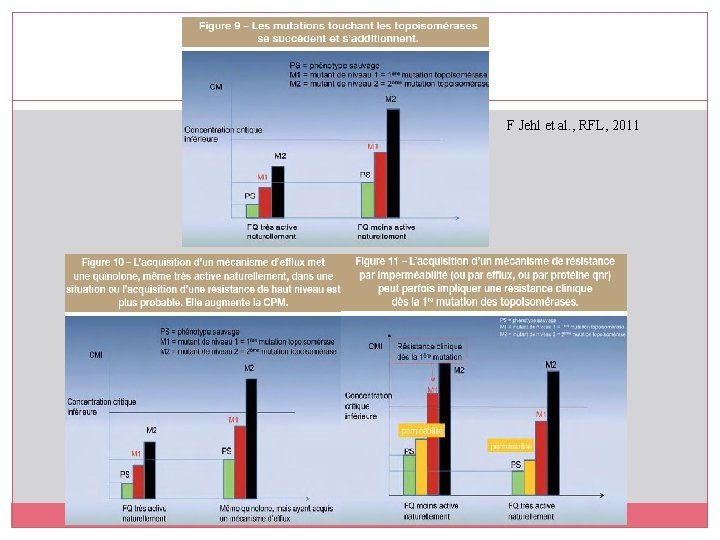
F Jehl et al. , RFL, 2011
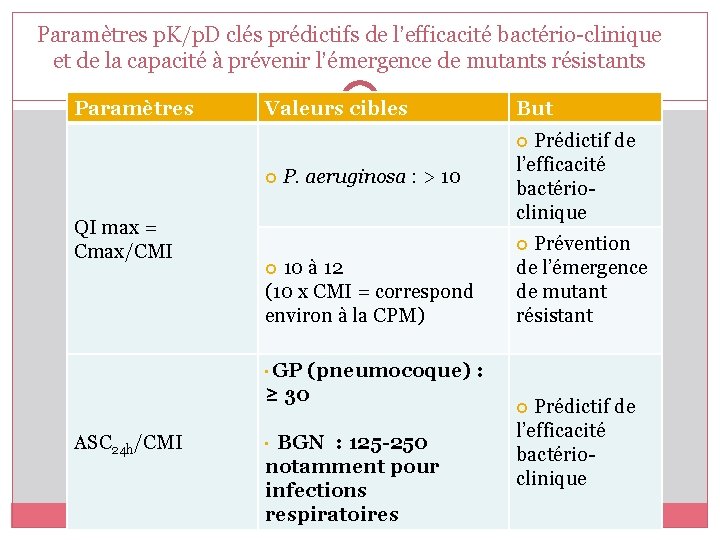
Paramètres p. K/p. D clés prédictifs de l’efficacité bactério-clinique et de la capacité à prévenir l’émergence de mutants résistants Paramètres Valeurs cibles But Prédictif de P. QI max = Cmax/CMI aeruginosa : > 10 l’efficacité bactérioclinique Prévention 10 à 12 (10 x CMI = correspond environ à la CPM) (pneumocoque) : ≥ 30 de l’émergence de mutant résistant • GP ASC 24 h/CMI BGN : 125 -250 notamment pour infections respiratoires • Prédictif de l’efficacité bactérioclinique
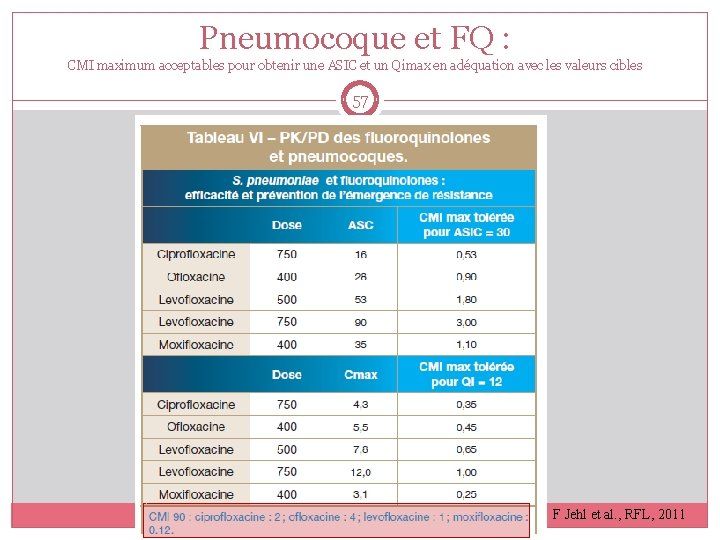
Pneumocoque et FQ : CMI maximum acceptables pour obtenir une ASIC et un Qimax en adéquation avec les valeurs cibles 57 F Jehl et al. , RFL, 2011
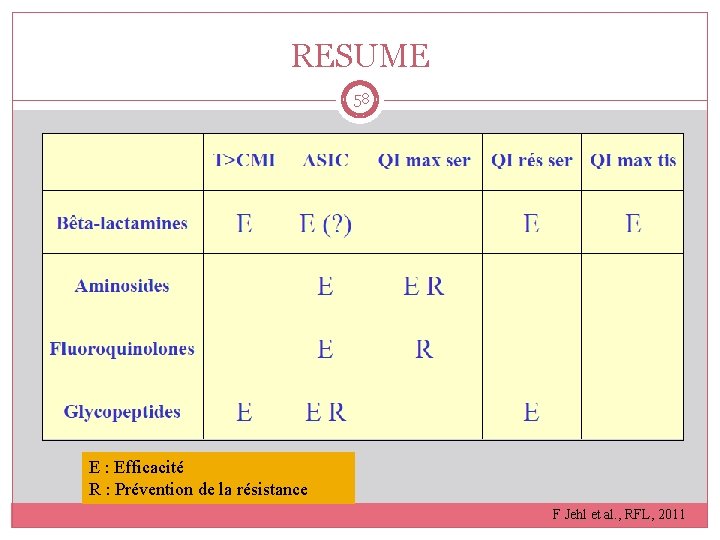
RESUME 58 E : Efficacité R : Prévention de la résistance F Jehl et al. , RFL, 2011

INTERET ET PLACE DU SUIVI THERAPEUTIQUE DES ANTIBIOTIQUES 59 Antibiotiques à spectre thérapeutique étroit (aminosides, glycopeptides) Echec thérapeutique : Mettre en évidence un sous-dosage par modifications des paramètres pharmacocinétiques et des paramètres p. K/p. D non atteints Infection à bactérie plus résistante Apparition d’effets indésirables dose-dépendantes rendant compte d’un surdosage par insuffisances fonctionnelles d’élimination Interactions médicamenteuses attendues Chez tous les patients où une modification des paramètres pharmacocinétiques est fortement suspectée (réanimation, obèses, brûlés, …) A quel moment : dès les premières prises pour optimiser le plus tôt possible le traitement BUT : schémas posologiques individualisés

DOS AGE DES ANTIBIOTIQUES AUX HCL 60 Aminosides Glycopeptides Fluoroquinolones β-lactaminnes

AMINOSIDES 61 Dosage méthode immunologique réalisé en biochimie: Amikacine, Gentamicine, Tobramycine CBS, HEH, CBN Sang (tube sec) T 0 (taux résiduel) = avant la perfusion Tmax (taux pic) = 1/2 h après la fin de la perfusion 24 h/24, délai de rendu<3 h

GLYCOPEPTIDES 62 Dosage méthode immunologique réalisé en biochimie: Vancomycine: Sang (tube sec) CBS, HEH (+LCR), CBN T 0 (taux résiduel) = avant la perfusion Tmax (taux pic) = 1 h après la fin de la perfusion 24 h/24, délai de rendu <3 h Teicoplanine: Sang (tube sec) CBN T 0 (taux résiduel) = avant la perfusion Tmax (taux pic) = 15 à 30 minutes après la fin de la perfusion 24 h/24, délai de rendu maximum 1 jour

DOSAGE DES FLUOROQUINOLONES ET DES β-LACTAMINES 63 Au CHLS Molécules dosées : Fluoroquinolones : Levofloxacine, Moxifloxacine, Ofloxacine, Ciprofloxacine, (Norfloxacine, Pefloxacine) Β- lactamines : Ceftazidine, Ceftriaxone, Céfotaxime, Céfépime, Pipéracilline (Imipénème, Méropénème, Amoxicilline en cours de validation de méthode) 2 systèmes HPLC et 1 technicien spécialement dédiés au dosages de ces antibiotiques Capable de prendre en charge dès leur arrivée les prélèvements arrivant pendant les jours ouvrables Permet de tenir les objectifs de délai de résultats: Dans la journée pour les prélèvements arrivant avant 13 h Le lendemain matin pour les prélèvements arrivant après 13 h

HPLC Fluoroquinolones 64 Gamme d’étalonnage en 4 points, réalisée tous les lundis (valable pour une semaine) Passage de 2 contrôles (un niveau bas et un élevé) Extraction du prélèvement sur colonne (phase solide/liquide) Colonne et phase mobile d’HPLC spécifique Passage de l’échantillon pur et dilué Détection fluorimétrique Temps de réalisation de l’analyse : Environ 2 h car extraction longue Compatible pour un rendu dans la journée

HPLC béta-lactamines 65 Gamme d’étalonnage en 5 points, réalisée tous les lundis (valable pour une semaine) Passage de 2 contrôles (un niveau bas et un élevé) Extraction du prélèvement par simple précipitation de protéines 2 colonnes et 2 phases mobiles d’HPLC spécifiques : Une colonne et une phase mobile pour les céphalosporines Une colonne et une phase mobile pour la pipéracilline Passage de l’échantillon pur et dilué Détection UV + barette de diode Temps de réalisation de l’analyse : Plus court que les FQ : 1 h 30 car extraction rapide

Services demandeurs 66 Patients mucoviscidose ++ Service des grands brûlés de St Luc St Joseph ++ Réanimations : CHLS : réanimation Sud > réanimation Nord HEH : réanimation P et N ++ Croix-Rousse Service d’infectiologie de la Croix Rousse Tuberculose Infection osseuse Toutes les demandes de la région : Saint-Etienne, Vienne, Mâcon, …
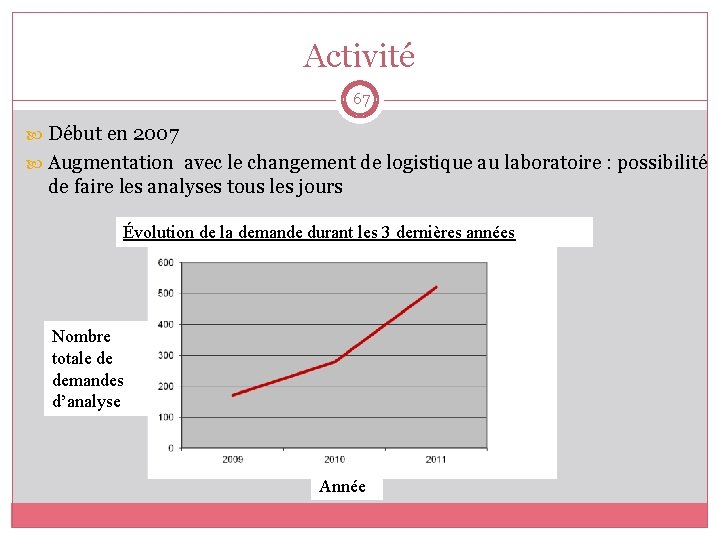
Activité 67 Début en 2007 Augmentation avec le changement de logistique au laboratoire : possibilité de faire les analyses tous les jours Évolution de la demande durant les 3 dernières années Nombre totale de demandes d’analyse Année
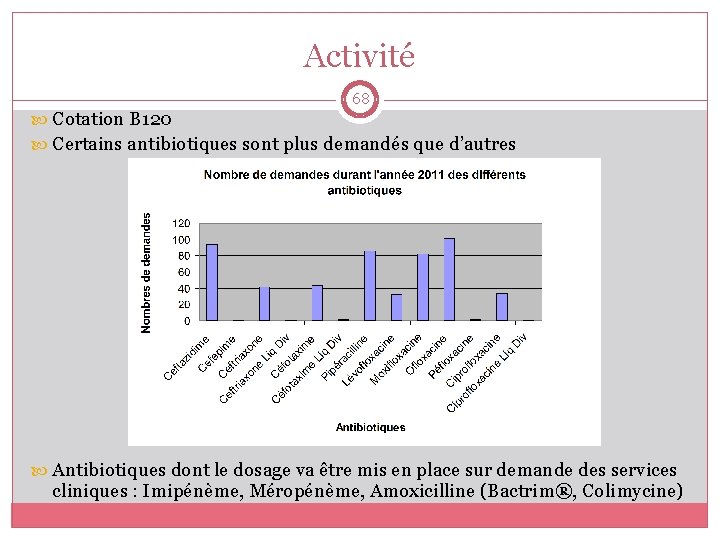
Activité 68 Cotation B 120 Certains antibiotiques sont plus demandés que d’autres Antibiotiques dont le dosage va être mis en place sur demande des services cliniques : Imipénème, Méropénème, Amoxicilline (Bactrim®, Colimycine)

Compte-rendu des résultats 69 Recommandations: Antibiotiques concentration-dépendant : taux pic Antibiotiques temps-dépendant : concentration résiduelle ou concentration à l’équilibre Quelques demandes de taux résiduels pour les FQ de la part des infectiologues de la Croix Rousse dans le cadre des tuberculoses résistantes ou d’infections osseuses. (Recher une toxicité? )

LIMITES DU CONCEPT p. K/p. D 70 Antibiogramme S, I, R réponse qualitative sur la sensibilité du germe : la CMI n’est pas effectuée dans tous les cas Prise en compte de la concentration critique inférieure c (CA-SFM) Mesure CMI quantitatif, mais : Explore un effet bactériostatique in vitro de l’antibiotique Or effet de l’antibiotique in vivo est bactéricide avec potentiellement un EPA et/ou un phénomène de tolérance non mesuré par la CMI Difficile de corréler les deux Explore seulement la sensibilité de la population majoritaire Nécessite un laboratoire de toxicologie de structure adaptée pour le dosage de certains antibiotiques (FQ, béta-lactamines)

CONCLUSION 71 Concept de pharmacodynamie des antibiotiques est un progrès dans la prise en charge des patients septiques sévères (efficacité, réduction de la morbi-mortalité). Son utilisation dans l’adaptation thérapeutique est une pratique en développement parce que leur dosage est devenu possible dans des délais compatibles. Aux HCL, son utilisation cible les patients sévères, de réanimation, grands brûlés, …mais est-ce suffisant? (patients en hématologie). Nécessaire pour que les «vieux» antibiotiques restent actifs (innovation dans le domaine des antibiotiques en perte de vitesse depuis une dizaine d’année).

Bibliographie 72 Livres: E. Pilly, maladies infectieuses et tropicales, 2010 F Jehl, M Chomarat, M Weber, A Gerard, De l’antibiogramme à la prescription, Editions Biomerieux 2004 Présentation: Cours DU infectiologie, M Tod, Relations p. K/p. D des antibiotiques, 2010 Cours DESC infectiologie, A Lefort, p. K-p. D, 2007 Publications: K. Hidayat, I. Hsu, R Quist, A. Shriner, MD; A Wong-Beringer, High-Dose Vancomycin Therapy for Methicillin-Resistant Staphylococcus aureus Infections Efficacy and Toxicity, AAC 2006 F Jehl, C Koebel, Antibiotiques-bactéries: une relation (pharmaco)dynamique, RFL, 2011 F Jehl, D Leveque, Perfusion continue des bêtalactamines: intérêts, inconvenients, modalités pratiques Réanimation 2009 F Jehl, La pharmacodynamie: un élément déterminant dans le choix d’un glycopeptide R. Garraffo Time-kill curves of Pseudomonas aeruginosa ATCC 27 27853 with exposures to tobramycin, ciprofloxacin and ticarcillin at 0. 25 to 64 -times MIC 1999 Mohr JF, Wanger A, Rex JH. Pharmacokinetic–pharmacodynamic modeling can help guide targeted antimicrobial therapy for nosocomial gramnegative infections in critically ill patients. Diagn Microbiol Infect Dis 2004 Garrafo R, Lavrut T. Signification clinique des corrélations pharmacocinétique–pharmacodynamie des antibiotiques chez les patients de réanimation. Réanimation 2005

Bibliographie 73 Publications: M. Gould, R. Cauda, S. Esposito, F. Gudiol, T. Mazzei, J. Garau, Management of serious meticillinresistant Staphylococcus aureus infections: what are limits? , IJAA, 2011 J Mouton, P Ambrose, R Canton, G Drusano, Conserving antibiotics for the future : New ways to use old and drugs from a pharmacokinetic and pharmacodynamic perspective, DRU, 2011 Owen R, Shorr A, Rational dosing of antimicrobial agents: Pharmacodynamic strategies, Am J Health, 2011 G Potel, J Caillon, C Jacqueline, D Navas, M-F Kergueris, E Batard, Dosage des antibiotiques en réanimation: quand et comment demander et interprêter les tests? , Reanimation, 2011 Dong Y et al. 1999. Antimicrob Agents and Chemother Benko AS, Cappelletty DM, Kruse JA, Rybak MJ. Continuous infusion versus intermittent administration of ceftazidime incritically ill patients with suspected Gram-negative infections. Antimicrob Agents Chemother 1996 Andes, AAC 2002 Rybak, Clin Infect Dis 2006 Infection expérimentale de souris ( SASM) efficacité de la vancomycine Lodise TP Jr, Graves J, Evans A et al. Relationship between vancomycin MIC and failure among patients with MRSA bacteremia treated with vancomycin. Antimicrob Agents Chemother 2008 M Wysocki, F Delatour, F Faurisson. , Continuous versus Intermittent Infusion of Vancomycin in Severe Staphylococcal Infections: Prospective Multicenter Randomized Study, AAC, 2001 Lodise TP Jr, B Lomaestro, L. Drusan, Piperacillin-Tazobactam for Pseudomonas aeruginosa infection: Clinical Implications of an Extended-Infusion Dosing Strategy, Clin Infect Dis 2007,

MERCI DE VOTRE ATTENTION! 74
- Slides: 74