La nomenclature Noms donns aux diffrents composes I


















- Slides: 19

La nomenclature (Noms donnés aux différents composées)

I. nomenclature des oxydes métalliques: Formule Général : MO(métal et oxygène). · Nomenclature: oxyde de M (M doit être remplacé par le nom du métal). · Exemple : Na 2 O = Oxyde de sodium Mg. O = Oxyde de magnésium

Nommes les oxydes métalliques suivants 1) Na 2 O 2) Ca. O 3) Al 2 O 3 4) Ba. O 5) Rb 2 O 6) Cs 2 O 7) Ga. O 2 8) Fe 2 O 3 9) Cu. O 10) Fe. O 11) Be. O 12) Zn. O 13) Cr 2 O 3 14) Hg. O

II. nomenclature des oxydes non-métalliques: · · Formule générale: N-MO (non-métal et oxygène). Nomenclature: oxyde de N-M (N-M doit être remplacé par le nom du non-métal). Le non-métal et l’oxygène devraient porter un préfixe représentant combien de chacun il y a. One – mono Two – di Three – tri Four – tetra Five – penta Six – hexa Seven – hepta Eight – octo Nine – nano Ten - deca

Exemple d’oxydes non-métalliques: CO 2 = dioxyde de carbone N 2 O 5 = pentoxyde de diazote P 4 O 10 = decaoxyde de tetraphosphore

Nommes les oxydes nonmétalliques suivants 1) P 2 O 5 2) SO 3) As 4 O 10 4) B 2 O 3 5) Si. O 2 6) H 2 O 7) CO 8) SO 2 9) H 2 O 2 10) Se. O 2

III. nomenclatures des hydroxydes: Formule générale: MOH · Nomenclature: Hydroxyde de M est le métal). · · Exemple : Li. OH : hydroxyde de lithium KOH : hydroxyde de potassium (M

Nommes les hydroxydes suivants: 1) Mg(OH)2 2) Na. OH 3) Cr(OH)3 4) Be(OH)2 5) Cs. OH 6) Al(OH)3 7) Ni(OH)2 8) Fe(OH)3 9) Zn(OH)2 10) Li. OH

IV. nomenclature des acides gazeux : n Formule générale : HX(g) · Nomenclature: X-ure d’hydrogène (le nom du non-métal avec la terminaison ure + d’hydrogène). · Exemple : HBr(g) = bromure d’hydrogène H 2 S = sulfure d’hydrogène

IV. nomenclature des acides en présence d’eau: n Formule générale : HX(aq) · Nomenclature: acide Hydro-X-ique (acide Hydro-nom du non-métal + -ique). · Exemple : HBr(aq) = acide bromhydrique H 2 S(aq) = acide sulfhydrique

Nommes les acides suivants: 1) HCl 2) HBr(aq) 3) H 2 S 4) HF(aq) 5) H 2 Se 6) H 3 P 7) H 2 Te(aq) 8) HCl(aq) 9) HBr 10) H 2 S

V. nomenclature des sels: Formule générale: MX (ou M est le métal et X le non-métal). · Nomenclature : X-ure de Métal Exemple : Na. Cl = chlorure de sodium Rb 2 S = sulfure de rubidium

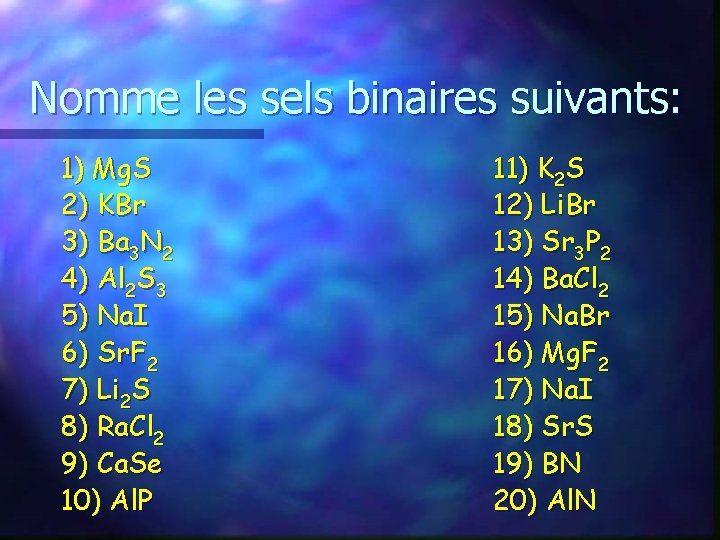
Nomme les sels binaires suivants: 1) Mg. S 2) KBr 3) Ba 3 N 2 4) Al 2 S 3 5) Na. I 6) Sr. F 2 7) Li 2 S 8) Ra. Cl 2 9) Ca. Se 10) Al. P 11) K 2 S 12) Li. Br 13) Sr 3 P 2 14) Ba. Cl 2 15) Na. Br 16) Mg. F 2 17) Na. I 18) Sr. S 19) BN 20) Al. N

Exercices de Nomenclature Nommes les composées suivants: n n n n n a. b. c. d. e. f. g. h. i. Na. Cl Sc(OH)3 Cs. F Al. I 3 HI(aq) Mg(OH)2 H 2 Se HI K 2 O

Nomenclature des sels ternaire Formule générale: MXO Nomenclature: nom de l’ion polyatomique(XO)+ M. Exemple : KCl. O 3 = chlorate de potassium Mg. SO 4 = sulfate de magnésium (NH 4)2 S = sulfure d’ammonium Ca. NO 3 = carbonate de calcium

Nommes les sels tertiaires suivants: 1) Na 2 SO 4 2) Na. Cl. O 3 3) Zn(NO 3)2 4) Cs 3 PO 4 5) Be(Cl. O 3)2 6) Fe 2(SO 4)3 7) Ba. CO 3 8) Ti. PO 4 9) K 2 CO 3 10) Al 2(SO 4)3

Nomenclature des acides ternaire Formule générale: HXO Nomenclature: nom de l’ion polyatomique(XO)+ Hydrogène. Exemple : HCl. O 3: chlorate d'hydrogène H 2 SO 4: sulfate d'hydrogène

Nomenclature des acides ternaire Formule générale: HXO(aq) Nomenclature: acide + nom de l’ion polyatomique(XO)-ique. Exemple : H 2 CO 3(aq): acide carbonique H 2 SO 4(aq): acide sulfurique HNO 3(aq): acide nitrique

Exercices de Nomenclature Nommes les composées suivants: n n n n n a. b. c. d. e. f. g. h. i. Na. Cl Sc(OH)3 Cs. F Al. I 3 HI(aq) CO K 2 CO 3 HI K 2 O j. k. l. m. n. o. p. q. r. Si. F 4 H 2 Se H 2 Te(aq) NH 4 OH Ba 3(PO 4)2 (NH 4)2 S Na 2 SO 4 Ca(Cl. O 3)2 N 2 O 5