La molecola di C 02 Il carbonio ha

La molecola di C 02 Il carbonio ha 6 elettroni di cui 4 sono nel secondo livello e sono spaiati. Il carbonio quindi può formare 4 legami L’ossigeno ha 8 elettroni di cui 6 nel secondo livello e quindi due spaiati. L’ossigeno può formare due legami. Il carbonio e l’ossigeno insieme formano dunque una molecola triatomica dove il carbonio è al centro e lega i due ossigeni con due doppi legami. Ogni atomo raggiunge così l’ottetto
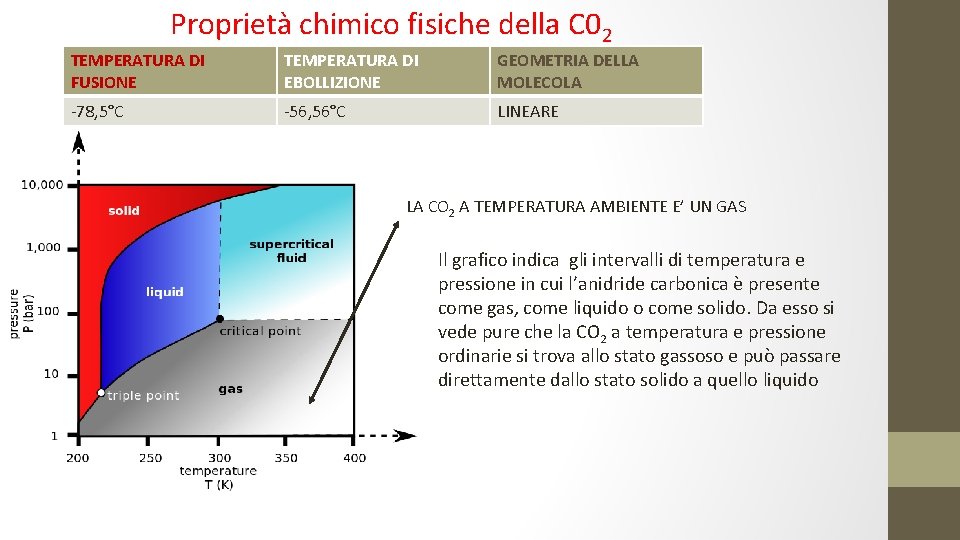
Proprietà chimico fisiche della C 02 TEMPERATURA DI FUSIONE TEMPERATURA DI EBOLLIZIONE GEOMETRIA DELLA MOLECOLA -78, 5°C -56, 56°C LINEARE LA CO 2 A TEMPERATURA AMBIENTE E’ UN GAS Il grafico indica gli intervalli di temperatura e pressione in cui l’anidride carbonica è presente come gas, come liquido o come solido. Da esso si vede pure che la CO 2 a temperatura e pressione ordinarie si trova allo stato gassoso e può passare direttamente dallo stato solido a quello liquido
Produzione di CO 2 RESPIRAZIONE La respirazione produce CO 2 COMBUSTIONE La combustione è una reazione chimica che comporta l'ossidazione di un combustibile da parte di un comburente (che in genere è rappresentato dall'ossigeno presente nell'aria), con sviluppo di calore e radiazioni elettromagnetiche, tra cui spesso anche radiazioni luminose

Combustione Combustibile Comburente La combustione è una reazione chimica che comporta l'ossidazione di un combustibile da parte di un comburente Un combustibile è una sostanza chimica che viene ossidata nel processo di combustione, Un comburente è una sostanza che agisce come agente ossidante Combustione parziale La combustione parziale e quella che avviene in un difetto di ossigeno e porta alla produzione di monossido di carbonio invece di anidride carbonica 2 C+O 2 2 CO

Monossido di carbonio Il monossido di carbonio non esiste libero in natura in quanto, pur avendo una molecola molto stabile, reagisce in presenza di O 2, formando CO 2; viene prodotto da reazioni di combustione in difetto di aria. Si miscela bene nell'aria, con la quale forma facilmente miscele esplosive e penetra facilmente attraverso le pareti e il soffitto. Combustione totale 2 C +O 2 2 CO + O 2 2 CO 2 2 C+2 O 2 2 CO 2

Avvelenamento da monossido di carbonio Il monossido di carbonio (o ossido di carbonio o ossido carbonico) ha formula CO, è un gas velenoso particolarmente insidioso in quanto inodore, incolore e insapore. La sua molecola è costituita da un atomo di ossigeno e un atomo di carbonio legati con un triplo legame (costituito da due legami covalenti e un legame dativo). Il monossido di carbonio non esiste libero in natura in quanto, pur avendo una molecola molto stabile, reagisce in presenza di O 2, formando CO 2; viene prodotto da reazioni di combustione in difetto di aria.

• • MAL DI TESTA DIFFICOLTA’ DI CONCENTRAZIONE ASTENIA SONNOLENZA

Facciamo qualche calcolo Calcolo del volume di CO 2 prodotto da 15 allievi che rimangono nella nostra aula per 6 ore a porte chiuse: Volume aula=6 m x 4 m x 2, 75=66 m 3 Volume CO 2 prodotto= 6 h x 0, 020 m 3/ore e persone x 15 persone= 1, 8 m 3 Percentuale di CO 2 prodotta = 1, 8/60 x 100= 3% Considerato che l’ 1% è il valore limite accettabile di anidride carbonica, il 3 % risulta eccesivo e quindi bisogna effettuare un ricambio d’aria efficace.

Come ridurre l’anidride carbonica Inserendo delle piante in aula Aprendo le finestre

La Fotosintesi Le piante con la fotosintesi si trasformano la CO 2 in O 2: 6 CO 2 + 6 H 2 O C 6 H 12 O 6 + 6 O 2

Utilizzo del rivelatore di anidride carbonica L’utilizzo del rivelatore di anidride carbonica può permettere di stabilire le condizioni migliori per un efficace ricambio di aria capace di determinare una tollerabile concentrazione di anidride carbonica.

Funzionamento del rilevatore di anidride carbonica Il rivelatore serve ad indicare quanta anidride carbonica è presente nell’aula. Se supera l’ 1% inizia ad emettere un suono, il suono ti indica che devono essere aperte le finestre per il ricambio dell’aria

Simone D’inverno 2 C grafica
- Slides: 13