La mente es como un paracadas trabaja slo

“La mente es como un paracaídas: trabaja sólo cuando está abierta” nimo ESTRUCTURAS DE LEWIS Presentado por Víctor Barrios
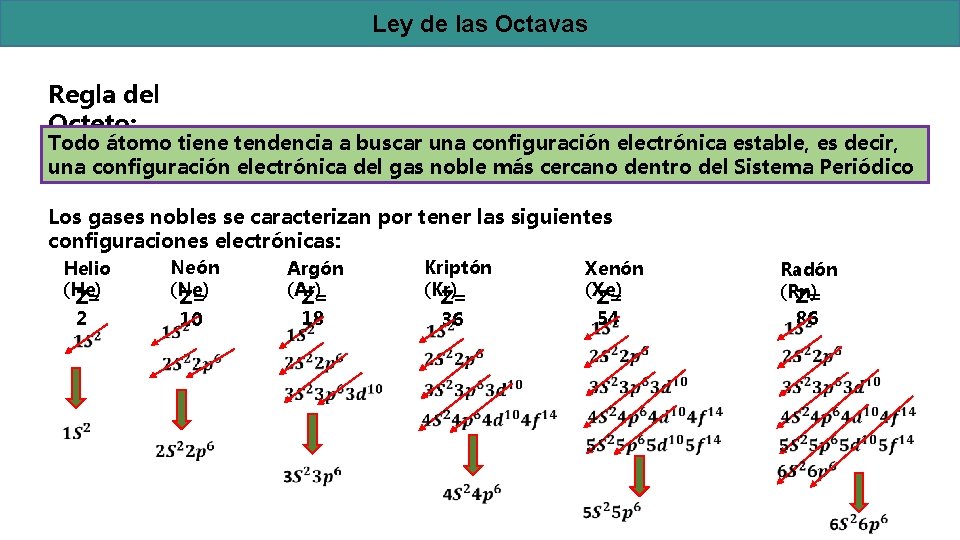
Ley de las Octavas Regla del Octeto: Todo átomo tiene tendencia a buscar una configuración electrónica estable, es decir, una configuración electrónica del gas noble más cercano dentro del Sistema Periódico Los gases nobles se caracterizan por tener las siguientes configuraciones electrónicas: Helio (He) Z= 2 Neón (Ne) Z= 10 Argón (Ar) Z= 18 Kriptón (Kr) Z= 36 Xenón (Xe) Z= 54 Radón (Rn) Z= 86
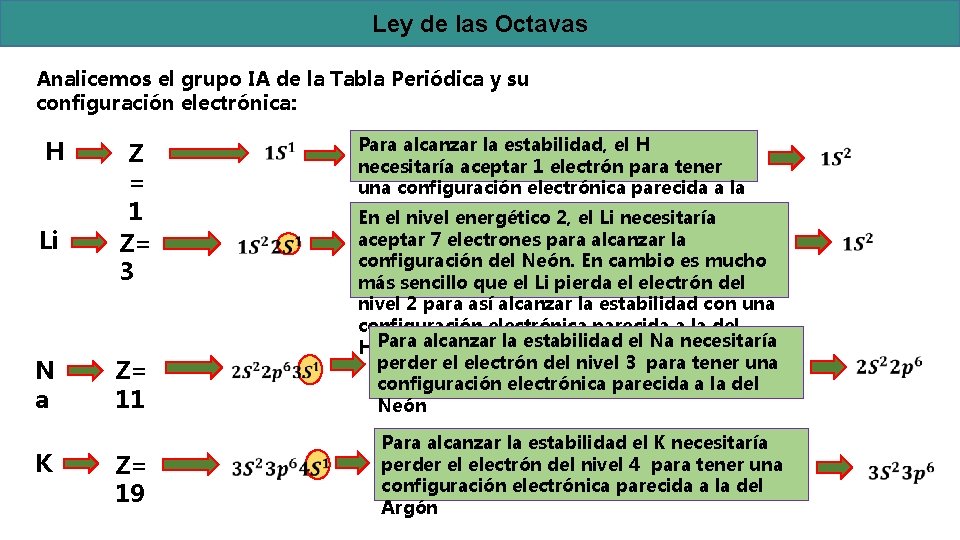
Ley de las Octavas Analicemos el grupo IA de la Tabla Periódica y su configuración electrónica: H Li N a K Z = 1 Z= 3 Z= 11 Z= 19 Para alcanzar la estabilidad, el H necesitaría aceptar 1 electrón para tener una configuración electrónica parecida a la del Helio En el nivel energético 2, el Li necesitaría aceptar 7 electrones para alcanzar la configuración del Neón. En cambio es mucho más sencillo que el Li pierda el electrón del nivel 2 para así alcanzar la estabilidad con una configuración electrónica parecida a la del Para alcanzar la estabilidad el Na necesitaría Helio perder el electrón del nivel 3 para tener una configuración electrónica parecida a la del Neón Para alcanzar la estabilidad el K necesitaría perder el electrón del nivel 4 para tener una configuración electrónica parecida a la del Argón

Enlace Químico Es la fuerza de unión que existe entre dos átomos, cualquiera que sea su naturaleza, debida a la transferencia total o parcial de electrones para adquirir ambos la configuración electrónica estable correspondiente los esfera gasesde En la figura adjuntaa cada nobles diferente color representa diferentes tipos de átomos y cada bracito representa el enlace En la formación de enlaces químicos sólo participan los electrones de valencia
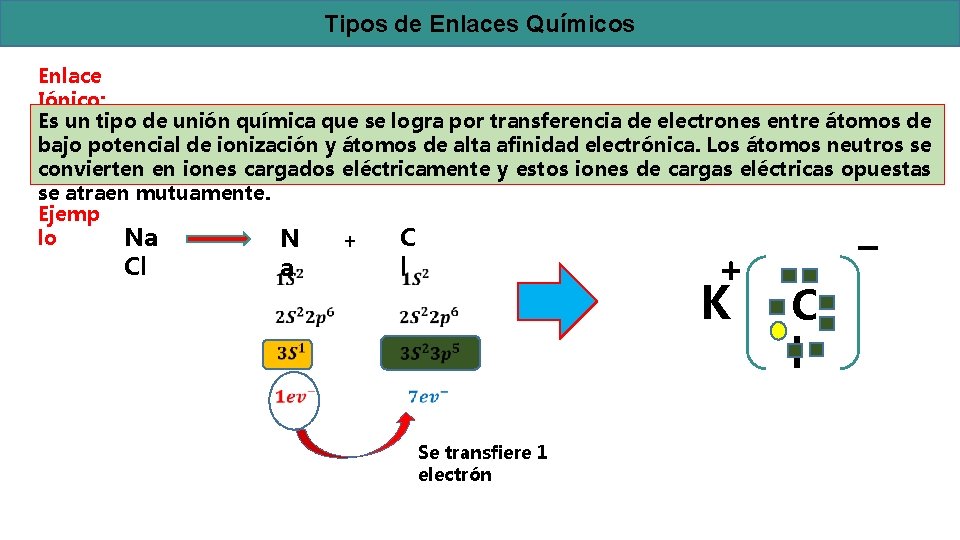
Tipos de Enlaces Químicos Enlace Iónico: Es un tipo de unión química que se logra por transferencia de electrones entre átomos de bajo potencial de ionización y átomos de alta afinidad electrónica. Los átomos neutros se convierten en iones cargados eléctricamente y estos iones de cargas eléctricas opuestas se atraen mutuamente. Ejemp lo C Na N + Cl a + l K Se transfiere 1 electrón C l
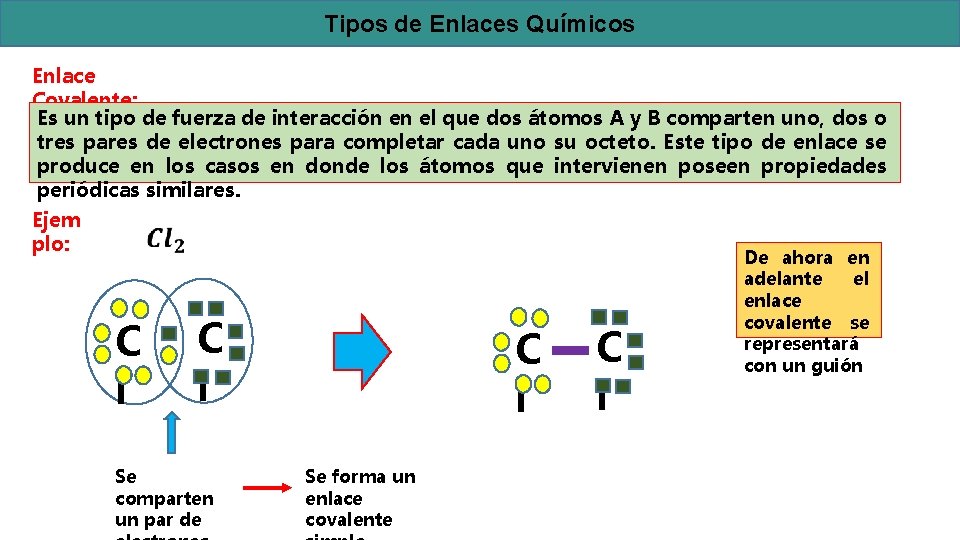
Tipos de Enlaces Químicos Enlace Covalente: Es un tipo de fuerza de interacción en el que dos átomos A y B comparten uno, dos o tres pares de electrones para completar cada uno su octeto. Este tipo de enlace se produce en los casos en donde los átomos que intervienen poseen propiedades periódicas similares. Ejem plo: C l Se comparten un par de C l Se forma un enlace covalente C l De ahora en adelante el enlace covalente se representará con un guión
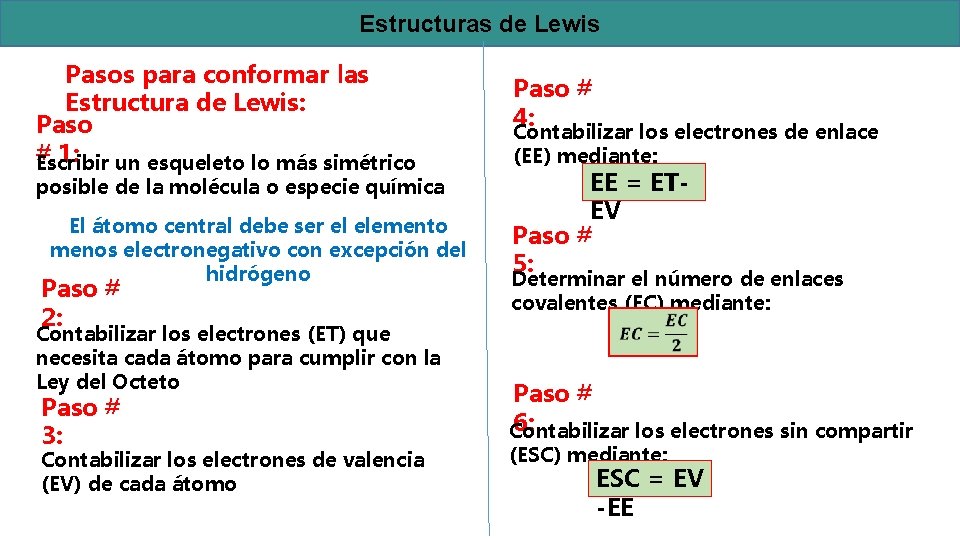
Estructuras de Lewis Pasos para conformar las Estructura de Lewis: Paso # 1: un esqueleto lo más simétrico Escribir posible de la molécula o especie química El átomo central debe ser el elemento menos electronegativo con excepción del hidrógeno Paso # 2: Contabilizar los electrones (ET) que necesita cada átomo para cumplir con la Ley del Octeto Paso # 3: Contabilizar los electrones de valencia (EV) de cada átomo Paso # 4: Contabilizar los electrones de enlace (EE) mediante: EE = ETEV Paso # 5: Determinar el número de enlaces covalentes (EC) mediante: Paso # 6: Contabilizar los electrones sin compartir (ESC) mediante: ESC = EV -EE
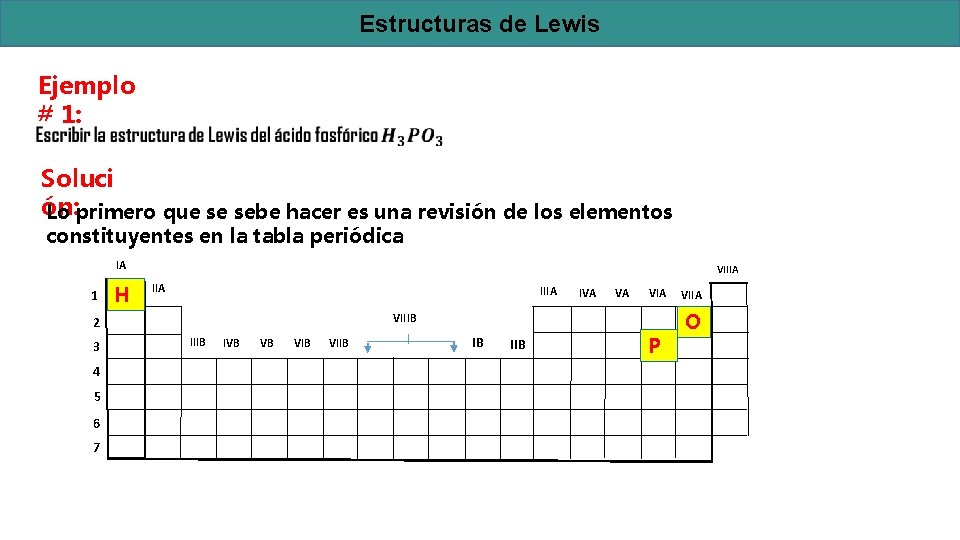
Estructuras de Lewis Ejemplo # 1: Soluci ón: Lo primero que se sebe hacer es una revisión de los elementos constituyentes en la tabla periódica IA 1 H VIIIA 4 5 6 7 VA VIIIB 2 3 IVA IIIB IVB VB VIIB IB IIB P VIIA O

Estructuras de Lewis De la inspección de la tabla periódica se concluye que: ü Existen 3 átomos de Hidrógenos (H) que necesitan 2 electrones de valencia cada uno para tener la configuración electrónica del Helio (He), es decir para cumplir con la Ley del Octeto ü Existe 1 átomo de Fósforo (P) que necesita 8 electrones de valencia para tener la configuración electrónica del Argón (Ar), es decir para cumplir con la Ley del Octeto ü Existen 4 átomos de Oxígeno (O) que necesitan 8 electrones de valencia para tener la configuración electrónica del Neón (Ne), es decir para cumplir con la Ley del Octeto ü El Hidrógeno (H) pertenece al grupo IA de la tabla periódica, por lo tanto posee 1 electrón de valencia ü El Fósforo (P) pertenece al grupo VA de la tabla periódica, por lo tanto posee 5 electrones de valencia ü El Oxígeno (O) pertenece al grupo VIA de la tabla periódica, por lo tanto posee 6 electrones de valencia ü Aparte del Hidrógeno, el Fósforo (P) es el elemento menos electronegativo de la molécula
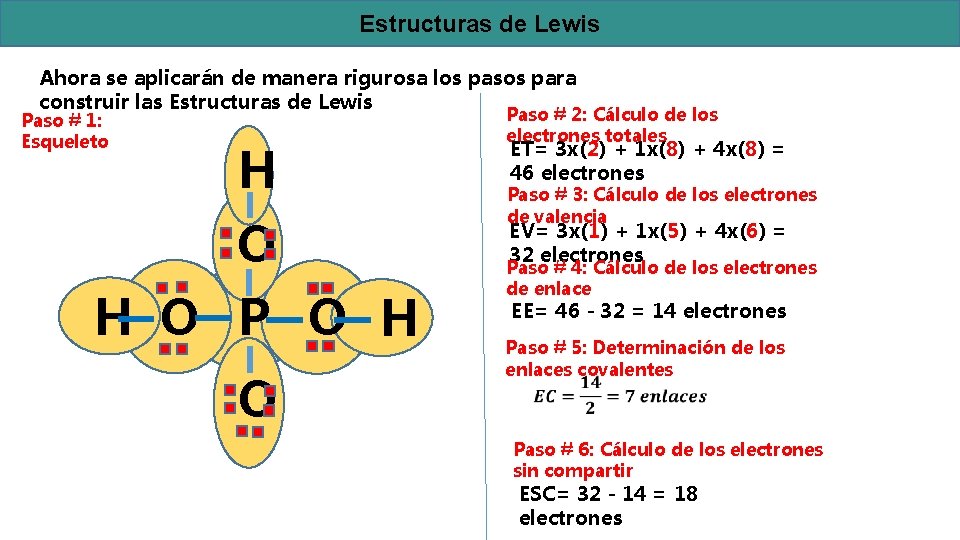
Estructuras de Lewis Ahora se aplicarán de manera rigurosa los pasos para construir las Estructuras de Lewis Paso # 1: Esqueleto H O P O H O Paso # 2: Cálculo de los electrones totales ET= 3 x(2) + 1 x(8) + 4 x(8) = 46 electrones Paso # 3: Cálculo de los electrones de valencia EV= 3 x(1) + 1 x(5) + 4 x(6) = 32 electrones Paso # 4: Cálculo de los electrones de enlace EE= 46 - 32 = 14 electrones Paso # 5: Determinación de los enlaces covalentes Paso # 6: Cálculo de los electrones sin compartir ESC= 32 - 14 = 18 electrones
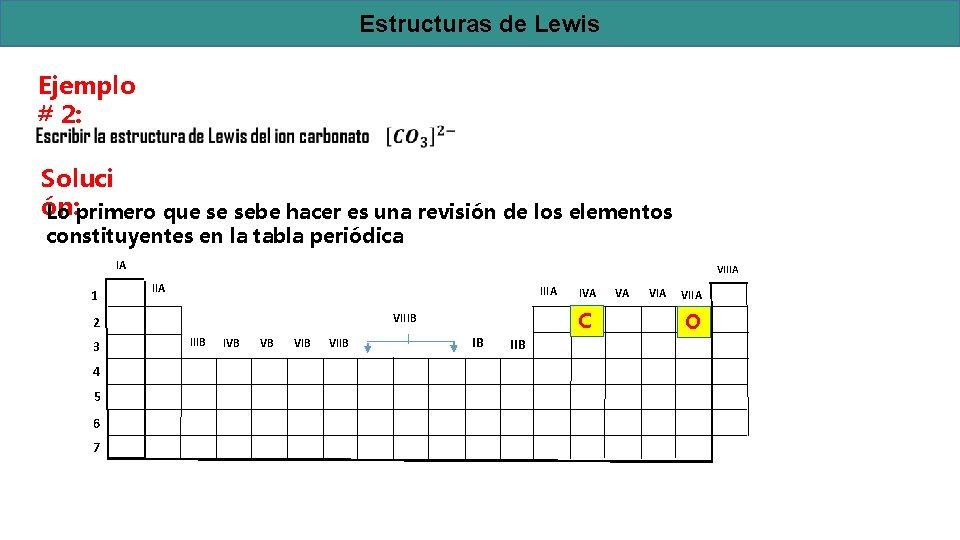
Estructuras de Lewis Ejemplo # 2: Soluci ón: Lo primero que se sebe hacer es una revisión de los elementos constituyentes en la tabla periódica IA 1 VIIIA 3 4 5 6 7 C VIIIB 2 IIIB IVB VB VIIB IVA IB IIB VA VIIA O

Estructuras de Lewis De la inspección de la tabla periódica se concluye que: ü Existen 3 átomos de Oxígeno (O) que necesitan 8 electrones de valencia cada uno para tener la configuración electrónica del Neón (Ne), es decir para cumplir con la Ley del Octeto ü Existe 1 átomo de Carbono (C) que necesita 8 electrones de valencia para tener la configuración electrónica del Neón (Ne), es decir para cumplir con la Ley del Octeto ü El Carbono (C) pertenece al grupo IVA de la tabla periódica, por lo tanto posee 4 electrones de valencia ü El Oxígeno (O) pertenece al grupo VIA de la tabla periódica, por lo tanto posee 6 electrones de valencia ü El Carbono (C) es el elemento menos electronegativo de la molécula ü El ion carbonato tiene carga negativa (-2) y eso significa que posee 2 electrones de valencia adicionales
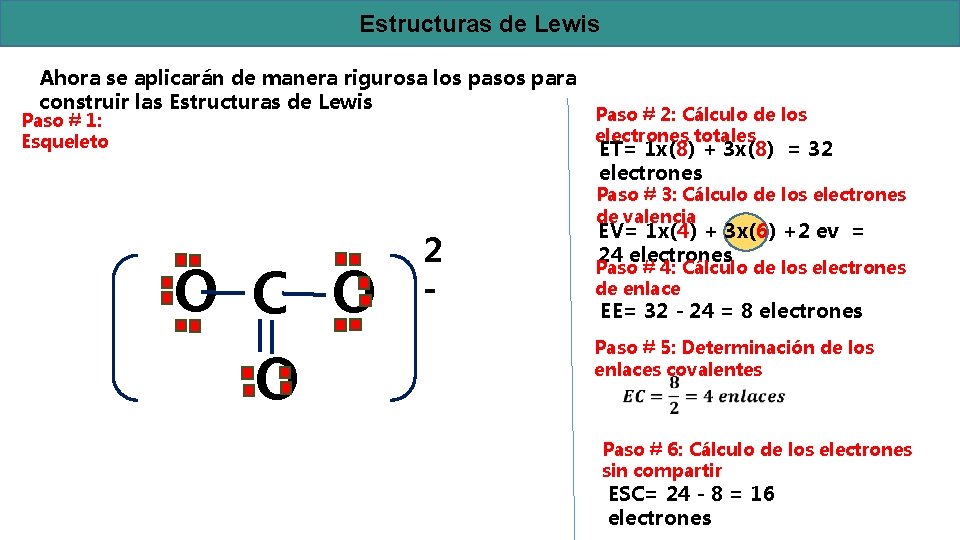
Estructuras de Lewis Ahora se aplicarán de manera rigurosa los pasos para construir las Estructuras de Lewis Paso # 1: Esqueleto Paso # 2: Cálculo de los electrones totales ET= 1 x(8) + 3 x(8) = 32 electrones Paso # 3: Cálculo de los electrones de valencia O C O O 2 - EV= 1 x(4) + 3 x(6) +2 ev = 24 electrones Paso # 4: Cálculo de los electrones de enlace EE= 32 - 24 = 8 electrones Paso # 5: Determinación de los enlaces covalentes Paso # 6: Cálculo de los electrones sin compartir ESC= 24 - 8 = 16 electrones
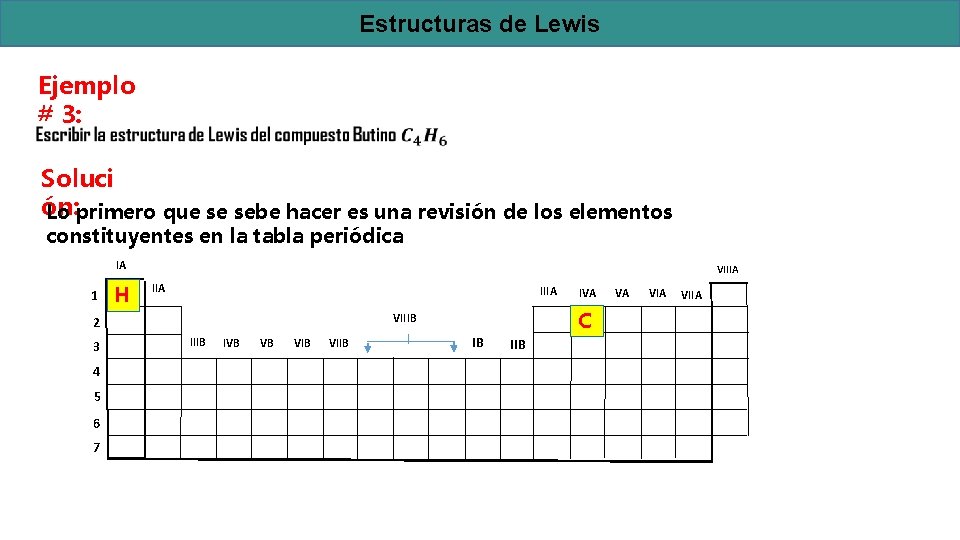
Estructuras de Lewis Ejemplo # 3: Soluci ón: Lo primero que se sebe hacer es una revisión de los elementos constituyentes en la tabla periódica IA 1 H VIIIA 3 4 5 6 7 C VIIIB 2 IIIB IVB VB VIIB IVA IB IIB VA VIIA

Estructuras de Lewis De la inspección de la tabla periódica se concluye que: ü Existen 4 átomos de Carbono (C) que necesitan 8 electrones de valencia cada uno para tener la configuración electrónica del Neón (Ne), es decir para cumplir con la Ley del Octeto ü Existen 6 átomos de Hidrógenos (H) que necesitan 2 electrones de valencia cada uno para tener la configuración electrónica del Helio (He), es decir para cumplir con la Ley del Octeto ü El Carbono (C) pertenece al grupo IVA de la tabla periódica, por lo tanto posee 4 electrones de valencia ü El Hidrógeno (H) pertenece al grupo IA de la tabla periódica, por lo tanto posee 1 electrones de valencia ü A excepción del hidrógeno, el Carbono (C) es el elemento menos electronegativo de la molécula

Estructuras de Lewis Ahora se aplicarán de manera rigurosa los pasos para construir las Estructuras de Lewis Paso # 1: Esqueleto H H H C C H H H Paso # 2: Cálculo de los electrones totales ET= 4 x(8) + 6 x(2) = 44 electrones Paso # 3: Cálculo de los electrones de valencia EV= 4 x(4) + 6 x(1) = 22 electrones Paso # 4: Cálculo de los electrones de enlace EE= 44 - 22 = 22 electrones Paso # 5: Determinación de los enlaces covalentes Paso # 6: Cálculo de los electrones sin compartir ESC= 22 - 22 = 0 electrones
- Slides: 16