La materia e tutto cio che possiede massa













- Slides: 16

La materia e’ tutto cio’ che possiede massa ed occupa spazio

Teoria atomica della materia • La materia e’ costituita da atomi • Gli atomi di un elemento sono diversi da quelli di un altro elemento • Gli atomi si combinano secondo rapporti definiti per formare composti • La combinazione degli atomi in un composto puo’ cambiare solo quando avviene una reazione chimica • Una reazione chimica cambia il rapporto con cui gli atomi si combinano, ma non altera la natura degli atomi

Atomi Gli atomi sono costituiti da particelle subatomiche dette elettroni, protoni e neutroni. Protoni e neutroni formano un minuscolo, denso corpo centrale detto nucleo dell’atomo. Gli elettroni si trovano distribuiti nello spazio intorno al nucleo.

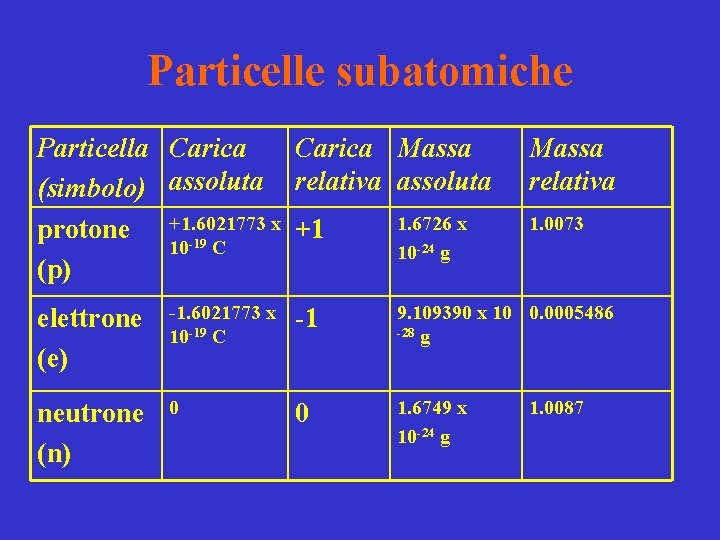
Particelle subatomiche Particella Carica Massa (simbolo) assoluta relativa assoluta x +1 1. 6726 x protone +1. 6021773 10 -19 C 10 -24 g (p) Massa relativa 1. 0073 elettrone (e) -1. 6021773 x 10 -19 C -1 9. 109390 x 10 0. 0005486 -28 g neutrone (n) 0 0 1. 6749 x 10 -24 g 1. 0087

Struttura dell’atomo • Gli atomi sono costituiti da un nucleo positivo e da elettroni negativi. • Il nucleo ha un raggio di 10 -5 Å. • Il raggio di un atomo è dell'ordine di 1 Å.

Ångstrom simbolo Å 1 Ångstrom corrisponde a -10 10 m Molto usato in chimica perché è dell’ordine di grandezza di un atomo

Nuclidi A Z X Un nuclide è un atomo caratterizzato dal numero atomico Z (numero di elettroni) e dal numero di massa A (numero di neutroni e di protoni). Il nuclide neutro ha un numero di elettroni uguale a quello di protoni. Il numero Z caratterizza la specie atomica. 1 H 1 12 C 6 16 O 8

Isotopi Nuclidi con lo stesso Z ma differente A possono esistere e si chiamano isotopi. Una stessa specie atomica ha, di norma, diversi isotopi: si parla di miscela isotopica naturale. Le specie atomiche sono 106, di cui 90 naturali; di queste, 81 hanno almeno un nuclide stabile. 12 C 6 13 C 6 14 C 6

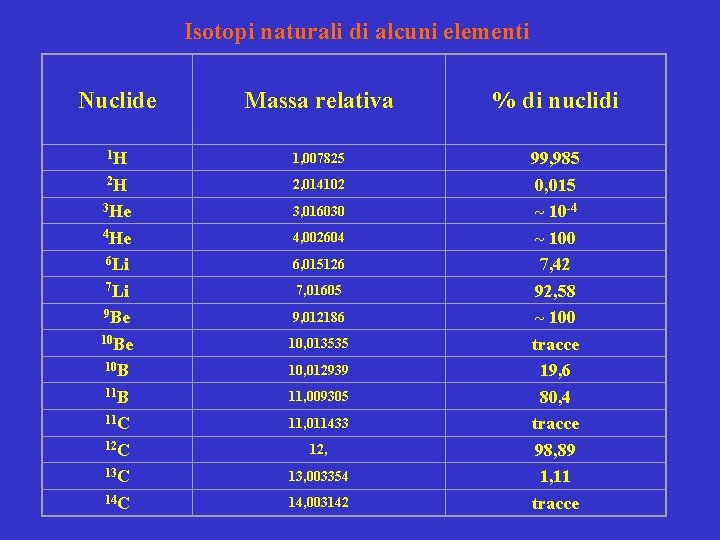
Isotopi naturali di alcuni elementi Nuclide Massa relativa % di nuclidi 1 H 1, 007825 2 H 2, 014102 3 He 3, 016030 4 He 4, 002604 6 Li 6, 015126 7 Li 7, 01605 9 Be 9, 012186 10 Be 10, 013535 10 B 10, 012939 11 B 11, 009305 11 C 11, 011433 12 C 12, 13 C 13, 003354 14 C 14, 003142 99, 985 0, 015 ~ 10 -4 ~ 100 7, 42 92, 58 ~ 100 tracce 19, 6 80, 4 tracce 98, 89 1, 11 tracce

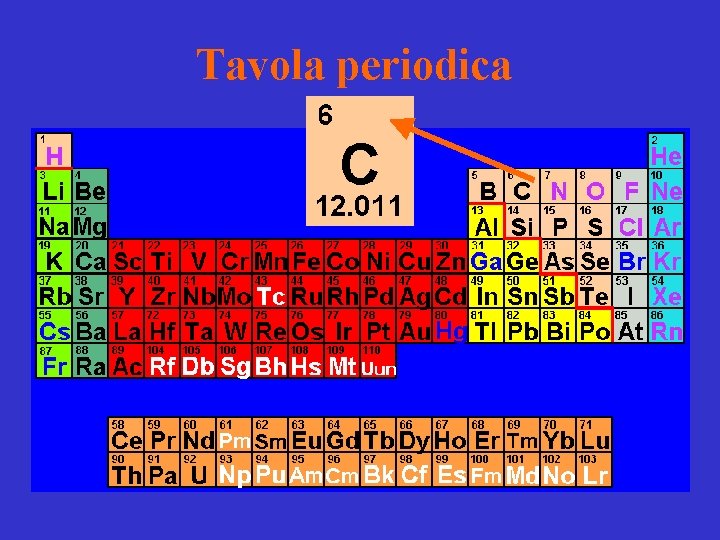
Tavola periodica

Ioni Un elemento e’ caratterizato dal suo numero atomico. Nell’atomo neutro il numero di elettroni e’ uguale a quello di protoni. Atomi che hanno ceduto o aquistato elettroni rispetto all’atomo neutro si dicono ioni: Catione + Anione -

Sostanze elementari Sono costituite da atomi della stessa specie (stesso numero atomico). Possono essere formate da: • Singoli atomi • Molecole = aggregati discreti di atomi • Insieme continuo di atomi

Composti Sono costituiti da atomi di specie diverse. Possono essere formati da: • Molecole • Concatenazioni di atomi • Ioni

Gli atomi si combinano secondo rapporti definiti per formare composti Formula chimica: deve indicare come minimo quali sono gli elementi che costituiscono la sostanza e in quale rapporto gli atomi di questi elementi si trovano. H 2 O CO 2 CO Formula minima o molecolare

Reazione chimica • La combinazione degli atomi in un composto puo’ cambiare solo quando avviene una reazione chimica • Una reazione chimica cambia il rapporto con cui gli atomi si combinano, ma non altera la natura degli atomi C + O 2 CO 2

Equazione chimica reagenti a. A + b. B c. C + d. D prodotti Conservazione della massa: la massa totale dei reagenti e dei prodotti non varia durante la reazione. Si deve avere lo stesso numero di atomi per ogni elemento, anche se in composti differenti, in ambedue i membri dell’equazione.