La liaison aux protines plasmatiques Alain BousquetMlou Fvrier

La liaison aux protéines plasmatiques Alain Bousquet-Mélou Février 2015

Importance de la liaison aux protéines plasmatiques n LOCALISATION VASCULAIRE n IMPORTANCE DE LA CONCENTRATION LIBRE ¨ Subit les processus pharmacocinétiques ¨ Responsable des actions pharmacodynamiques
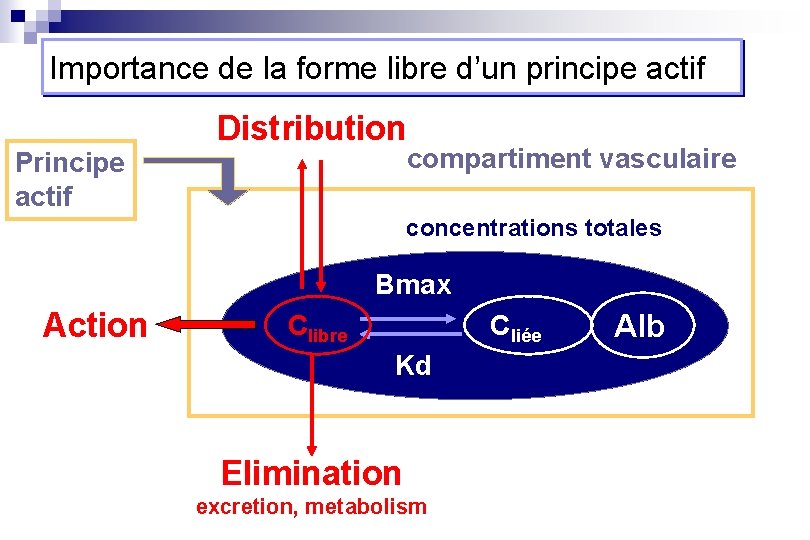
Importance de la forme libre d’un principe actif Principe actif Distribution compartiment vasculaire concentrations totales Bmax Action Clibre Cliée Kd Elimination excretion, metabolism Alb
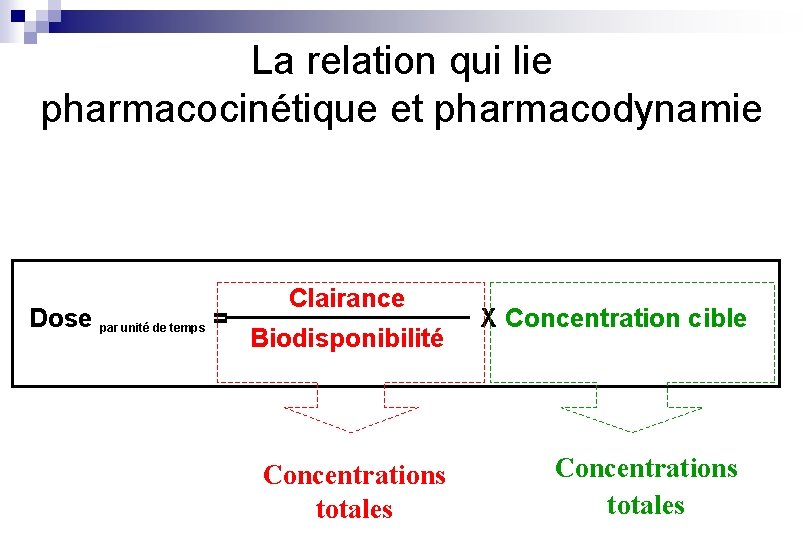
La relation qui lie pharmacocinétique et pharmacodynamie Dose par unité de temps = Clairance Biodisponibilité Concentrations totales X Concentration cible Concentrations totales

La fraction libre : fu (unbound fraction) • Definition:
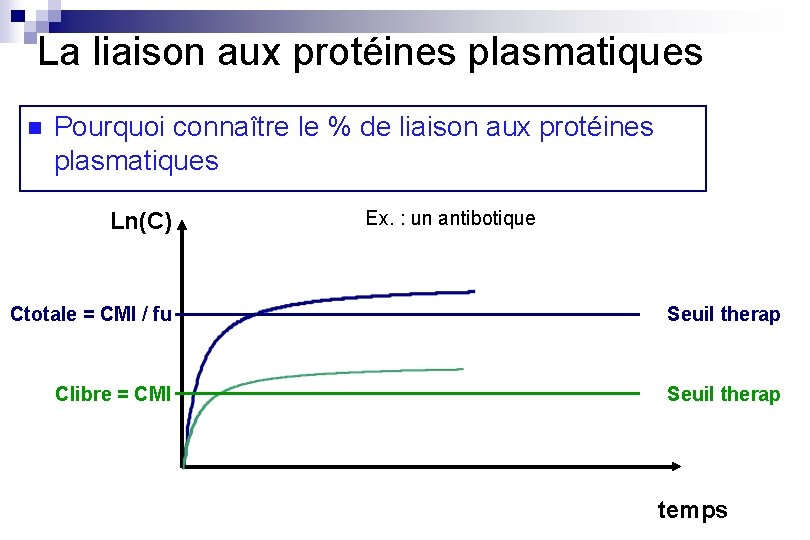
La liaison aux protéines plasmatiques n Pourquoi connaître le % de liaison aux protéines plasmatiques Ln(C) Ex. : un antibotique Ctotale = CMI / fu Seuil therap Clibre = CMI Seuil therap temps

La liaison aux protéines plasmatiques n Pourquoi connaître le % de liaison aux protéines plasmatiques ¨ Pour passer des concentrations libres efficaces déterminées in vitro au concentrations totales cibles correspondantes in vivo ¨ Pour comparer des gammes espèces de concentrations cibles entre

La liaison aux protéines plasmatiques méthodes d’étude n PRINCIPE ¨ Mesure des concentrations libres et liées n TECHNIQUES DE SEPARATION ¨ Dialyse à l’équilibre, ultrafiltration ¨ Ultracentrifugation n PARAMETRE ¨ La fraction libre fu = C libre C totale

La liaison aux protéines plasmatiques Les protéines impliquées n
La liaison aux protéines plasmatiques n Les modalités de fixation
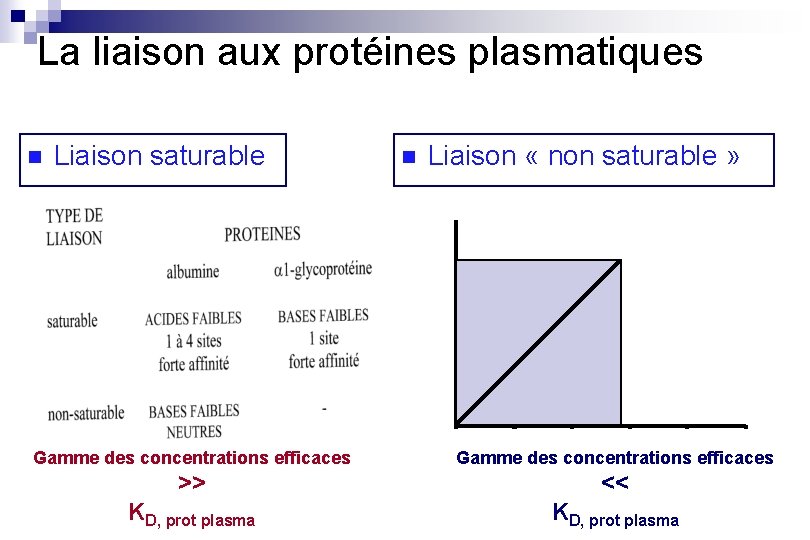
La liaison aux protéines plasmatiques n Liaison saturable n Liaison « non saturable » Gamme des concentrations efficaces >> << KD, prot plasma
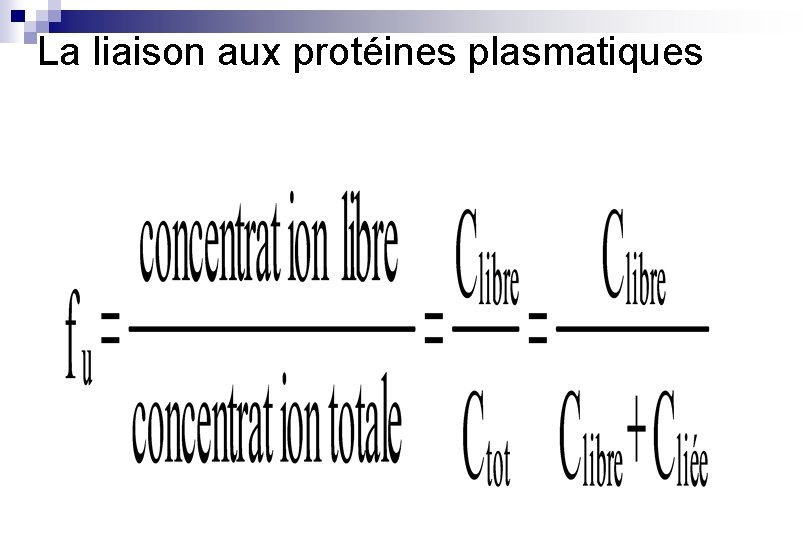
La liaison aux protéines plasmatiques

Quels sont les facteurs déterminants de la fraction libre ?

La fraction libre : fu (unbound fraction) • Definition:

La fraction libre : fu (unbound fraction) • La concentration liée Cliée Bmax/2 KD Clibre Bmax : - concentration maximale de sites - proportionnelle à la concentration de protéines de liaison KD : - concentration liant la moitié des site de liaison - inversement proportionnel à l’affinité pour la protéine
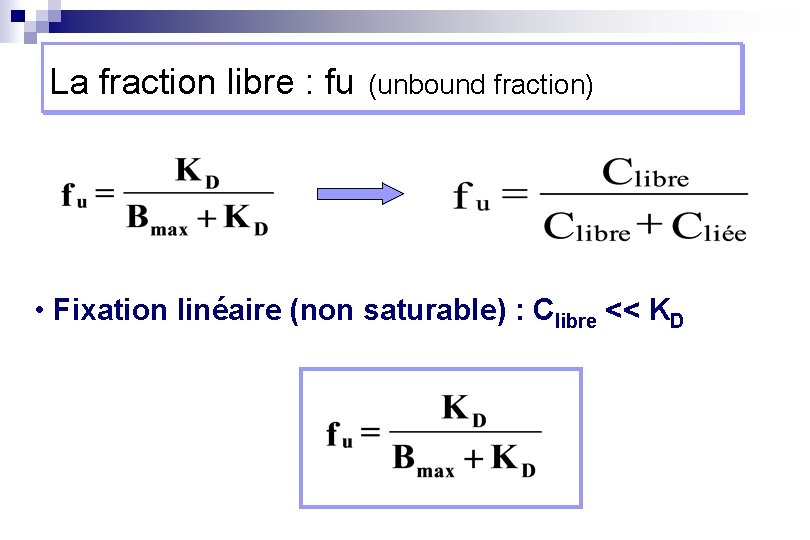
La fraction libre : fu (unbound fraction) • Fixation linéaire (non saturable) : Clibre << KD
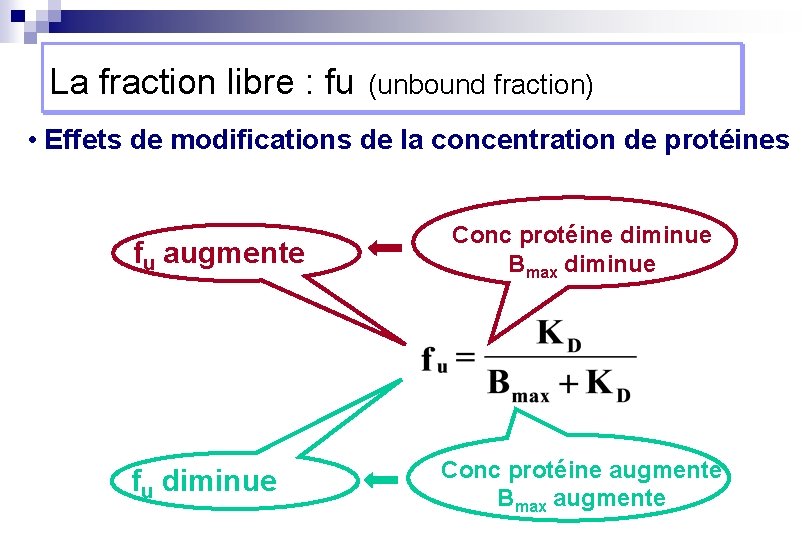
La fraction libre : fu (unbound fraction) • Effets de modifications de la concentration de protéines fu augmente fu diminue Conc protéine diminue Bmax diminue Conc protéine augmente Bmax augmente

La fraction libre : fu (unbound fraction) • Effets d’un déplacement par compétition La concentration libre requise pour occuper la moitié des sites de liaison est augmentée déplacement par compét. KD augmente fu augmente

Variations de la fraction libre n Variations de Bmax : nombre de sites de liaison ¨ Albumine ¨ a 1 -glycoprotéine acide Insuffisance rénale chronique Insuffisance hépatique Foetus, nouveau-né Inflammation Gestation
Variations de la fraction libre

Variations de la fraction libre n Variations de Bmax : nombre de sites de liaison ¨ Albumine ¨ a 1 -glycoprotéine acide n Insuffisance rénale chronique Insuffisance hépatique Foetus, nouveau-né Inflammation Gestation Variations de KD : affinité de la liaison ¨ Phénomène de compétition ¨ Albumine foetale Produits endogènes : urée, AGV Médicaments

Variations de la fraction libre fu = Clibre Ctotale fu = KD KD + Bmax n Des modifications au niveau des capacités de liaison (Bmax) et de l’affinité entre le ligand et les protéines (KD) sont à l’origine de variations de la fraction libre (fu) n Faut-il en déduire que ces variations de la fraction libre entraînent des variations de la concentration libre ?

Quelle importance clinique pour les phénomènes de compétition au niveau des protéines plasmatiques ?

FIXATION DES MEDICAMENTS SUR LES PROTEINES PLASMATIQUES par J. -P. Tillement In : PHARMACOLOGIE CLINIQUE - Bases de la thérapeutique (Giroud, Mathé, Meyniel) « Sur le plan pharmacologique, ce type d’interférence se traduit par l’augmentation de la fraction libre plasmatique de l’un ou des deux médicaments présents. Il en résulte une augmentation des intensités des effets observés par rapport à ceux escomptés. Les principales substances ionisées susceptibles d’entrer en compétition au niveau des sites albuminiques sont indiquées sur le tableau 11. 10. L’interaction la plus classique est celle de la warfarine associée à la phénylbutazone (O’Reilly et Aggeler, 1970). Chez un sujet traité par l’antivitamine K à dose efficace, l’administration de phénylbutazone provoque sa défixation partielle, majorant l’effet anticoagulant. Aux concentrations thérapeutiques de ces deux substances, le pourcentage de forme libre plasmatique de warfarine passe de 10 à 30 p. cent … Il en résulte une augmentation importante des concentrations tissulaires de warfarine, celles-ci étant sensiblement trois fois plus élevées. Au niveau du foie où se trouvent les récepteurs de la warfarine, l’effet anticoagulant est multiplié par trois, ce qui, compte tenu du mauvais coefficient chimiothérapeutique de cette substance, se traduit par un surdosage générateur d’hémorragies. »

Phénomènes de compétition au niveau des protéines plasmatiques n Très souvent évoqué comme une cause d’interactions médicamenteuses ¨ Le “déplaceur” augmente la fraction libre du “déplacé” VRAI ¨ Il est déduit que la concentration libre du “déplacé” augmente FAUX

Phénomènes de compétition au niveau des protéines plasmatiques n A l’origine, une confusion dans la relation entre fu, Clibre et Ctotale n Lorsqu’un déplacement existe, la concentration libre de la molécule déplacée n’est généralement pas affectée, avec une absence de conséquence sur l’exposition de la cible (récepteur, pathogène. . . ) et sur les effets associés

Relations entre fu, Clibre and Ctot : la situation in vitro
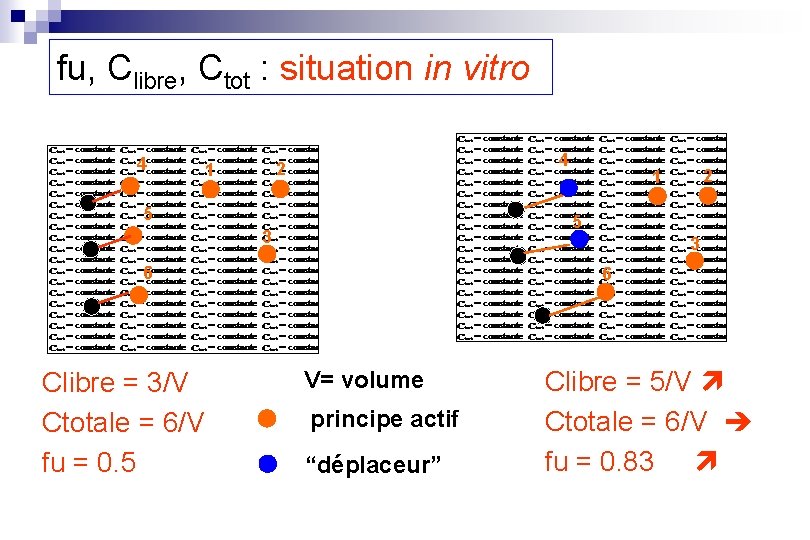
fu, Clibre, Ctot : situation in vitro 4 4 2 1 5 5 3 3 6 Clibre = 3/V Ctotale = 6/V fu = 0. 5 2 1 6 V= volume principe actif “déplaceur” Clibre = 5/V Ctotale = 6/V fu = 0. 83
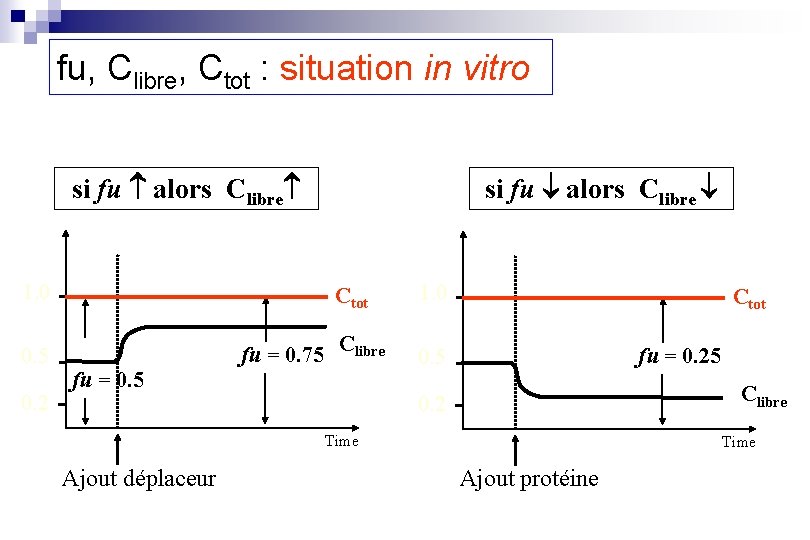
fu, Clibre, Ctot : situation in vitro si fu alors Clibre 1. 0 0. 5 0. 2 si fu alors Clibre Ctot fu = 0. 75 Clibre fu = 0. 5 1. 0 Ctot fu = 0. 25 0. 5 Clibre 0. 2 Time Ajout déplaceur Time Ajout protéine
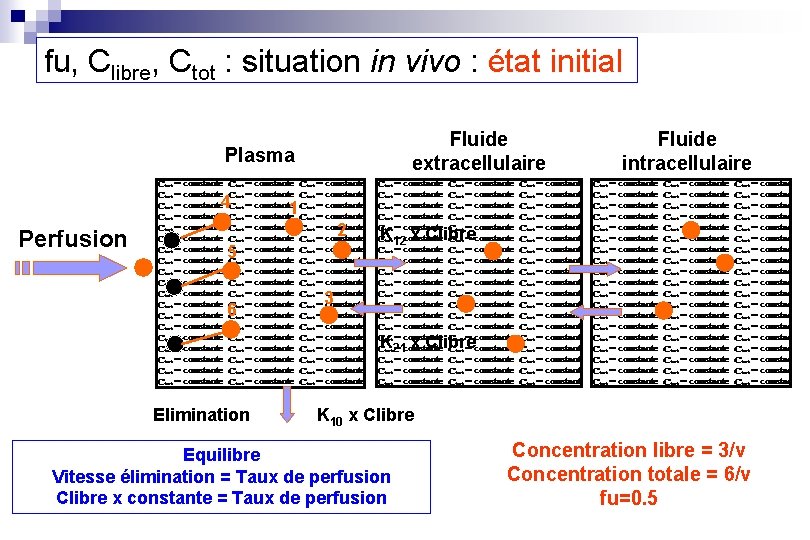
fu, Clibre, Ctot : situation in vivo : état initial Fluide extracellulaire Plasma 4 Perfusion 1 2 5 6 Fluide intracellulaire K 12 x Clibre 3 K 21 x Clibre Elimination K 10 x Clibre Equilibre Vitesse élimination = Taux de perfusion Clibre x constante = Taux de perfusion Concentration libre = 3/v Concentration totale = 6/v fu=0. 5
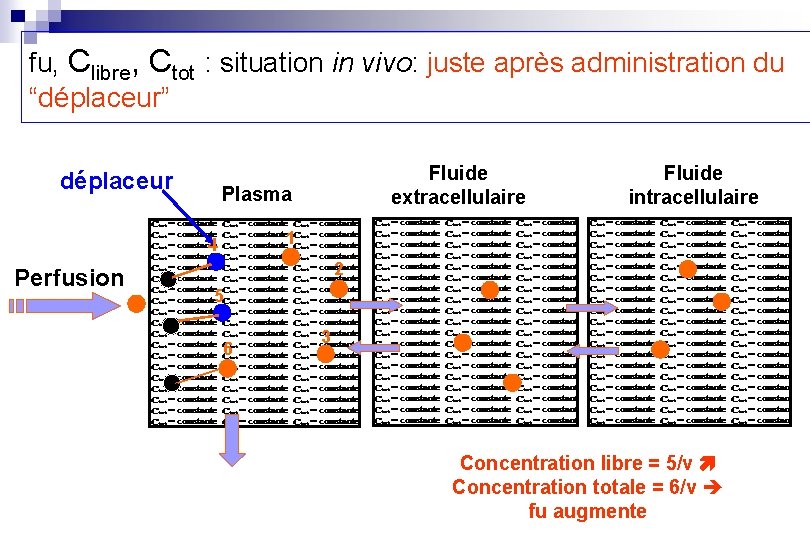
fu, Clibre, Ctot : situation in vivo: juste après administration du “déplaceur” déplaceur Plasma Fluide intracellulaire 1 4 Perfusion Fluide extracellulaire 2 5 6 3 Concentration libre = 5/v Concentration totale = 6/v fu augmente
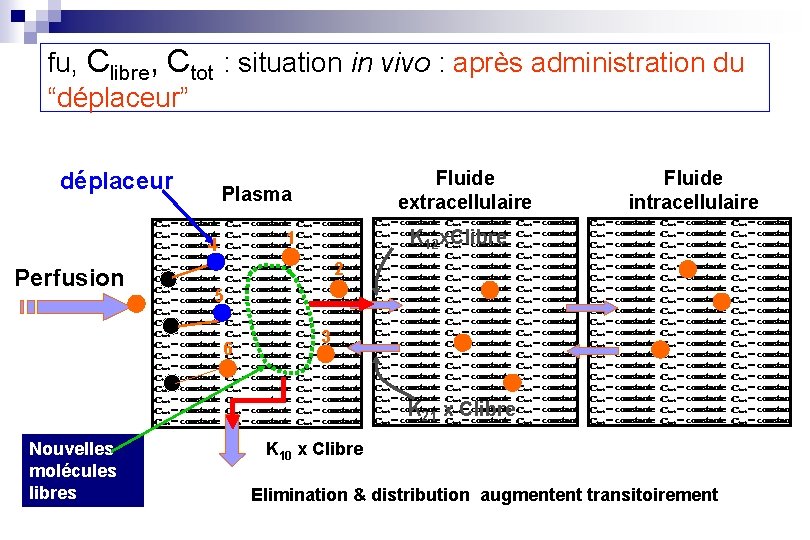
fu, Clibre, Ctot : situation in vivo : après administration du “déplaceur” déplaceur Plasma Fluide intracellulaire K 12 x. Clibre 1 4 Perfusion Fluide extracellulaire 2 5 6 3 K 21 x Clibre Nouvelles molécules libres K 10 x Clibre Elimination & distribution augmentent transitoirement
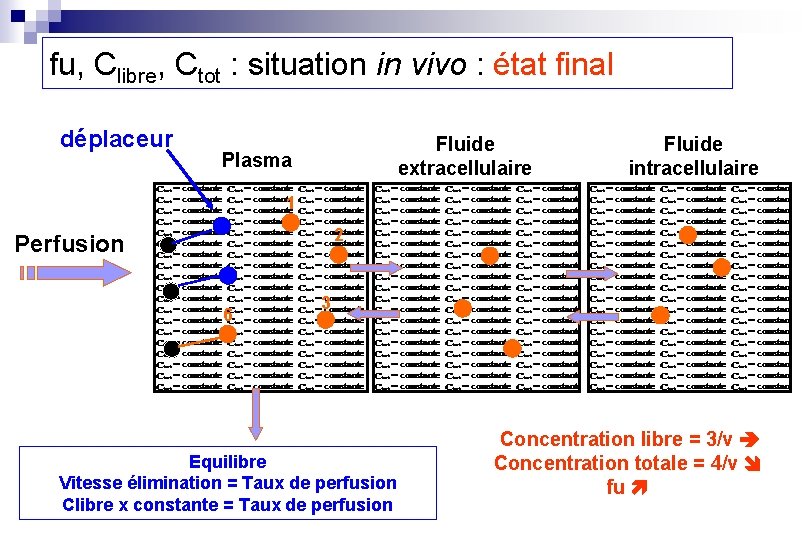
fu, Clibre, Ctot : situation in vivo : état final déplaceur Fluide extracellulaire Plasma Fluide intracellulaire 1 2 Perfusion 6 3 Equilibre Vitesse élimination = Taux de perfusion Clibre x constante = Taux de perfusion Concentration libre = 3/v Concentration totale = 4/v fu
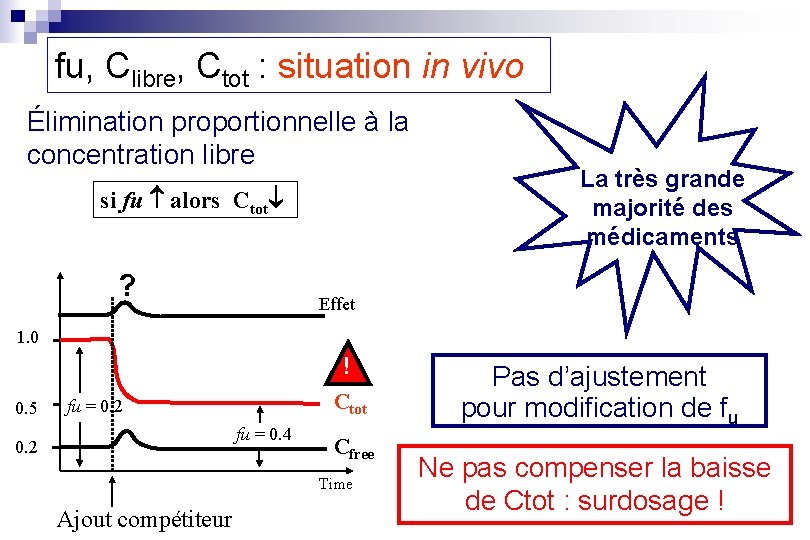
fu, Clibre, Ctot : situation in vivo Élimination proportionnelle à la concentration libre si fu alors Ctot ? La très grande majorité des médicaments Effet 1. 0 ! 0. 5 Ctot fu = 0. 2 fu = 0. 4 0. 2 Cfree Time Ajout compétiteur Pas d’ajustement pour modification de fu Ne pas compenser la baisse de Ctot : surdosage !
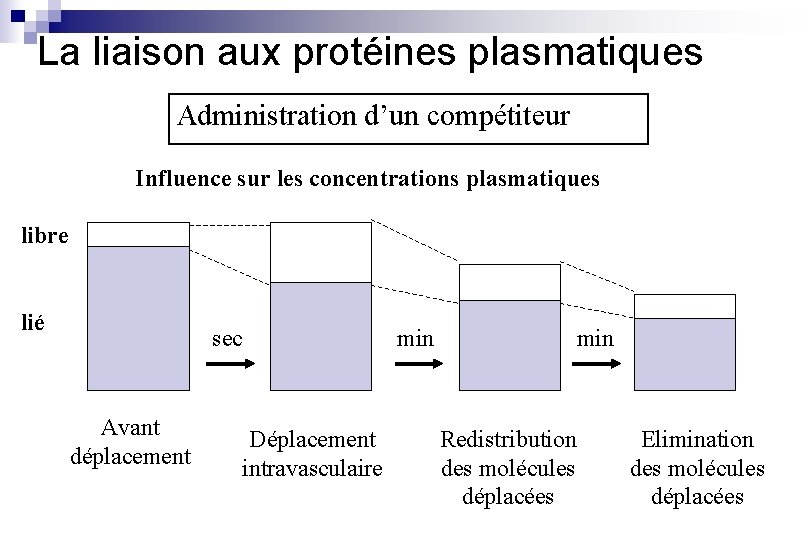
La liaison aux protéines plasmatiques Administration d’un compétiteur Influence sur les concentrations plasmatiques libre lié sec Avant déplacement Déplacement intravasculaire min Redistribution des molécules déplacées Elimination des molécules déplacées
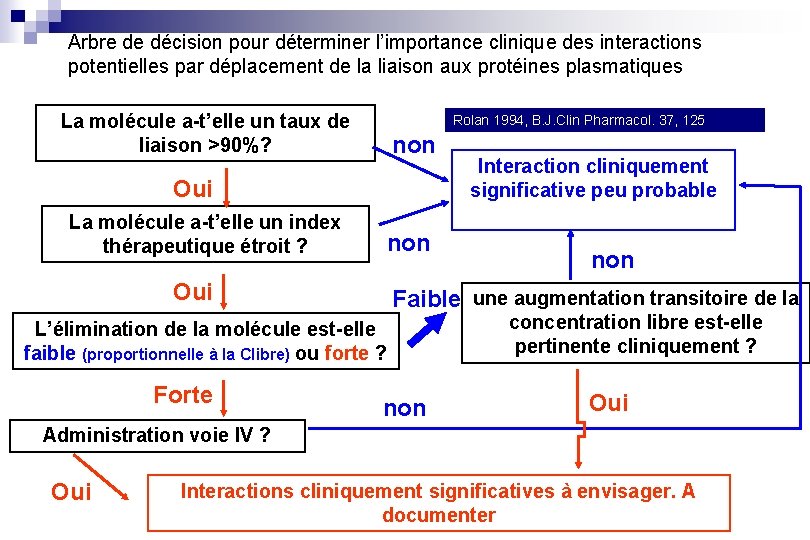
Arbre de décision pour déterminer l’importance clinique des interactions potentielles par déplacement de la liaison aux protéines plasmatiques La molécule a-t’elle un taux de liaison >90%? Rolan 1994, B. J. Clin Pharmacol. 37, 125 non Oui La molécule a-t’elle un index thérapeutique étroit ? non Oui non Faible une augmentation transitoire de la L’élimination de la molécule est-elle faible (proportionnelle à la Clibre) ou forte ? Forte Interaction cliniquement significative peu probable non concentration libre est-elle pertinente cliniquement ? Oui Administration voie IV ? Oui Interactions cliniquement significatives à envisager. A documenter

Retour sur l’interaction warfarine-phénylbutazone (PBZ) n L’interaction médicamenteuse est réelle L’augmentation des concentrations libres est réelle ! Le déplacement de la warfarine est réel : fu augmente ! n Mais la warfarine a une élimination faible n n ¨ le déplacement de la liaison en présence de PBZ augmente fu MAIS N’EST PAS responsable de l’augmentation des concentrations libres à l’équilibre n Le mécanisme responsable de l’interaction : ¨ La PBZ inhibe de manière stereoselective le metabolisme de la s-warfarine : une action directe sur l’élimination !

La liaison aux protéines plasmatiques n Conclusion : importance de la liaison aux protéines plasmatiques ? ¨ Surestimée comme cause d’interactions médicamenteuses ¨ Ne pas interpréter des variations de fu comme causes de variations de la concentration libre n n Pas d’exemple d’adaptations de posologies lorsque fu varie En particulier : ne pas mal interpréter une diminution de Ctotale ¨ Réelle pour extrapoler des concentrations efficaces de l’in vitro vers l’in vivo : ex. CMI pour les antibiotiques ¨ Réelle pour comparer les concentrations totales efficaces entre espèces ¨ Réelle pour évaluer l’étendue de la distribution du principe actif
- Slides: 38