La gestion des dchets Biochimie Laurence Chavant Gestion

La gestion des déchets Biochimie Laurence Chavant

Gestion des déchets lors d’une séance de Tp de Biochimie
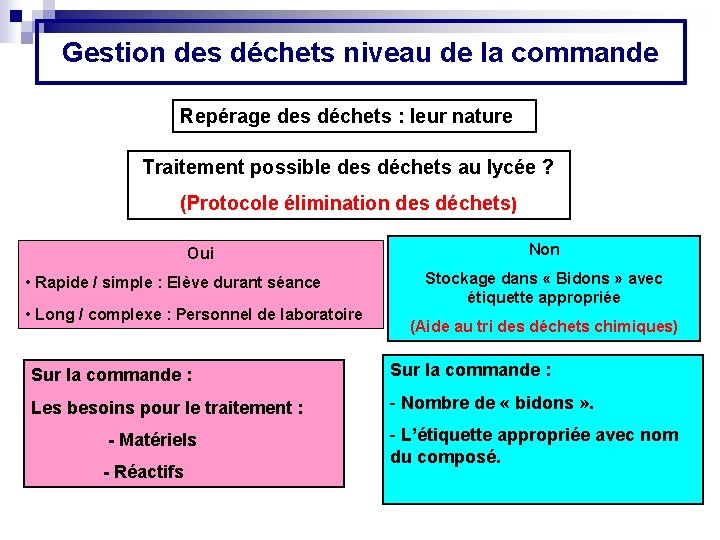
Gestion des déchets niveau de la commande Repérage des déchets : leur nature Traitement possible des déchets au lycée ? (Protocole élimination des déchets) Non Oui • Rapide / simple : Elève durant séance • Long / complexe : Personnel de laboratoire Stockage dans « Bidons » avec étiquette appropriée (Aide au tri des déchets chimiques) Sur la commande : Les besoins pour le traitement : - Nombre de « bidons » . - Matériels - Réactifs - L’étiquette appropriée avec nom du composé.

Documents destinés aux élèves n Fiche technique « Détermination de l’étiquette présente sur le bidon » . n Dans la salle : « Aide au tri des déchets chimiques » n Sur protocole : v Symbole v Tableau : Devenir des produits sur la paillasse. : Elimination des déchets de l’analyse à compléter.
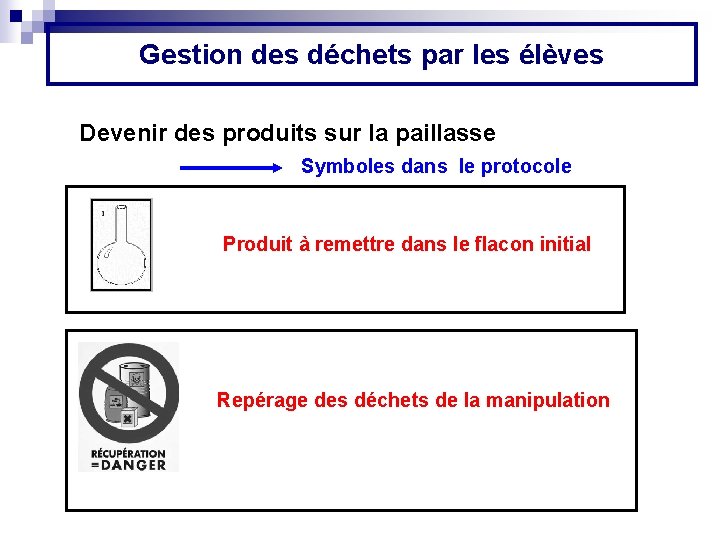
Gestion des déchets par les élèves Devenir des produits sur la paillasse Symboles dans le protocole Produit à remettre dans le flacon initial Repérage des déchets de la manipulation
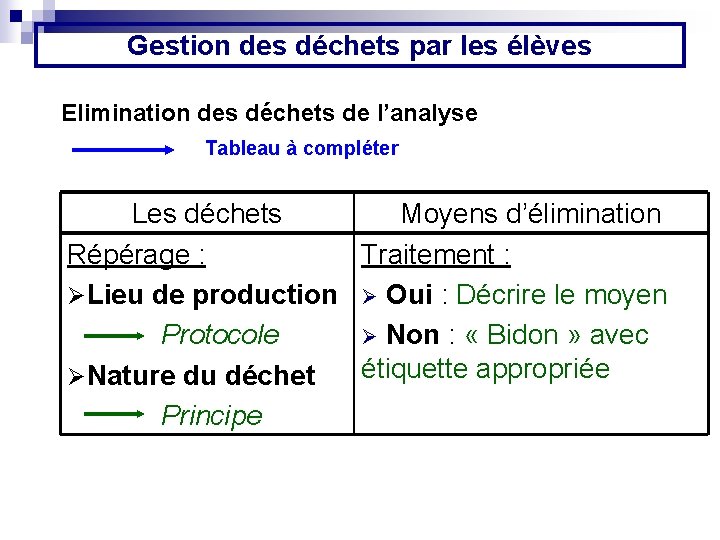
Gestion des déchets par les élèves Elimination des déchets de l’analyse Tableau à compléter Les déchets Moyens d’élimination Répérage : Traitement : ØLieu de production Ø Oui : Décrire le moyen Protocole Ø Non : « Bidon » avec étiquette appropriée ØNature du déchet Principe

Gestion des déchets par élèves Exemple : Dosage des chlorures Le protocole : - Etalonnage de la solution nitrate d’argent par méthode de Mohr : pesée indirecte n - Dosage des chlorures par méthode de Charpentier et Volhard.
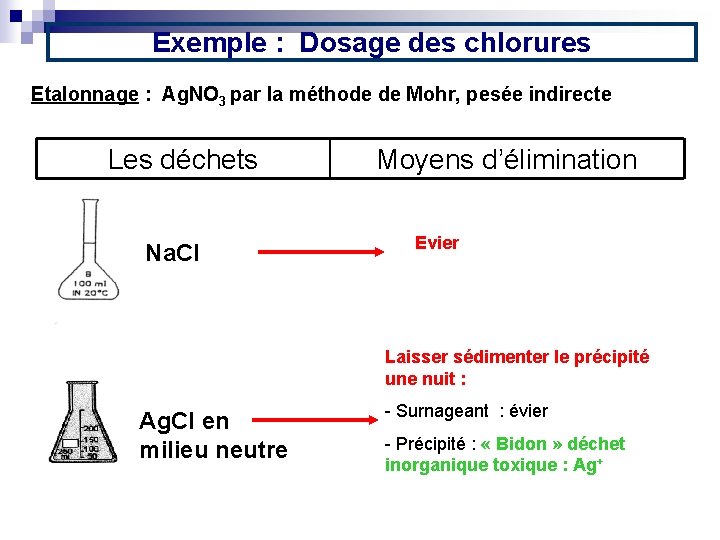
Exemple : Dosage des chlorures Etalonnage : Ag. NO 3 par la méthode de Mohr, pesée indirecte Les déchets Na. Cl Moyens d’élimination Evier Laisser sédimenter le précipité une nuit : Ag. Cl en milieu neutre - Surnageant : évier - Précipité : « Bidon » déchet inorganique toxique : Ag+
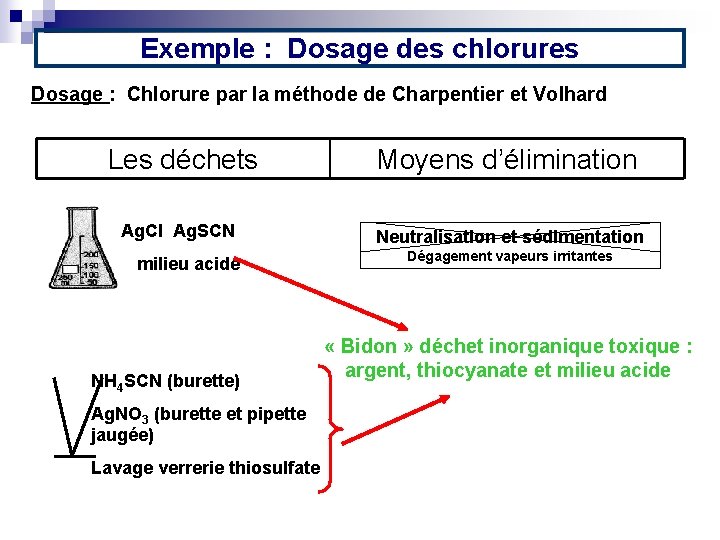
Exemple : Dosage des chlorures Dosage : Chlorure par la méthode de Charpentier et Volhard Les déchets Moyens d’élimination Ag. Cl Ag. SCN Neutralisation et sédimentation Dégagement vapeurs irritantes milieu acide NH 4 SCN (burette) « Bidon » déchet inorganique toxique : argent, thiocyanate et milieu acide Ag. NO 3 (burette et pipette jaugée) Lavage verrerie thiosulfate

Gestion des déchets : Réduction de volume Quelques pistes
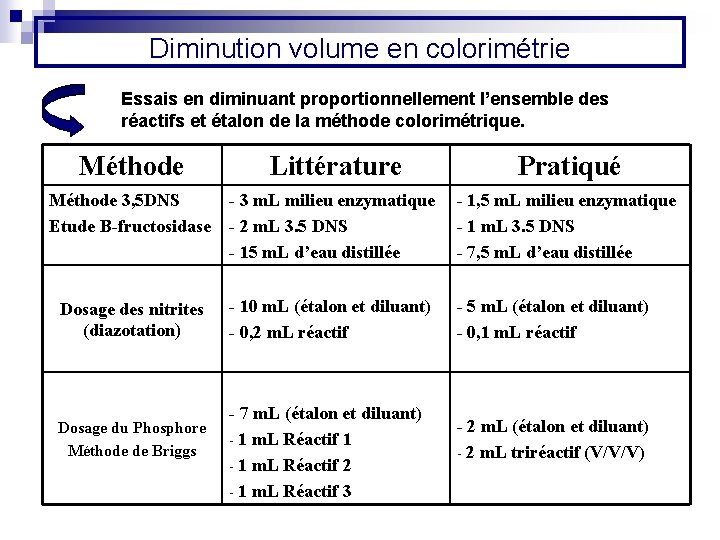
Diminution volume en colorimétrie Essais en diminuant proportionnellement l’ensemble des réactifs et étalon de la méthode colorimétrique. Méthode Littérature Pratiqué Méthode 3, 5 DNS Etude B-fructosidase - 3 m. L milieu enzymatique - 2 m. L 3. 5 DNS - 15 m. L d’eau distillée - 1, 5 m. L milieu enzymatique - 1 m. L 3. 5 DNS - 7, 5 m. L d’eau distillée Dosage des nitrites (diazotation) - 10 m. L (étalon et diluant) - 0, 2 m. L réactif - 5 m. L (étalon et diluant) - 0, 1 m. L réactif - 7 m. L (étalon et diluant) Dosage du Phosphore - 1 m. L Réactif 1 Méthode de Briggs - 1 m. L Réactif 2 - 1 m. L Réactif 3 - 2 m. L (étalon et diluant) - 2 m. L triréactif (V/V/V)

Diminution des déchets : CCM des acides aminés v Solvant : Volume préparé nécessaire à 2 groupes de 16 élèves (1 L). Ø Récupérer et stocker en flacon fermé. Ø Utiliser par les groupes suivants dans la semaine. Ø v Révélateur à la ninhydrine (pinceau) Composition : 0, 6 g de ninhydrine 6 m. L d’acide éthanoïque n-butanol qsp 200 m. L En flacon brun fermé le réactif est stable plusieurs mois à + 4°C. v Dimension des plaques : CCM ( « secondaire » ) Séparation des AA lors chromatographie échange d’ions/Identification des AA par CCM : plaque de 4 cm x 4 cm

Diminution des déchets : Fractionnement des protéines sériques par sulfate d’ammonium Préparation de la fraction « globulines » - Dans un tube à centrifuger, placé dans de la glace, introduire : n n - 5 m. L de sérum - 5 m. L de sulfate d’ammonium à 100 % (goutte à goutte). - Mélanger, laisser reposer 10 minutes. - Centrifuger 10 min à 4500 rpm (Jouan , E 96). - Dans un tube Eppendorf de 1, 5 m. L , placé dans de la glace, introduire : n n n - 0, 5 m. L de sérum dilué (= Unitrol dilué au ½) - 0, 5 m. L de sulfate d’ammonium à 100 % (goutte à goutte). - Mélanger, laisser reposer 10 minutes. - Centrifuger 5 min à 10 000 rpm (microcentrifugeuse). La fraction obtenue est la fraction de globuline. On cherche à obtenir un volume total proche de 1 m. L Noter le volume exacte obtenu soit V G.

Diminution des déchets : Fractionnement des protéines sériques par sulfate d’ammonium n Dosage des protéines par la méthode au Biuret Ø 1 m. L de solution étalon ou fractions à doser. Ø 4 m. L de réactif du biuret. 0, 5 m. L de solution étalon ou fractions à doser. Ø 2 m. L de réactif du biuret. Ø
- Slides: 14