La dsescalade thrapeutique dans les MICI Aurlien AMIOT


- Slides: 24

La désescalade thérapeutique dans les MICI Aurélien AMIOT Gastroentérologie, CHU Henri Mondor aurelien. amiot@aphp. fr

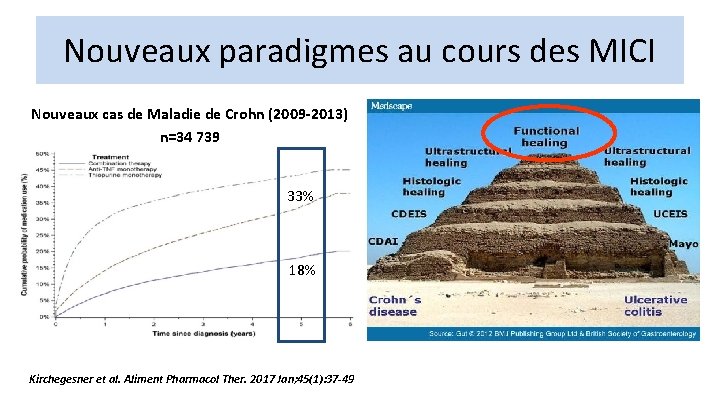
Nouveaux paradigmes au cours des MICI Nouveaux cas de Maladie de Crohn (2009 -2013) n=34 739 33% 18% Kirchegesner et al. Aliment Pharmacol Ther. 2017 Jan; 45(1): 37 -49

MICI active Treat to target: une fois la cible atteinte …

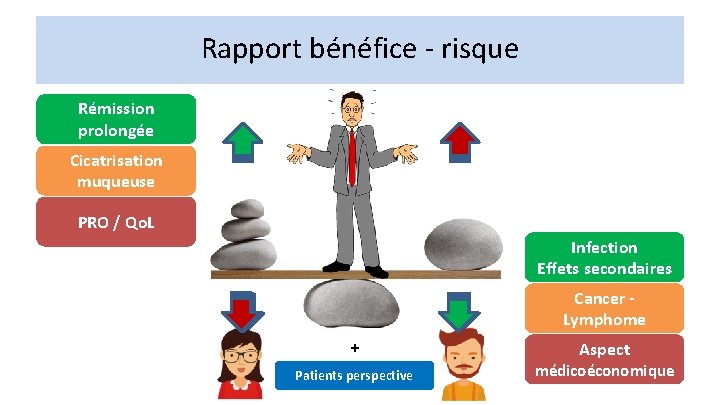
Rapport bénéfice - risque Rémission prolongée Cicatrisation muqueuse PRO / Qo. L Infection Effets secondaires Cancer - Lymphome + Patients perspective Aspect médicoéconomique

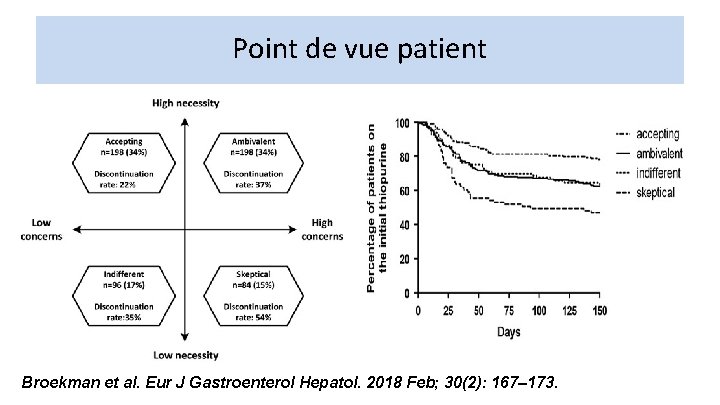
Point de vue patient Broekman et al. Eur J Gastroenterol Hepatol. 2018 Feb; 30(2): 167– 173.

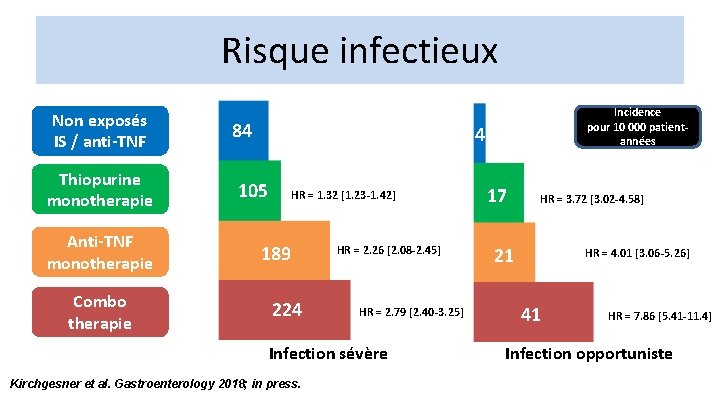
Risque infectieux Non exposés IS / anti-TNF Thiopurine monotherapie Anti-TNF monotherapie Combo therapie 84 Incidence pour 10 000 patientannées 44 105 HR = 1. 32 [1. 23 -1. 42] 189 224 HR = 2. 26 [2. 08 -2. 45] HR = 2. 79 [2. 40 -3. 25] Infection sévère Kirchgesner et al. Gastroenterology 2018; in press. 17 HR = 3. 72 [3. 02 -4. 58] 21 HR = 4. 01 [3. 06 -5. 26] 41 HR = 7. 86 [5. 41 -11. 4] Infection opportuniste

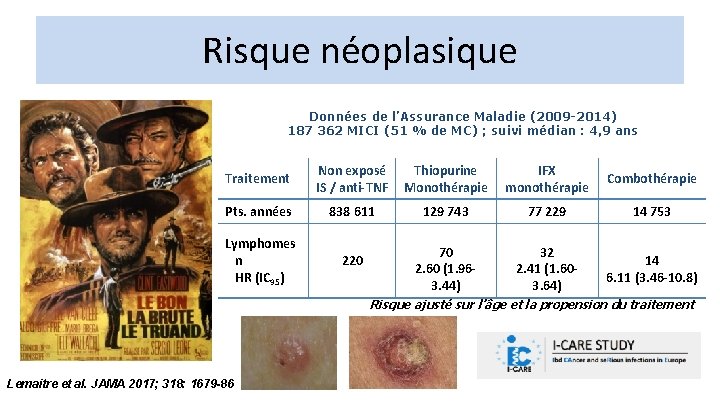
Risque néoplasique Données de l’Assurance Maladie (2009 -2014) 187 362 MICI (51 % de MC) ; suivi médian : 4, 9 ans Traitement Non exposé IS / anti-TNF Thiopurine Monothérapie IFX monothérapie Combothérapie Pts. années 838 611 129 743 77 229 14 753 Lymphomes n HR (IC 95) 220 70 2. 60 (1. 963. 44) 32 2. 41 (1. 603. 64) 14 6. 11 (3. 46 -10. 8) Risque ajusté sur l’âge et la propension du traitement Lemaitre et al. JAMA 2017; 318: 1679 -86

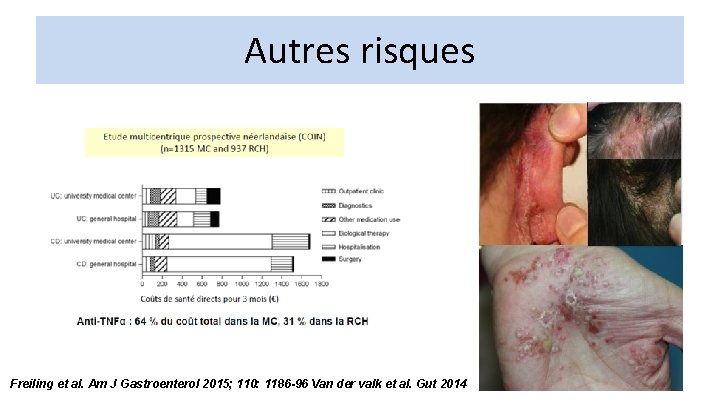
Autres risques Freiling et al. Am J Gastroenterol 2015; 110: 1186 -96 Van der valk et al. Gut 2014

Désescalade thérapeutique Réduire la posologie Interrompre le traitement

Réduction posologique Thiopurine Meilleure tolérance Cut-off efficacité? Anti-TNF Combothérapie Monothérapie

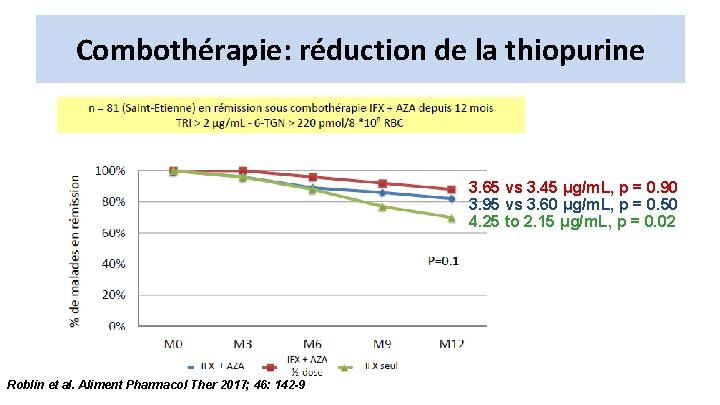
Combothérapie: réduction de la thiopurine 3. 65 vs 3. 45 μg/m. L, p = 0. 90 3. 95 vs 3. 60 μg/m. L, p = 0. 50 4. 25 to 2. 15 μg/m. L, p = 0. 02 Roblin et al. Aliment Pharmacol Ther 2017; 46: 142 -9

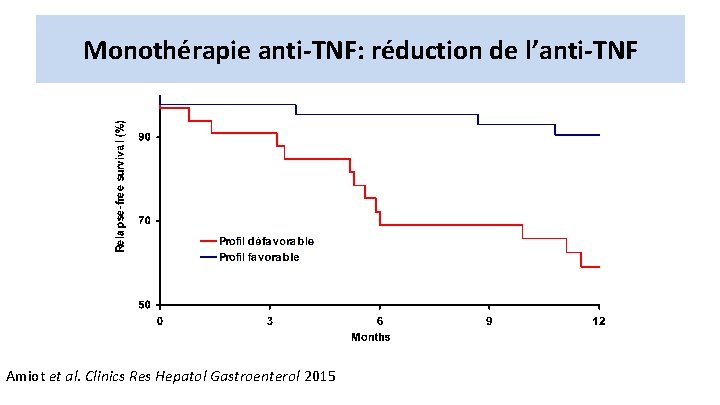
Monothérapie anti-TNF: réduction de l’anti-TNF Amiot et al. Clinics Res Hepatol Gastroenterol 2015

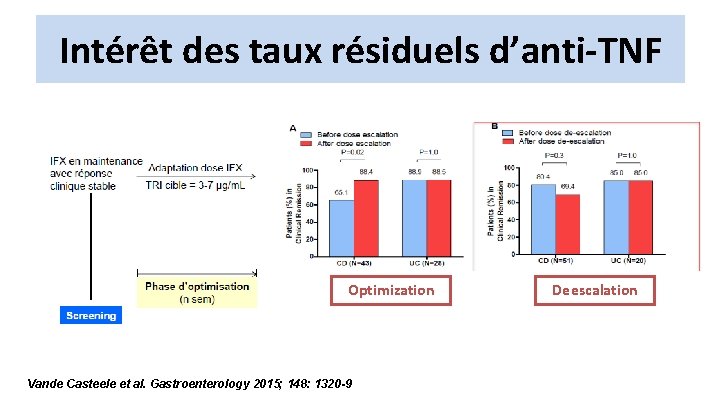
Intérêt des taux résiduels d’anti-TNF Optimization Vande Casteele et al. Gastroenterology 2015; 148: 1320 -9 Deescalation

Désescalade à l’arrêt Réduire la posologie Interrompre le traitement

Interrompre le traitement Thiopurine Anti-TNF Combo thérapie

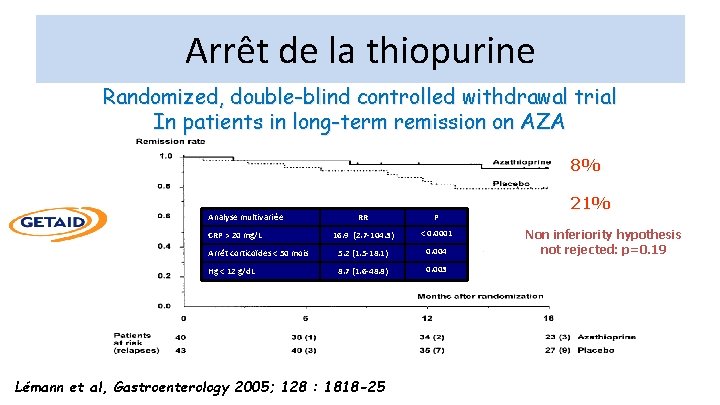
Arrêt de la thiopurine Randomized, double-blind controlled withdrawal trial In patients in long-term remission on AZA 8% Analyse multivariée RR P 16. 9 (2. 7 -104. 3) < 0. 0001 Arrêt corticoïdes < 50 mois 5. 2 (1. 5 -18. 1) 0. 004 Hg < 12 g/d. L 8. 7 (1. 6 -48. 8) 0. 003 CRP > 20 mg/L Lémann et al, Gastroenterology 2005; 128 : 1818 -25 21% Non inferiority hypothesis not rejected: p=0. 19

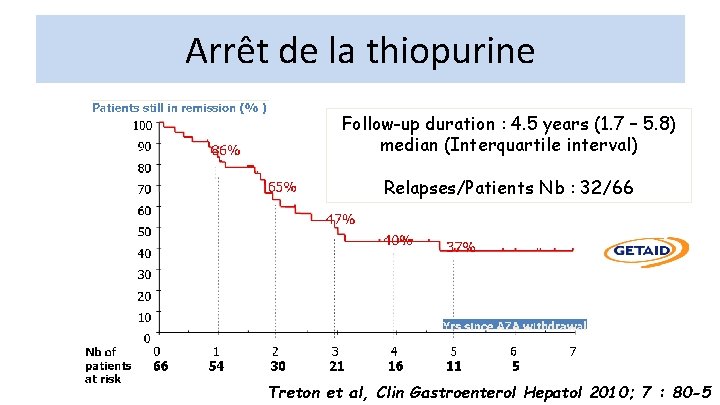
Arrêt de la thiopurine Follow-up duration : 4. 5 years (1. 7 – 5. 8) median (Interquartile interval) Relapses/Patients Nb : 32/66 Treton et al, Clin Gastroenterol Hepatol 2010; 7 : 80 -5

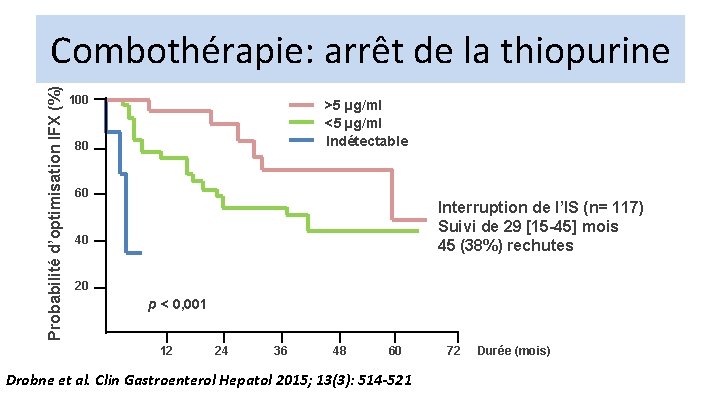
Probabilité d’optimisation IFX (%) Combothérapie: arrêt de la thiopurine 100 >5 µg/ml <5 µg/ml Indétectable 80 60 Interruption de l’IS (n= 117) Suivi de 29 [15 -45] mois 45 (38%) rechutes 40 20 p < 0, 001 12 24 36 48 60 Drobne et al. Clin Gastroenterol Hepatol 2015; 13(3): 514 -521 72 Durée (mois)

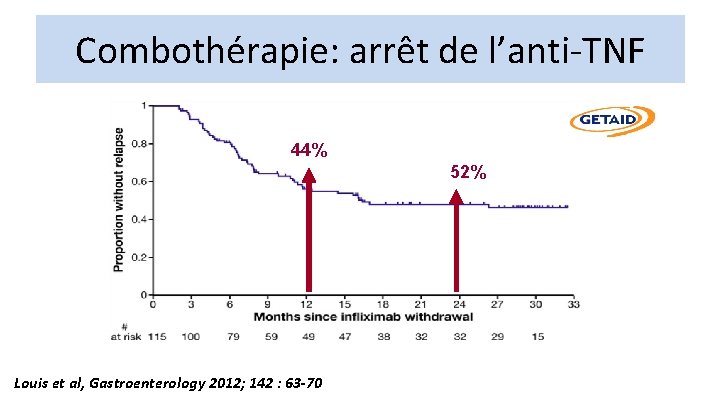
Combothérapie: arrêt de l’anti-TNF 44% 52% Louis et al, Gastroenterology 2012; 142 : 63 -70

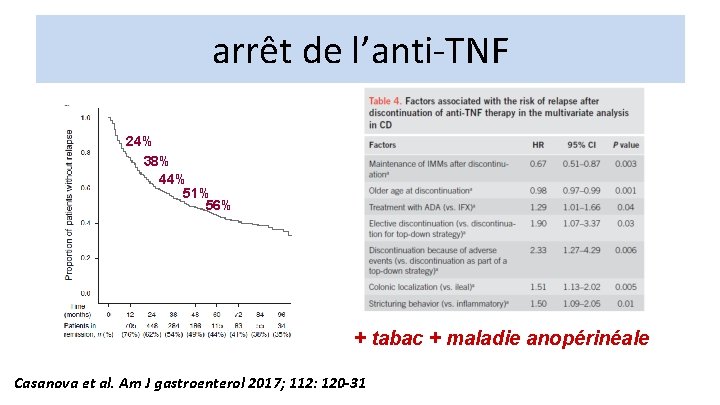
arrêt de l’anti-TNF 24% 38% 44% 51% 56% + tabac + maladie anopérinéale Casanova et al. Am J gastroenterol 2017; 112: 120 -31

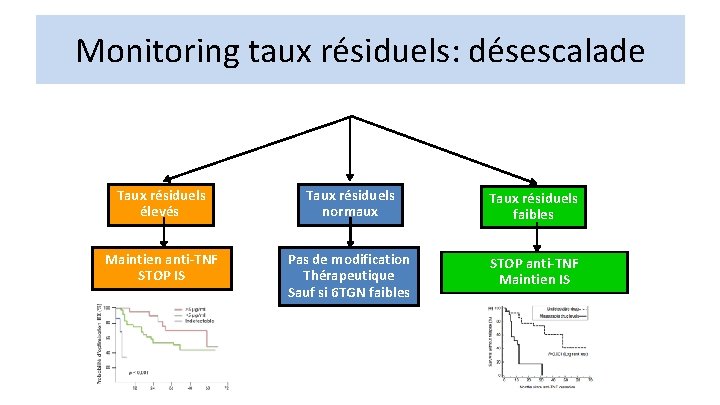
Monitoring taux résiduels: désescalade Taux résiduels élevés Taux résiduels normaux Taux résiduels faibles Maintien anti-TNF STOP IS Pas de modification Thérapeutique Sauf si 6 TGN faibles STOP anti-TNF Maintien IS Roblin et al. Am J Gastroenterol 2014 Yanai et al. Clin Gastro and Hepatol 2015

Retraitement cycles de traitement Thiopurine Efficacité restaurée dans 85% des cas Tolérance identique Anti-TNF Efficacité restaurée dans 85% des cas Tolérance discutée réinduction hybride S 0 S 4 S 8

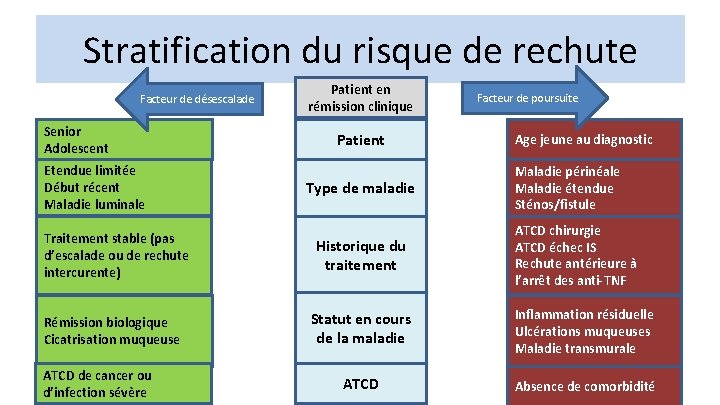
Stratification du risque de rechute Facteur de désescalade Senior Adolescent Etendue limitée Début récent Maladie luminale Traitement stable (pas d’escalade ou de rechute intercurente) Rémission biologique Cicatrisation muqueuse ATCD de cancer ou d’infection sévère Patient en rémission clinique Patient Type de maladie Historique du traitement Facteur de poursuite Age jeune au diagnostic Maladie périnéale Maladie étendue Sténos/fistule ATCD chirurgie ATCD échec IS Rechute antérieure à l’arrêt des anti-TNF Statut en cours de la maladie Inflammation résiduelle Ulcérations muqueuses Maladie transmurale ATCD Absence de comorbidité

Points à retenir • Problématique reposant sur une demande légitime des patients, des arguments de tolérance et un aspect médico-économique • Arrêt à discuter en fonction – Du terrain, du risque et de la sévérité potentielle de la rechute (activité résiduelle +++) – Des taux résiduels de médicament +++ – Les modalités prévisibles du retraitement