La clula habla distintos idiomas Idioma de 4

La célula habla distintos idiomas Idioma de 4 nucleótidos: ADN RNA Idioma de 20 aminoácidos: proteínas NECESITA UN CODIGO PARA TRADUCIR!!
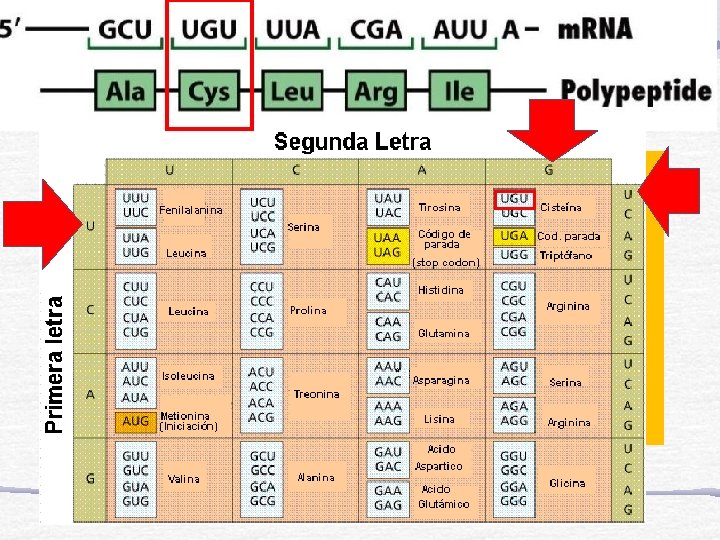
CÓDIGO GENÉTICO CODIGO GENÉTICO!!
RECORDAR (TEMA 1) Macromoléculas Proteínas Unidades: Aminoácidos Ácidos Nucleicos Unidades: Nucleótidos

Area Química Biológica Curso: Bioquímica Tema 6: AMINOÁCIDOS Y PROTEINAS 2018 Dra. Silvia M. Varas


Funciones biológicas de las proteínas Enzimas Proteínas de transporte: Hemoglobina, Lp Proteínas nutrientes y de reserva: caseína, ferritina Proteínas contráctiles: actina, miosina. Proteínas estructurales: colágeno, elastina, queratina Proteínas de defensa: anticuerpos, fibrinógeno trombina Proteínas reguladoras: hormonas insulina

Las proteínas están formadas por unidades básicas que corresponden a los aminoácidos, los cuales se unen entre sí para formar una estructura en cadena. Son macromoléculas, de PM muy elevados.

Estructura básica de un AMINOÁCIDO
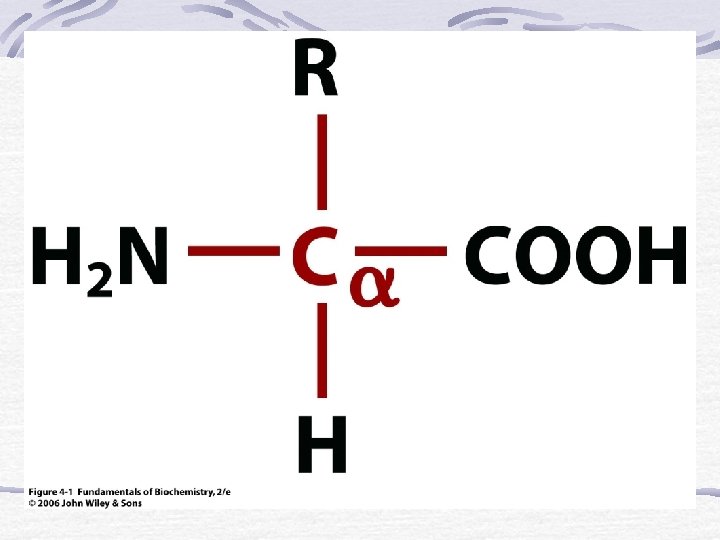
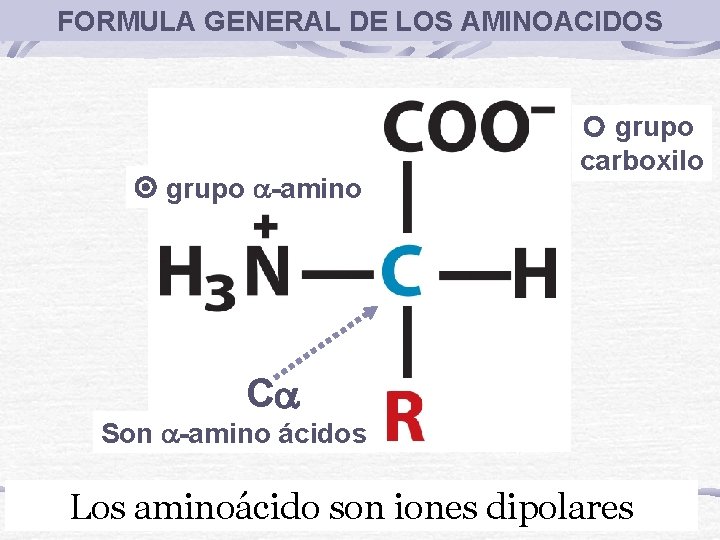
FORMULA GENERAL DE LOS AMINOACIDOS grupo -amino grupo carboxilo C Son -amino ácidos Los aminoácido son iones dipolares

Iones Dipolares o Zwiteriones Son las moléculas (como los aminoácidos) que tienen grupos cargados de polaridad opuesta
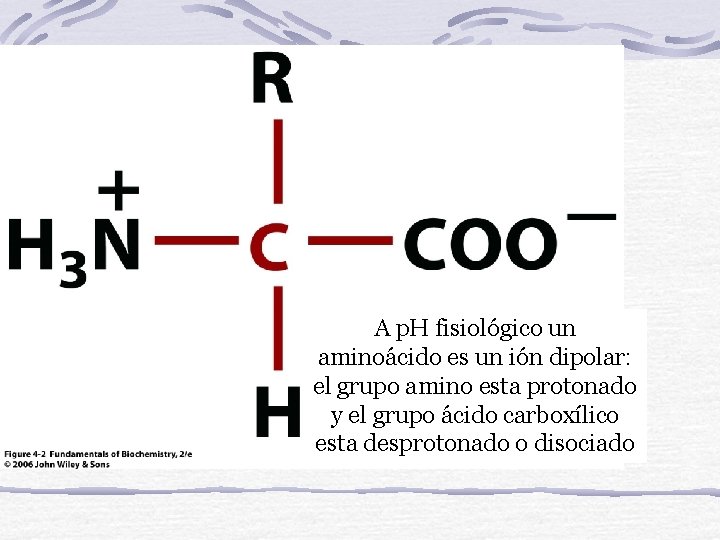
A p. H fisiológico un aminoácido es un ión dipolar: el grupo amino esta protonado y el grupo ácido carboxílico esta desprotonado o disociado

Los aminoácidos se comportan como iones dipolos y son ANFÓTEROS: PUEDEN REACCIONAR COMO ÁCIDOS O BASES DÉBILES PUEDEN ACTUAR COMO BUFFER O AMORTIGUADORES DEL p. H
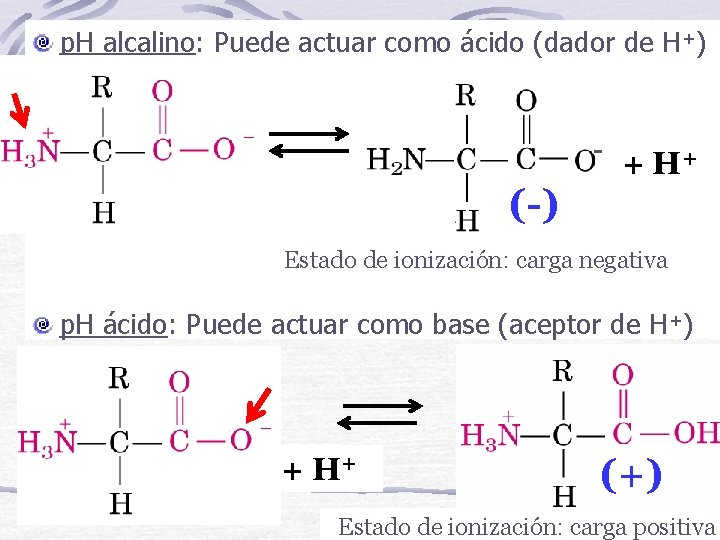
p. H alcalino: Puede actuar como ácido (dador de H+) - (-) + H+ Estado de ionización: carga negativa p. H ácido: Puede actuar como base (aceptor de H+) + H+ (+) Estado de ionización: carga positiva

Tipos de RADICALES Cadenas Cadenas NO POLAR: 7 AROMATICOS: 3 SIN CARGA, POLAR: 5 CARGADAS POSITIVAMENTE (+): 3 CARGADAS NEGATIVAMENTE (-): 2

NATURALEZA DE LOS RADICALES O CADENAS LATERALES DE LOS AMINOACIDOS 7 5 3 20 aminoácidos 3 2
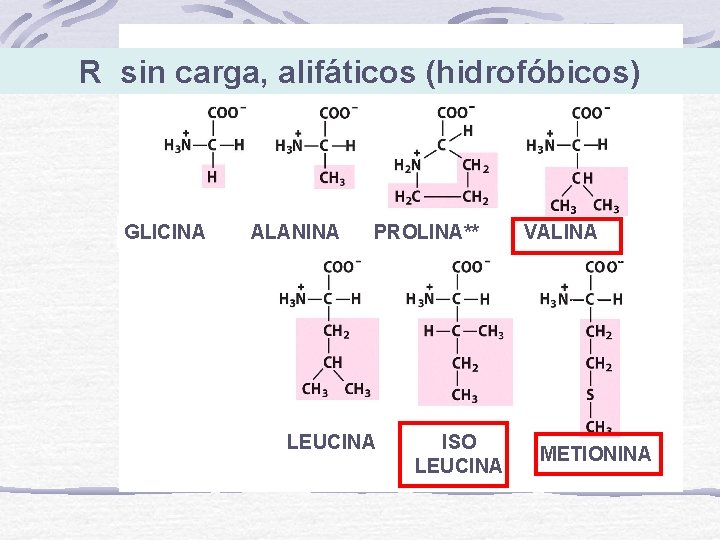
R sin carga, alifáticos (hidrofóbicos) GLICINA ALANINA PROLINA** LEUCINA ISO LEUCINA VALINA METIONINA
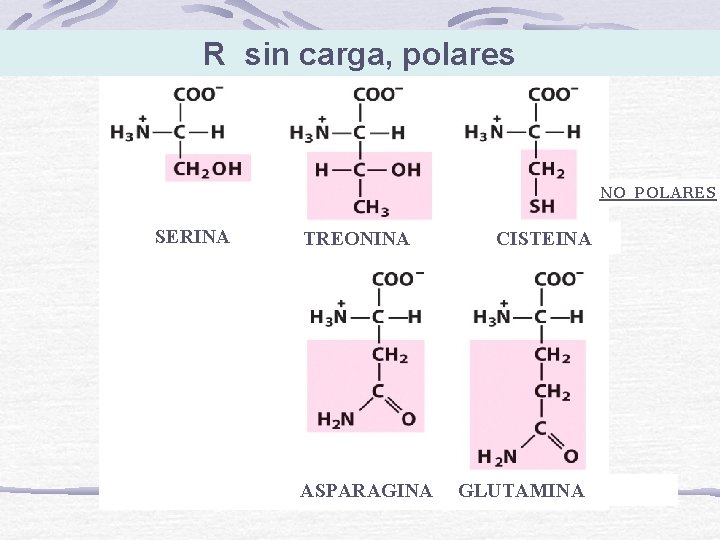
R sin carga, polares NO POLARES SERINA TREONINA ASPARAGINA CISTEINA GLUTAMINA
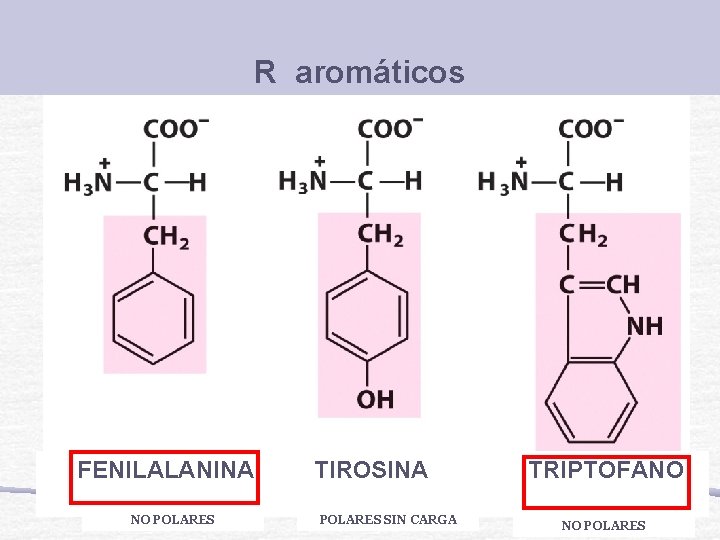
R aromáticos FENILALANINA NO POLARES TIROSINA POLARES SIN CARGA TRIPTOFANO NO POLARES
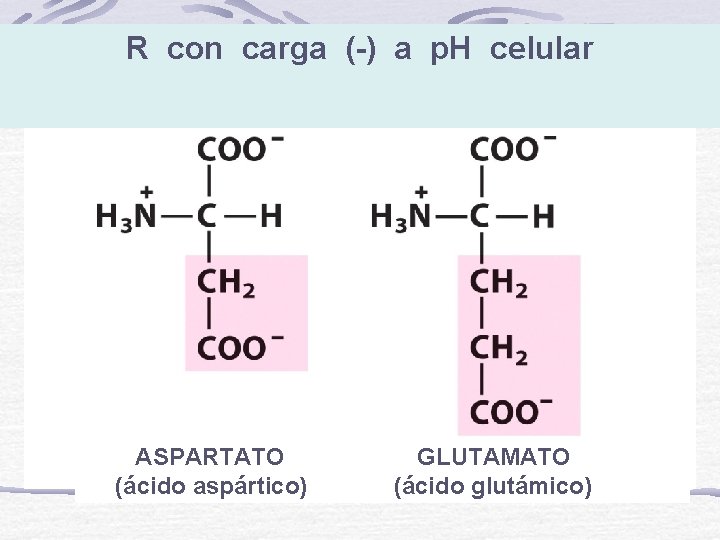
R con carga (-) a p. H celular ASPARTATO (ácido aspártico) GLUTAMATO (ácido glutámico)
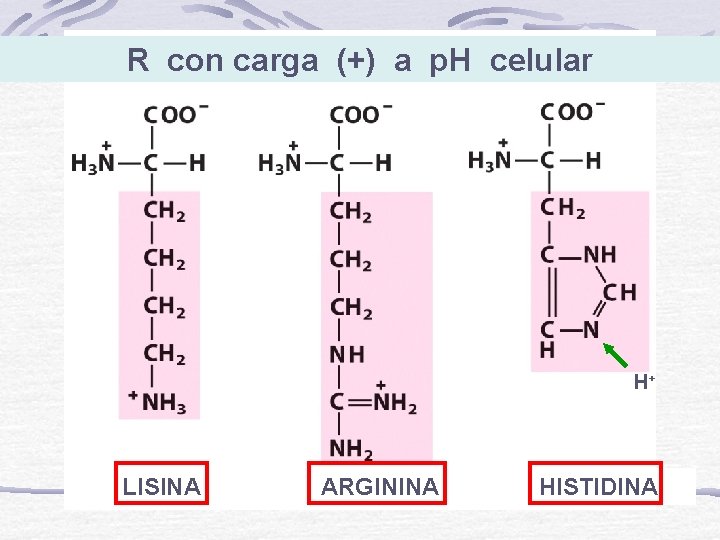
R con carga (+) a p. H celular H+ LISINA ARGININA HISTIDINA

Comportamiento ácido-base de las cadenas laterales Ka=constante de disociación ácida. Los aminoácidos (Asp y Glu), los básicos (Lys, Arg e His) y la Tyr y Cys pueden presentar carga a determinados valores de p. H.
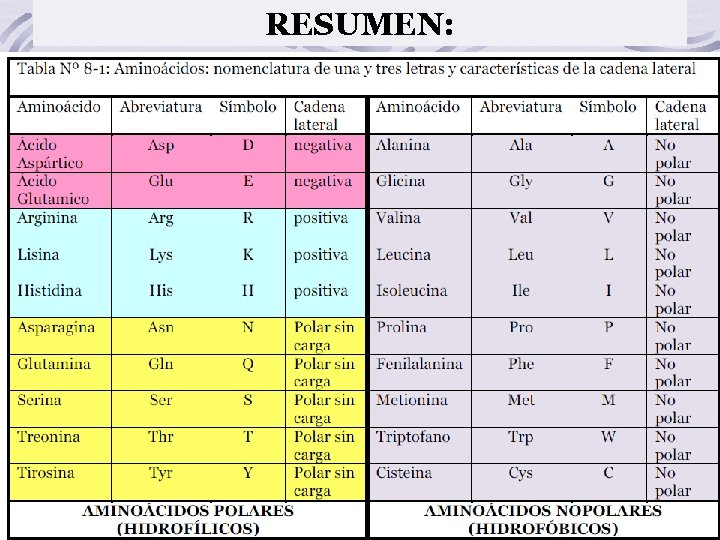
RESUMEN:

Las propiedades de las cadenas laterales determinan las interacciones no covalentes: Hidrofobicidad Fuerzas de Van der Waals Interacciones electrostáticas
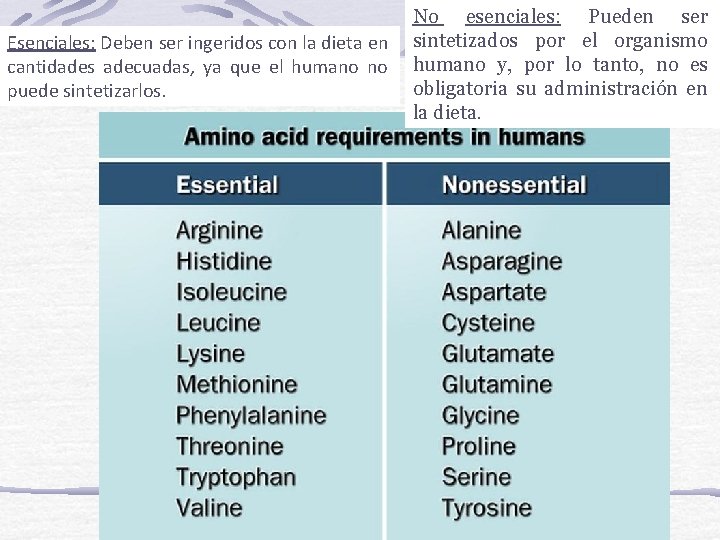
Esenciales: Deben ser ingeridos con la dieta en cantidades adecuadas, ya que el humano no puede sintetizarlos. No esenciales: Pueden ser sintetizados por el organismo humano y, por lo tanto, no es obligatoria su administración en la dieta.
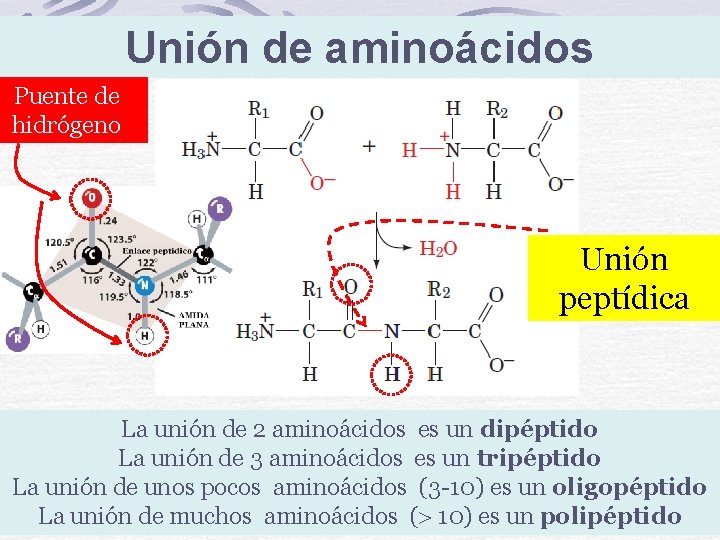
Unión de aminoácidos Puente de hidrógeno Unión peptídica La unión de 2 aminoácidos es un dipéptido La unión de 3 aminoácidos es un tripéptido La unión de unos pocos aminoácidos (3 -10) es un oligopéptido La unión de muchos aminoácidos ( 10) es un polipéptido
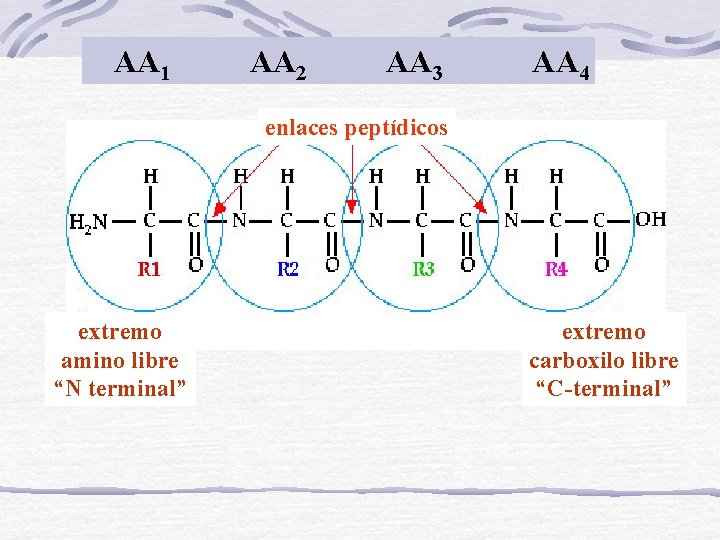
AA 1 AA 2 AA 3 AA 4 enlaces peptídicos extremo amino libre “N terminal” extremo carboxilo libre “C-terminal”
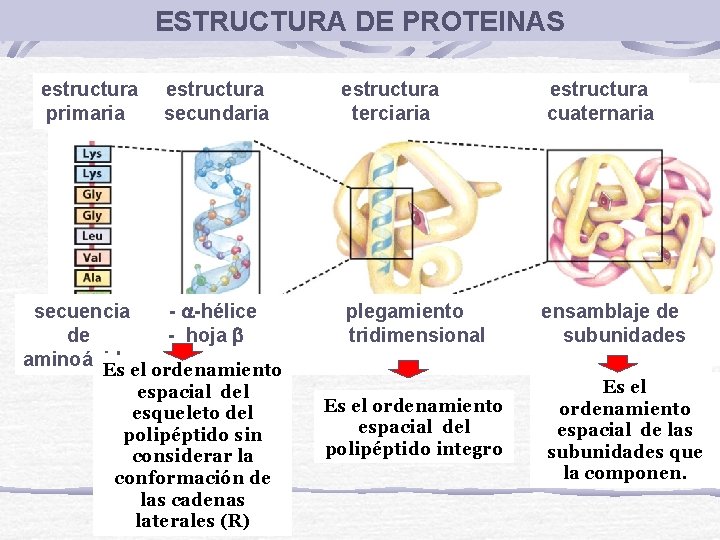
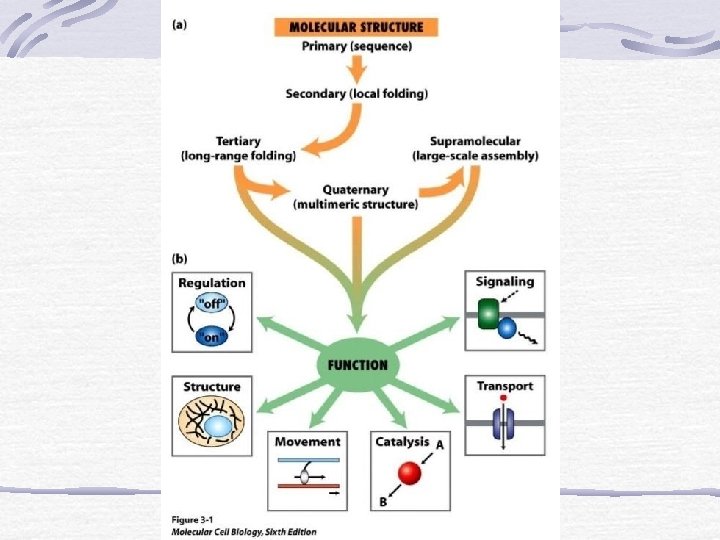
ESTRUCTURA DE PROTEINAS estructura primaria estructura secundaria estructura terciaria estructura cuaternaria secuencia de aminoácidos - -hélice - hoja plegamiento tridimensional ensamblaje de subunidades Es el ordenamiento espacial del esqueleto del polipéptido sin considerar la conformación de las cadenas laterales (R) Es el ordenamiento espacial del polipéptido integro Es el ordenamiento espacial de las subunidades que la componen.
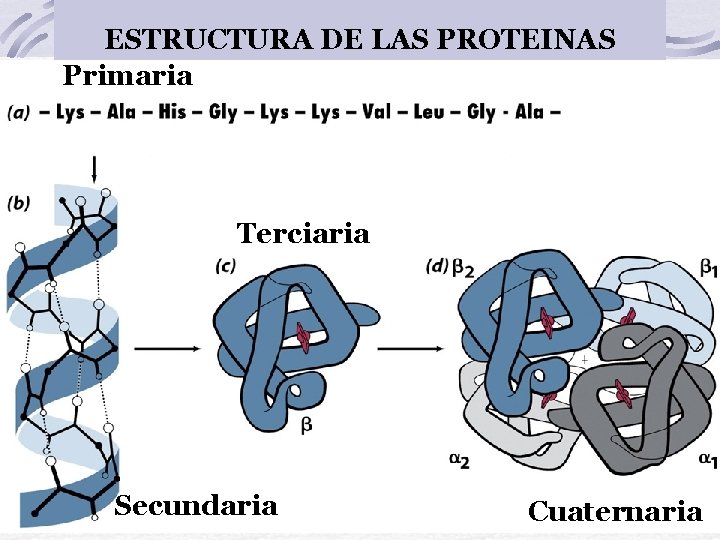
ESTRUCTURA DE LAS PROTEINAS Primaria Terciaria Secundaria Cuaternaria

Polipéptido: Péptido aminoácidos. formado por más de 10 Proteína: Se llama así cuando la cadena polipeptídica tiene una masa molecular de más de 6. 000 Daltons (más de 50 unidades de aminoácidos).
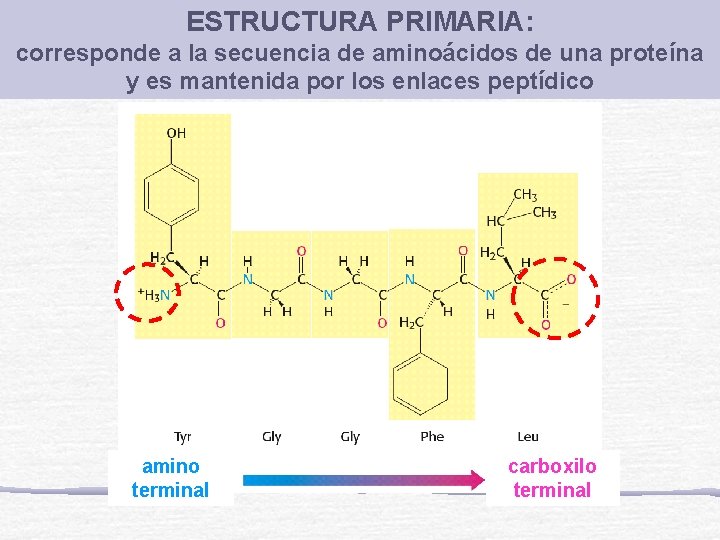
ESTRUCTURA PRIMARIA: corresponde a la secuencia de aminoácidos de una proteína y es mantenida por los enlaces peptídico amino terminal carboxilo terminal
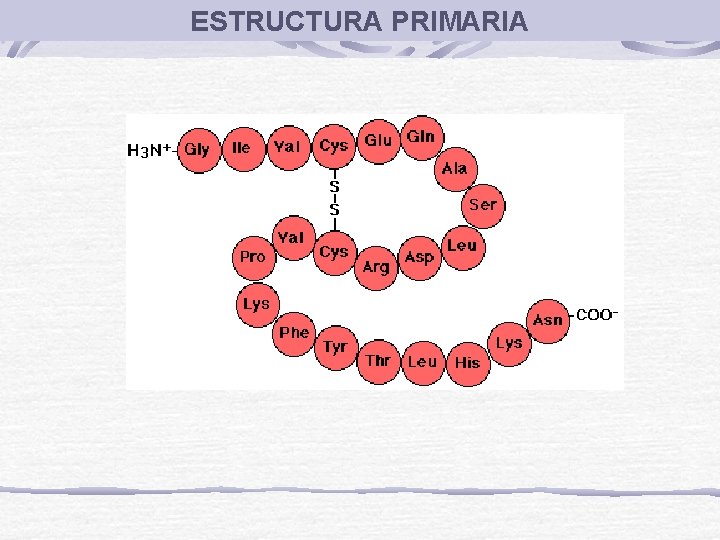
ESTRUCTURA PRIMARIA
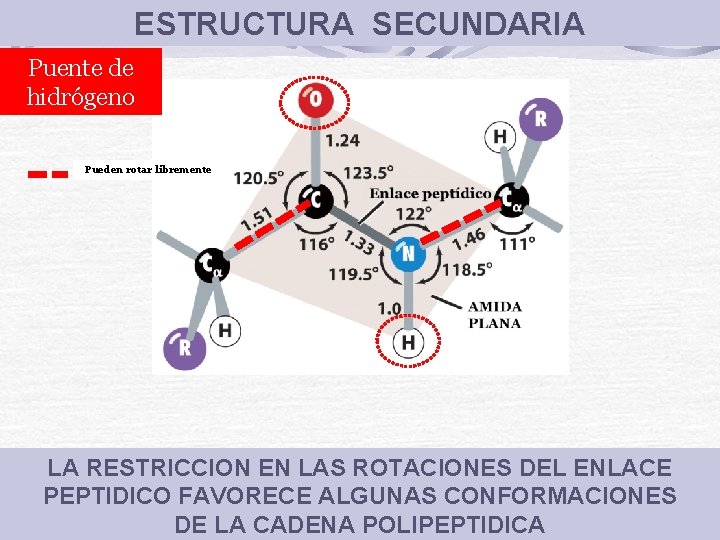
ESTRUCTURA SECUNDARIA Puente de hidrógeno Pueden rotar libremente LA RESTRICCION EN LAS ROTACIONES DEL ENLACE PEPTIDICO FAVORECE ALGUNAS CONFORMACIONES DE LA CADENA POLIPEPTIDICA
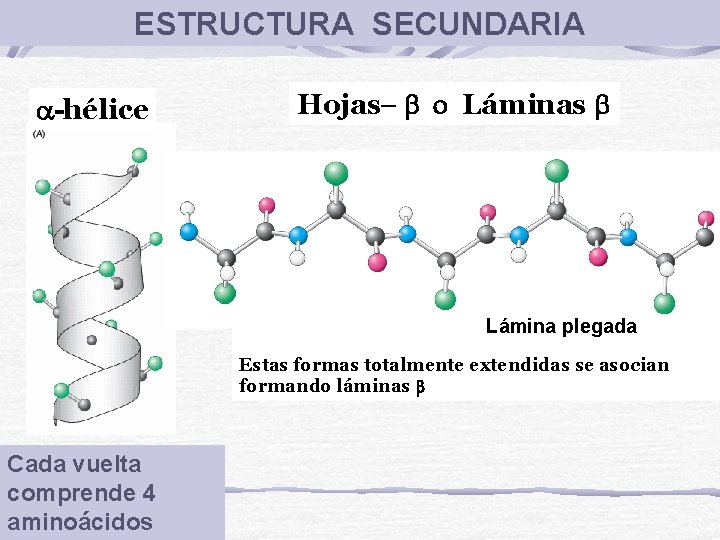
ESTRUCTURA SECUNDARIA -hélice Hojas- o Láminas Lámina plegada Estas formas totalmente extendidas se asocian formando láminas Cada vuelta comprende 4 aminoácidos
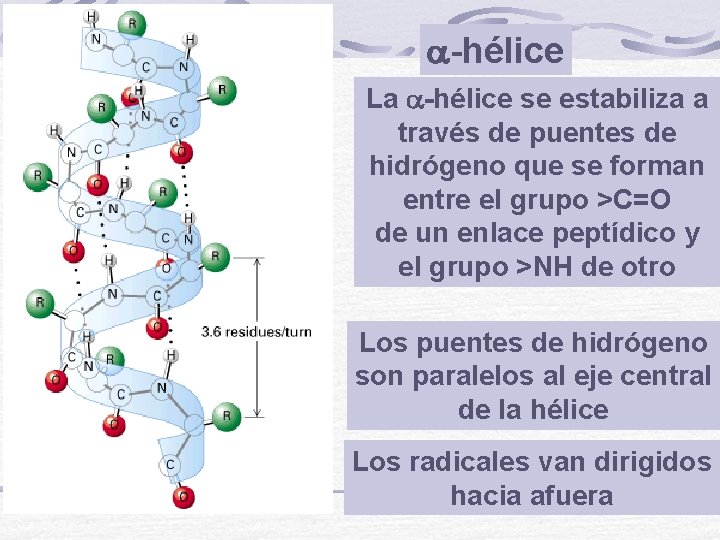
-hélice La -hélice se estabiliza a través de puentes de hidrógeno que se forman entre el grupo >C=O de un enlace peptídico y el grupo >NH de otro Los puentes de hidrógeno son paralelos al eje central de la hélice Los radicales van dirigidos hacia afuera
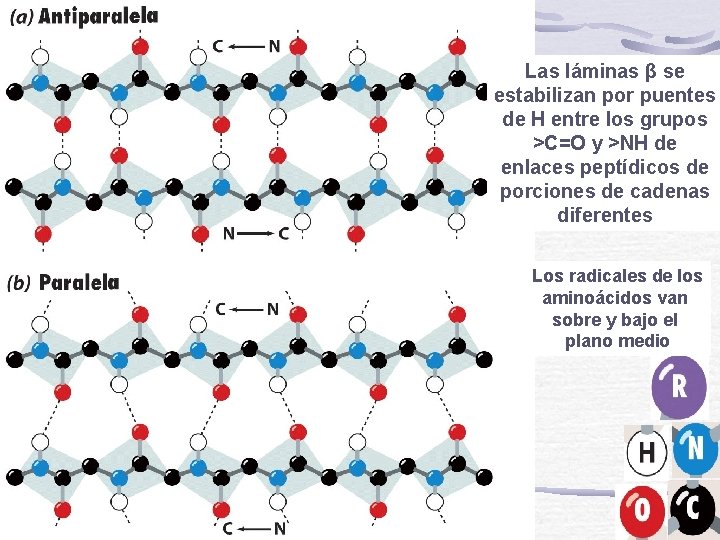
Las láminas β se estabilizan por puentes de H entre los grupos >C=O y >NH de enlaces peptídicos de porciones de cadenas diferentes Los radicales de los aminoácidos van sobre y bajo el plano medio
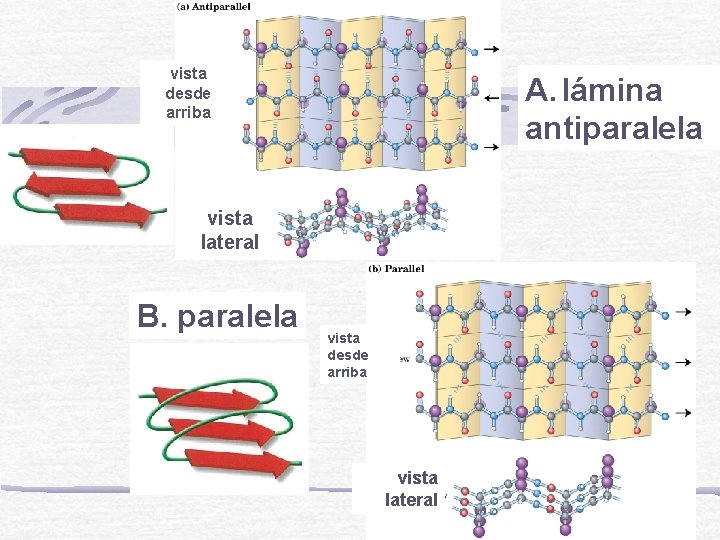
vista desde arriba A. lámina antiparalela vista lateral B. paralela vista desde arriba vista lateral

ESTRUCTURA TERCIARIA La ESTRUCTURA TERCIARIA corresponde a plegamientos tridimensionales. La proteína se pliega sobre sí misma y tiende a una forma “globular” En su mantención participan los grupos radicales de los aminoácidos.
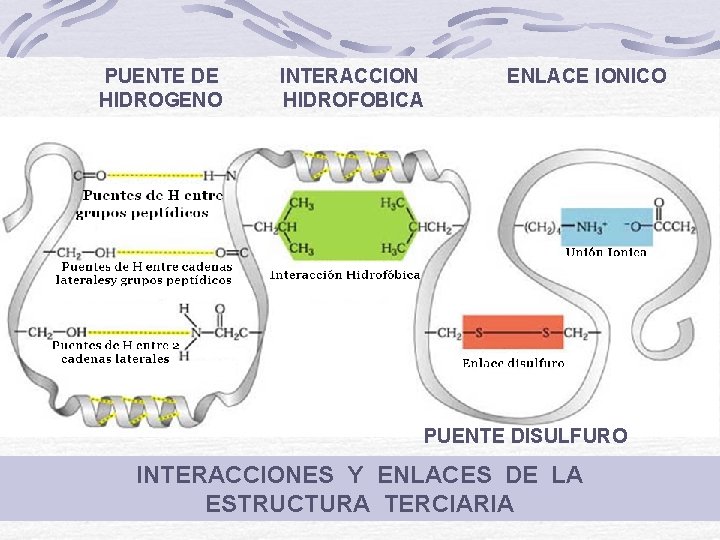
PUENTE DE HIDROGENO INTERACCION HIDROFOBICA ENLACE IONICO PUENTE DISULFURO INTERACCIONES Y ENLACES DE LA ESTRUCTURA TERCIARIA

ESTRUCTURA CUATERNARIA La ESTRUCTURA CUATERNARIA corresponde a la asociacion de cadenas polipeptídicas o SUBUNIDADES, cada una de ella con su estructura terciaria. Se mantiene por enlaces entre los radicales de cadenas diferentes. Son los mismos enlaces que mantienen la estructura terciaria, pero intercadenas. Se excluye el puente disulfuro.

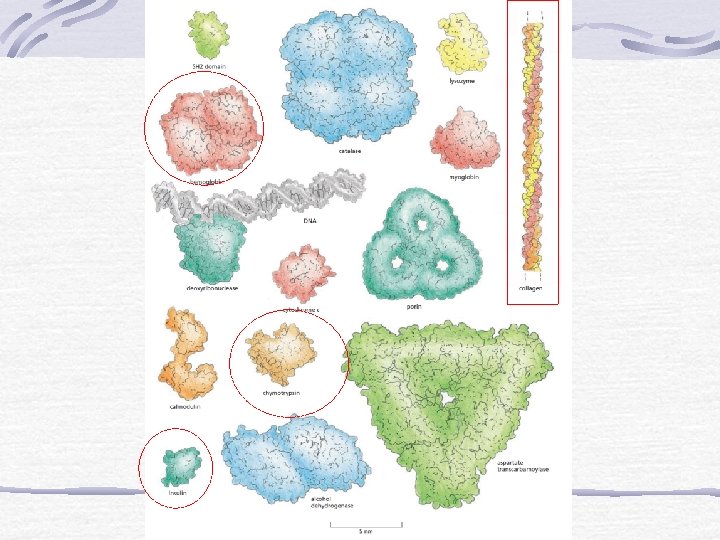
Clasificación de proteínas según su forma molecular Proteínas globulares: La cadena de aminoácidos se pliega sobre si misma, adquiriendo la forma de un ovillo. Son solubles en medios acuosos. En general, se trata de proteínas de gran actividad funcional (enzimas, anticuerpos, hormonas, la hemoglobina, etc) Proteínas fibrosas: Los aminoácidos que las forman se ubican paralelamente, formando fibras o láminas extendidas. En general son poco solubles o insolubles en agua y participan en la constitución de estructuras de sostén, como el tejido conjuntivo. Ej: queratina ; colágeno
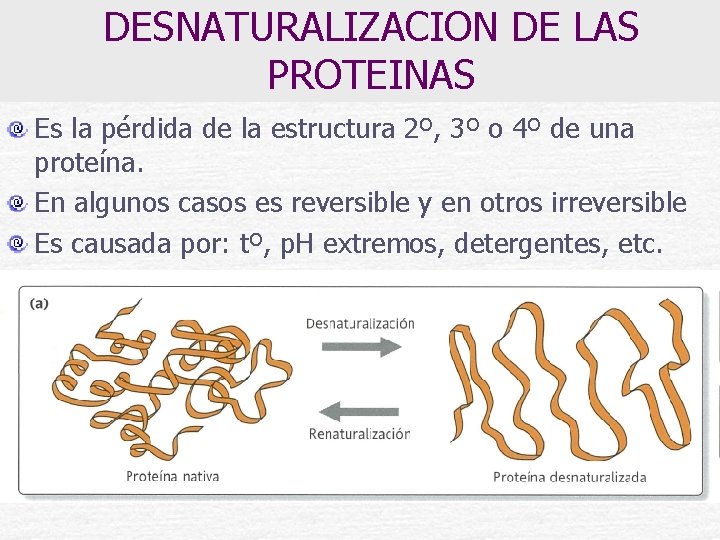
DESNATURALIZACION DE LAS PROTEINAS Es la pérdida de la estructura 2º, 3º o 4º de una proteína. En algunos casos es reversible y en otros irreversible Es causada por: tº, p. H extremos, detergentes, etc.

Propiedades Generales de las Proteínas Acido-Base Solubilidad de las proteínas Efecto del p. H Efecto de sales Acido-Base: a p. H fisiológico, la cantidad de grupos ácidos y básicos que poseas dependerá de los aminoácidos que formen la proteína.

Solubilidad de las proteínas Depende de varios factores, entre ellos: 1. De la cantidad de grupos polares presentes en los aminoácidos que conforman la proteína. 2. De factores externos a la proteína como son: el p. H, la temperatura, la presencia de sales inorgánicas, o solventes polares.

Efecto de las sales A bajas concentraciones, las sales favorecen la solubilidad de muchas proteínas, debido a la interacción de los iones inorgánicos con los grupos ionizados de las moléculas proteicas. Sin embargo, a altas concentraciones de sal, los iones atraen demasiadas moléculas de agua, quitándole a la proteína su cubierta hidratante. Esto disminuye la solubilidad de la proteína. Efecto del p. H Cuando una proteína se encuentra en un medio cuyo p. H es igual a su punto isoeléctrico (la proteína no presenta carga neta) su solubilidad es mínima.
Clasificación de las proteínas • Albúminas Proteínas Simples • Globulinas • Histonas • Escleroproteínas • Nucleoproteínas • Cromoproteínas Proteínas Conjugadas (Apoproteína + Grupos Prostético) • Glicoproteínas • Fosfoproteínas • Lipoproteínas • Metaloproteínas
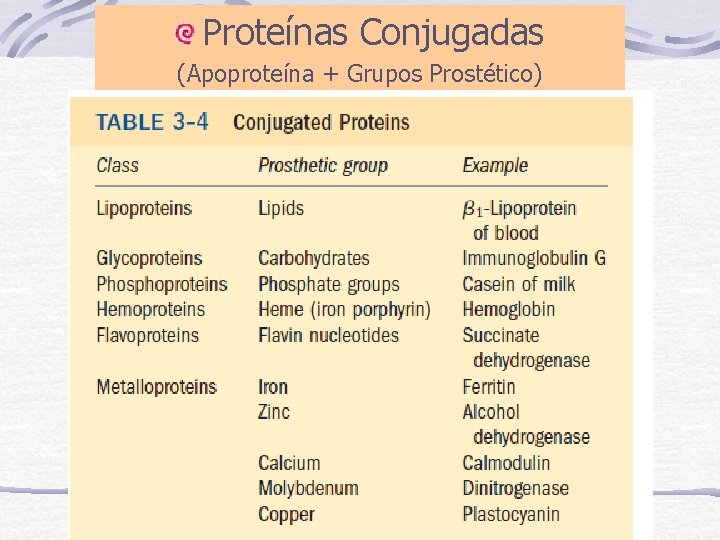
Proteínas Conjugadas (Apoproteína + Grupos Prostético)
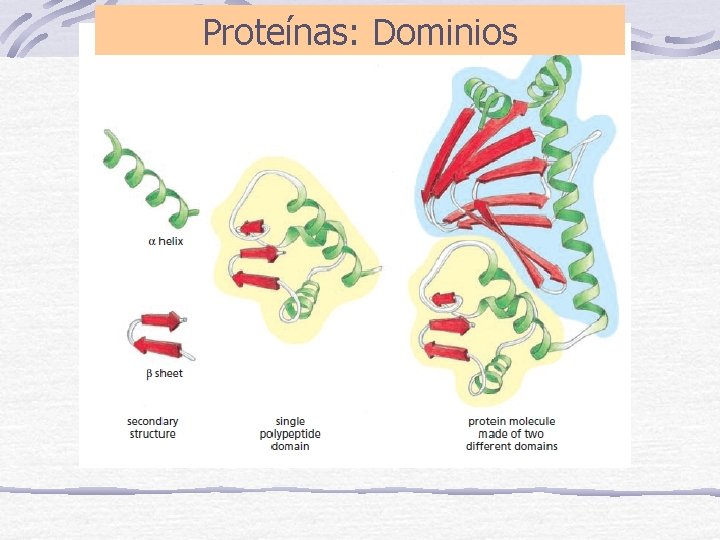
Proteínas: Dominios
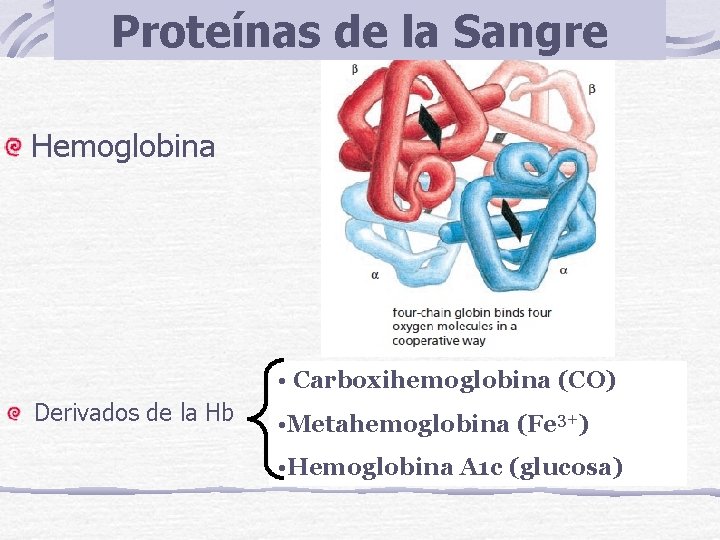
Proteínas de la Sangre Hemoglobina • Carboxihemoglobina (CO) Derivados de la Hb • Metahemoglobina (Fe 3+) • Hemoglobina A 1 c (glucosa)
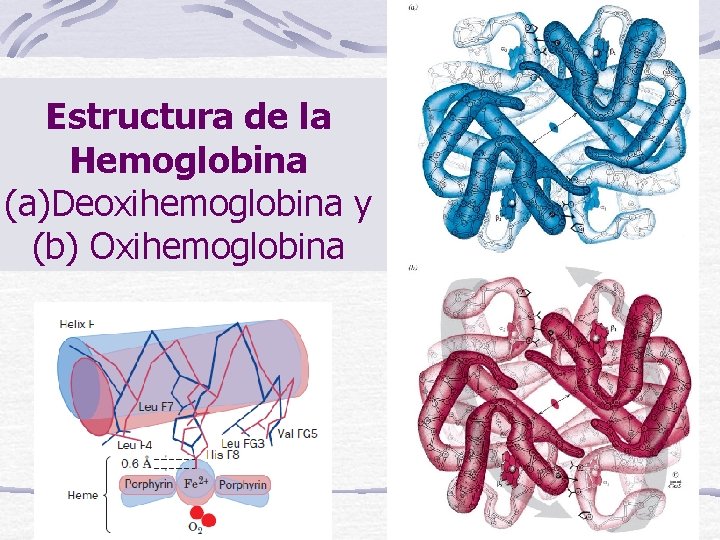
Estructura de la Hemoglobina (a)Deoxihemoglobina y (b) Oxihemoglobina

Digestión y Absorción de Proteínas
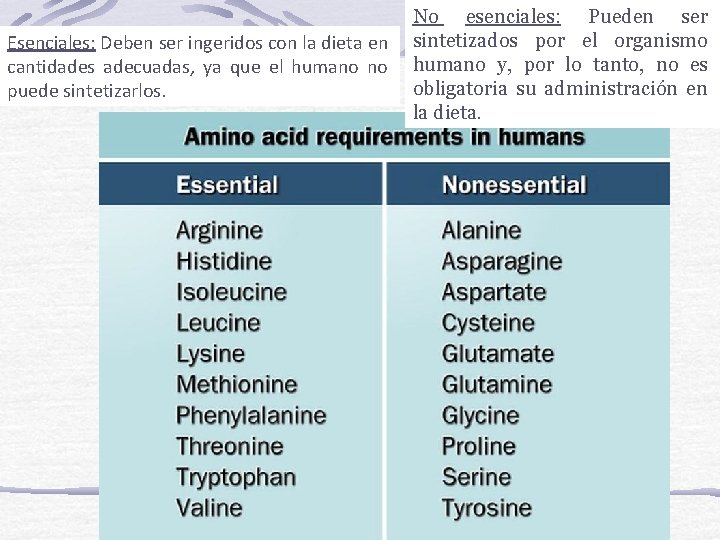
Esenciales: Deben ser ingeridos con la dieta en cantidades adecuadas, ya que el humano no puede sintetizarlos. No esenciales: Pueden ser sintetizados por el organismo humano y, por lo tanto, no es obligatoria su administración en la dieta.
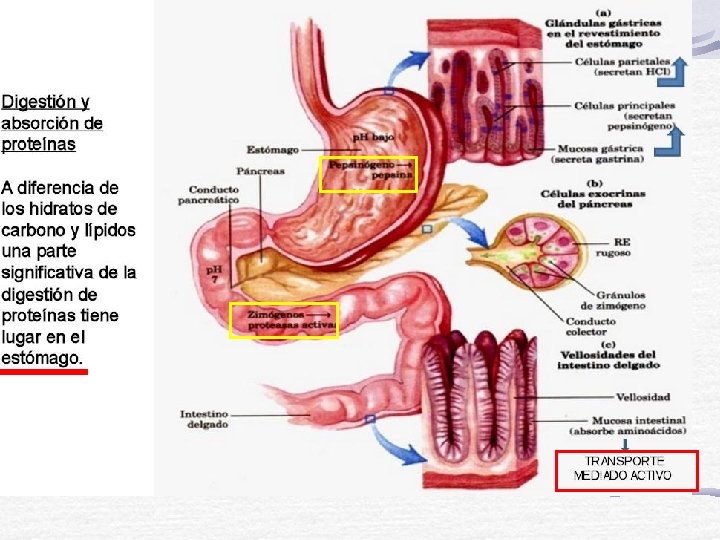

Digestión Estomago se produce: HCl 1. Pepsinógeno----------- Pepsina PEPSINA: su actividad máxima es a p. H 2 -3 y se inactiva a p. H=5 Gran capacidad para digerir el colágeno de las carnes
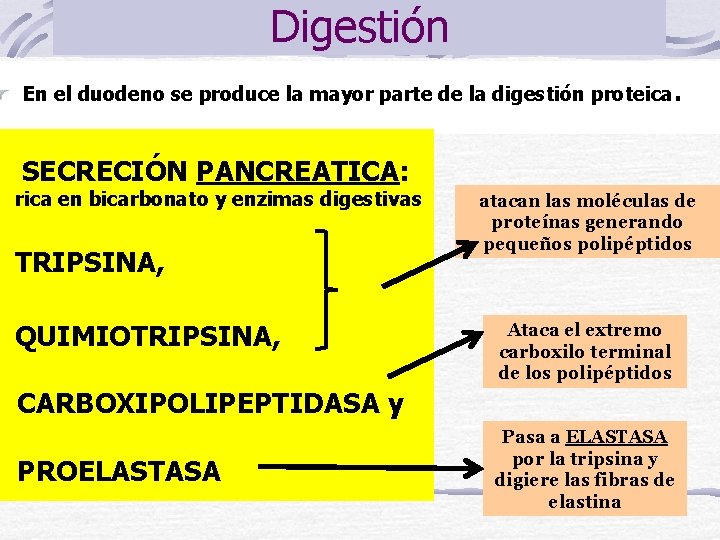
Digestión En el duodeno se produce la mayor parte de la digestión proteica. SECRECIÓN PANCREATICA: rica en bicarbonato y enzimas digestivas TRIPSINA, QUIMIOTRIPSINA, atacan las moléculas de proteínas generando pequeños polipéptidos Ataca el extremo carboxilo terminal de los polipéptidos CARBOXIPOLIPEPTIDASA y PROELASTASA Pasa a ELASTASA por la tripsina y digiere las fibras de elastina
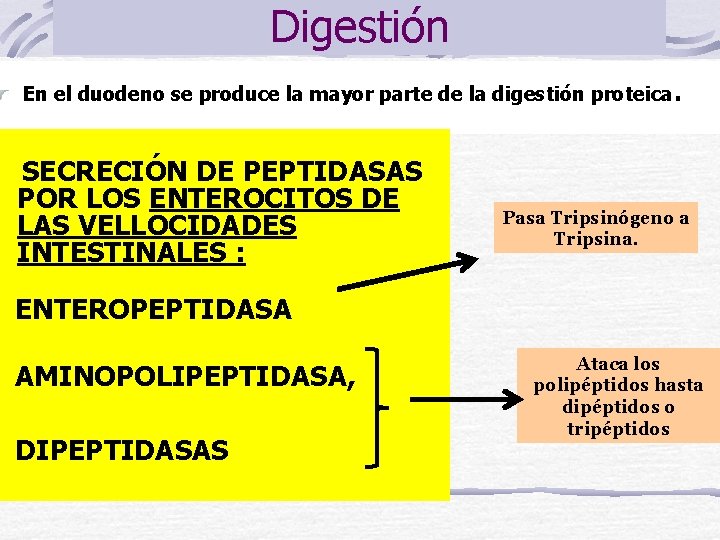
Digestión En el duodeno se produce la mayor parte de la digestión proteica. SECRECIÓN DE PEPTIDASAS POR LOS ENTEROCITOS DE LAS VELLOCIDADES INTESTINALES : Pasa Tripsinógeno a Tripsina. ENTEROPEPTIDASA AMINOPOLIPEPTIDASA, DIPEPTIDASAS Ataca los polipéptidos hasta dipéptidos o tripéptidos

Digestión En el duodeno hay una cascada de activación de las enzimas Enteropeptidasa 1. Tripsinógeno------------ Tripsina 2. Quimotripsinógeno ----------- Quimotripsina Tripsina 3. Procarboxipeptidasa A y B ------- Carboxipeptidasa A y B Tripsina 4. Proelastasa --------- Elastasa
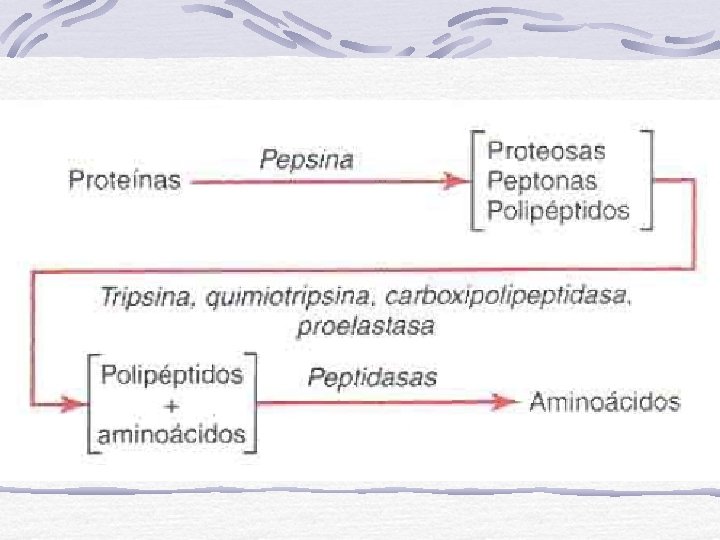

Digestión II Las proteínas parcialmente hidrolizadas en las luz del intestino penetran en el interior de las células del enterocito como oligopéptidos donde son atacados por enzimas peptidasas y aminopeptidasas y se convierten en aminoácidos libres.

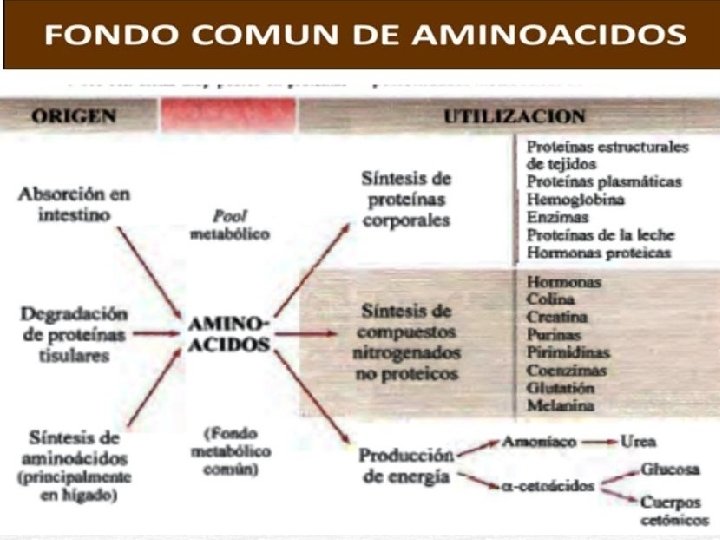
Destino de los aminoácidos
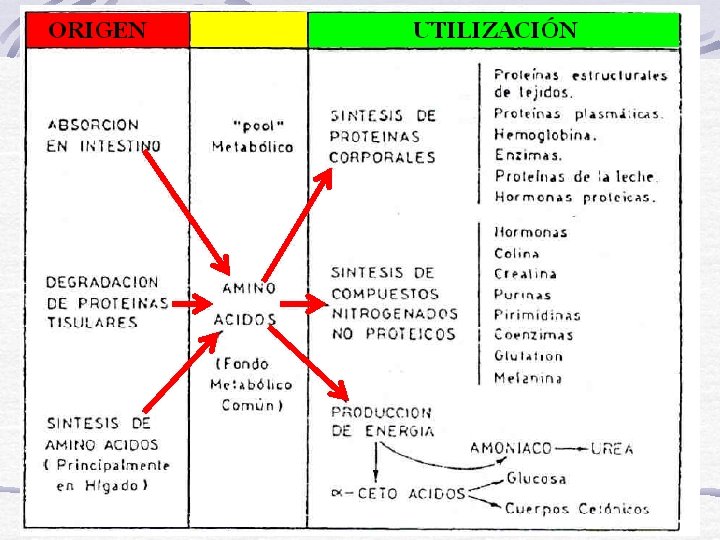
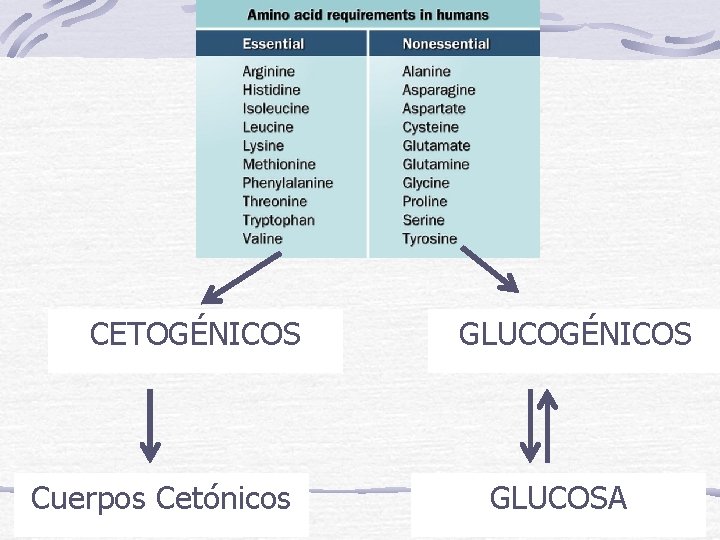
CETOGÉNICOS Cuerpos Cetónicos GLUCOGÉNICOS GLUCOSA

Alguna pregunta?
- Slides: 66