La chimie organique les hydrocarbures I Dfinition 1

La chimie organique : les hydrocarbures I. Définition 1. La chimie organique est la chimie des composés du carbone végétaux Les et les constituent les matières premières combustibles fossiles de la chimie organique.
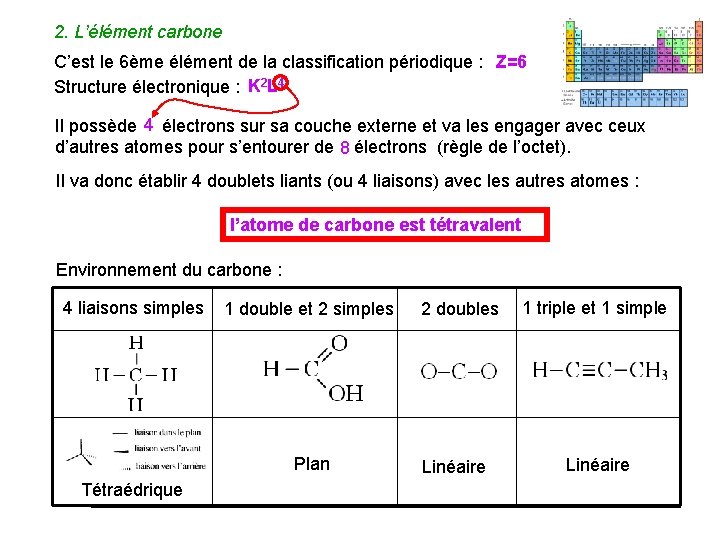
2. L’élément carbone C’est le 6ème élément de la classification périodique : Z=6 Structure électronique : K 2 L 4 4 Il possède électrons sur sa couche externe et va les engager avec ceux d’autres atomes pour s’entourer de électrons (règle de l’octet). 8 Il va donc établir 4 doublets liants (ou 4 liaisons) avec les autres atomes : l’atome de carbone est tétravalent Environnement du carbone : 4 liaisons simples 1 double et 2 simples Plan Tétraédrique 2 doubles Linéaire 1 triple et 1 simple Linéaire
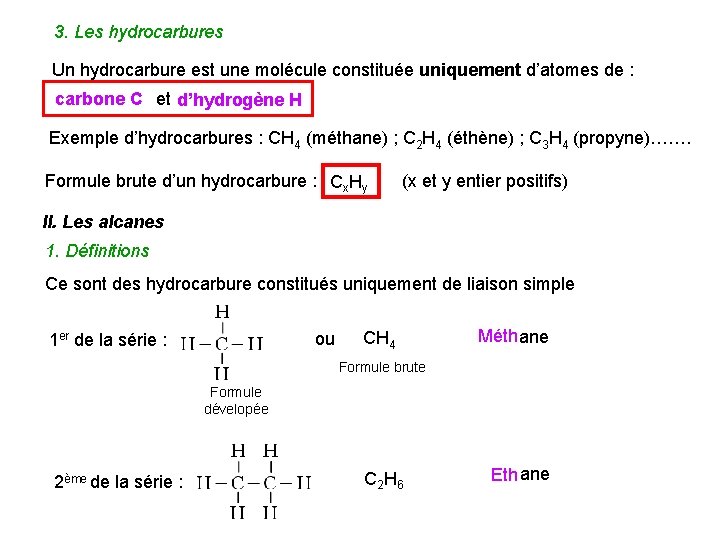
3. Les hydrocarbures Un hydrocarbure est une molécule constituée uniquement d’atomes de : carbone C et d’hydrogène H Exemple d’hydrocarbures : CH 4 (méthane) ; C 2 H 4 (éthène) ; C 3 H 4 (propyne)……. Formule brute d’un hydrocarbure : Cx. Hy (x et y entier positifs) II. Les alcanes 1. Définitions Ce sont des hydrocarbure constitués uniquement de liaison simple ou 1 er de la série : CH 4 Méthane Formule brute Formule dévelopée 2ème de la série : C 2 H 6 Eth ane
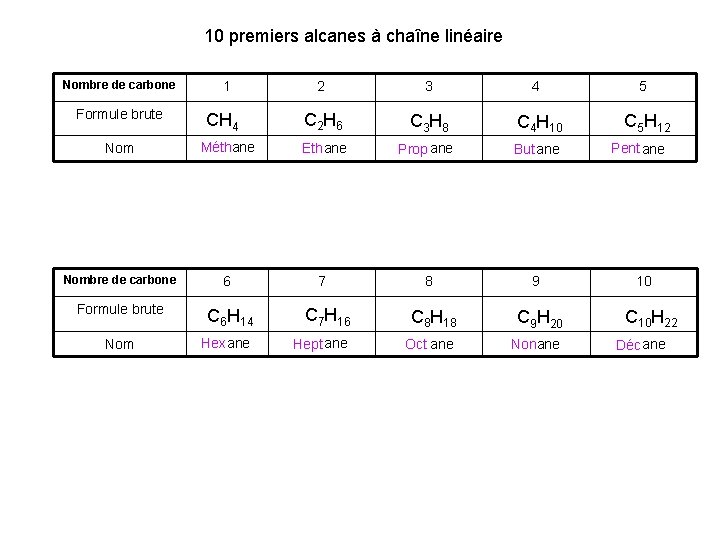
10 premiers alcanes à chaîne linéaire Nombre de carbone 1 2 3 4 5 C 5 H 12 Formule brute CH 4 C 2 H 6 C 3 H 8 C 4 H 10 Nom Méthane Eth ane Prop ane But ane Nombre de carbone 6 7 8 9 Formule brute C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 Hex ane Hept ane Oct ane Nonane Nom Pent ane 10 C 10 H 22 Déc ane
Prop Pent Méth Hept Oct Hex But Eth Non Déc 3 8 4 1 5 10 6 2 7 9
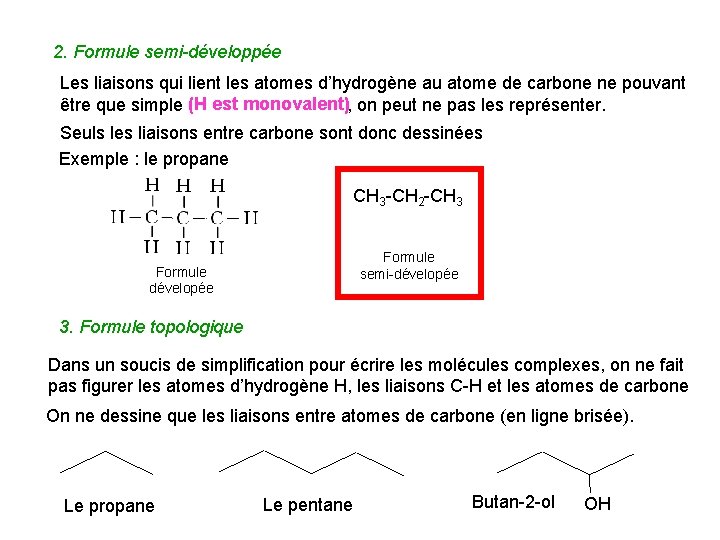
2. Formule semi-développée Les liaisons qui lient les atomes d’hydrogène au atome de carbone ne pouvant (H est monovalent) être que simple , on peut ne pas les représenter. Seuls les liaisons entre carbone sont donc dessinées Exemple : le propane CH 3 -CH 2 -CH 3 Formule semi-dévelopée Formule dévelopée 3. Formule topologique Dans un soucis de simplification pour écrire les molécules complexes, on ne fait pas figurer les atomes d’hydrogène H, les liaisons C-H et les atomes de carbone On ne dessine que les liaisons entre atomes de carbone (en ligne brisée). Le propane Le pentane Butan-2 -ol OH
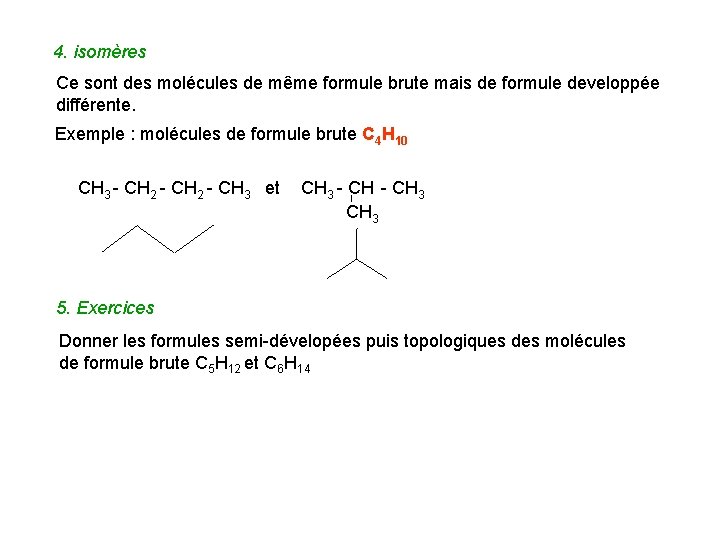
4. isomères Ce sont des molécules de même formule brute mais de formule developpée différente. Exemple : molécules de formule brute C 4 H 10 CH 3 - CH 2 - CH 3 et CH 3 - CH 3 5. Exercices Donner les formules semi-dévelopées puis topologiques des molécules de formule brute C 5 H 12 et C 6 H 14

6. Nomenclature Ce sont des règles internationales qui permettent de nommer sans ambiguïté les hydrocarbures. Exemple : nommer l’alcane de formule Règle IUPAC n° 1 : Repérer et nommer la chaîne la plus longue que l'on puisse trouver au sein de la molécule. Règle IUPAC n° 2 : Numéroter les carbones de la chaîne la plus longue en commençant par l'extrémité la plus proche d'un substituant. 2 1 5 3 4 6 4 5 6 Substituants sur le carbone 3 3 2 1 Substituants sur le carbone 4
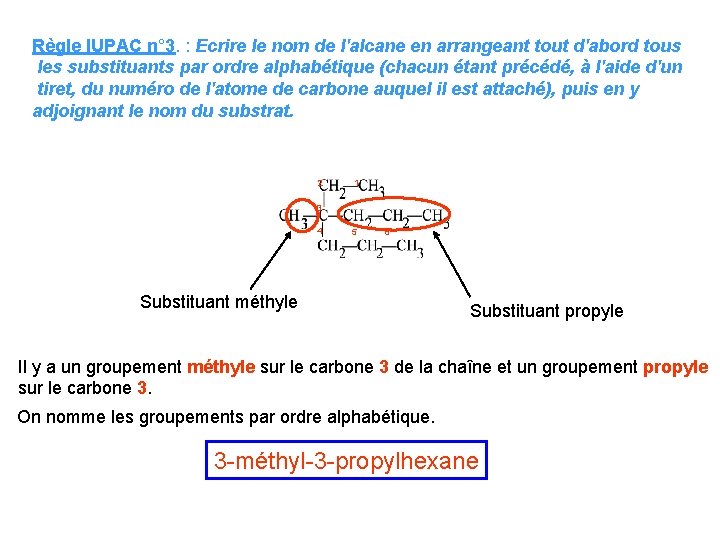
Règle IUPAC n° 3. : Ecrire le nom de l'alcane en arrangeant tout d'abord tous les substituants par ordre alphabétique (chacun étant précédé, à l'aide d'un tiret, du numéro de l'atome de carbone auquel il est attaché), puis en y adjoignant le nom du substrat. 2 1 3 4 5 6 Substituant méthyle Substituant propyle Il y a un groupement méthyle sur le carbone 3 de la chaîne et un groupement propyle sur le carbone 3. On nomme les groupements par ordre alphabétique. 3 -méthyl-3 -propylhexane

II. Les alcènes 1. Définitions Ce sont des hydrocarbures qui possèdent au minimum une double liaisons entre deux carbones (C=C) 1 er de la série : H 2 C=CH 2 éthène 2ème de la série : H 2 C=CH-CH 3 propène 3ème de la série : H 2 C=CH-CH 2 -CH 3 ou H 3 C-CH=CH-CH 3 Règle n° 1 : Recher la plus longue chaîne qui contient le groupe fonctionnel, c'est à dire la double liaison C=C. H 2 C=CH-CH 2 -CH 3 H 3 C-CH=CH-CH 3
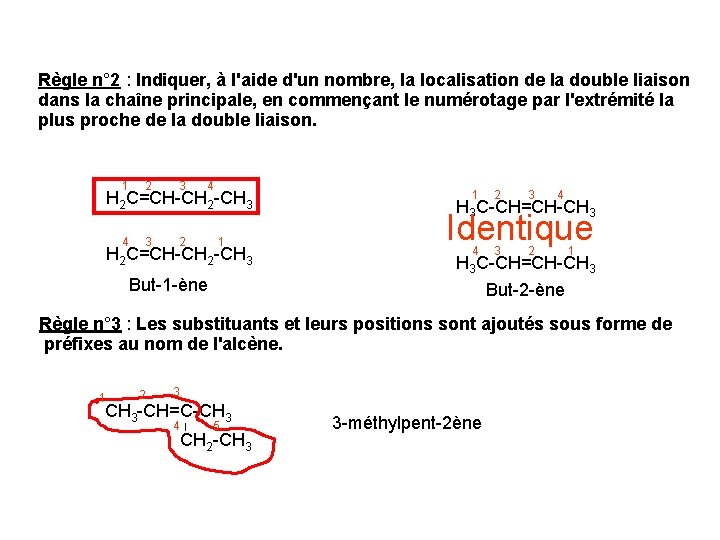
Règle n° 2 : Indiquer, à l'aide d'un nombre, la localisation de la double liaison dans la chaîne principale, en commençant le numérotage par l'extrémité la plus proche de la double liaison. 1 2 3 4 H 2 C=CH-CH 2 -CH 3 4 3 2 1 H 2 C=CH-CH 2 -CH 3 But-1 -ène 1 2 3 4 H 3 C-CH=CH-CH 3 Identique 4 3 2 1 H 3 C-CH=CH-CH 3 But-2 -ène Règle n° 3 : Les substituants et leurs positions sont ajoutés sous forme de préfixes au nom de l'alcène. 1 2 3 CH 3 -CH=C-CH 3 4 5 CH 2 -CH 3 3 -méthylpent-2ène
- Slides: 11