La chimica del Carbonio Le sostanze organiche v

La chimica del Carbonio Le sostanze organiche v Composti binari o idrocarburi: contengono solo C e H: alcani, alcheni, alchini e idrocarburi aromatici; v Composti ternari: contengono tre elementi che possono variare 1
2
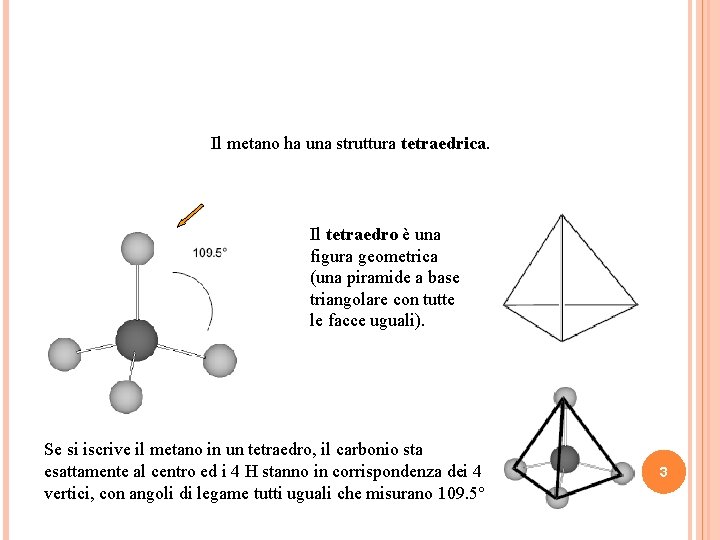
Il metano ha una struttura tetraedrica. Il tetraedro è una figura geometrica (una piramide a base triangolare con tutte le facce uguali). Se si iscrive il metano in un tetraedro, il carbonio sta esattamente al centro ed i 4 H stanno in corrispondenza dei 4 vertici, con angoli di legame tutti uguali che misurano 109. 5° 3
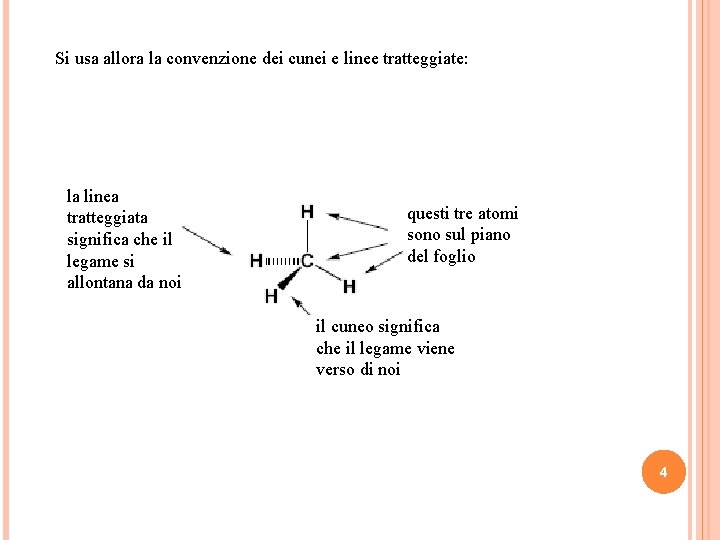
Si usa allora la convenzione dei cunei e linee tratteggiate: la linea tratteggiata significa che il legame si allontana da noi questi tre atomi sono sul piano del foglio il cuneo significa che il legame viene verso di noi 4
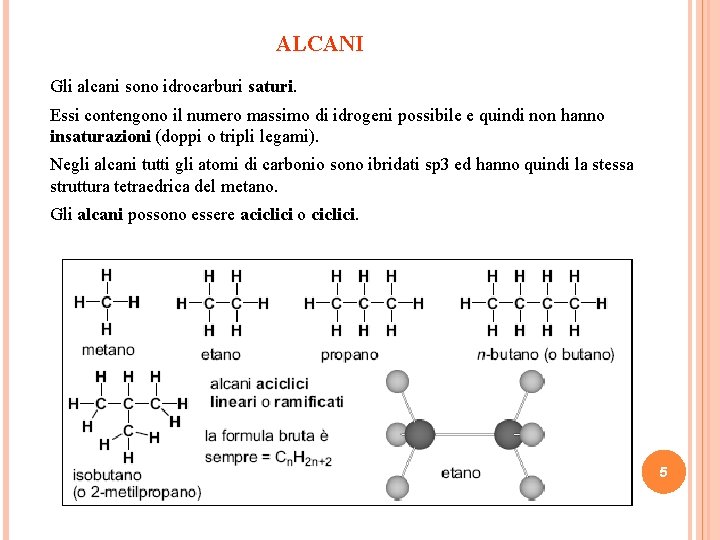
ALCANI Gli alcani sono idrocarburi saturi. Essi contengono il numero massimo di idrogeni possibile e quindi non hanno insaturazioni (doppi o tripli legami). Negli alcani tutti gli atomi di carbonio sono ibridati sp 3 ed hanno quindi la stessa struttura tetraedrica del metano. Gli alcani possono essere aciclici o ciclici. 5
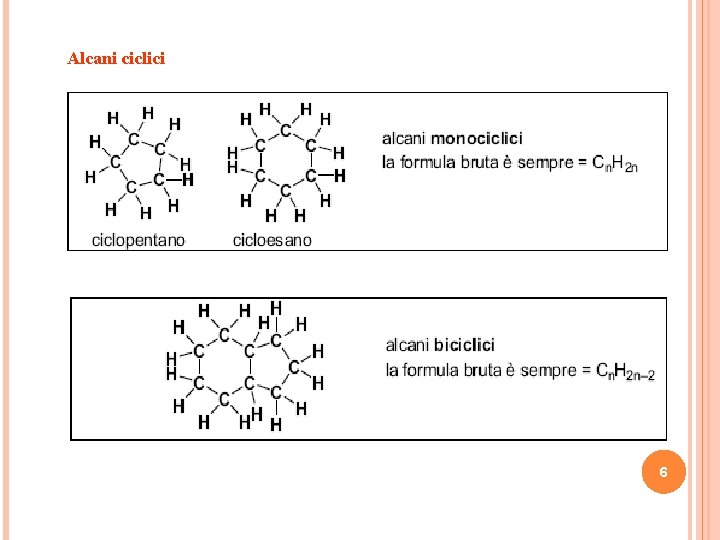
Alcani ciclici 6
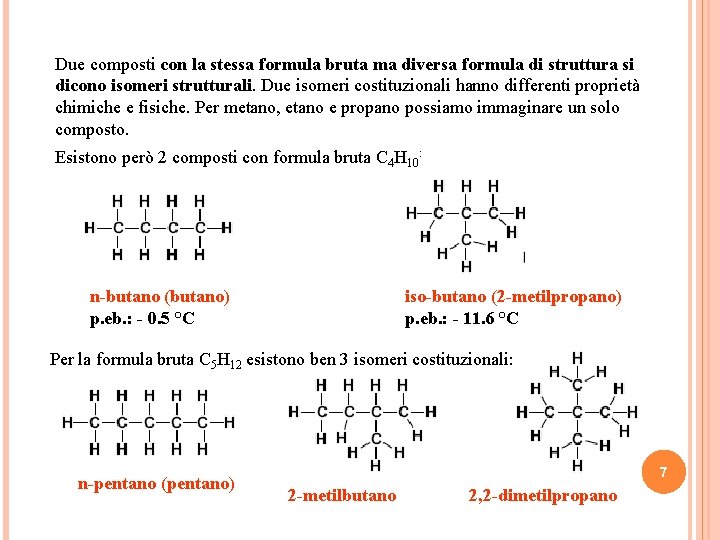
Due composti con la stessa formula bruta ma diversa formula di struttura si dicono isomeri strutturali. Due isomeri costituzionali hanno differenti proprietà chimiche e fisiche. Per metano, etano e propano possiamo immaginare un solo composto. Esistono però 2 composti con formula bruta C 4 H 10: n-butano (butano) p. eb. : - 0. 5 °C iso-butano (2 -metilpropano) p. eb. : - 11. 6 °C Per la formula bruta C 5 H 12 esistono ben 3 isomeri costituzionali: n-pentano (pentano) 7 2 -metilbutano 2, 2 -dimetilpropano

Il numero di isomeri aumenta vertiginosamente al crescere del numero di atomi di carbonio: abbiamo 5 isomeri con 6 C, 75 isomeri con 10 C. Con 30 atomi di carbonio gli isomeri possibili sono addirittura 4 x 109 8

Classificazione degli atomi di carbonio Gli atomi di carbonio sono classificati (primario, secondario, terziario, quaternario) in base al numero di carboni a cui sono legati: 9
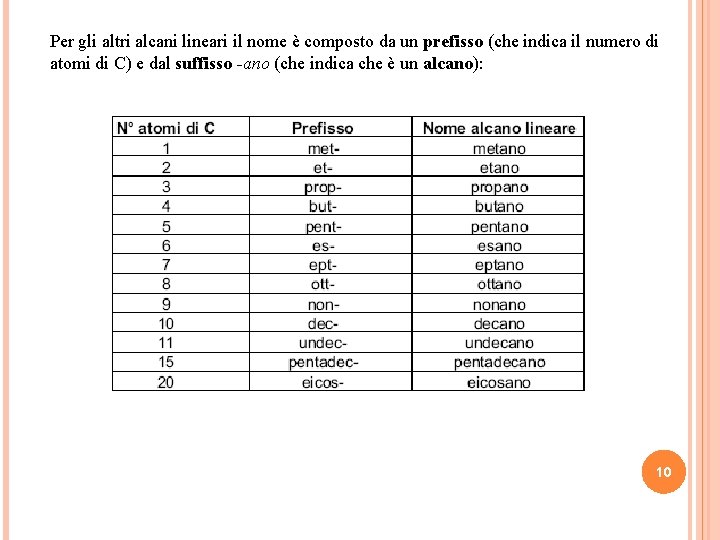
Per gli altri alcani lineari il nome è composto da un prefisso (che indica il numero di atomi di C) e dal suffisso -ano (che indica che è un alcano): 10

Quando gli alcani fungono da sostituenti essi vengono denominati sostituendo il suffisso ano con il suffisso -il. Sono chiamati gruppi alchilici. -CH 3 metil -CH 2 -CH 3 propil CH 3 -CH-CH 3 isopropil 11
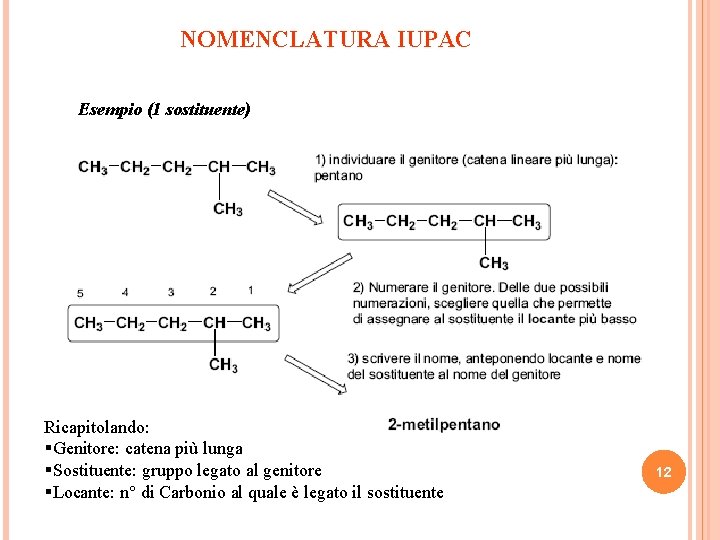
NOMENCLATURA IUPAC Esempio (1 sostituente) Ricapitolando: §Genitore: catena più lunga §Sostituente: gruppo legato al genitore §Locante: n° di Carbonio al quale è legato il sostituente 12

Esempio (più sostituenti uguali) Esempio (più sostituenti diversi) 13
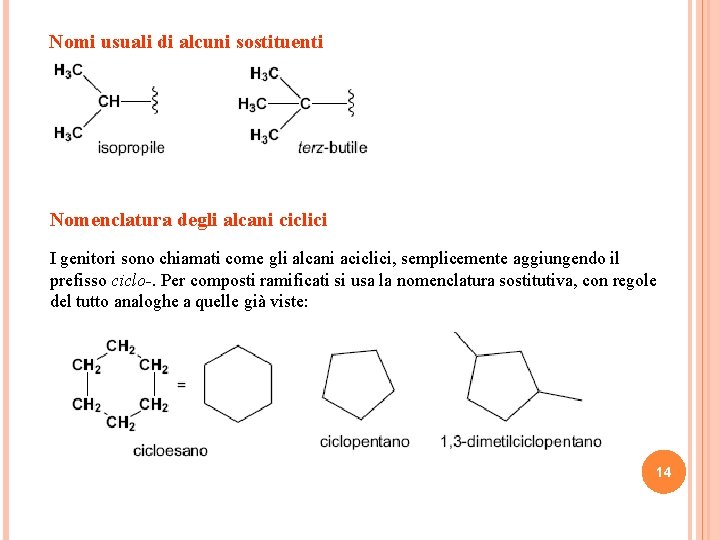
Nomi usuali di alcuni sostituenti Nomenclatura degli alcani ciclici I genitori sono chiamati come gli alcani aciclici, semplicemente aggiungendo il prefisso ciclo-. Per composti ramificati si usa la nomenclatura sostitutiva, con regole del tutto analoghe a quelle già viste: 14
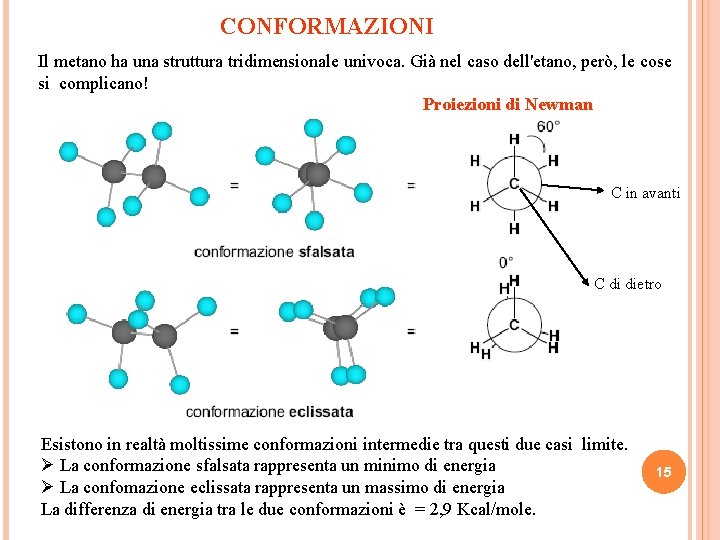
CONFORMAZIONI Il metano ha una struttura tridimensionale univoca. Già nel caso dell'etano, però, le cose si complicano! Proiezioni di Newman C in avanti C di dietro Esistono in realtà moltissime conformazioni intermedie tra questi due casi limite. Ø La conformazione sfalsata rappresenta un minimo di energia Ø La confomazione eclissata rappresenta un massimo di energia La differenza di energia tra le due conformazioni è = 2, 9 Kcal/mole. 15
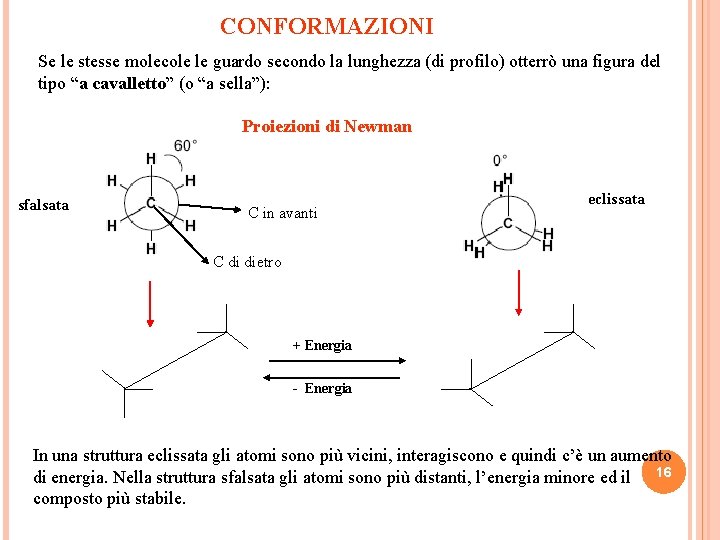
CONFORMAZIONI Se le stesse molecole le guardo secondo la lunghezza (di profilo) otterrò una figura del tipo “a cavalletto” (o “a sella”): Proiezioni di Newman sfalsata C in avanti eclissata C di dietro + Energia - Energia In una struttura eclissata gli atomi sono più vicini, interagiscono e quindi c’è un aumento di energia. Nella struttura sfalsata gli atomi sono più distanti, l’energia minore ed il 16 composto più stabile.

La conformazione sfalsata e quella eclissata sono due composti distinti (due isomeri)? La risposta è NO. Le due conformazioni si interconvertono molto velocemente. La velocità di una qualunque trasformazione dipende dalla barriera energetica che deve essere superata. Quando la barriera è < 18 -20 Kcal/mole circa, l'interconversione è molto rapida e le strutture non possono essere separate. Due strutture differenziate solo da rotazione di uno o più legami sono dette conformeri quando la loro interconversione è molto rapida. CONFORMERI DEI CICLOALCANI Il ciclopropano. E‘ molto meno stabile di altri alcani perché: a) gli angoli di legame sono 60° anziché 109, 5° b) tutti i legami sono eclissati 17

I sistemi ciclici più stabili (e pertanto più importanti) sono quelli a 5 e 6 termini: Come si calcola l’angolo di legame di una molecola planare? [180 * (n-2)]/n (con n = numero di angoli presenti nel ciclo) quindi: [180 * (5 -2)]/5 = 108°, ossia molto vicino all’angolo tetraedrico ideale. Tuttavia il ciclopentano preferisce conformazioni non planari, per evitare l'eclissamento dei legami. Se fosse planare, l'angolo di legame sarebbe = 120° Il cicloesano preferisce conformazioni non planari sia per evitare l'eclissamento, che per avere angoli di legame pari a 109. 5°. Il cicloesano è l'alcano ciclico più stabile in assoluto. TEORIA DI BAYER: Più l’angolo di legame si discosta da 109°, maggiore è l’instabilità del composto. Inoltre, dal ciclo-esano in su aumentando gli atomi di C aumentano i gradi di libertà del composto, pertanto la struttura ciclica può essere distorta con maggiore facilità e minore 18 consumo di energia, per cui è più stabile.
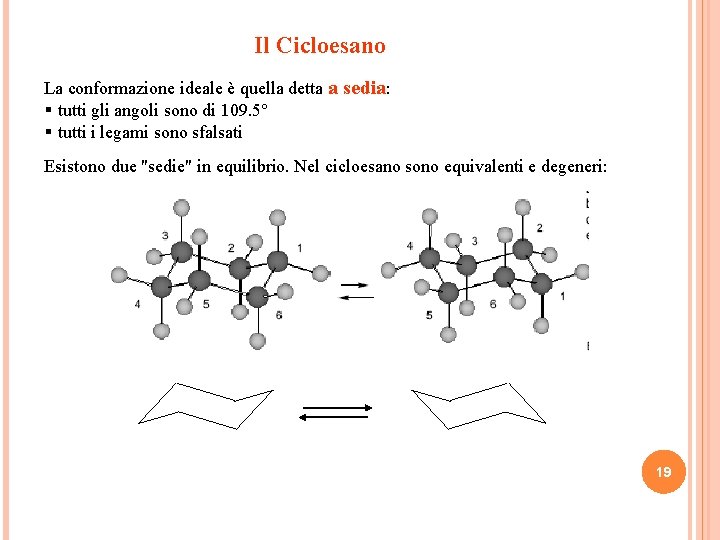
Il Cicloesano La conformazione ideale è quella detta a sedia: § tutti gli angoli sono di 109. 5° § tutti i legami sono sfalsati Esistono due "sedie" in equilibrio. Nel cicloesano sono equivalenti e degeneri: 19
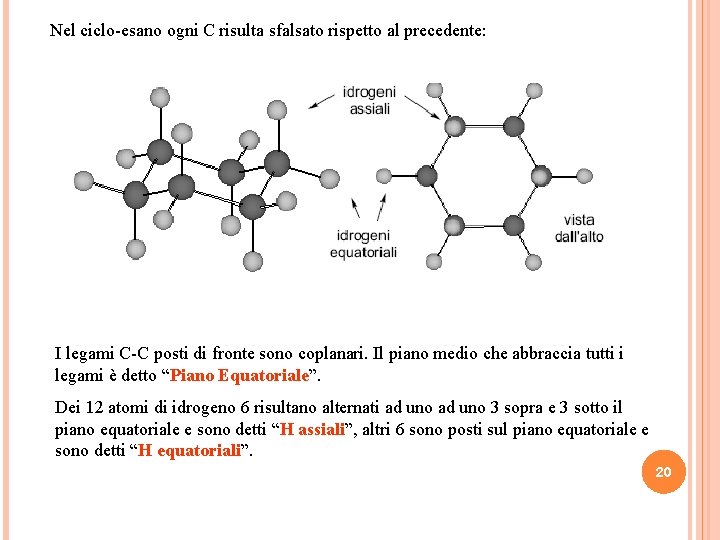
Nel ciclo-esano ogni C risulta sfalsato rispetto al precedente: I legami C-C posti di fronte sono coplanari. Il piano medio che abbraccia tutti i legami è detto “Piano Equatoriale”. Dei 12 atomi di idrogeno 6 risultano alternati ad uno 3 sopra e 3 sotto il piano equatoriale e sono detti “H assiali”, altri 6 sono posti sul piano equatoriale e sono detti “H equatoriali”. 20
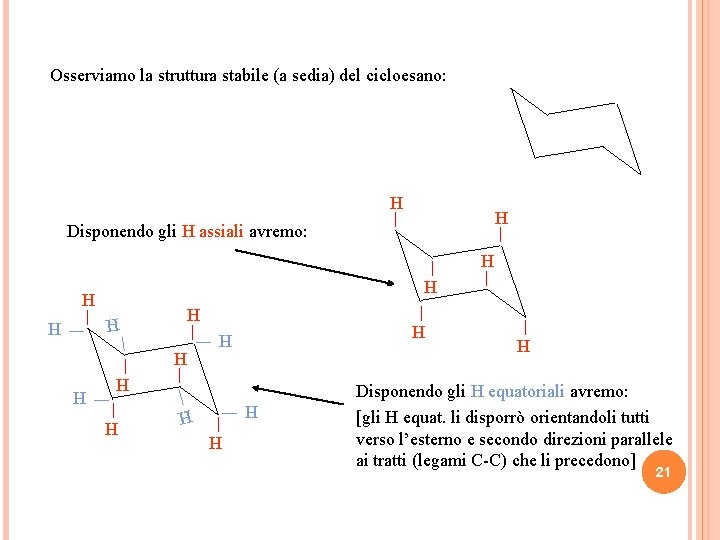
Osserviamo la struttura stabile (a sedia) del cicloesano: H H Disponendo gli H assiali avremo: H H H H Disponendo gli H equatoriali avremo: [gli H equat. li disporrò orientandoli tutti verso l’esterno e secondo direzioni parallele ai tratti (legami C-C) che li precedono] 21 H H
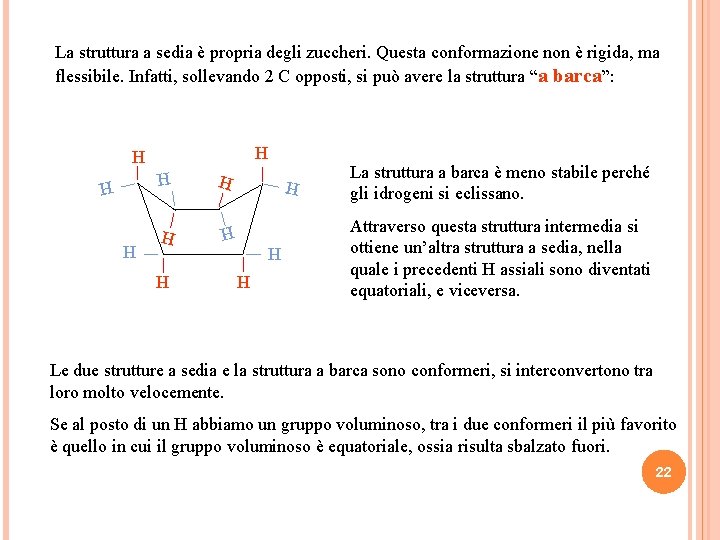
La struttura a sedia è propria degli zuccheri. Questa conformazione non è rigida, ma flessibile. Infatti, sollevando 2 C opposti, si può avere la struttura “a barca”: H H H H La struttura a barca è meno stabile perché gli idrogeni si eclissano. Attraverso questa struttura intermedia si ottiene un’altra struttura a sedia, nella quale i precedenti H assiali sono diventati equatoriali, e viceversa. H H Le due strutture a sedia e la struttura a barca sono conformeri, si interconvertono tra loro molto velocemente. Se al posto di un H abbiamo un gruppo voluminoso, tra i due conformeri il più favorito è quello in cui il gruppo voluminoso è equatoriale, ossia risulta sbalzato fuori. 22
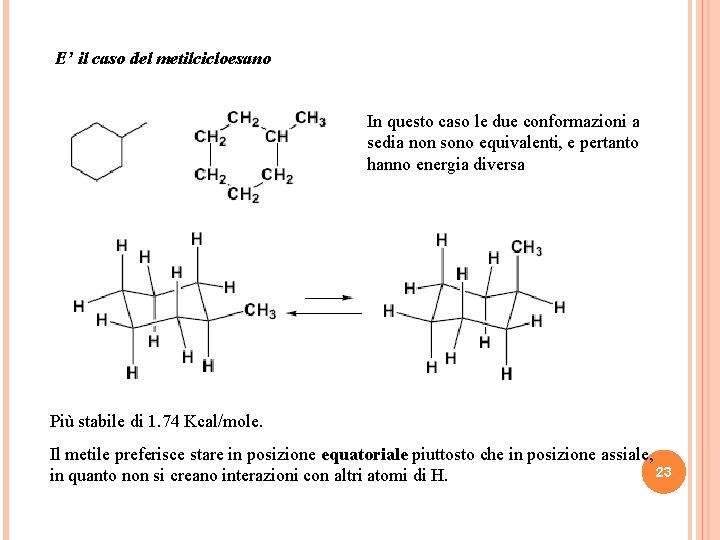
E’ il caso del metilcicloesano In questo caso le due conformazioni a sedia non sono equivalenti, e pertanto hanno energia diversa Più stabile di 1. 74 Kcal/mole. Il metile preferisce stare in posizione equatoriale piuttosto che in posizione assiale, 23 in quanto non si creano interazioni con altri atomi di H.
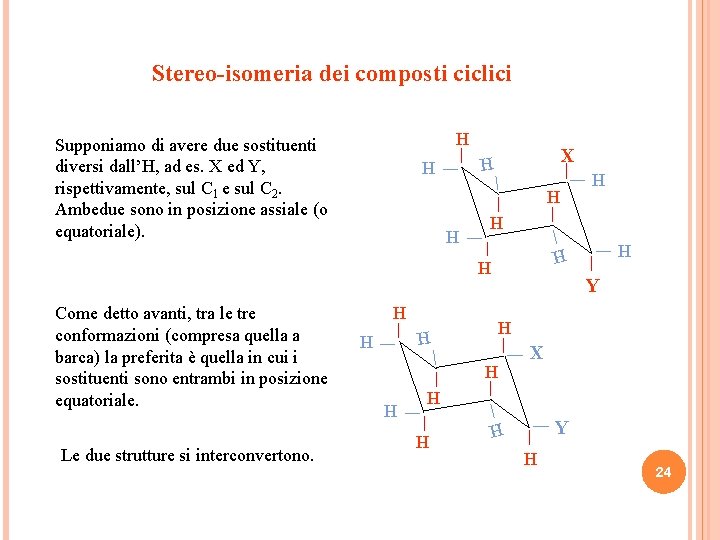
Stereo-isomeria dei composti ciclici H X H H H H H Y H H H Le due strutture si interconvertono. H Y X Come detto avanti, tra le tre conformazioni (compresa quella a barca) la preferita è quella in cui i sostituenti sono entrambi in posizione equatoriale. H H Supponiamo di avere due sostituenti diversi dall’H, ad es. X ed Y, rispettivamente, sul C 1 e sul C 2. Ambedue sono in posizione assiale (o equatoriale). H 24
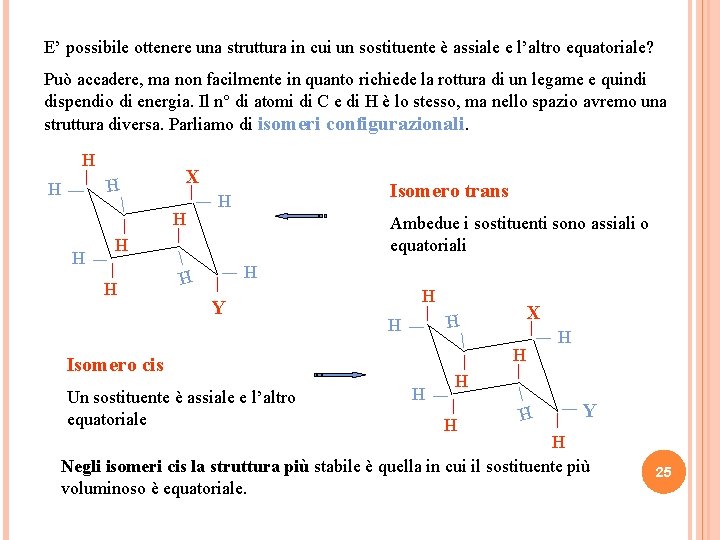
E’ possibile ottenere una struttura in cui un sostituente è assiale e l’altro equatoriale? Può accadere, ma non facilmente in quanto richiede la rottura di un legame e quindi dispendio di energia. Il n° di atomi di C e di H è lo stesso, ma nello spazio avremo una struttura diversa. Parliamo di isomeri configurazionali. X Ambedue i sostituenti sono assiali o equatoriali H H H H Isomero cis H Un sostituente è assiale e l’altro equatoriale X H H H Y H H H Isomero trans H H Y H Negli isomeri cis la struttura più stabile è quella in cui il sostituente più voluminoso è equatoriale. 25
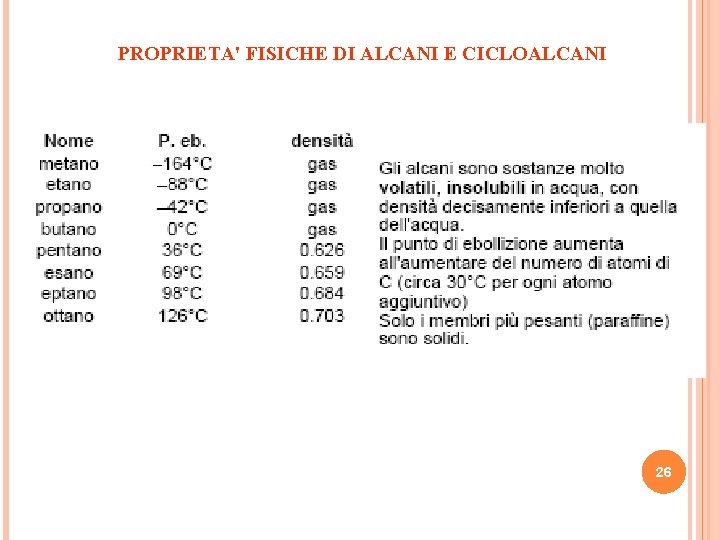
PROPRIETA' FISICHE DI ALCANI E CICLOALCANI 26

REAZIONI DEGLI ALCANI Gli alcani sono specie chimiche molto poco reattive e per tale proprietà sono detti “paraffine”. La reazione più importante degli alcani è la combustione, che segue le seguenti stechiometrie: CH 4 + 2 O 2 → CO 2 + 2 H 2 O Ma queste sono reazioni facili o difficili? Tutte le volte che scriviamo una reazione, dobbiamo considerare due aspetti: A) L'aspetto termodinamico B) L'aspetto cinetico 27

Reazione di Sostituzione negli Alcani: la Clorurazione Consideriamo una reazione qualsiasi di sostituzione: CH 4 + X → CH 3 X + H Perché avvenga questa generica reazione bisogna rompere prima il legame C-H il che richiede molta energia, la reazione infatti è endotermica e difficilmente si realizza. In condizioni opportune e secondo un particolare tipo di reazione però gli alcani possono reagire. Più esattamente si è osservato che: a) CH 4 + Cl 2 (in condizioni di buio) → b) CH 4 + Cl 2 (alla luce) → nessuna reazione CH 3 Cl + H Si è formato l’alcano clorurato, nel caso specifico il Clorometano. La stessa reazione si avrà trattando qualsiasi alcano con un alogeno che sia Cl, F e 28 Br.

§ Legame C - H = 96 Kcalorie/mole § Legame Cl - Cl = 58 Kcalorie/mole La radiazione nel caso della nostra reazione romperà prima il legame ad energia minore: Cl – Cl + h ν 2 Cl • (1) Si ha quindi la rottura del legame C-H ad opera del Cl • : H 3–C-H + Cl • HCl + • CH 3 + 20 Kcalorie (2) Il radicale • CH 3 possiede intorno a sé 7 elettroni, per cui ne richiede 1 per completare l’ottetto. Sono questi i cosiddetti gruppi “elettrofili”. Anche il Cl • tende a completare l’ottetto acquisendo 1 elettrone. Il gruppo radicale • CH 3 non può prendere l’elettrone da un’altra molecola di metano in quanto un radicale scomparirebbe, ma se ne formerebbe uno nuovo. E’ il secondo stadio della reazione: • CH 3 + Cl – Cl CH 3 Cl + Cl • (3) 29

Facendo la somma delle due reazioni parziali si ottiene: CH 4 + Cl 2 CH 3 Cl + HCl + x. Kcal La reazione globale è dunque formata da due reazioni parziali inscindibili: La reazione (1) Cl – Cl + h ν 2 Cl • Reazione di Iniziazione (1) le due fasi successive (2) e (3) H 3–C-H + Cl • HCl + • CH 3 + 20 Kcalorie • CH 3 + Cl – Cl CH 3 Cl + Cl • (2) Reazioni di Propagazione (3) cioè sia l’atomo di Cl • che il metile vengono continuamente rimessi in circolo. La reazione (2) è esotermica in quanto 96 Kcal vengono utilizzate per rompere in legame C-H, ma 116 Kcal vengono prodotte per la formazione del legame H-Cl. Anche la reazione (3) è leggermente esotermica, per cui in totale la reazione è fortemente esotermica. 30

E’ evidente che l’atomo di Cl • può riunirsi ad un altro atomo di Cl a dare Cl 2, oppure si possono avere reazioni del tipo: a) Cl • + Cl • Cl 2 b) • CH 3 + Cl • CH 3 - Cl c) • CH 3 + • CH 3 – CH 3 Tali reazioni non sono produttive per la reazione di partenza perché consumano i prodotti intermedi e quindi la bloccano. Per tale motivo vengono chiamate “Reazioni di Arresto”. In realtà la reazione non viene bloccata in quanto le quantità di radicali CH 3 e Cl sono molto piccole rispetto a quelle di CH 4 e Cl 2. Ovviamente, mano che la reazione di clorurazione va avanti e le quantità di CH 4 e Cl 2 diminuiscono, le tre reazioni di arresto diventano più probabili. Gli stessi sottoprodotti della reazione, ad es. la quantità di etano (CH 3 -CH 3), possono essere utilizzati come indici diagnostici dei meccanismi di reazione. 31

Tutti gli alcani reagiscono con Cl, F, e Br secondo il meccanismo illustrato, compresi i ciclo-alcani a 5 e 6 atomi di C. Consideriamo il propano CH 3 – CH 2 – CH 3 : CH 3 – CH 2 Cl 1 -cloropropano (1) CH 3 – CHCl – CH 3 2 -cloropropano (2) Tenendo conto del fattore probabilistico, ho 6 atomi di H all’estremità della molecola e solo 2 atomi di H al centro. Ci sono dunque 6 probabilità su 2 che si formi la molecola (1) rispetto alla molecola (2). Se andiamo a verificare tali quantità, scopriamo che in realtà si forma un po’ di più del prodotto (2) a spese del prodotto (1). Come si giustifica questo comportamento? 32

Perché un H terziario è strappato con maggiore velocità? La velocità di estrazione di un H terziario è maggiore perché il radicale terziario si rivela più stabile di un radicale secondario, e questo di un primario: CH 3 – CH 3 • radicale IIIario CH 3 CH – CH 3 • radicale IIario • CH 2 – CH 3 radicale Iario Il radicale terziario viene a trovarsi immerso in una nuvola di carica più densa, data dai legami intorno al C, rispetto al radicale secondario ed a quello primario. E’ come se ciascun C che circonda il C radicalico prendesse su di sé una frazione dell’elettrone di tale C. Per tale motivo, è chiaro allora che se i C ad assorbire la carica dell’elettrone spaiato sono tre, più velocemente tale carica viene delocalizzata ed il composto risultante è più stabile 33
- Slides: 33