Kvantnomehaniki model atoma Najprije je Luis de Broglie

Kvantno-mehanički model atoma • Najprije je Luis de Broglie napravio materija-talas hipotezu a onda su Erwin Schrodinger i Werner Heisenberg odvojeno jedan od drugog i na različite načine razvili novu teoriju o atomu. Iako sasvim različita ova dva pristupa su se pokazala sasvim kompatibilnim. • Nova teorija, nazvana KVANTNA MEHANIKA objedinjuje talas-čestica dualnost u jedinstvenu konzistentnu teoriju.

Valna/talasna priroda svjetlosti 1924. Louis de Broglie postavio hipotezu prema kojoj svaka čestica koja se kreće osim čestičnih ima i valna svojstva.

De Broglie-v talas/val Talasni paket : Sadrži broj talasa čija amplituda opisuje vjerovatnost nalaženja čestice na određenom mjestu. Gdje je : talasna dužina, h : Planck-ova konst. i m 0 : masa čestice. de Broglie-eva hipoteza (1924 njegova Ph. D teza za koju je 1929 dobio Nobel ovu nagradu Prema relaciji ekvivalencije mase i energije : Gdje je p : impuls i : frequencija. Korištenjem E = h , dobije se * http: //www. wikipedia. org/
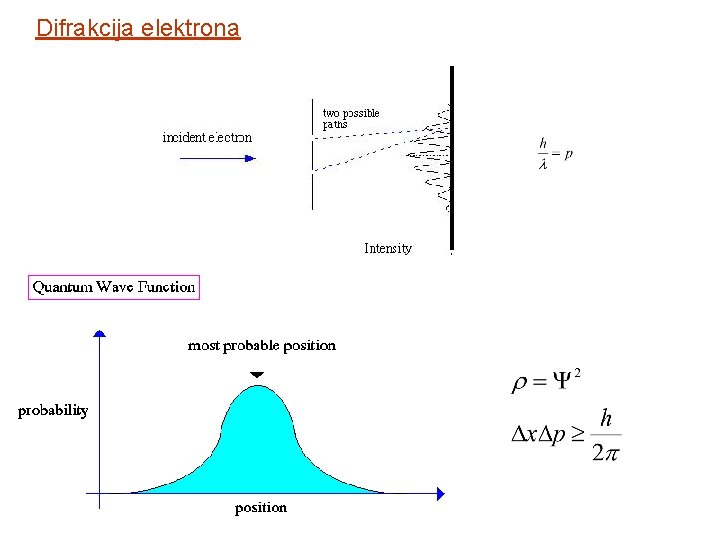
Difrakcija elektrona
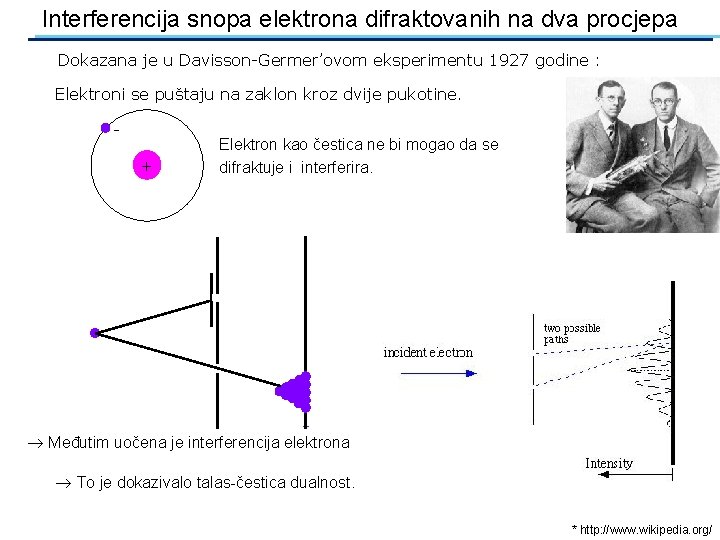
Interferencija snopa elektrona difraktovanih na dva procjepa Dokazana je u Davisson-Germer’ovom eksperimentu 1927 godine : Elektroni se puštaju na zaklon kroz dvije pukotine. + Elektron kao čestica ne bi mogao da se difraktuje i interferira. Međutim uočena je interferencija elektrona To je dokazivalo talas-čestica dualnost. * http: //www. wikipedia. org/

Gustoća vjerovatnosti (da česticu nađemo na nekom mjestu) Normiranje Valni broj

Schrödinger-ova jednačina. . Je uvedena 1926. g. kako bi se uveo elektron kao de Broglie-v talas : E : vlastita vrijednost energije : talasna funkcija Vjerovatnost nalaženja čestice * : compleksno konjugovana (tj. , z = x + iy and z* = x - iy) de Broglie-ev talas : normiranje operator

Schrödingerova jednačina
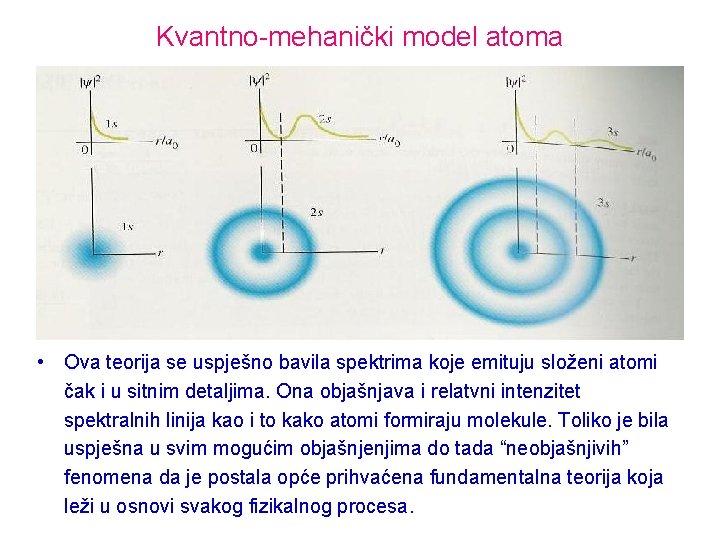
Kvantno-mehanički model atoma • Ova teorija se uspješno bavila spektrima koje emituju složeni atomi čak i u sitnim detaljima. Ona objašnjava i relatvni intenzitet spektralnih linija kao i to kako atomi formiraju molekule. Toliko je bila uspješna u svim mogućim objašnjenjima do tada “neobjašnjivih” fenomena da je postala opće prihvaćena fundamentalna teorija koja leži u osnovi svakog fizikalnog procesa.

Kvantno-mehanički model atoma • Po ovom modelu atoma elektroni ne postoje u jasno definiranim kružnim orbitama kao u Bohr-ovom modelu. Radi svoje valne prirode elektron predstavlja oblak negativnog naboja. Veličina i oblik elektronskog oblaka može da se izračuna za dato stanje atoma. Za osnovno stanje atoma vodonika elektronski oblak je sferno simetričan. Elektronski oblak ugrubo određuje “veličinu” atoma; ali baš kao što oblak nema preciznu granicu, tako ni atomi nemaju jasnu granicu niti dobro definiranu veličinu. Međutim, nemaju svi elektronski oblaci sferni oblik. Elektronski oblak

Elektronski oblak • Elektronski oblak može da se interpretira bilo kao čestica ili kao talas. Čestica je nešto mislimo da je lokalizovano u prostoru – ima tačno definirani položaj u svakom momentu. Nasuprot tome, talas je nešto se širi negdje u prostoru i elektronski oblak može tako da se interpretira. • Međutim, elektronski oblak može da se interpretira i kao raspodjela vjerovatnih položaja čestice. Ako bismo napravili 500 različitih mjerenja položaja elektrona posmatrajući ga kao česticu, većina rezultata bi pala u tačke velike vjerovatnosti (oblast veće gustine tačaka). • Ovdje ne možemo odrediti putanju po kojoj bi se elektron kretao. Samo možemo odrediti vjerovatnost njegovog nalaženja u raznim tačkama. Matematička vrijednost ove vjerovatnosti leži između 0 i 1. Ovdje 0 znači “nikad”, a 1 znači “uvijek”. Na primjer ako je vjerovatnost nalaženja elektrona u okviru nekog radijusa 0, 4, to znači 40% mogućnosti da se elektron nađe u tom ptostoru.

Kvantno-mehanički model atoma • Pojedinačni elektron može u raznim trenucima biti detektovan bilo gdje u ovom oblaku vjerovatnosti; on čak ima i izvjesnu, mada veoma malu, vjerovatnost da se nađe unutar jezgra. Međutim, najčešće se kroz proračun vjerovatnosti njegovog nalaženja na nekom mjestu, detektuje na mjestima koja su nagomilana oko udaljenosti od jezgra koja odgovara prvom Bohrovom radijusu i tu je elektronski oblak vodikovog atoma u osnovnom stanju najgušći. Elektronski oblak

Kvantni brojevi Rješavanje Schrodingerove jednačine (r, , )=R(r)Y( , ) nlm=Rnl Ylm Rješenje za vodikov atom (svojstvene vrijednosti): n - glavni kvantni broj; svi elektroni istog kvantnog broja n pripadaju istoj ljusci; n=1 K n=2 L n=3 M

l- orbitalni kvantni broj Bohrov model kružnih putanja ne može objasniti finu strukturu, ni Starkov ni Zeemanov efekt. Sommerfeld je proširio model na eliptički model atoma. Valna mehanika pokazuje, umjesto Bohrovog L=nħ, da je: Gdje orbitalni kvantni broj l može za određeni glavni kvantni broj n poprimiti ove vrijednosti: l=0, 1, 2. . . n-1 Orbitalni kvantni broj određuje moment količine gibanje. l=0 s l=1 p l=2 d Moguća stanja: 1 s, 2 p, 3 s, 3 p, 3 d. . .

ml - magnetni kvantni broj Elektron koji se oko jezgre čini zatvorenu strujnu petlju određenog magnetskog momenta. Pretpostavimo da je staza kružnica polumjera r: Ako imamo vanjsko magnetsko polje u smjeru z-osi, slijedi: ml je magnetni kvantni broj. Za određeni l magnetni kvantni broj može poprimiti 2 l+1 cjelobrojnih vrijednosti između –l i l, tj. ml=0, 1, 2, . . . , ± l
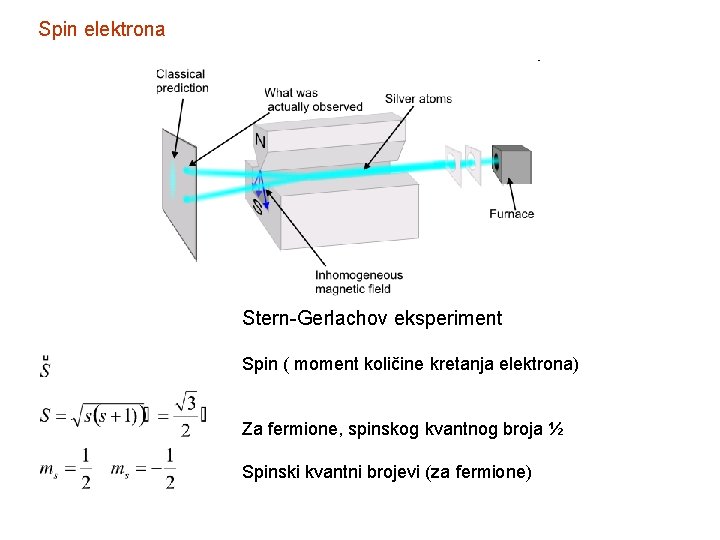
Spin elektrona Stern-Gerlachov eksperiment Spin ( moment količine kretanja elektrona) Za fermione, spinskog kvantnog broja ½ Spinski kvantni brojevi (za fermione)

Ukupni moment količine kretanja: Russel-Sandersovo vezanje 1. Kretanje elektrona u atomu određeno je sa četiri kvantna broja. 2. U elektronskom omotaču elektroni su raspoređeni po tzv. Paulijevom principu isključenja. Taj princip kaže da dva elektrona u atomu ne mogu imati sva četiri kvantna broja jednaka.

Cijepanje spektralnih linija kada se atomi koji emitiraju svjetlost nalaze u magnetnom polju opazio je 1896. Zeeman. Cijepanje energetskih nivoa u magnetnom polju (EB= z. B) uzrokuje cijepanje spektralnih linija tj. Nastaje Zeemanov efekt.
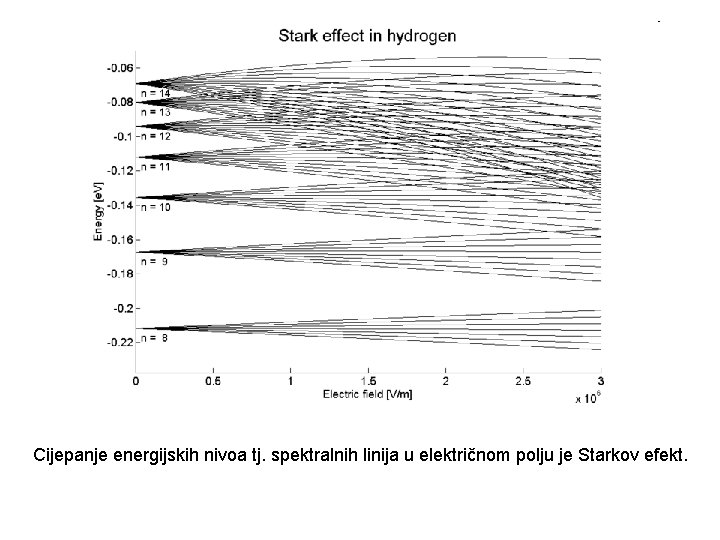
Cijepanje energijskih nivoa tj. spektralnih linija u električnom polju je Starkov efekt.

Kako “vidjeti” atom? Skanujući elektronski mikroskop sa tuneliranjem • No kako atom zaista «izgleda» nakon svega čini se gotovo neumjesnim pitanjem. Atom, naime, «izgleda» različito za različite metode opažanja. Ako ga posmatramo našim okom, onda atom ne postoji. Međutim, čovjek je izumio mnoge osjetljive instrumente kojima može opažati i ono što je za njegovo oko nedostižno. Najpreciznije «slike» pojedinačnih atoma dobijene su pomoću tzv. skanujućeg elektronskog mikroskopa sa tuneliranjem. • Na slici su pronalazači STM-a (1981. g. ) George Bennig i H. Rohrer sa “komorom” svoga izuma.
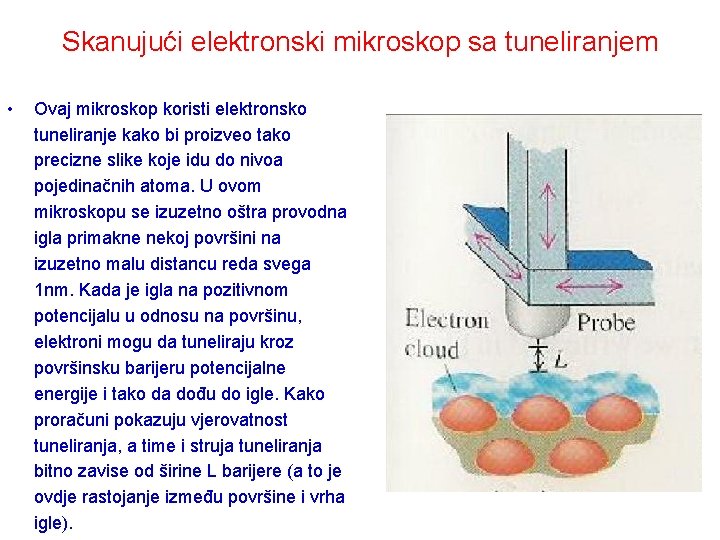
Skanujući elektronski mikroskop sa tuneliranjem • Ovaj mikroskop koristi elektronsko tuneliranje kako bi proizveo tako precizne slike koje idu do nivoa pojedinačnih atoma. U ovom mikroskopu se izuzetno oštra provodna igla primakne nekoj površini na izuzetno malu distancu reda svega 1 nm. Kada je igla na pozitivnom potencijalu u odnosu na površinu, elektroni mogu da tuneliraju kroz površinsku barijeru potencijalne energije i tako da dođu do igle. Kako proračuni pokazuju vjerovatnost tuneliranja, a time i struja tuneliranja bitno zavise od širine L barijere (a to je ovdje rastojanje između površine i vrha igle).

Skanujući elektronski mikroskop sa tuneliranjem • Igla se skenira preko površine i u isto vrijeme se pomijera okomito na površinu tako da se održi stalna struja tuneliranja. Pomijeranje igle se registruje i nakon mnogo paralelnih skeniranja može se rekonstruisati izgled površine Ovdje je bitno da se obezbijedi izuzetno precizna kontrola kretanja igle i njena izolacija od vibracija.

Slike pojedinačnih atoma na STM-u • Dodalno obojeni izgled atoma joda koji su adsorbovani na površini kristala platine. • Ovdje žuti spot pri dnu slike predstavlja mjesto gdje nedostaje atom

Slika galijumovog arsenida Ga. As na skanujućem elektronskom mikroskopu sa tuneliranjem • Plave tačke su atomi galijuma Ga, a crvene tačke su atomi arsena As.

Još jedna STM slika • Lijeva slika predstavlja površinu kristala zlata orjentacije (111). • Na desnoj slici je ista površina od bakra.

Krug prečnika 14 nm kojeg čine atomi željeza na bakarnoj površini: slika sa STM-a (Scanning Tunneling Microscope)
- Slides: 26