Kurva Titrasi Jika suatu asam atau basa dititrasi


Kurva Titrasi Jika suatu asam atau basa dititrasi, setiap penambahan pereaksi akan mengakibatkan perbahan p. H. Grafik yang diperoleh dengan mengalurkan p. H terhadap volume pereaksi yang ditambahkan disebut kurva titrasi.

Ada 4 macam perhitungan jika suatu asam dititrasi dengan suatu basa 1. 2. 3. 4. Titik awal, sebelum penambahan basa. p. H larutan ditentukan oleh konsentrasi asam Pada tahap sebelum titik ekivalen Pada titik ekivalen Setelah titik ekivalensi

A. Titrasi asam kuat dengan basa kuat 1. Pada awal titrasi, p. H larutan ditentukan oleh konsentrasi asam 2. Pada tahap sebelum titik ekivalensi 3. Pada titik ekivalensi, asam tepat dinetralkan oleh basa Vb (ekiv) = Va Ma/Mb

4. Setelah titik ekivalensi, p. H larutan ditentukan oleh konsentrasi OHberlebih
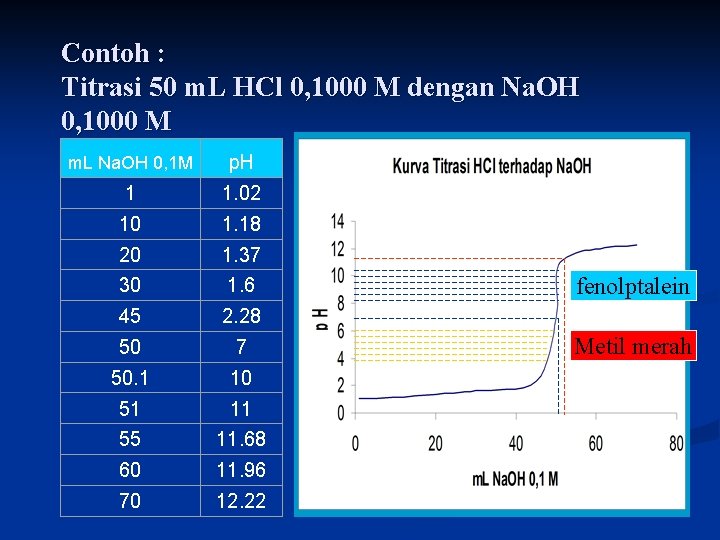
Contoh : Titrasi 50 m. L HCl 0, 1000 M dengan Na. OH 0, 1000 M m. L Na. OH 0, 1 M p. H 1 1. 02 10 1. 18 20 1. 37 30 1. 6 45 2. 28 50 7 50. 1 10 51 11 55 11. 68 60 11. 96 70 12. 22 fenolptalein Metil merah

B. Titrasi asam lemah dengan basa kuat 1. Pada awal titrasi p. H ditentukan oleh konsentrasi larutan asam 2. Pada tahap sebelum titik ekivalensi 3. Pada titik ekivalensi semua asam telah berubah menjadi garam

4. Setelah titik ekivalensi, p. H ditentukan oleh kelebihan Na. OH
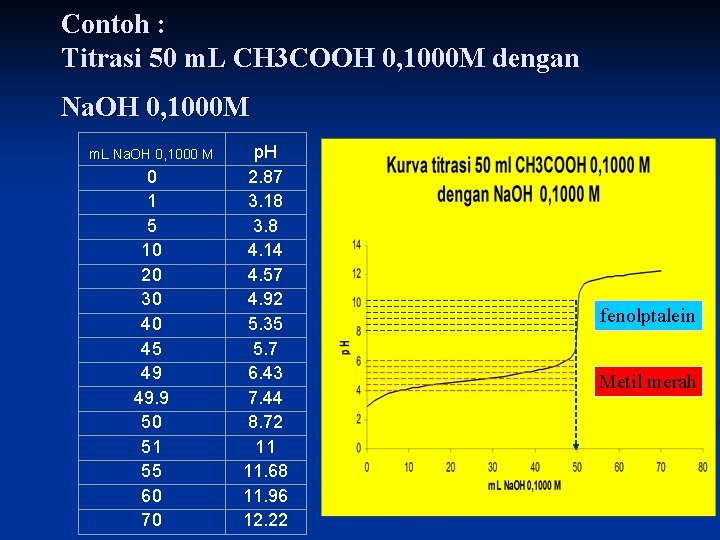
Contoh : Titrasi 50 m. L CH 3 COOH 0, 1000 M dengan Na. OH 0, 1000 M m. L Na. OH 0, 1000 M 0 1 5 10 20 30 40 45 49 49. 9 50 51 55 60 70 p. H 2. 87 3. 18 3. 8 4. 14 4. 57 4. 92 5. 35 5. 7 6. 43 7. 44 8. 72 11 11. 68 11. 96 12. 22 fenolptalein Metil merah

C. Titrasi asam kuat dengan basa lemah 1. 2. Pada awal titrasi, p. H ditentukan oleh konsentrasi asam H+ = Ca Pada tahap sebelum titik ekivalensi C larutan ditentukan oleh konsentrasi asam

3. Pada titik ekivalensi, semua asam bereaksi dengan basa 4. Setelah titik ekivalensi, dlm lar. Terdapat kelebihan basa lemah dan garam yang terbentuk (buffer)
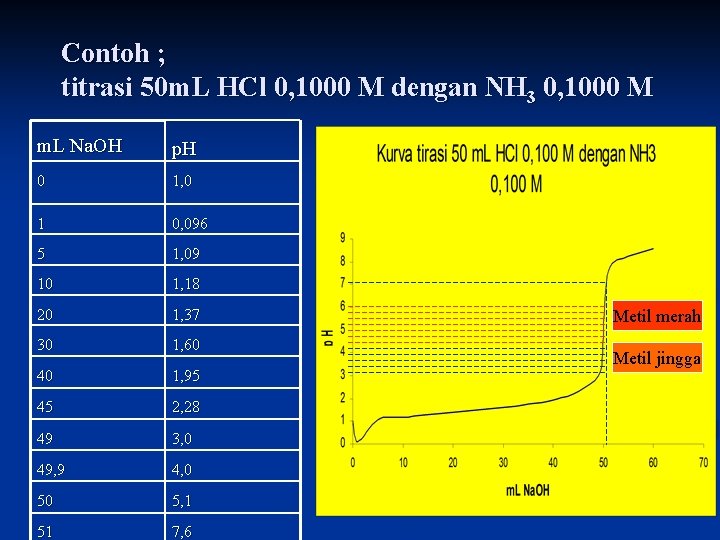
Contoh ; titrasi 50 m. L HCl 0, 1000 M dengan NH 3 0, 1000 M m. L Na. OH p. H 0 1, 0 1 0, 096 5 1, 09 10 1, 18 20 1, 37 30 1, 60 40 1, 95 45 2, 28 49 3, 0 49, 9 4, 0 50 5, 1 51 7, 6 Metil merah Metil jingga

Kesimpulan § § § Untuk titrasi HCl dengan Na. OH, bagian vertikal kurva titrasi terletak diantara p. H 4 dan 11. Indikator yang dipakai metil merah dan fenolfthalin. Untuk titrasi CH 3 COOH dengan Na. OH bagian vertikal kurva terletak pada p. H 6, 5 dan 1. Indikator yang dipakai fenol merah dan fenolftalin. Untuk titrasi HCl dengan NH 3 bagian vertikal kurva terletak diantara p. H 4 dan 8

§ Untuk titrasi CH 3 COOH dengan NH 3 tidak terdapat kenaikan p. H yang tajam pada titik ekivalensi. Tidak ada indikator untuk titrasi ini.
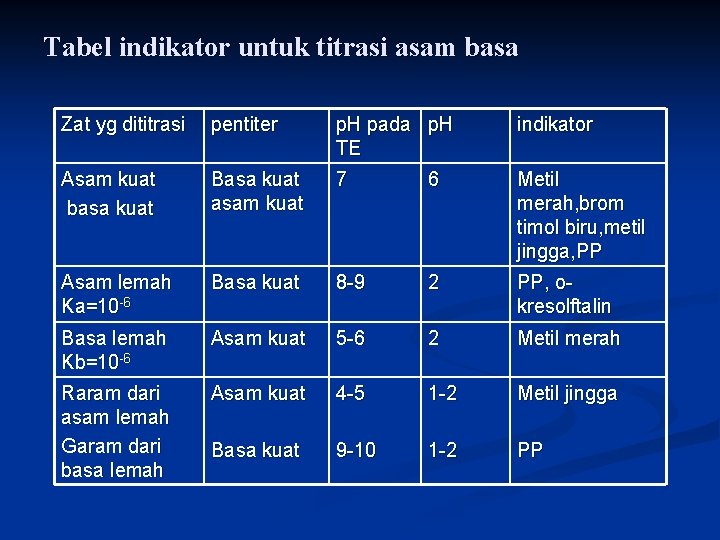
Tabel indikator untuk titrasi asam basa Zat yg dititrasi pentiter p. H pada p. H TE indikator Asam kuat basa kuat Basa kuat asam kuat 7 6 Metil merah, brom timol biru, metil jingga, PP Asam lemah Ka=10 -6 Basa kuat 8 -9 2 PP, okresolftalin Basa lemah Kb=10 -6 Asam kuat 5 -6 2 Metil merah Raram dari asam lemah Garam dari basa lemah Asam kuat 4 -5 1 -2 Metil jingga Basa kuat 9 -10 1 -2 PP
- Slides: 15