Kupfer Ein besonderes Element Kupfer mathematisch Gliederung 1

Kupfer Ein besonderes Element

Kupfer mathematisch Gliederung: 1. Historische Aspekte 2. Technische Darstellung 3. Elementares Kupfer 4. Kupferverbindungen 5. Physiologische Bedeutung 6. Kupfer in der Schule 2

Kupfer mathematisch Historische Aspekte • „aes cyprium“ (lat. ) = Erz aus Zypern „cuprum“ (lat. ) = Kupfer • Zypriotische Kupfererze im Altertum • • • Kupfer ist erstes Gebrauchsmetall Kupferzeit vor ca. 8000 Jahren Entdeckung der Bronze ca. 3000 v. Chr. Bronzezeitmensch Ötzi 3
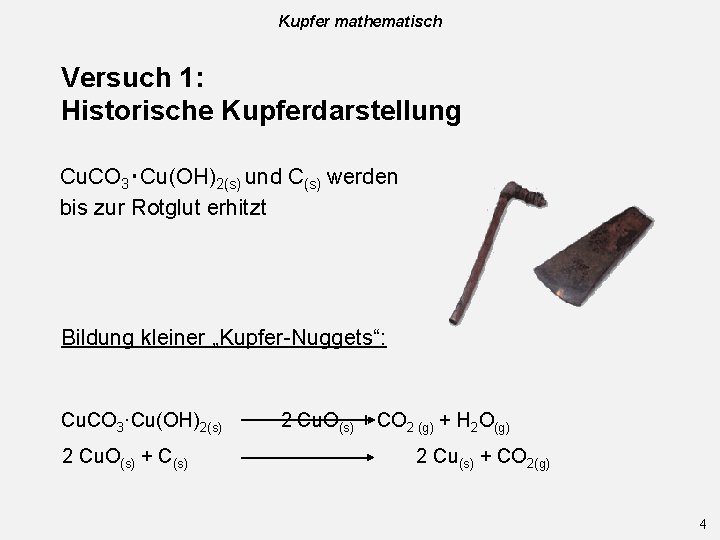
Kupfer mathematisch Versuch 1: Historische Kupferdarstellung Cu. CO 3‧Cu(OH)2(s) und C(s) werden bis zur Rotglut erhitzt Bildung kleiner „Kupfer-Nuggets“: Cu. CO 3·Cu(OH)2(s) 2 Cu. O(s) + CO 2 (g) + H 2 O(g) 2 Cu(s) + CO 2(g) 4

Kupfer mathematisch Technische Darstellung von Reinkupfer • Wichtigste Ausgangsmaterialien: Bornit („Buntkupferkies“ Cu 2 S·Fe 2 S 3) Chalkosin („Kupferglanz“ Cu 2 S, Kupfersulfid) • Darstellung über mehrere Stufen. 5
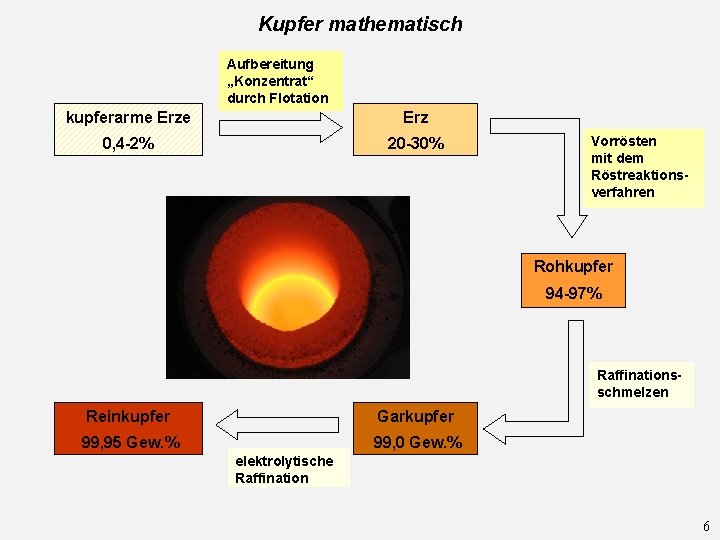
Kupfer mathematisch Aufbereitung „Konzentrat“ durch Flotation kupferarme Erz 0, 4 -2% 20 -30% Vorrösten mit dem Röstreaktionsverfahren Rohkupfer 94 -97% Raffinationsschmelzen Reinkupfer Garkupfer 99, 95 Gew. % 99, 0 Gew. % elektrolytische Raffination 6
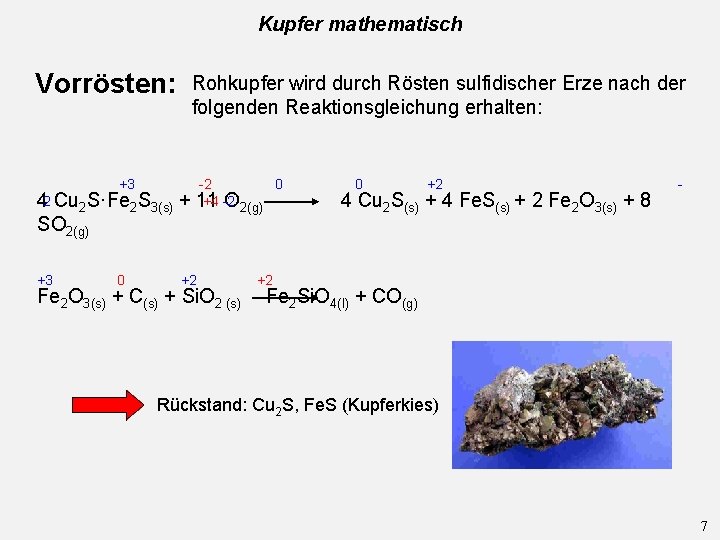
Kupfer mathematisch Vorrösten: +3 Rohkupfer wird durch Rösten sulfidischer Erze nach der folgenden Reaktionsgleichung erhalten: 42 Cu 2 S·Fe 2 S 3(s) + SO 2(g) +3 0 -2 0 +4 -2 11 O 2(g) +2 Fe 2 O 3(s) + C(s) + Si. O 2 (s) 0 +2 4 Cu 2 S(s) + 4 Fe. S(s) + 2 Fe 2 O 3(s) + 8 - +2 Fe 2 Si. O 4(l) + CO(g) Rückstand: Cu 2 S, Fe. S (Kupferkies) 7
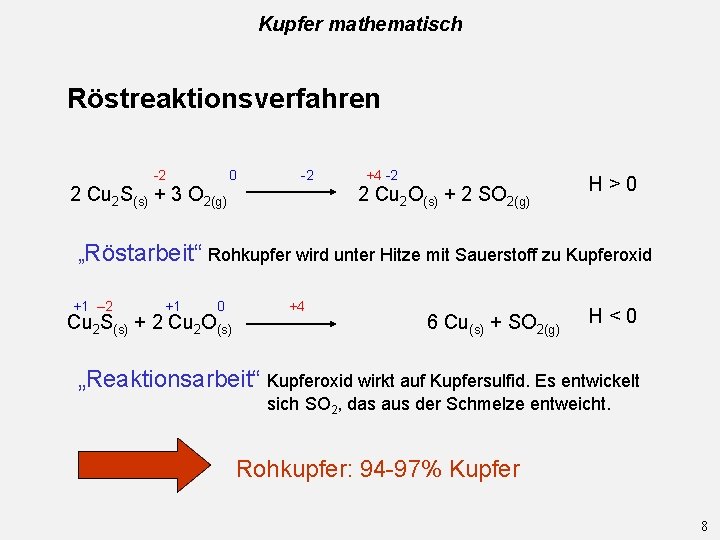
Kupfer mathematisch Röstreaktionsverfahren -2 0 -2 2 Cu 2 S(s) + 3 O 2(g) +4 -2 2 Cu 2 O(s) + 2 SO 2(g) H>0 „Röstarbeit“ Rohkupfer wird unter Hitze mit Sauerstoff zu Kupferoxid +1 – 2 +1 0 Cu 2 S(s) + 2 Cu 2 O(s) +4 6 Cu(s) + SO 2(g) H<0 „Reaktionsarbeit“ Kupferoxid wirkt auf Kupfersulfid. Es entwickelt sich SO 2, das aus der Schmelze entweicht. Rohkupfer: 94 -97% Kupfer 8

Kupfer mathematisch Reinigung des Rohkupfers: Raffinationsschmelzen Entfernung der Verunreinigungen: • Zn, Sn, Pb, As als flüchtige Oxide • Fe und Ni werden verschlackt Restliche Kupfersulfide und Oxide werden reduziert. Garkupfer: 99% Kupfer 9
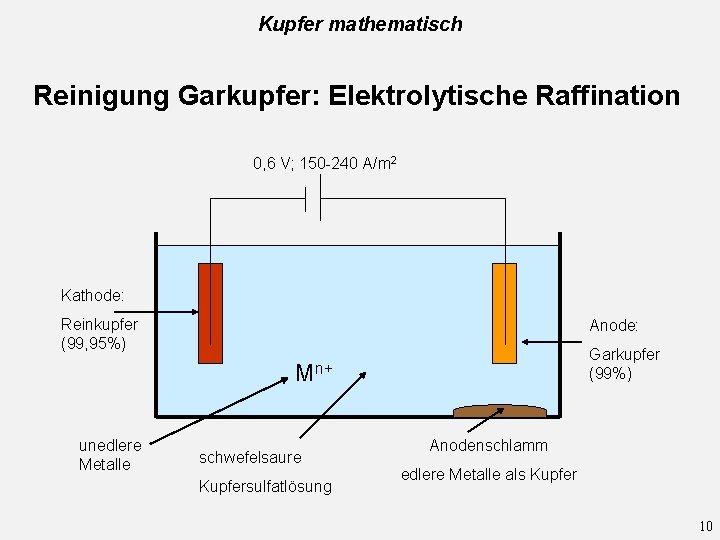
Kupfer mathematisch Reinigung Garkupfer: Elektrolytische Raffination 0, 6 V; 150 -240 A/m 2 Kathode: Reinkupfer (99, 95%) Anode: Garkupfer (99%) Mn+ unedlere Metalle schwefelsaure Kupfersulfatlösung Anodenschlamm edlere Metalle als Kupfer 10

Kupfer mathematisch Reaktionen bei der Elektrolyse Hauptreaktionen: 0 +2 Anode: Cugar(s) Cu 2+(aq) + 2 e+2 Kathode: 0 Cu 2+(aq) + 2 e- Curein(s) 11
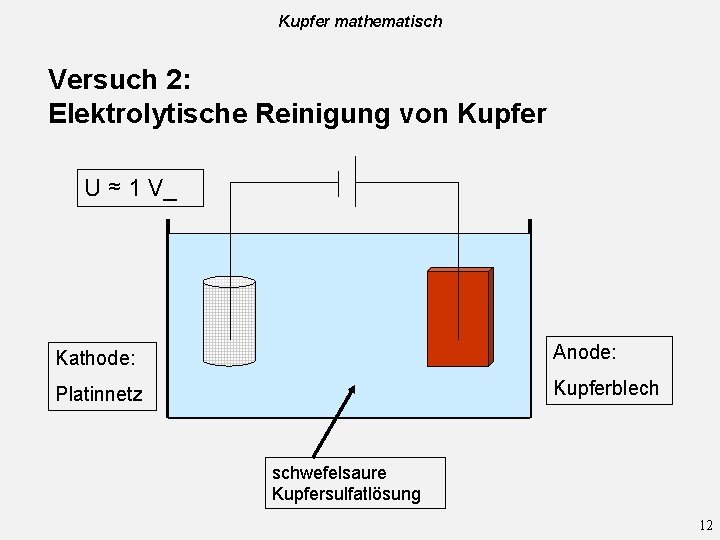
Kupfer mathematisch Versuch 2: Elektrolytische Reinigung von Kupfer U ≈ 1 V_ Kathode: Anode: Platinnetz Kupferblech schwefelsaure Kupfersulfatlösung 12
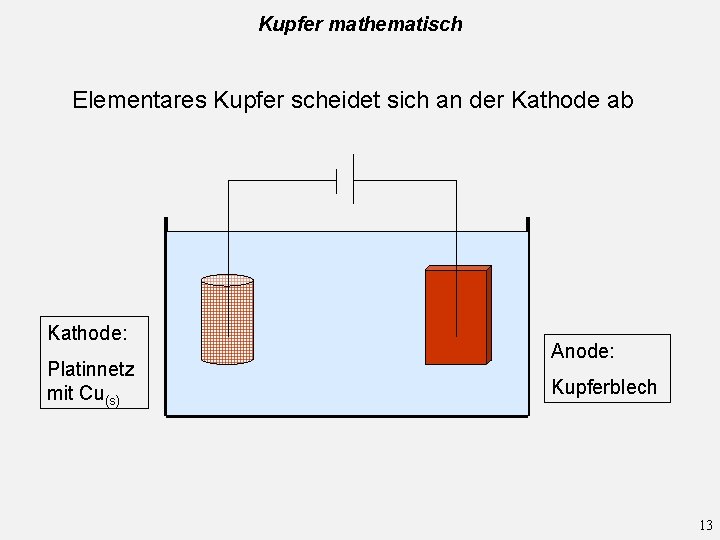
Kupfer mathematisch Elementares Kupfer scheidet sich an der Kathode ab Kathode: Platinnetz mit Cu(s) Anode: Kupferblech 13
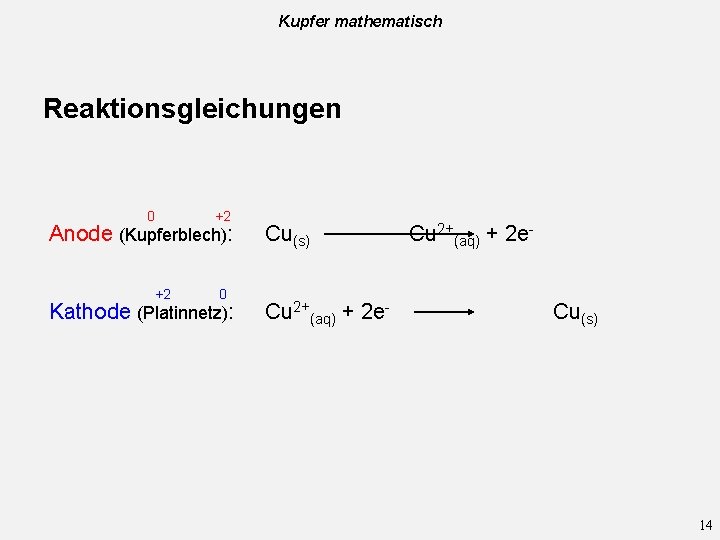
Kupfer mathematisch Reaktionsgleichungen 0 +2 Anode (Kupferblech): +2 0 Kathode (Platinnetz): Cu(s) Cu 2+(aq) + 2 e- Cu 2+(aq) + 2 e. Cu(s) 14
Kupfer mathematisch 3. Kupfer - elementar Vorkommen: Gediegen: Nordamerika, Chile und Australien Kupfererze: USA, Chile und Simbabwe Eigenschaften: • • Elektrische Leitfähigkeit Legierbarkeit Korrosionsbeständigkeit Bakterizid 15

Kupfer mathematisch Physikalische Eigenschaften des Kupfers • Hohe elektrische Leitfähigkeit • Gute Legierungsfähigkeit 16

Kupfer mathematisch Chemische Eigenschaften des Kupfers • Hohe Korrosionsbeständigkeit • Bakterizide Eigenschaften 17
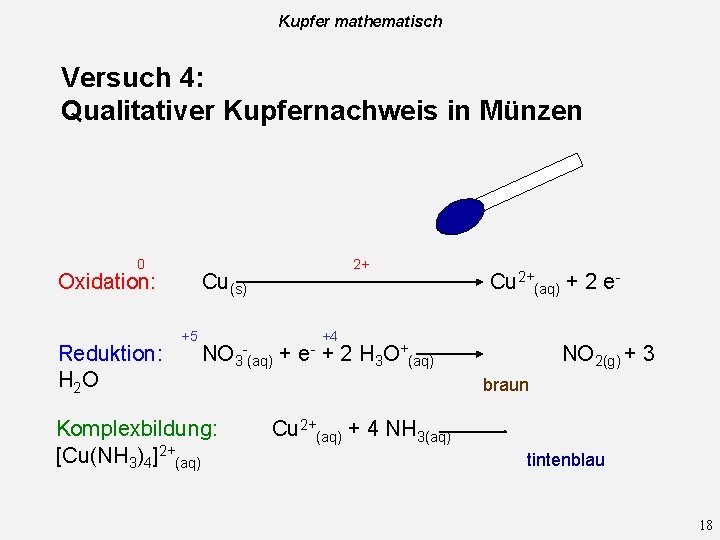
Kupfer mathematisch Versuch 4: Qualitativer Kupfernachweis in Münzen 0 Oxidation: Reduktion: H 2 O 2+ Cu(s) +5 NO 3 (aq) + Komplexbildung: [Cu(NH 3)4]2+(aq) - e- Cu 2+(aq) + 2 e- +4 + 2 H 3 O+(aq) NO 2(g) + 3 braun Cu 2+(aq) + 4 NH 3(aq) tintenblau 18

Kupfer mathematisch Versuch 5: Kupfergehalt eines 1 -Cent-Stückes • 1 -Cent Münze mit HNO 3(konz) aufgeschlossen • Aufschlusslösung: 1 Liter • Probe: 500 µL 19
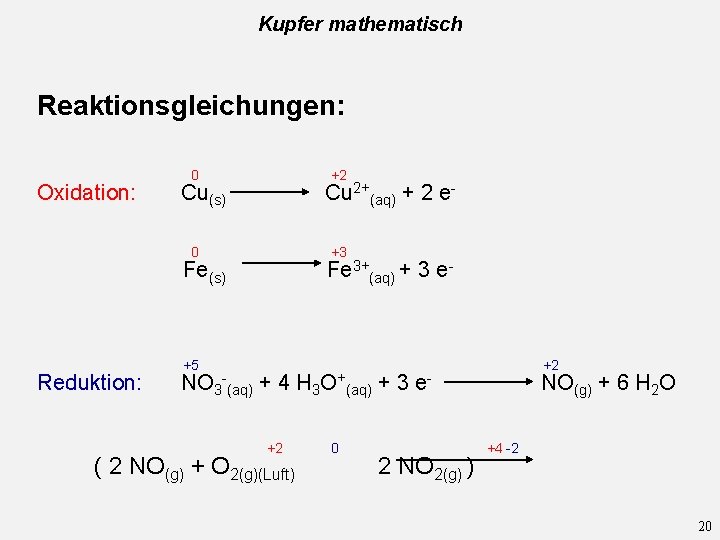
Kupfer mathematisch Reaktionsgleichungen: Oxidation: 0 +2 Cu(s) Cu 2+(aq) + 2 e- 0 +3 Fe(s) Reduktion: +5 Fe 3+(aq) + 3 e- NO 3 (aq) + 4 H 3 - +2 ( 2 NO(g) + O 2(g)(Luft) O+ 0 (aq) +3 +2 e- 2 NO 2(g) ) NO(g) + 6 H 2 O +4 -2 20
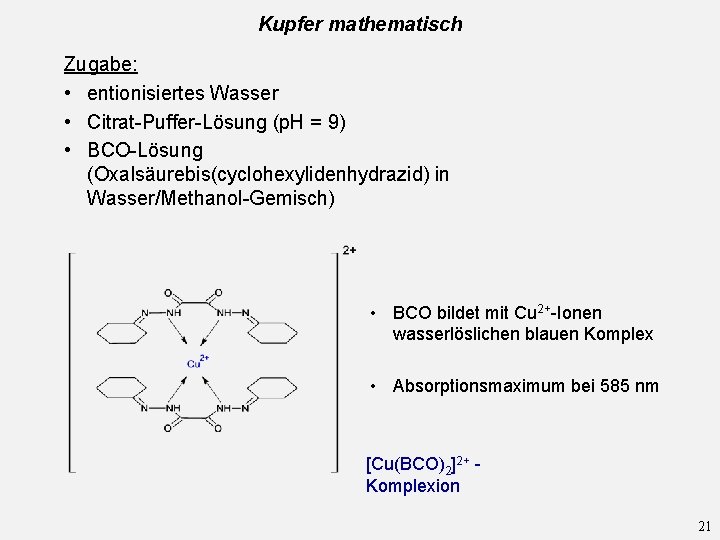
Kupfer mathematisch Zugabe: • entionisiertes Wasser • Citrat-Puffer-Lösung (p. H = 9) • BCO-Lösung (Oxalsäurebis(cyclohexylidenhydrazid) in Wasser/Methanol-Gemisch) • BCO bildet mit Cu 2+-Ionen wasserlöslichen blauen Komplex • Absorptionsmaximum bei 585 nm [Cu(BCO)2]2+ Komplexion 21
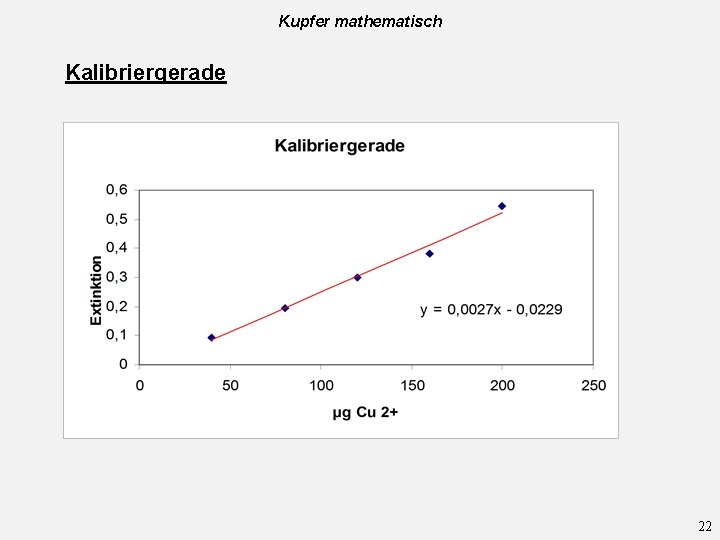
Kupfer mathematisch Kalibriergerade 22
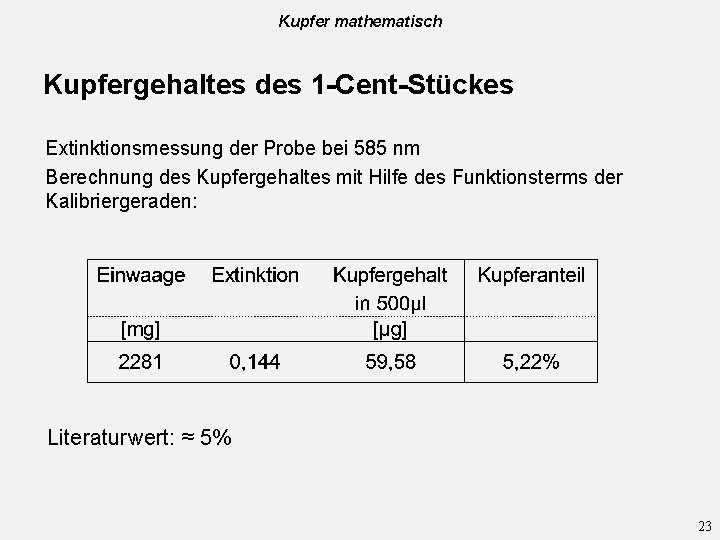
Kupfer mathematisch Kupfergehaltes des 1 -Cent-Stückes Extinktionsmessung der Probe bei 585 nm Berechnung des Kupfergehaltes mit Hilfe des Funktionsterms der Kalibriergeraden: Literaturwert: ≈ 5% 23
![Kupfer mathematisch Zusammensetzung der Euro-Münzen Legierungs. System Legierungs. Anteile [%] 1 -, 2 -, Kupfer mathematisch Zusammensetzung der Euro-Münzen Legierungs. System Legierungs. Anteile [%] 1 -, 2 -,](http://slidetodoc.com/presentation_image_h/1c95807226a53f41698346b419a93140/image-24.jpg)
Kupfer mathematisch Zusammensetzung der Euro-Münzen Legierungs. System Legierungs. Anteile [%] 1 -, 2 -, 5 -Cent Stahl mit Kupferauflage Cu ≈ 5 10 -, 20 -, 50 -Cent Cu. Al. Zn. Sn Cu 89; Al 5; Zn 5; Sn 1 1 -, 2 -Euro Cu. Ni Cu 75; Ni 25 (silberfarbene Legierung) Cu. Zn. Ni (goldfarbene Legierung) Anmerkung Nordisches Gold Zweikomponenten. Cu 75; Zn 20; Ni 5 system 24

Kupfer mathematisch Kupfer in der Atmungskette: Hämocyanin Säugetiere und Vögel: Häm-System für Bindung und Transport von Sauerstoff (Porphyrin-Makrozyklus) Viele Weichtiere und Gliederfüssler, (Spinnen, Krebse und Würmer): Sauerstofftransport mit Hilfe zweikerniger Metallkomplexe, die durch Aminosäurenreste koordiniert sind • Eisen (Hämerythrin) oder • Kupfer (Hämocyanin) 25
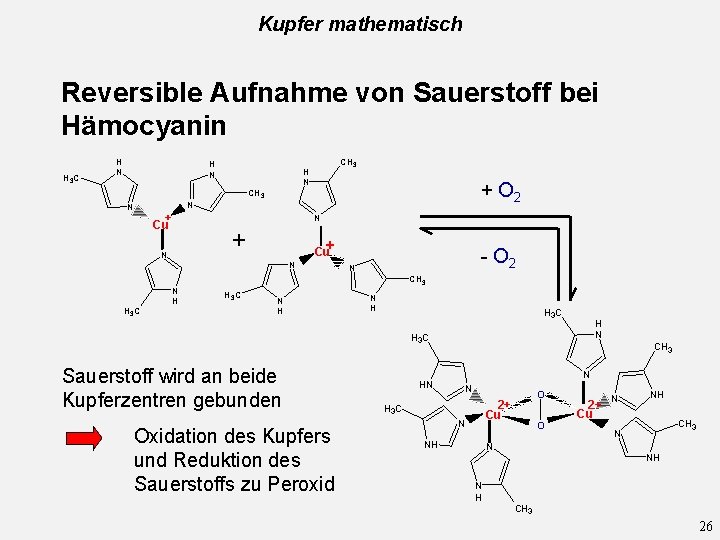
Kupfer mathematisch Reversible Aufnahme von Sauerstoff bei Hämocyanin H 3 C H N + Cu N + N Cu+ N N H H 3 C + O 2 CH 3 N N CH 3 H N - O 2 N CH 3 H 3 C N H H 3 C H N H 3 C Sauerstoff wird an beide Kupferzentren gebunden Oxidation des Kupfers und Reduktion des Sauerstoffs zu Peroxid HN CH 3 N N O 2+ Cu H 3 C N NH O N N H 2+ Cu N NH CH 3 26

Kupfer mathematisch Versuch: 5 Der Kressewurzeltest - ein Beispiel für biologische Testverfahren Grenzwert von Kupferionen im Trinkwasser : 0, 1 mg/L (c = 6 mmol/L) Keimverhalten von Gartenkresse ist Indikator für: Schadstoffgehalt bzw. Kupferionengehalt des Trinkwassers. 27
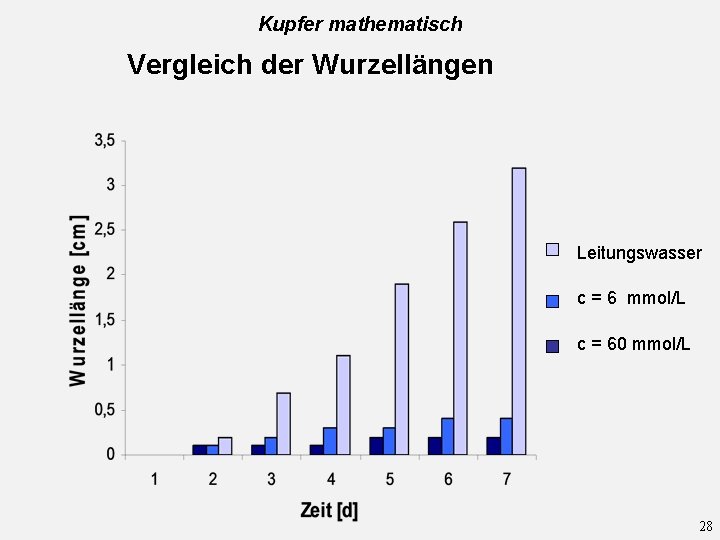
Kupfer mathematisch Vergleich der Wurzellängen Leitungswasser c = 6 mmol/L c = 60 mmol/L 28

Kupfer mathematisch 29
- Slides: 29