KRIVA TITRACIJE SLABE BAZE JAKOM KISELINOM B H
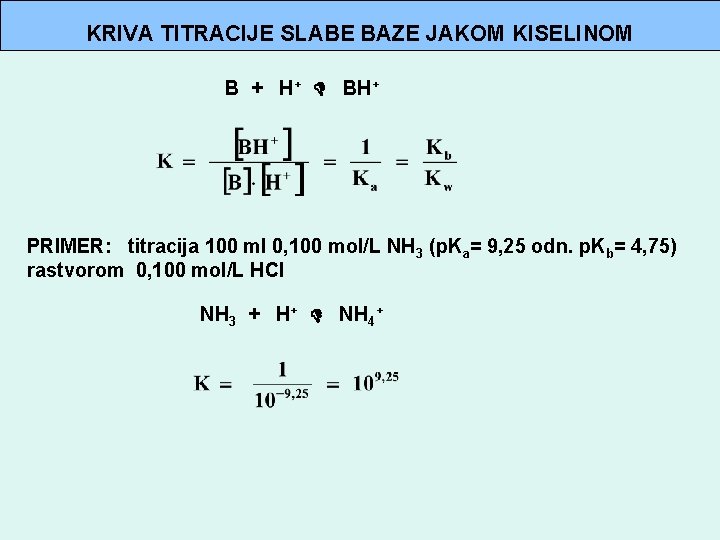
KRIVA TITRACIJE SLABE BAZE JAKOM KISELINOM B + H+ BH+ PRIMER: titracija 100 ml 0, 100 mol/L NH 3 (p. Ka= 9, 25 odn. p. Kb= 4, 75) rastvorom 0, 100 mol/L HCl NH 3 + H+ NH 4+
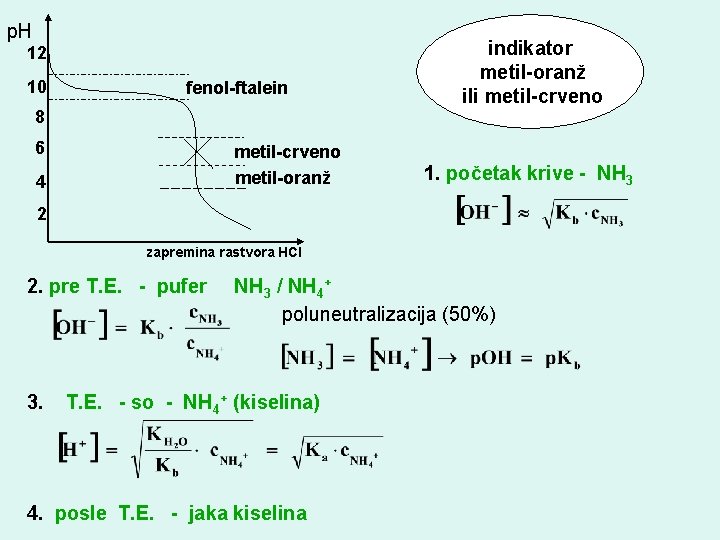
p. H 12 10 fenol-ftalein 8 6 metil-crveno metil-oranž 4 indikator metil-oranž ili metil-crveno 1. početak krive - NH 3 2 zapremina rastvora HCl 2. pre T. E. - pufer 3. NH 3 / NH 4+ poluneutralizacija (50%) T. E. - so - NH 4+ (kiselina) 4. posle T. E. - jaka kiselina
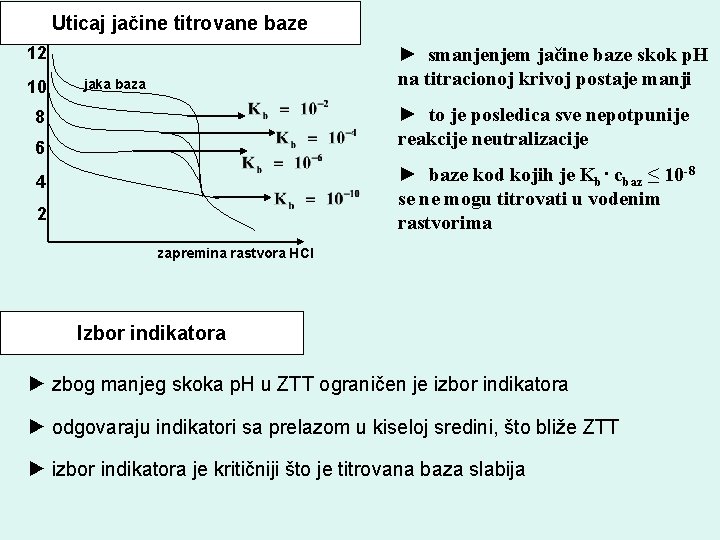
Uticaj jačine titrovane baze 12 10 ► smanjenjem jačine baze skok p. H na titracionoj krivoj postaje manji jaka baza ► to je posledica sve nepotpunije reakcije neutralizacije 8 6 ► baze kod kojih je Kb· cbaz ≤ 10 -8 se ne mogu titrovati u vodenim rastvorima 4 2 zapremina rastvora HCl Izbor indikatora ► zbog manjeg skoka p. H u ZTT ograničen je izbor indikatora ► odgovaraju indikatori sa prelazom u kiseloj sredini, što bliže ZTT ► izbor indikatora je kritičniji što je titrovana baza slabija

TITRACIJE SMEŠE KISELINA ILI BAZA ♣ ako se titruje smeša dve kiseline približno jednake jačine, dobija se samo jedan skok i jedna ZTT - titracijom se određuje samo UKUPNA kiselost ♣ ako se titruje smeša dve kiseline različite jačine, prvo se titruje jača kiselina uz odgovarajuči skok p. H na ZTT 1, a zatim druga kiselina dajući ZTT 2 Ovo je moguće samo ako je odnos konstanti kiselosti dve kiseline veći od 104 (uz tačnost od oko 1%) ili 106 (uz tačnost od oko 0, 1%) - pod uslovom da su obe kiseline dovoljno jake da mogu da se titruju u vodenim rastvorima !!! p. H Titracione krive titracije smeše jake kiseline i slabe kiseline jakom bazom zapremina rastvora Na. OH

TITRACIJE POLIPROTONSKIH KISELINA ILI BAZA ► titracione krive pokazuju više ekvivalentnih tačaka, ukoliko se sukcesivne konstante disocijacije međusobno dovoljno razlikuju , za tačnost 1% , za tačnost 0, 1% ► PRIMERI: -maleinska kiselina - oksalna kiselina - sulfatna kiselina , mogu se koristiti obe ZTT mada je druga izraženija , uvek se određuje druga ZTT , i drugi proton je toliko disosovan da može da se titruje kao jaka kiselina, jedna ZTT
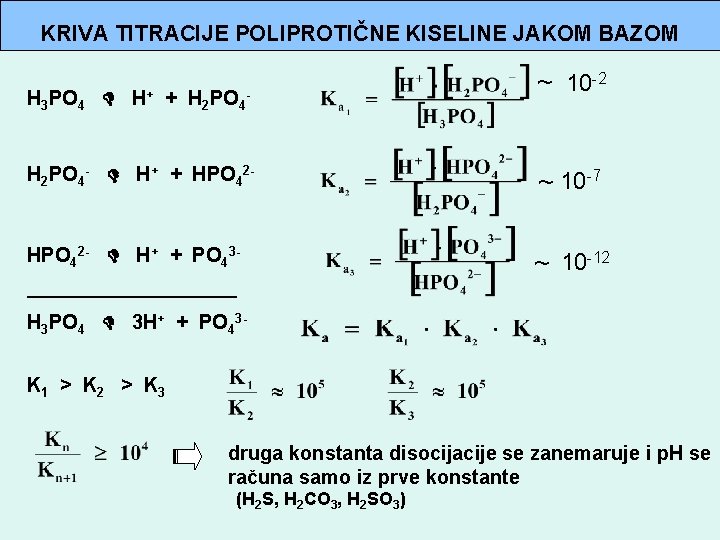
KRIVA TITRACIJE POLIPROTIČNE KISELINE JAKOM BAZOM H 3 PO 4 H+ + H 2 PO 4 - ~ 10 -2 H 2 PO 4 - H+ + HPO 42 - ~ 10 -7 HPO 42 - H+ + PO 43 - ~ 10 -12 ___________ H 3 PO 4 3 H+ + PO 43 K 1 > K 2 > K 3 druga konstanta disocijacije se zanemaruje i p. H se računa samo iz prve konstante (H 2 S, H 2 CO 3, H 2 SO 3)
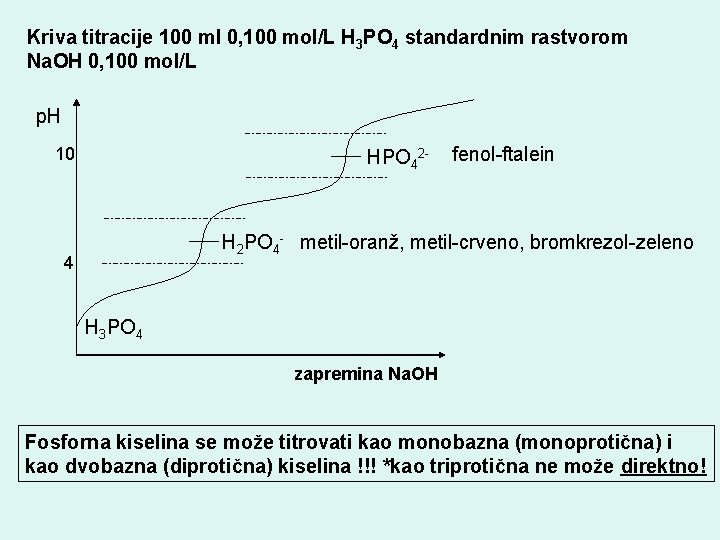
Kriva titracije 100 ml 0, 100 mol/L H 3 PO 4 standardnim rastvorom Na. OH 0, 100 mol/L p. H 10 HPO 42 - fenol-ftalein H 2 PO 4 - metil-oranž, metil-crveno, bromkrezol-zeleno 4 H 3 PO 4 zapremina Na. OH Fosforna kiselina se može titrovati kao monobazna (monoprotična) i kao dvobazna (diprotična) kiselina !!! *kao triprotična ne može direktno!

TITRACIJA NATRIJUM-KARBONATA ► slaba dvofunkcionalna baza koja jonizuje: CO 32 - + H 2 O HCO 3 - + OHHCO 3 - + H 2 O H 2 CO 3 + OH- Kb 1 = 10 -3, 68, odn. Ka 2 = 10 -10, 32 Kb 2 = 10 -7, 65, odn. Ka 1 = 10 -6, 35 titracija teče u dva stepena i dobijaju se dve ZTT - prva odgovara titraciji karbonata do hidrogen-karbonata: CO 32 - + H+ HCO 3 - druga odgovara titraciji nastalog hidrogen-karbonata do ugljene kiseline: HCO 3 - + H+ H 2 CO 3 ♦♦♦ druga ZTT je oštrija, jer je proizvod reakcije (H 2 CO 3) nestabilan i razgrađuje se na H 2 O i CO 2 koji odlazi iz sistema, tako da se ravnoteža pomera u desno, konstanta postaje povoljnija
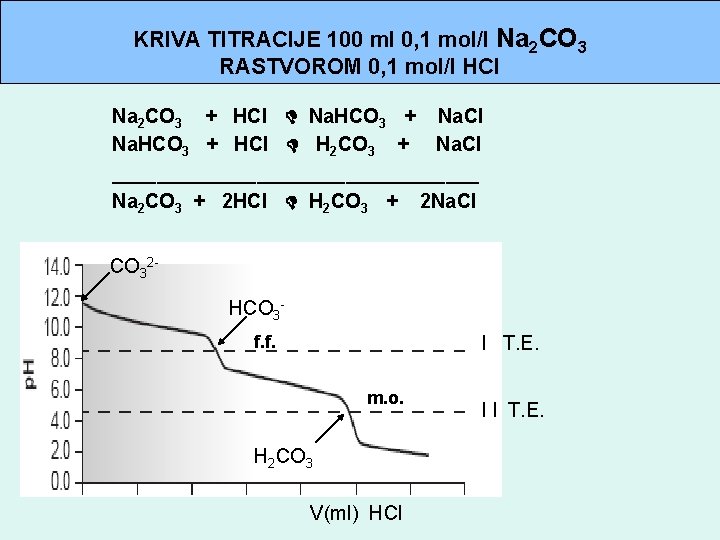
KRIVA TITRACIJE 100 ml 0, 1 mol/l Na 2 CO 3 RASTVOROM 0, 1 mol/l HCl Na 2 CO 3 + HCl Na. HCO 3 + Na. Cl Na. HCO 3 + HCl H 2 CO 3 + Na. Cl _________________ Na 2 CO 3 + 2 HCl H 2 CO 3 + 2 Na. Cl CO 32 HCO 3 f. f. I T. E. m. o. H 2 CO 3 V(ml) HCl I I T. E.

PRIMENA KISELINSKO-BAZNIH TITRACIJA ♣ Brzo i tačno se određuju mnoge neorganske i organske kiseline i baze. STANDARDNI RASTVORI KISELINA HCl (najčešće), H 2 SO 4, HCl. O 4, retko HNO 3 Standardizacija pomoću baznih supstanci primarnih standarda Natrijum- karbonat: - pre upotrebe 30 min. zagrevanje 270 -300 o. C - da se odstrani sva voda i tragovi bikarbonata prevedu u karbonate - titracija se vrši do druge ZTT Natrijum- tetraborat dekahidrat (boraks): B 4 O 72 - + 2 H+ + 5 H 2 O 4 H 3 BO 3

STANDARDNI RASTVORI BAZA Na. OH (najčešće), retko KOH, Ba(OH)2 ‚‚karbonatna greška‚‚ zbog rastvaranja CO 2 PRIPREMANJE “BESKARBONATNIH” RASTVORA ALKALIJA 1. Serensenov postupak- natrijum-karbonat je praktično nerastvoran u koncentrovanim rastvorima alkalija (samo natrijum-hidroksid, ali ne i kalijum-hidroksid) 2. Hidroksidi alkalnim metala rastvorni u alkoholu a karbonati nisu (primenljiv je i na kalijum-hidroksid) 3. Jako bazni jonski izmenjivači
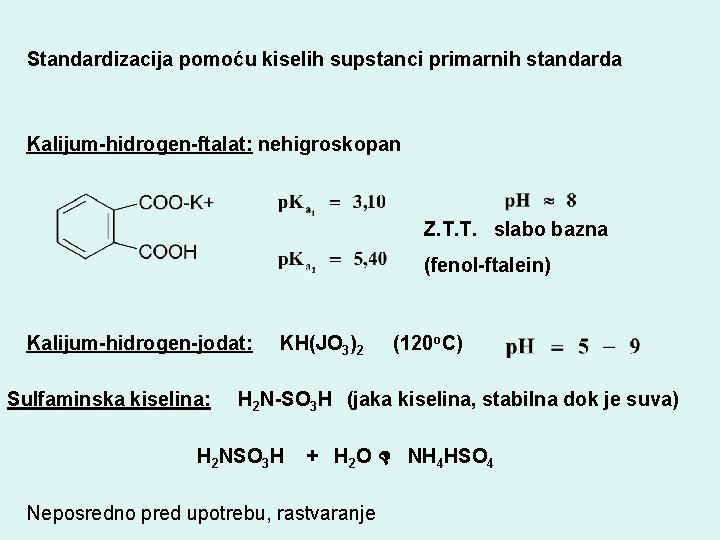
Standardizacija pomoću kiselih supstanci primarnih standarda Kalijum-hidrogen-ftalat: nehigroskopan Z. T. T. slabo bazna (fenol-ftalein) Kalijum-hidrogen-jodat: Sulfaminska kiselina: KH(JO 3)2 (120 o. C) H 2 N-SO 3 H (jaka kiselina, stabilna dok je suva) H 2 NSO 3 H + H 2 O NH 4 HSO 4 Neposredno pred upotrebu, rastvaranje
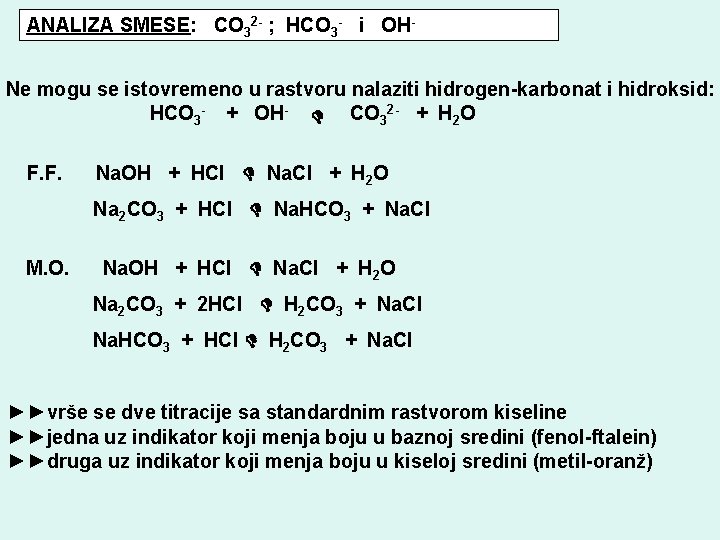
ANALIZA SMESE: CO 32 - ; HCO 3 - i OHNe mogu se istovremeno u rastvoru nalaziti hidrogen-karbonat i hidroksid: HCO 3 - + OH- CO 32 - + H 2 O F. F. Na. OH + HCl Na. Cl + H 2 O Na 2 CO 3 + HCl Na. HCO 3 + Na. Cl M. O. Na. OH + HCl Na. Cl + H 2 O Na 2 CO 3 + 2 HCl H 2 CO 3 + Na. Cl Na. HCO 3 + HCl H 2 CO 3 + Na. Cl ►►vrše se dve titracije sa standardnim rastvorom kiseline ►►jedna uz indikator koji menja boju u baznoj sredini (fenol-ftalein) ►►druga uz indikator koji menja boju u kiseloj sredini (metil-oranž)

Prisutno: VF. F. : VM. O. OH- VF. F. = VM. O. CO 32 - VF. F. = ½ VM. O. HCO 3 - VF. F. = 0 OH- + CO 32 - VF. F. > ½ VM. O. CO 32 - + HCO 3 - VF. F. < ½ VM. O. Analiza može da se izvede i pomoću jedne jedine titracije, jer je fenol-ftalein jednobojan indikator pa ne smeta nastavku titracije uz metil-oranž kao indikator*. *tada se menja odnos zapremina u gornjoj tabeli
- Slides: 14