Kreft II Oncogentumor suppressor mekanisme og genomstabilitet l

Kreft II: Oncogen/tumor suppressor mekanisme, og genomstabilitet l l l l Mutasjoner som forårsaker tap av cellesykluskontroll Onkogener: Cyclin D 1 Tumor suppressorer: p 16 Rb TGFb-signalisering og cellevekst Mutasjoner som påvirker genom stabilitet p 53 DNA reparasjonsmekanismer Kromosomabnormaliteter i humane tumorer Telomerase og immortalisering av celler

Mutasjoner som forårsaker tap av cellesykluskontroll l l cellers overgang fra ikke-delende til delende og progresjon gjennom syklus er nøye kontrollert for å sikre DNA replikasjon og koordinering av cellesyklus består av : G 1, S, G 2 og M, og reguleres av cycliner og cyclin-avhengige kinaser (Cdks) og Rb protein viktig kontrollpunkt overgang G 1 til S: restriksjonspunkt extracellulære stimuli regulerer uttrykk av cyclin D 1, D 2, D 3 som assosierer med Cdk 4/6 som resulterer i katalytisk aktive kinaser fravær av mitogener fører til akkumulering av p 27 eller p 16 som hemmer Cdk-aktivitet og fører til G 1 arrest
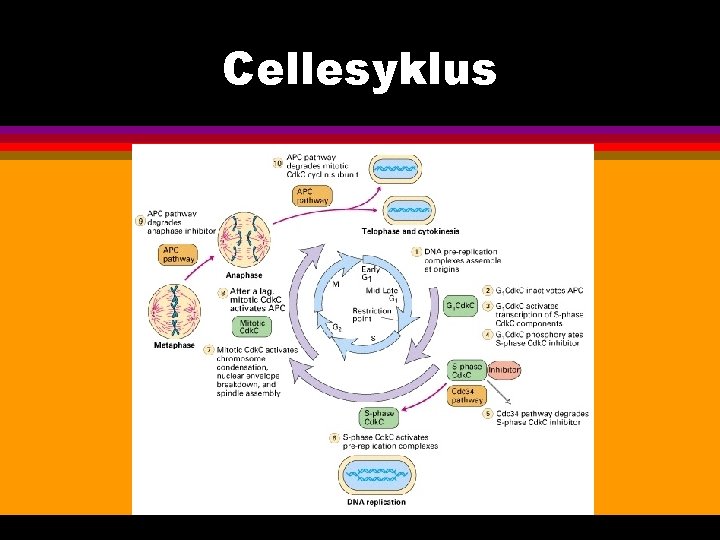
Cellesyklus

l l l Rb binder E 2 F transkripsjonsfaktorer og hindrer derved E 2 F-mediert transkripsjonsaktivering nødvendig for DNA syntese Cdk 4 -cyclin. D fosforylering av Rb frigjør aktiv E 2 F tap/endring av uttrykk av enten cyclin D 1, p 16 eller Rb er nok for uhindret progresjon gjennom cellesyklus
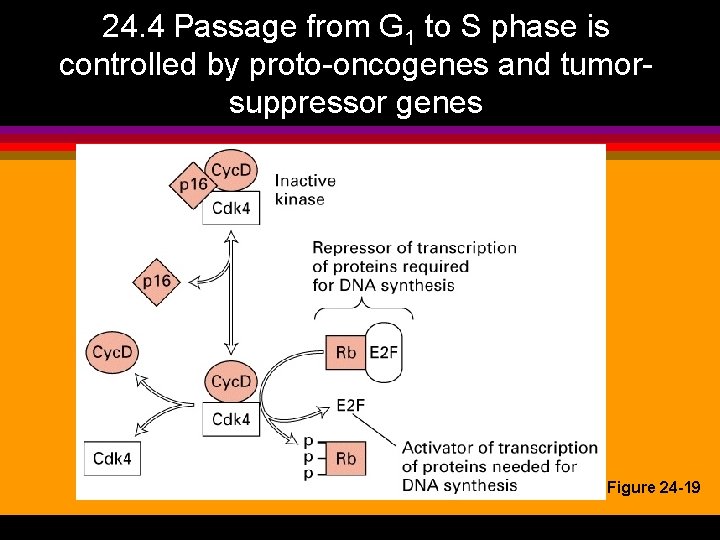
24. 4 Passage from G 1 to S phase is controlled by proto-oncogenes and tumorsuppressor genes Figure 24 -19

Onkogener: Cyclin D 1 l l overuttrykk av cyclin D 1 enten som genamplifikasjon eller kromosomal translokasjon fører til cellesyklus progresjon uavhengig av extracellulære stimuli observeres i forskjellige kreftformer, bl. a. brystkreft

Tumor suppressorer: p 16 og Rb l l l tap av p 16 vil etterligne overuttrykk av cyclin D 1 og føre til hyperfosforylering av Rb og frigiving av transkripsjonsfaktoren E 2 F tap av Rb fører til transformert cellevekst grunnet konstant aktivering av E 2 F observeres i mange kreftfromer, bl. a. i retinoblastoma hos barn

TGFb-signalisering og cellevekst l l l l Tumor derivert vekstfaktor, TGFb skilles ut av de fleste celletyper og har mange biologiske funksjoner TGFb hemmer vekst av bl. a. epitel- og immunsystem-celler tap av TGFb mediert veksthemming karakteriserer mange kreftformer TGFb har to reseptorer, type. I og type. II som dimeriserer ved ligand binding, har intern ser/thr-kinase aktivitet ligand aktivert type. I reseptor fosforylerer ser i Smad proteiner som entrer kjernen og aktiverer transkripsjon av forskjellige protein, inkludert p 15 erstatter p 27 i Cdk 4 -cyclin D komplekset, som igjen binder til og hemmer Cdk 2 -cyclin E komplekset som er nødvendig for inngang i S fasen TGFb indusert uttrykk av p 15 arresterer derfor celler i G 1

l l l overuttrykk av protooncogenet cyclin D 1 eller tap av tumorsuppressorgenene p 16 eller Rb kan føre til uregulert passage gjennom cellesyklus restriksjonspunktet seint i G 1 TGFb induserer uttrykk av p 15 som fører til arrest i G 1 og dessuten syntese av extracellulære matrix proteiner tap av TGFb reseptorer eller Smad 4 ødelegger TGFb regulert vekstkontroll
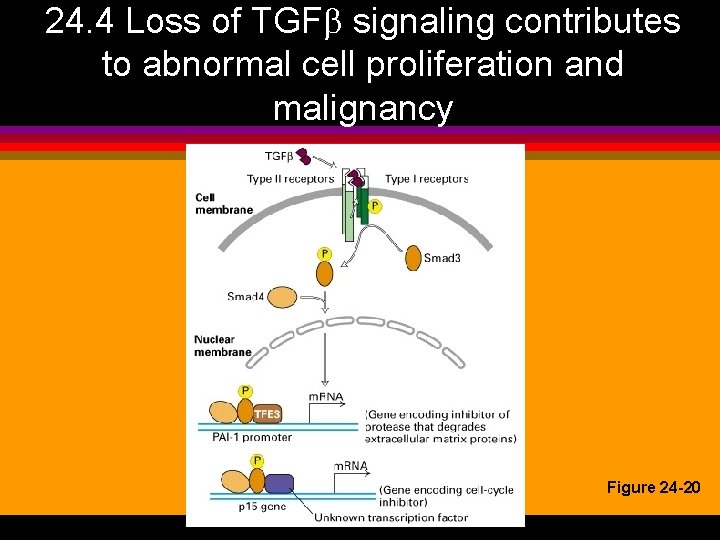
24. 4 Loss of TGF signaling contributes to abnormal cell proliferation and malignancy Figure 24 -20

Mutasjoner som påvirker genom stabilitet: p 53 og DNA reparasjonsmekanismer l l l DNA i kreftceller inneholder insersjoner, delesjoner og punktmutasjoner i sentrale vekst- og cellesykluskontrollerende gener de fleste kreftceller mangler dessuten ett eller flere DNA-reparasjonssystemer, noe som tillater mutasjonsakkumulering kreftceller er ofte defekte i sentrale kontrollmekanismer for deteksjon av ødelagt DNA, som normalt hindrer deling av celler induserer apoptose

l l l p 53 -proteinet er essensielt for kontroll og cellesyklus arrest av celler med ødelagt DNA i G 1 mutasjon i p 53 sees i mer enn 50 % av humane krefttilfeller p 53 -proteinet er uttrykt i lave konsentrasjoner i celler fordi det er ekstremt ustabilt og hurtig nedbrytbart mus som mangler p 53 utvikles normalt, men er predisponert for å utvikle flere former tumorer p 53 aktiveres under stressede betingelser (varme, UV-lys etc) ved fosforylering p 53 har mange funksjoner, hvor transkripsjonsaktivering er mest relevant som tumor suppressor
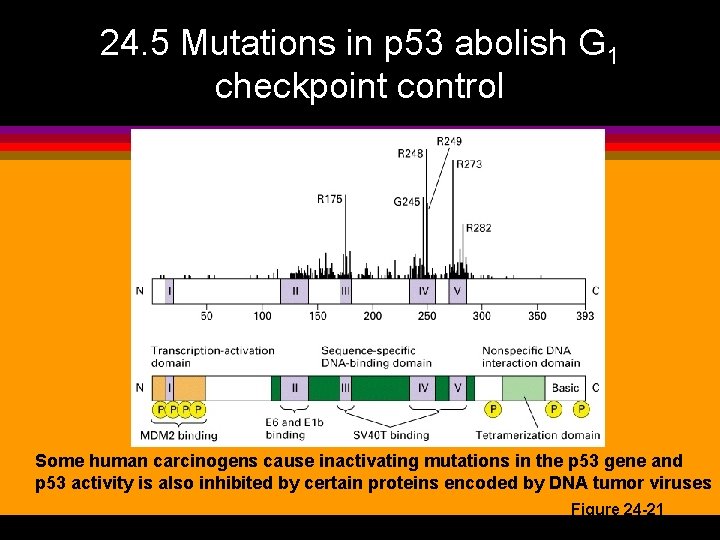
24. 5 Mutations in p 53 abolish G 1 checkpoint control Some human carcinogens cause inactivating mutations in the p 53 gene and p 53 activity is also inhibited by certain proteins encoded by DNA tumor viruses Figure 24 -21

l l l alle p 53 -mutasjoner hindrer proteinets DNA-binding p 53 induserer cyclin kinase-hemmeren p 21 som binder og og hemmer mammalske G 1 Cdk-cyclin-komplekser, noe som fører til at celler med ødelagt DNA blir arrestert i G 1 inntil skadene er reparert hvis p 53 akkumulerer, dvs at skaden ikke repareres, induseres proteiner som fører til apoptose p 53 er også viktig for overgangen G 2 til M, men detaljert mekanisme enda uviss den aktive formen av p 53 er tetramer og mutasjon i ett allel nok til å ødelegge all p 53 -aktivitet, dvs. dominant negativ mutasjon

Proteiner kodet i DNA virus kan hemme p 53 aktivitet l l HPV er istand til å indusere stabil transformasjon og forbigående vekststimulering av kultiverte celler HPV protein E 7 binder og hemmer Rb, mens E 6 hemmer p 53 HPV E 6/7 er tilstrekkelig for å transformere en celle i fravær av mutasjon i regulatoriske proteiner SV 40, lite transformerende papovavirus fra ape danner to tidlige protein, Large T og small t antigen, som translokerer til kjernen og binder p 53 og Rb, noe som fører til funksjonshemming

Defekter i DNA reparasjonssystemer forsterker mutasjoner og er assosiert med visse kreftformer l l kobling mellom carcinogenese og mangel av DNAreparasjon er foreslått da individ med nedarvede defekter i spesielle reparasjonssystemer har en dramatisk økt risiko for utvikling av visse krefttyper Xeroderma pigmentosum er en autosomal recessiv sykdom og individ med denne sykdommen utvikler hudkreft av typen melanom og squamos cell carcinomas ved eksponering til UV-stråler i sollys årsaken er mangel på reparasjon av UV-skader (bl. a. TTdimer) eller mangel til å fjerne store substituerende grupper på DNA-baser andre eksempler på mangel på DNA reparasjon og kreft i mennesket, se tabell 24 -1.

24. 5 Defects in DNA-repair systems perpetuate mutations and are associated with certain cancers
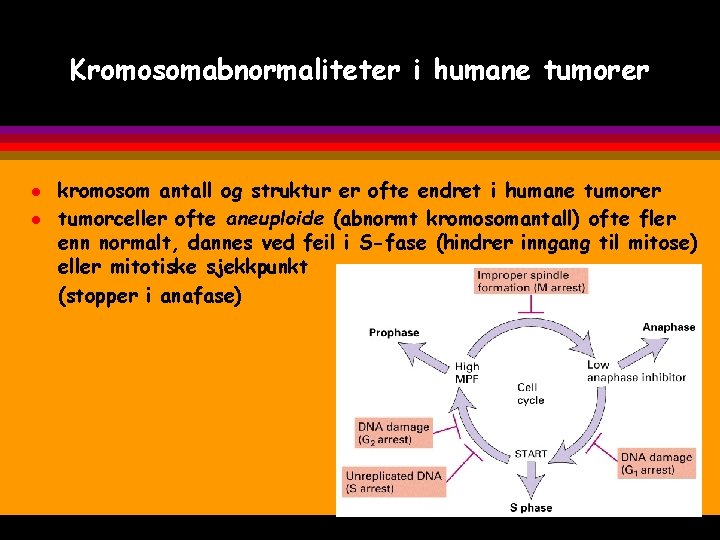
Kromosomabnormaliteter i humane tumorer l l kromosom antall og struktur er ofte endret i humane tumorer tumorceller ofte aneuploide (abnormt kromosomantall) ofte fler enn normalt, dannes ved feil i S-fase (hindrer inngang til mitose) eller mitotiske sjekkpunkt (stopper i anafase)
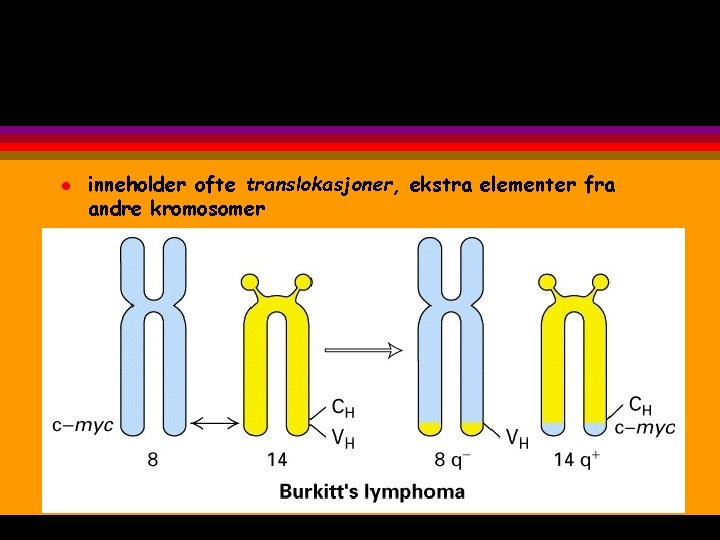
l inneholder ofte translokasjoner, ekstra elementer fra andre kromosomer
l l Lokalisert reduplisering av DNA: HSR regioner, “Double minute” kromosom Begge tilfeller av polymere former av lange strekninger med DNA, kan inneholde oncogener, f. eks. N-myc, funnet i tumorer i nervesystemet
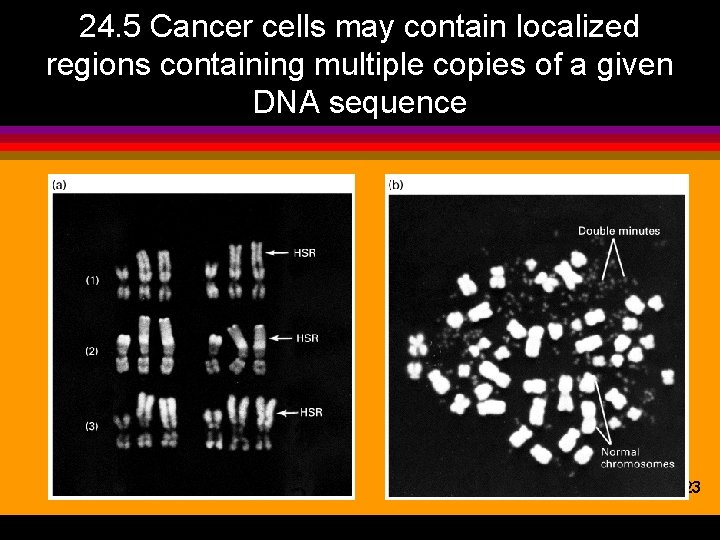
24. 5 Cancer cells may contain localized regions containing multiple copies of a given DNA sequence Figure 24 -23

Telomerase og immortalisering av celler l l l telomere sekvenser er fysiske endestykker i lineære kromosom og består av multiple repetisjoner av TTAGGG funksjon av telomere sekvenser er å hindre ufullstendig replikasjon av endestykket i ”lagging” tråd i DNA kjønnsceller og normalt hurtig delende somatiske celler, så som stamceller har egen telomerase som forlenger DNA-tråden, mens mesteparten av humane somatiske celler ikke har telomeraseaktivitet normale telomere sekvenser tillater et visst antall celledelinger 30 -40, mens tap fører til kromosomfusjoner og celledød tumorceller har overkommet telomerproblemet ved å uttrykke egen telomerase aktuell cancerterapi er hemmere mot telomerase
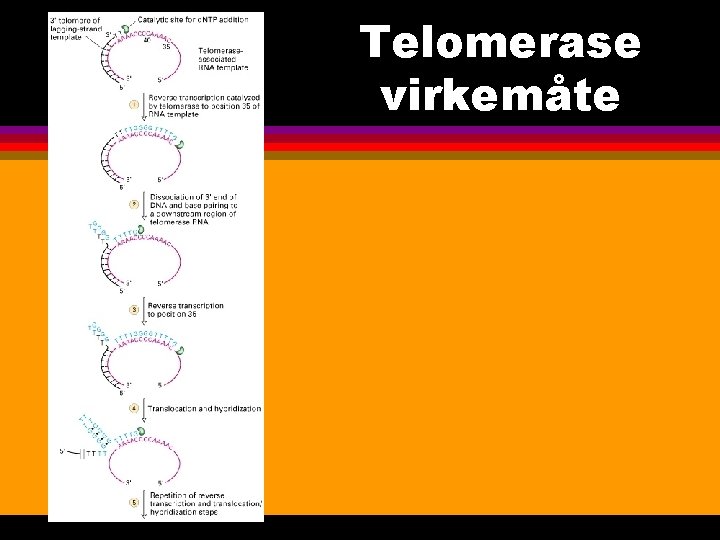
Telomerase virkemåte

DNA mikroarray i lymphom klassifisering og overlevelsesanalyser l l l Genuttrykksanalyser ved hjelp av DNA mikroarray kan skjelne mellom patologisk like tumorer systematiske analyser av genuttrykk i ”diffuse large Bcell lymphomas” (DLBCLs) den mest vanlige typen av non. Hodgkins Lymphoma indikerer at disse tumortypene kan deles inn i to subtyper -germinalt senterlike B celler -in vitro aktiverte B celler klassifisering av tumorer inn i de enkelte grupper kan utnyttes prognostisk, til å forutsi høyere/lavere risk for spredning

Konklusjoner l l l p 53 proteinet er nødvendig for kontroll og arrest av celler med skadet DNA i G 1 p 53 virker som transkripsjonsfaktor og regulerer uttrykk av p 21, en hemmer av G 1 cdk-cyclin komplekser mutasjoner i p 53 forekommer i mer enn 50% humane kreftformer p 53 er tetramer, og mutasjon i ett allel kan være nok til å hemme all aktivitet MDM 2, et protein som normalt hemmer p 53 evne til å motvirke cellesyklus eller drepe cellen, er overuttrykt i flere kreftformer defekter i DNA reparasjonsprosesser er ofte forbundet med økt kreftrisiko

l l kromosomabnormiteter, inkludert aneuploidi og translokasjoner resulterer ofte i dublisering av oncogener, f. eks. myc kreftceller, kjønnsceller og stamceller, men sjelden differensierte celler, uttrykker telomerase som medvirker ved immortalisering
- Slides: 26