KOROZIJA Pripremio Varga Itvan HEMIJSKOPREHRAMBENA SREDNJA KOLA OKA

KOROZIJA Pripremio: Varga Ištvan HEMIJSKO-PREHRAMBENA SREDNJA ŠKOLA ČOKA varga. i@neobee. net

�Definicija: Korozija predstavlja razaranje materijala koje nastaje složenim fizičko-hemijskim dejstvom okolne sredine. Naziv korozija potiče od latinske reči corrodere = izglodati, izgristi. üKorozija metala je obrnut proces od postupka dobijanja metala, i ona predstavlja prirodnu pojavu povratka metala u početno ravnotežno stanje, pri čemu sistem smanjuje slobodnu energiju.


�Prema mestu nastanka korozija može da bude: • atmosferska, • korozija u tečnosti, • podzemna korozija.

�Prema mehanizmu nastajanja razlikujemo dva osnovna tipa korozije: • elektrohemijsku koroziju - Koroziju u elektro provodljivoj sredini (u tečnim elektrolitima) i • hemijsku koroziju - Koroziju u elektro neprovodljivim sredinama (oksidaciju).

Elektrohemijska korozija �Elektrohemijska korozija nastaje stvaranjem galvanskih elemenata izmedju dva različito provodljiva metala (sa različitim standardnim potencijalom), koji se nalaze u elektrolitu.
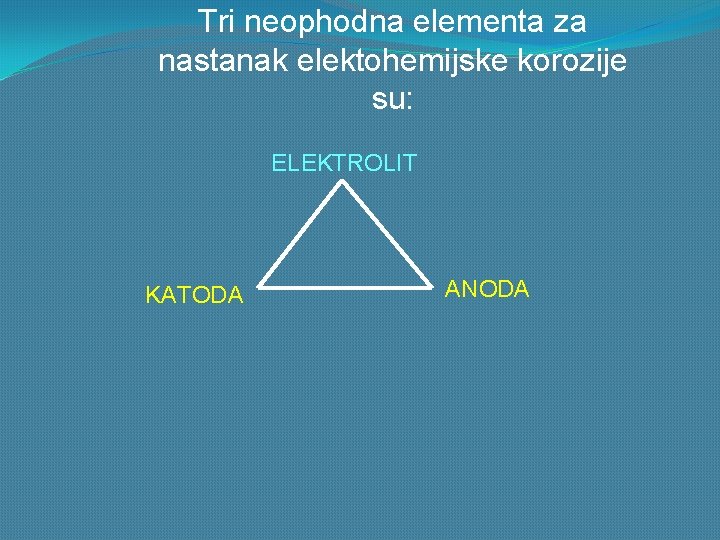
Tri neophodna elementa za nastanak elektohemijske korozije su: ELEKTROLIT KATODA ANODA
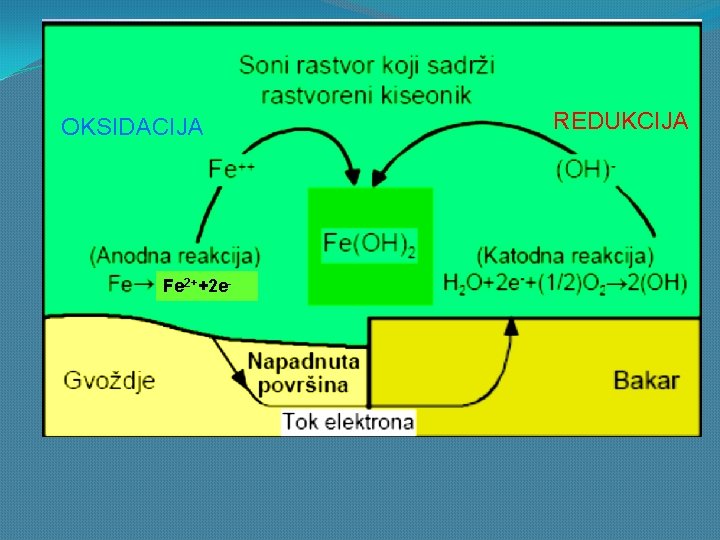
OKSIDACIJA Fe 2++2 e- REDUKCIJA
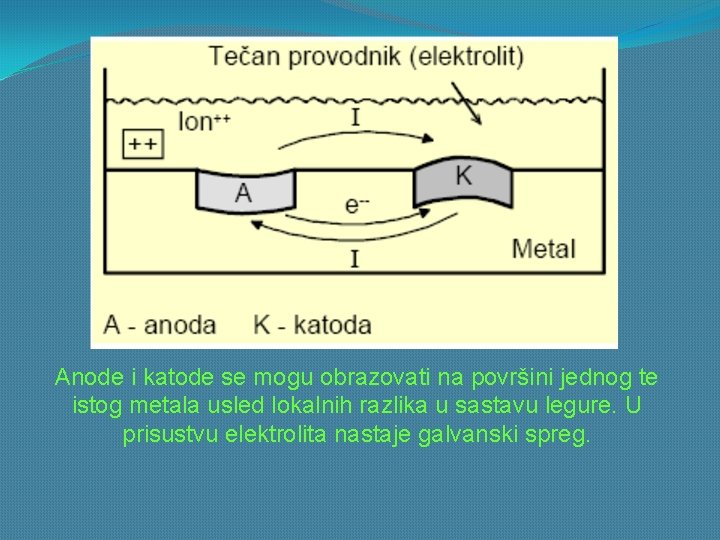
Anode i katode se mogu obrazovati na površini jednog te istog metala usled lokalnih razlika u sastavu legure. U prisustvu elektrolita nastaje galvanski spreg.



Vrste elektrohemijske korozije �Prema načinu napadanja metala, korozija može biti: • Ravnomerna, koja se karakteriše gotovo ujednačenim gubitkom metala po celoj površini izloženoj koroziji, • Neravnomerna, kad materijal biva napadan samo na odredjenim mestima.

ravnomerna neravnomerna

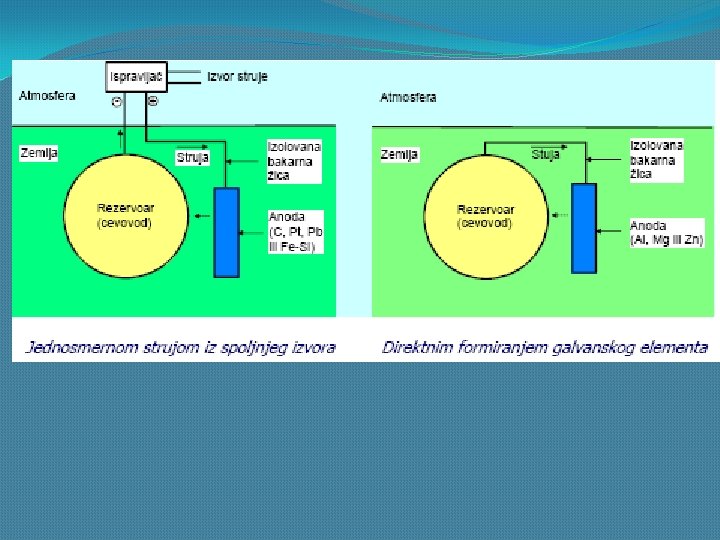
Zaštita od galvanske (elektrohemijske) korozije Galvanska (elektrohemijska) korozija nastaje kad se ispune sledeći uslovi: • spregnuti metali se razlikuju po elektrodnim potencijalima više od 50 m. V, • metali su u direktnom medjusobnom kontaktu, • oba metala su u dodiru sa istim elektrolitom i • elektrolit sadrži rastvoren O 2 ili kiselinu, što doprinosi održavanju katodnog procesa.

Zaštitne prevlake �Zaštitni slojevi ili prevlake sprečavaju kretanje elektrona i rastvaranje jona, čime impregniraju površine metalnih predmeta. �Organske prevlake deluju tako što sprečavaju da vlaga, vazduh ili druge materije prodru u osnovni metal. Pošto se ove prevlake razaraju na povišenim temperaturama, mogu se upotrebljavati samo za delove koji rade na sobnim temperaturama. Organske materije za prevlake su: boje, lakovi, adhezione plastične mase, katran, masti ulje.

�Neorganske prevlake se dele na: staklaste, smolaste ili emajlne. One u stvari predstavljaju barijeru izmedju okolne sredine i štićenog predmeta. �Metalne prevlake nanose se različitim metodama. Cinkane i kalajne prevlake obično se nanose potapanjem čistih čeličnih limova u kupatila rastopljenog Zn ili Sn. Tanje i ravnomernije prevlake nanose se elektrolitičkim postupkom (Zn, Sn). Isto se tako dobijaju dekorativne prevlake od Ni, Cr i Cd. Difuzione prevlake se formiraju na visokim tempera-turama u prisustvu sprašenog Al, Cr, Fe -Si, Zn i dr.
- Slides: 17