Konfigurasi Elektron II Bagian ini berisi Dua cara

Konfigurasi Elektron II

Bagian ini berisi: Dua cara penulisan konfigurasi elektron. Menyingkat penulisan konfigurasi elektron. Konfigurasi elektron ion positif dan negatif. Kulit valensi dan elektron valensi Elektron terakhir.

Dua cara penulisan urutan subkulit Urutan penulisan subkulit pada konfigurasi elektron ada 2, yaitu 1. Subkulit ditulis sesuai urutan tingkat energi (urut subkulit). 2. Subkulit dari kulit yang sama dikumpulkan. Contoh, konfigurasi elektron skandium 21 Sc. 1. 21 Sc : 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1 Urut tingkat 2. 21 Sc : 1 s 2 2 p 6 3 s 2 3 p 6 3 d 1 4 s 2 Urut Kulit energi

Menyingkat Konfigurasi Elektron. Penulisan konfigurasi elektron yang panjang dapat disingkat dengan menggunakan konfigurasi Gas Mulia. Unsur gas mulia Konfigurasi elektron Subkulit terakhir 2 He 1 s 2 10 Ne 1 s 2 2 p 6 18 Ar 1 s 2 2 p 6 3 s 2 3 p 6 36 Kr 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 54 Xe 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 86 Ra 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 6 s 2 4 f 14 5 d 10 6 p 6 Cara menghafalkan: Heboh Negara Argentina Karena Xepakan Ronaldo

Menyingkat Konfigurasi Elektron. 79 Au 54 Xe: Perhatikan konfigurasi Na dan Ne berikut! 1 s 2 2 p 6 11 Na : 10 Ne : 1 s 2 2 p 6 Disingkat menjadi 1 3 s 11 Na : [Ne] 3 s 1 Disingkat menjadi : 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 6 s 1 4 f 14 5 d 10 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 79 Au : [Xe] 6 s 1 4 f 14 5 d 10

Konfigurasi elektron ion Kation Anion (ion +) terbentuk dari atom yang melepas elektron (ion −) tebentuk dari atom yang menyerap elektron

Konfigurasi Kation (ion +) “Elektron yang dilepas adalah elektron dari Contoh menulis konfigurasi Fe 2+ dan Fe 3+ Kulit terluar 26 Fe: [Ar] 4 s 2 3 d 6 Elektron Fe 2+ terbentuk dari Fe yang melepas 2 elektron, sehingga: Fe 2+: [Ar] 3 d 6 (jumlah elektron = 24) Fe 3+ terbentuk dari Fe yang melepas 3 elektron, sehingga: Fe 3+: [Ar] 3 d 5 (jumlah elektron = 23) kulit terluar”. Tips langkah menentukan: 1. Tulis konfigurasi elektron atom netralnya. 2. Tentukan subkulit yang berada pada kulit terluar 3. Kurangi jumlah elektron pada subkulit terluar sejumlah muatan
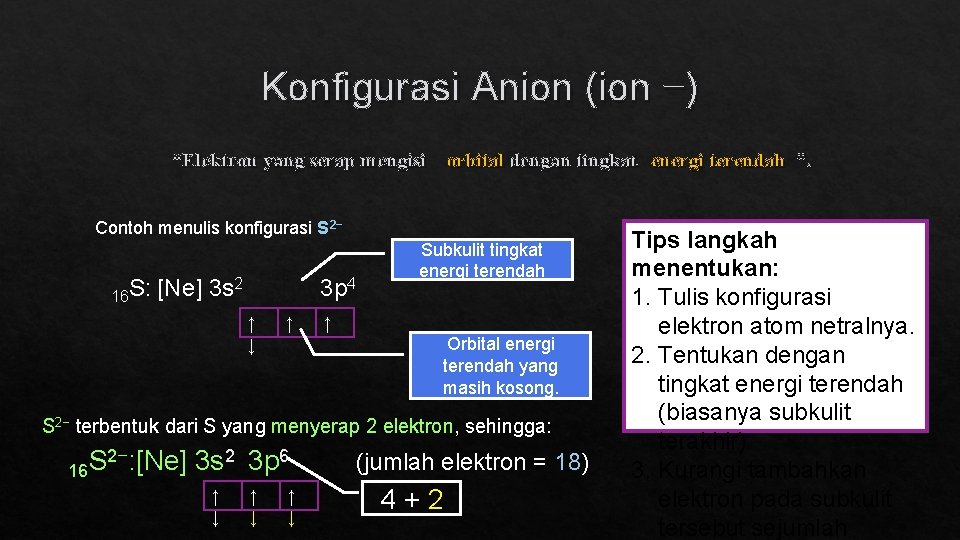
Konfigurasi Anion (ion −) “Elektron yang serap mengisi orbital dengan tingkat energi terendah ”. Contoh menulis konfigurasi S 2− 16 S: [Ne] 3 s 2 3 p 4 ↑ ↓ ↑ Subkulit tingkat energi terendah ↑ Orbital energi terendah yang masih kosong. S 2− terbentuk dari S yang menyerap 2 elektron, sehingga: 2−: [Ne] 3 s 2 3 p 6 S 16 ↑ ↓ ↑ ↓ (jumlah elektron = 18) 4+2 Tips langkah menentukan: 1. Tulis konfigurasi elektron atom netralnya. 2. Tentukan dengan tingkat energi terendah (biasanya subkulit terakhir) 3. Kurangi tambahkan elektron pada subkulit tersebut sejumlah
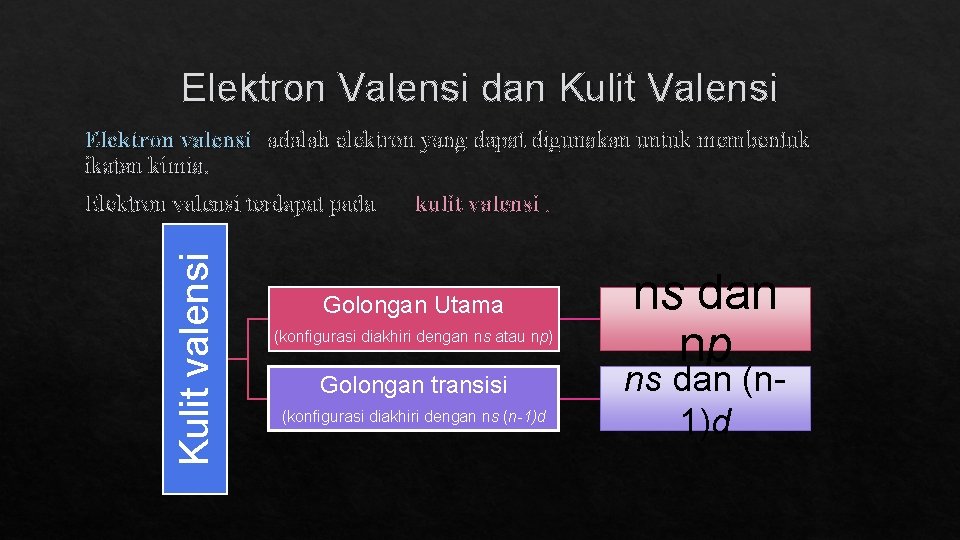
Elektron Valensi dan Kulit Valensi Elektron valensi adalah elektron yang dapat digunakan untuk membentuk ikatan kimia. Kulit valensi Elektron valensi terdapat pada kulit valensi. Golongan Utama (konfigurasi diakhiri dengan ns atau np) Golongan transisi (konfigurasi diakhiri dengan ns (n-1)d ns dan np ns dan (n 1)d

Elektron Valensi dan Kulit Valensi Contoh menentukan kulit valensi dan elektron valensi unsur. Tentukan kulit valensi dan elektron valensi dari unsur 17 Cl dan 26 Fe 17 Cl Golongan utama karena diakhiri dengan np : 1 s 2 2 p 6 3 s 2 3 p 5 Elektron Valensi = 2 + 5 = 7 Kulit valensi = 3 s 2 3 p 5 26 Fe : 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 6 Golongan transisi karena diakhiri dengan ns (n 1)d Kulit valensi = 4 s 2 3 d 6 Elektron Valensi = 2 + 6 = 8
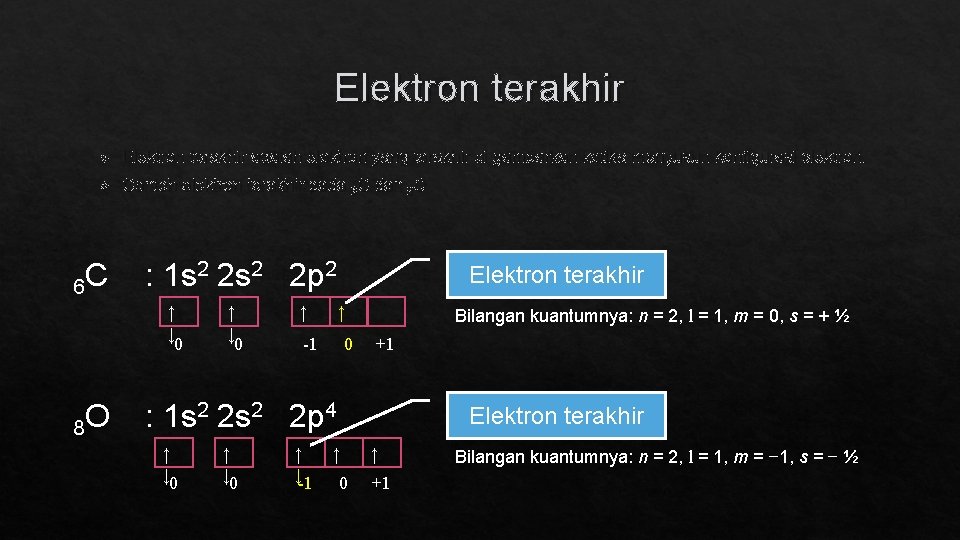
Elektron terakhir adalah elektron yang terakhir di gambarkan ketika menyusun konfigurasi elektron. Contoh elektron terakhir pada 6 C dan 8 O 6 C : 1 s 2 2 p 2 ↑ ↓ 0 8 O ↑ ↓ 0 Elektron terakhir ↑ ↑ 0 -1 Bilangan kuantumnya: n = 2, l = 1, m = 0, s = + ½ +1 : 1 s 2 2 p 4 ↑ ↓ 0 ↑ ↓-1 Elektron terakhir ↑ 0 ↑ +1 Bilangan kuantumnya: n = 2, l = 1, m = − 1, s = − ½
- Slides: 11