Komplexchemie Experimentalvortrag 21 06 2007 Drthe Fillbrandt Gliederung

Komplexchemie Experimentalvortrag, 21. 06. 2007 Dörthe Fillbrandt

Gliederung 1. 2. 3. 4. 5. 6. 7. Einstieg Geschichte Theorien - Valence-Bond-Theorie – Magnetismus - Ligandenfeldtheorie – Farbigkeit Stabilität Bestimmung der Koordinationszahl Bedeutung und Verwendung Schulrelevanz
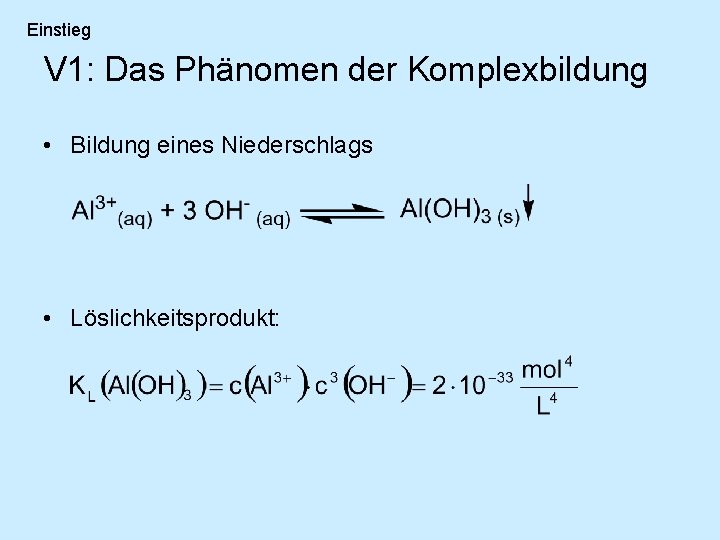
Einstieg V 1: Das Phänomen der Komplexbildung • Bildung eines Niederschlags • Löslichkeitsprodukt:
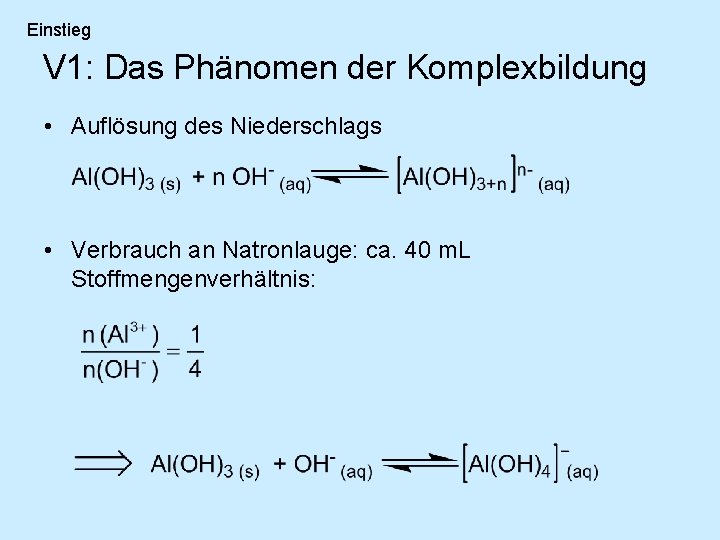
Einstieg V 1: Das Phänomen der Komplexbildung • Auflösung des Niederschlags • Verbrauch an Natronlauge: ca. 40 m. L Stoffmengenverhältnis:

Einstieg Definition „Das Prinzip der Bindung in Komplexen ist die Wechselwirkung eines elektronisch ungesättigten Zentralteilchens mit Partnern (= Liganden), die mindestens ein freies Elektronenpaar besitzen. Bindet dabei das Zentralteilchen mehr Bindungspartner, als dies nach dessen Ladung oder Stellung im PSE zu erwarten ist, so liegt ein Komplex vor. “ (Friedhelm Kober in „Komplex – Versuch einer Definition“, Pd. N-Ch. 4/34. Jahrgang 1985, S. 7)

Geschichte der Komplexchemie • 1597 Erster dokumentierter Beleg einer Komplexverbindung vom Arzt Libavius • 1704 Diesbach und Dippel entdecken das „Berliner Blau“ • 19. Jh. Führende Chemiker Frémy (Benennung von Komplexen nach Farben) und Jørgensen (Synthese einer Vielzahl von Komplexverbindungen)
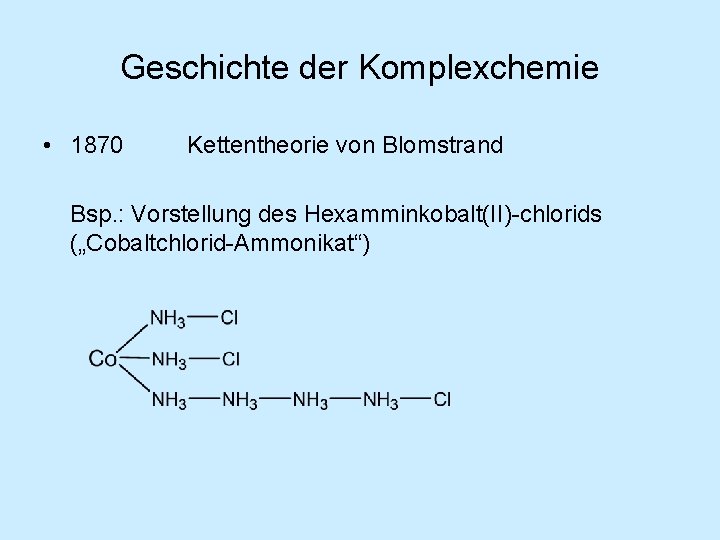
Geschichte der Komplexchemie • 1870 Kettentheorie von Blomstrand Bsp. : Vorstellung des Hexamminkobalt(II)-chlorids („Cobaltchlorid-Ammonikat“)

Geschichte Werners Koordinationstheorie • Alfred Werner (1866 -1919) – „Vater der Komplexchemie“ • 1893 „Beiträge zur Konstitution anorganischer Verbindungen“ • Werners Koordinationstheorie – „eine geniale Frechheit“ • Bindung von Liganden in erster oder zweiter Sphäre

Geschichte Werners Koordinationstheorie • Jedes Ion besitzt Hauptvalenzen, einige außerdem Nebenvalenzen • Festere Bindung der Bindungspartner durch die Nebenvalenzen • Nebenvalenzen sind räumlich gerichtet • Geometrie: KZ 4: tetraedrische oder quadratisch-planare Anordnung
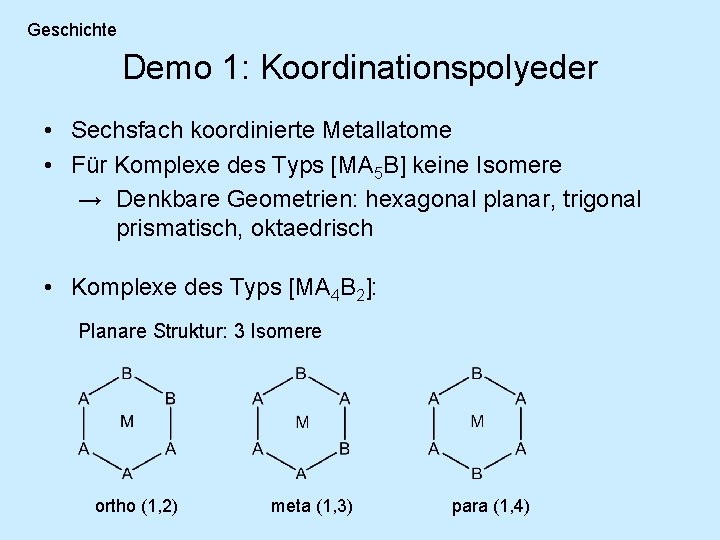
Geschichte Demo 1: Koordinationspolyeder • Sechsfach koordinierte Metallatome • Für Komplexe des Typs [MA 5 B] keine Isomere → Denkbare Geometrien: hexagonal planar, trigonal prismatisch, oktaedrisch • Komplexe des Typs [MA 4 B 2]: Planare Struktur: 3 Isomere ortho (1, 2) meta (1, 3) para (1, 4)
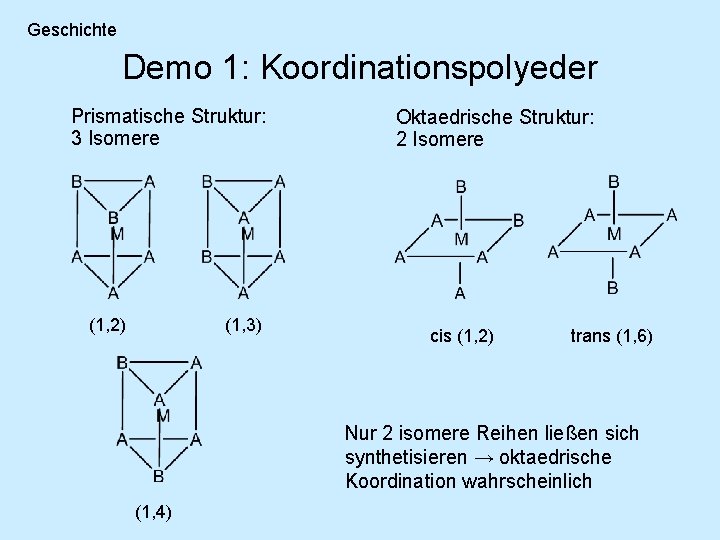
Geschichte Demo 1: Koordinationspolyeder Prismatische Struktur: 3 Isomere (1, 2) (1, 3) Oktaedrische Struktur: 2 Isomere cis (1, 2) trans (1, 6) Nur 2 isomere Reihen ließen sich synthetisieren → oktaedrische Koordination wahrscheinlich (1, 4)

Geschichte Werners Koordinationstheorie Werners Erfolge • 1894 Erklärung der Ergebnisse von Leitfähigkeitsmessungen an Amminkobaltkomplexen • 1911 Beweis der stereochemischen Vorstellung durch Enantiomerentrennung durch den Doktoranden Victor King • 1913 Nobelpreis für Chemie → seine Hypothesen noch heute theoretische Basis der Komplexchemie

Theorien V 2: Magnetische Eigenschaften • Elektron: magnetisches Moment durch Bahndrehimpuls und Eigendrehimpulses (Spin) • Gesamtes magnetisches Moment von Stoffen: resultiert aus Bahn- und Spinmomenten aller Ionen • Substanzen mit abgeschlossenen Schalen oder Unterschalen: Diamagnetismus → Abstoßung aus äußerem Magnetfeld • Substanzen mit ungepaarten Elektronen: Paramagnetismus → Anziehung
![Theorien V 2: Magnetische Eigenschaften Diamagnetischer Stoff Paramagnetischer Stoff K 4[Fe(CN)6] [Fe(H 2 O)6]SO Theorien V 2: Magnetische Eigenschaften Diamagnetischer Stoff Paramagnetischer Stoff K 4[Fe(CN)6] [Fe(H 2 O)6]SO](http://slidetodoc.com/presentation_image_h/e010f3fd517e8423cf82084d94e4afe4/image-14.jpg)
Theorien V 2: Magnetische Eigenschaften Diamagnetischer Stoff Paramagnetischer Stoff K 4[Fe(CN)6] [Fe(H 2 O)6]SO 4 Binnen= Induktion des äußeren Magnetfeldes Baußen= Induktion im Innern des Körpers
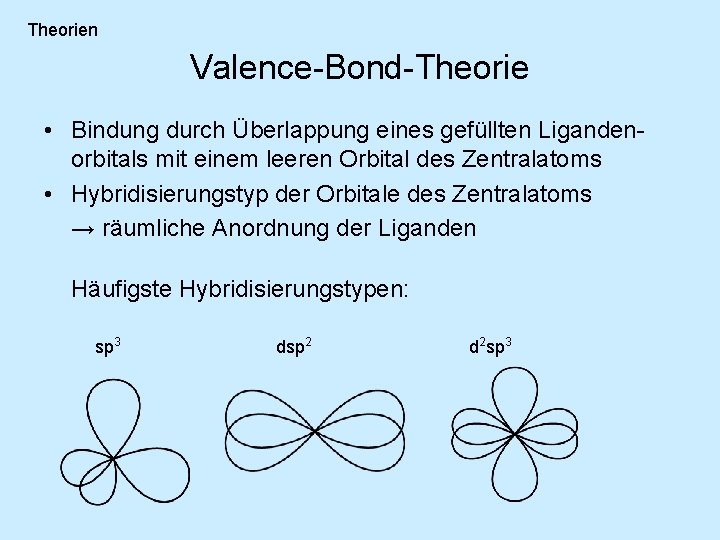
Theorien Valence-Bond-Theorie • Bindung durch Überlappung eines gefüllten Ligandenorbitals mit einem leeren Orbital des Zentralatoms • Hybridisierungstyp der Orbitale des Zentralatoms → räumliche Anordnung der Liganden Häufigste Hybridisierungstypen: sp 3 dsp 2 d 2 sp 3
![Theorien Valence-Bond-Theorie 3 d 4 s 4 p Fe 2+ [Fe(H 2 O)6]2+ paramagnetisch Theorien Valence-Bond-Theorie 3 d 4 s 4 p Fe 2+ [Fe(H 2 O)6]2+ paramagnetisch](http://slidetodoc.com/presentation_image_h/e010f3fd517e8423cf82084d94e4afe4/image-16.jpg)
Theorien Valence-Bond-Theorie 3 d 4 s 4 p Fe 2+ [Fe(H 2 O)6]2+ paramagnetisch sp 3 d 2 -Hybrid [Fe(CN)6]4 diamagnetisch durch Spinpaarung d 2 sp 3 -Hybrid 4 d
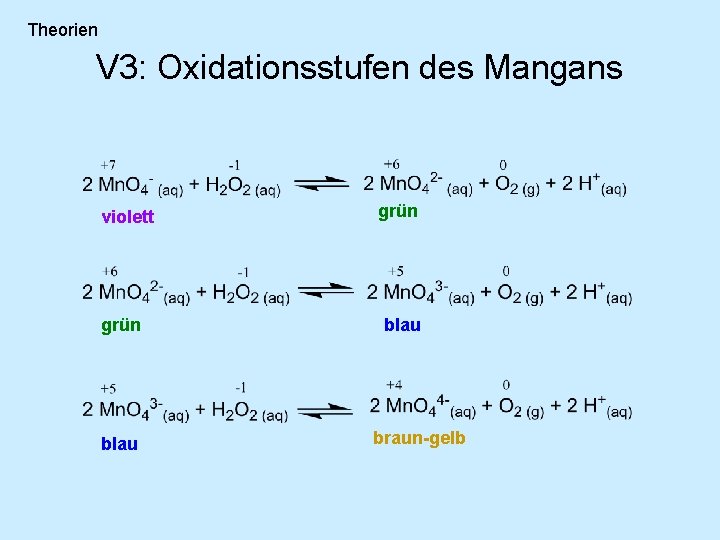
Theorien V 3: Oxidationsstufen des Mangans violett grün blau braun-gelb
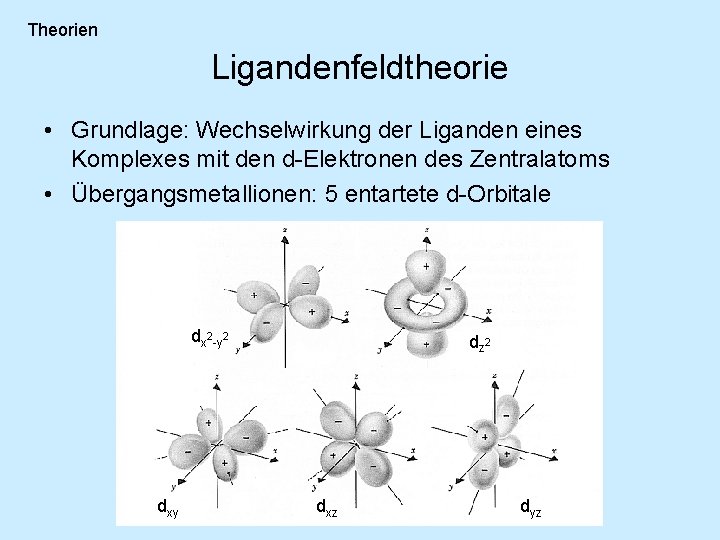
Theorien Ligandenfeldtheorie • Grundlage: Wechselwirkung der Liganden eines Komplexes mit den d-Elektronen des Zentralatoms • Übergangsmetallionen: 5 entartete d-Orbitale dx 2 -y 2 dxy dz 2 dxz dyz
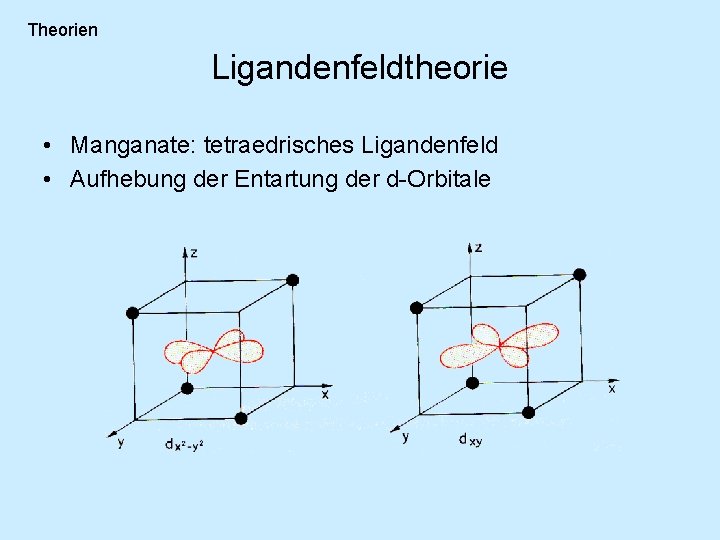
Theorien Ligandenfeldtheorie • Manganate: tetraedrisches Ligandenfeld • Aufhebung der Entartung der d-Orbitale
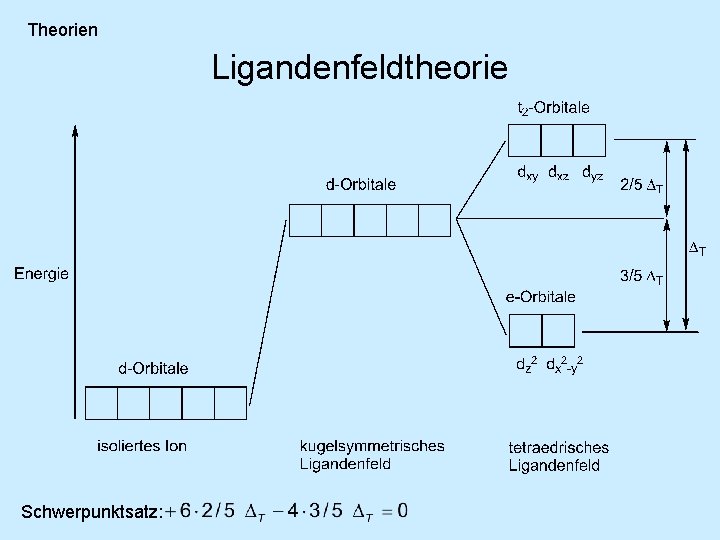
Theorien Ligandenfeldtheorie Schwerpunktsatz:
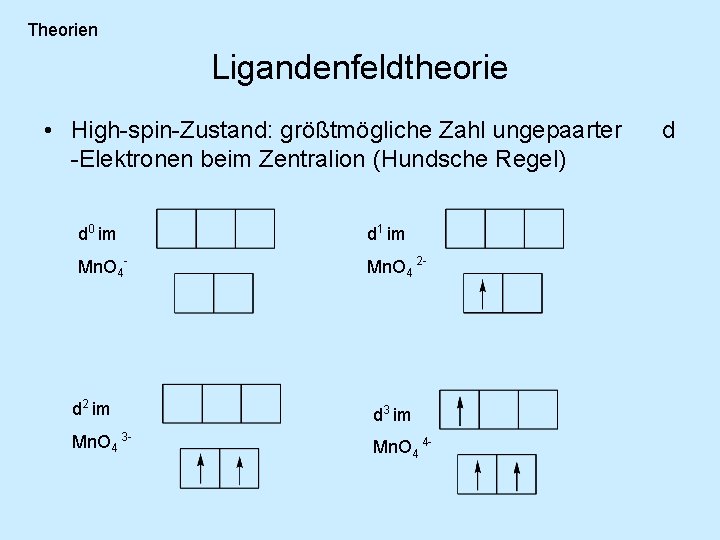
Theorien Ligandenfeldtheorie • High-spin-Zustand: größtmögliche Zahl ungepaarter -Elektronen beim Zentralion (Hundsche Regel) d 0 im d 1 im Mn. O 4 - Mn. O 4 2 - d 2 im d 3 im Mn. O 4 3 - Mn. O 4 4 - d
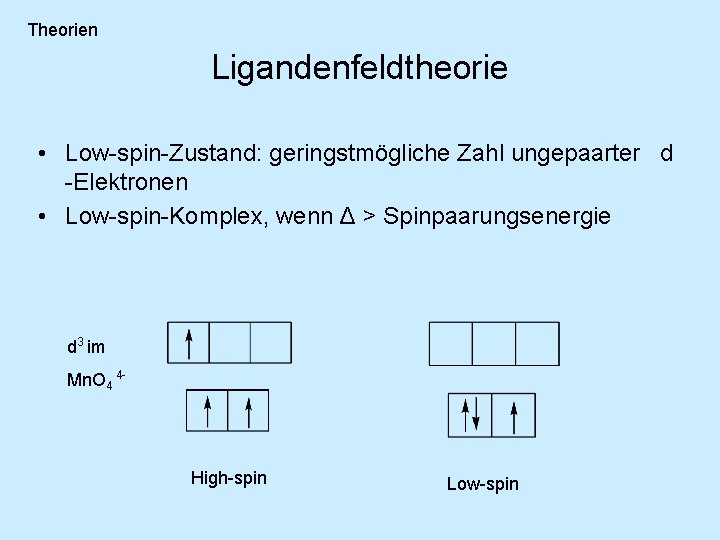
Theorien Ligandenfeldtheorie • Low-spin-Zustand: geringstmögliche Zahl ungepaarter d -Elektronen • Low-spin-Komplex, wenn Δ > Spinpaarungsenergie d 3 im Mn. O 4 4 - High-spin Low-spin
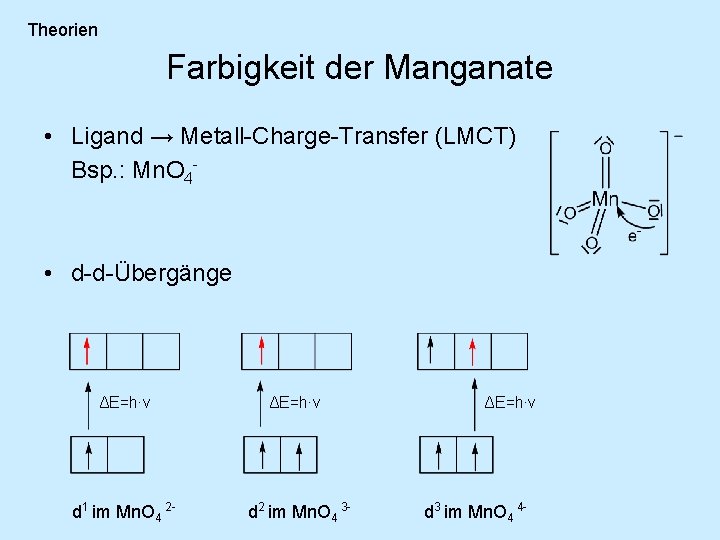
Theorien Farbigkeit der Manganate • Ligand → Metall-Charge-Transfer (LMCT) Bsp. : Mn. O 4 - • d-d-Übergänge ΔE=h∙ν d 1 im Mn. O 4 2 - ΔE=h∙ν d 2 im Mn. O 4 3 - ΔE=h∙ν d 3 im Mn. O 4 4 -

Theorien im Vergleich Valenzbindungstheorie Ligandenfeldtheorie Grundlage Kovalente Bindung Elektrostatische Wechselwirkung Struktur Ja Nein (keine Bindungstheorie) Magnetismus Richtig erklärt, aber Ja nicht vorhersagbar Farbigkeit Nein Ja
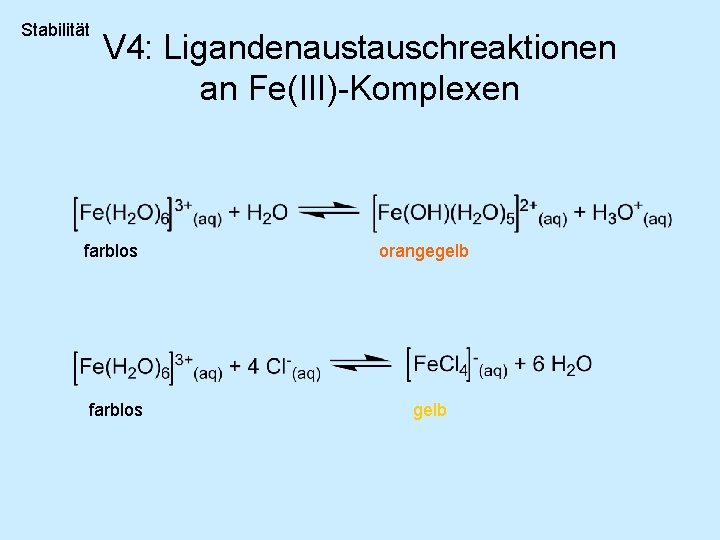
Stabilität V 4: Ligandenaustauschreaktionen an Fe(III)-Komplexen farblos orangegelb

Stabilität gelb rot V 4: Ligandenaustauschreaktionen an Fe(III)-Komplexen rot farblos → Maskierung des Fe 3+(aq) gegenüber SCN-(aq) im Fluorokomplex

Stabilität V 4: Ligandenaustauschreaktionen an Fe(III)-Komplexen Reihe der relativen Stabilität für Fe(III)-Komplexe: < < < Begründung mit HSAB-Konzept: Fe 3+: harte Säure Bindung an harte Basen SCN-: Bindung über Stickstoffatom LFSE durch Low-Spin-Komplex
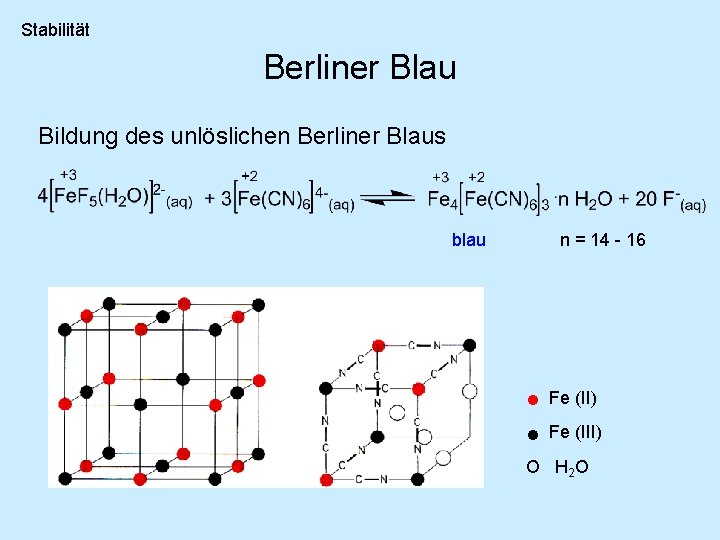
Stabilität Berliner Blau Bildung des unlöslichen Berliner Blaus blau n = 14 - 16 • Fe (II) • Fe (III) O H 2 O
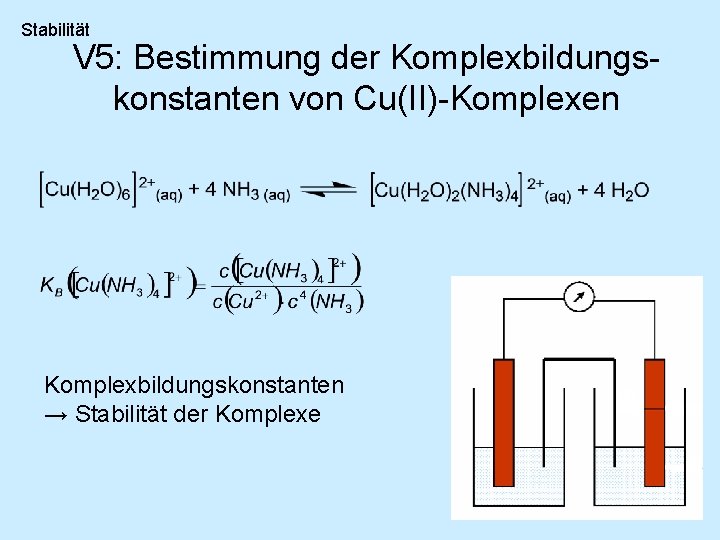
Stabilität V 5: Bestimmung der Komplexbildungskonstanten von Cu(II)-Komplexen Komplexbildungskonstanten → Stabilität der Komplexe

Stabilität V 5: Bestimmung der Komplexbildungskonstanten von Cu(II)-Komplexen Anfangskonzentration von NH 3: Halbzelle 1: Cu(SO 4)-Lsg. Halbzelle 2: Cu(SO 4)-Lsg. + NH 3 für ΔE = 0, 4 V

Stabilität V 5: Bestimmung der Komplexbildungskonstanten von Cu(II)-Komplexen Halbzelle 2: Konzentration der Cu 2+-Ionen

Stabilität V 5: Bestimmung der Komplexbildungskonstanten von Cu(II)-Komplexen Annahme: praktisch alle Cu 2+-Ionen komplexiert Gleichgewichtskonzentrationen: Literaturwert:
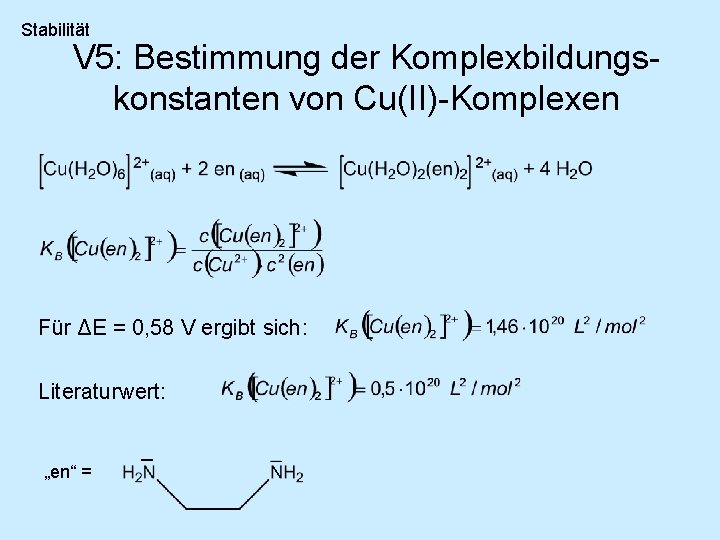
Stabilität V 5: Bestimmung der Komplexbildungskonstanten von Cu(II)-Komplexen Für ΔE = 0, 58 V ergibt sich: Literaturwert: „en“ =
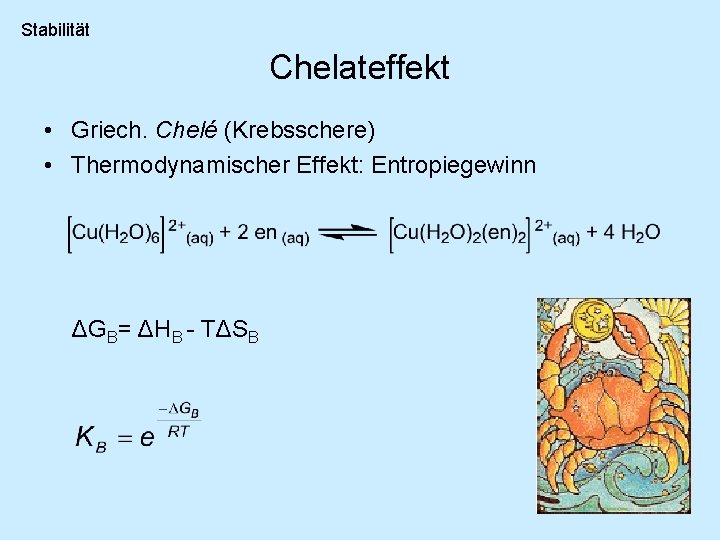
Stabilität Chelateffekt • Griech. Chelé (Krebsschere) • Thermodynamischer Effekt: Entropiegewinn ΔGB= ΔHB - TΔSB
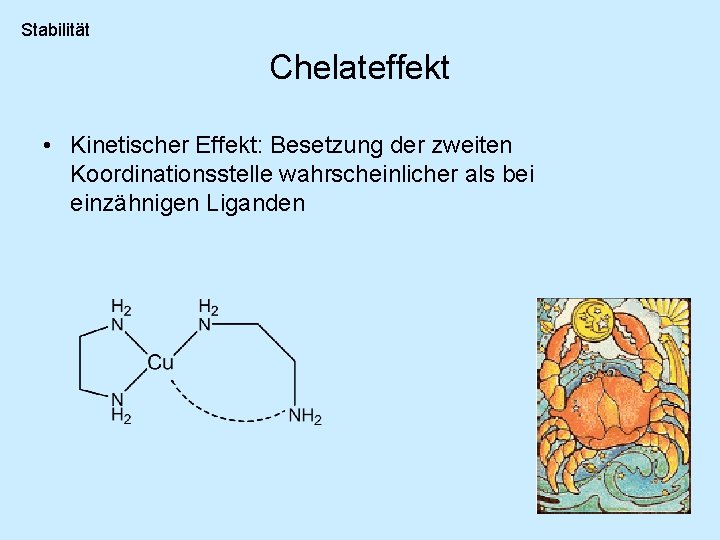
Stabilität Chelateffekt • Kinetischer Effekt: Besetzung der zweiten Koordinationsstelle wahrscheinlicher als bei einzähnigen Liganden
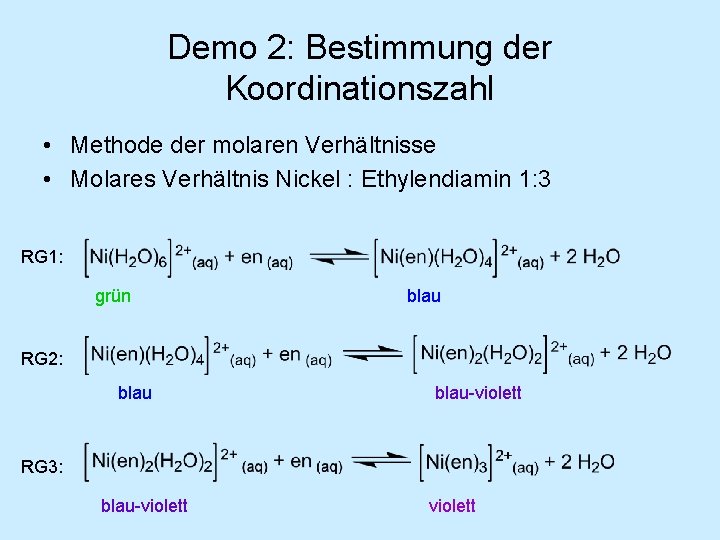
Demo 2: Bestimmung der Koordinationszahl • Methode der molaren Verhältnisse • Molares Verhältnis Nickel : Ethylendiamin 1: 3 RG 1: grün blau RG 2: blau-violett RG 3: blau-violett
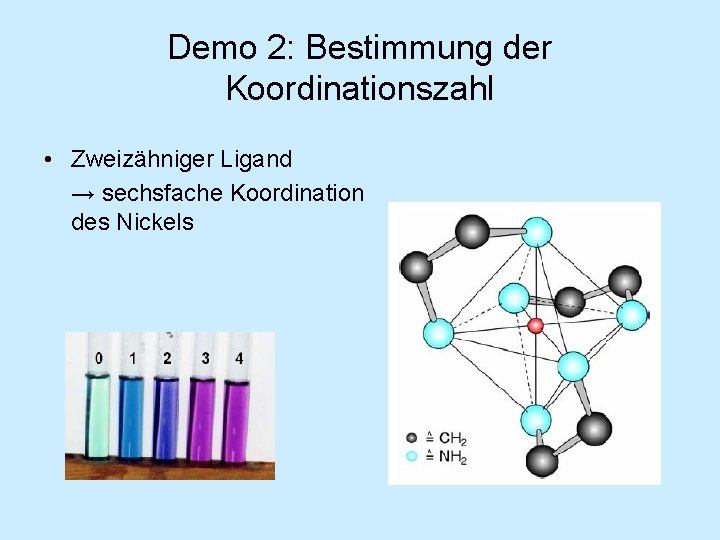
Demo 2: Bestimmung der Koordinationszahl • Zweizähniger Ligand → sechsfache Koordination des Nickels

Bedeutung und Verwendung • • • Blutfarbstoff Hämoglobin Pflanzenfarbstoff Chlorophyll Vitamin B 12 Photographie (Fixiersalz) Bestimmung der Wasserhärte Galvanotechnik Cyanidlaugerei Reaktionen mit Kronenethern „optische Thermometer“
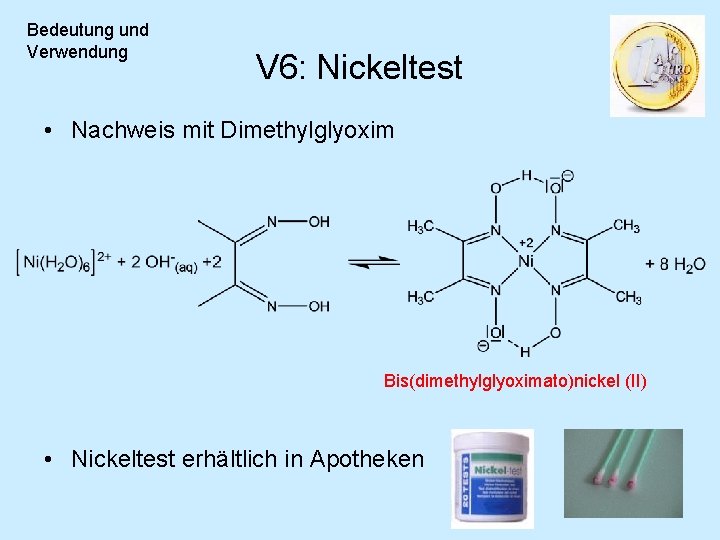
Bedeutung und Verwendung V 6: Nickeltest • Nachweis mit Dimethylglyoxim Bis(dimethylglyoximato)nickel (II) • Nickeltest erhältlich in Apotheken
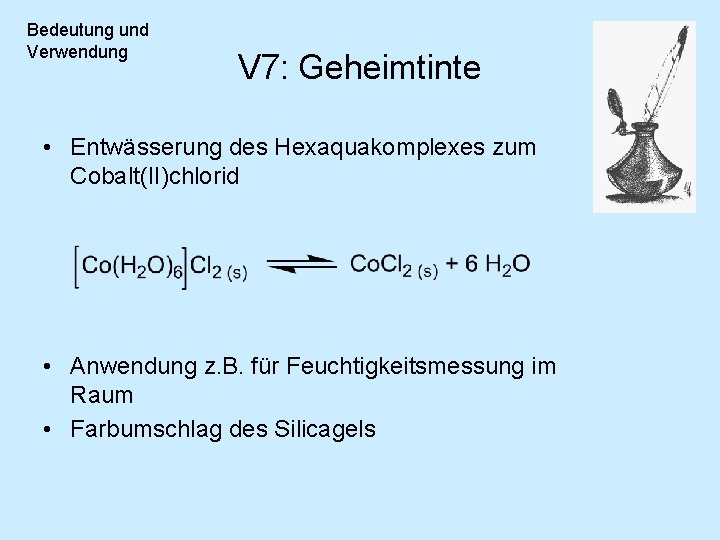
Bedeutung und Verwendung V 7: Geheimtinte • Entwässerung des Hexaquakomplexes zum Cobalt(II)chlorid • Anwendung z. B. für Feuchtigkeitsmessung im Raum • Farbumschlag des Silicagels

Schulrelevanz • LK 12 G. 2: Wahlthema Komplexchemie – – Eigenschaften und Reaktionen Aufbau und Struktur Stabilität Modellvorstellungen zur chemischen Bindung in Komplexen – Bedeutung/ Verwendung von Komplexen

Vielen Dank für die Aufmerksamkeit!
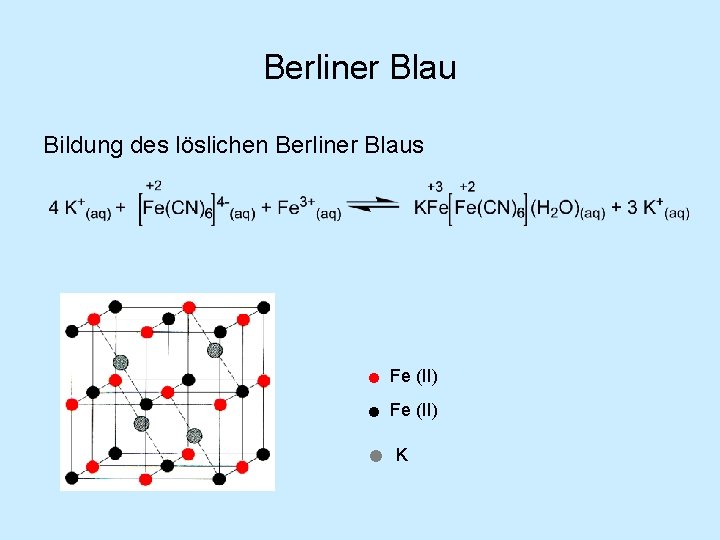
Berliner Blau Bildung des löslichen Berliner Blaus • Fe (II) • K
![Einführung V 1: Das Phänomen der Komplexbildung Elektronenstruktur Al 3+-Ion [Al(OH)4]--Komplex Einführung V 1: Das Phänomen der Komplexbildung Elektronenstruktur Al 3+-Ion [Al(OH)4]--Komplex](http://slidetodoc.com/presentation_image_h/e010f3fd517e8423cf82084d94e4afe4/image-44.jpg)
Einführung V 1: Das Phänomen der Komplexbildung Elektronenstruktur Al 3+-Ion [Al(OH)4]--Komplex
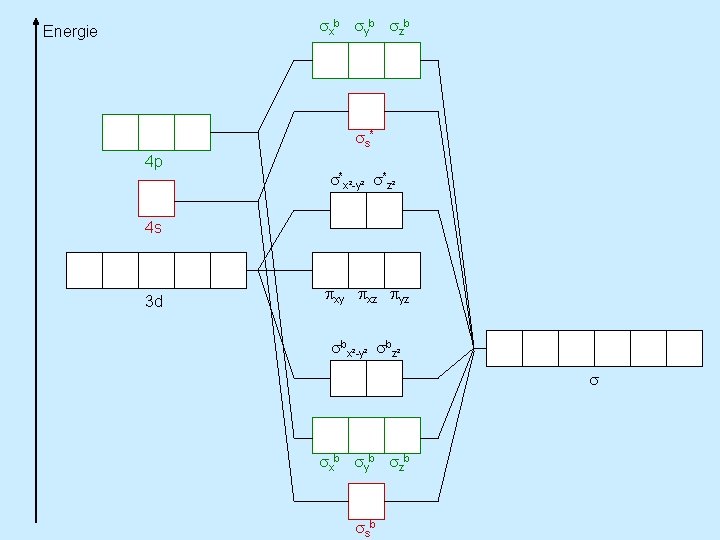
xb yb zb Energie s* 4 p *x²-y² *z² 4 s 3 d xy xz yz bx²-y² bz² xb yb zb sb
- Slides: 45