KOMPLEKSOMETRI v v v Titrasi kompleksometri berdasarkan pada
KOMPLEKSOMETRI

v v v Titrasi kompleksometri berdasarkan pada reaksi antara logam dengan ligan untuk membentuk komplek logam-ligan. Dasarnya adalah reaksi asam-basa Lewis, dimana terjadi pendonoran elektron dari satu senyawa ke senyawa lain Ligan yang dipakai dalam kompleksometri dikenal juga sebagai senyawa pengkhelat Ligan yang digunakan mengikat logam dengan lebih dari satu atom v Biasanya senyawa pengkhelat memiliki atom N atau O Unsur tersebut memiliki pasangan elektron bebas untuk didonorkan pada logam v Ligan yang memberikan 1 PEB monodentat, 2 PEB bidentat, dst…. v Ion logam membentuk ikatan koordinasi sebanyak 2, 4 atau lebih bilangan koordinasi.
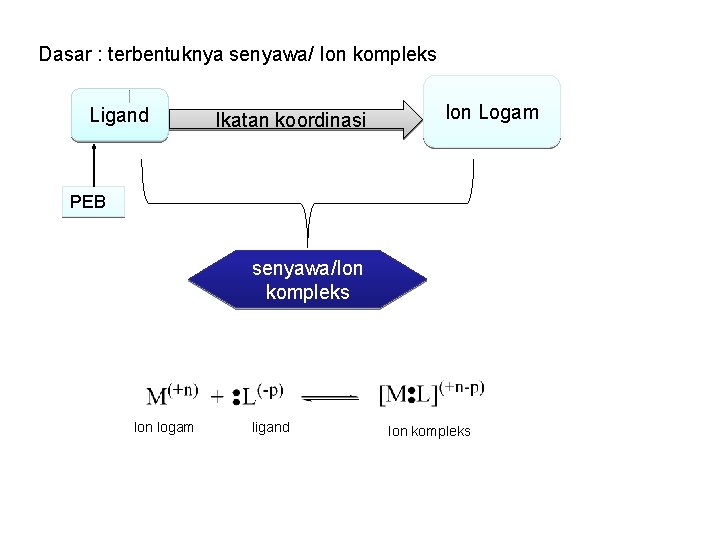
Dasar : terbentuknya senyawa/ Ion kompleks Ligand Ikatan koordinasi Ion Logam PEB senyawa/Ion kompleks Ion logam ligand Ion kompleks
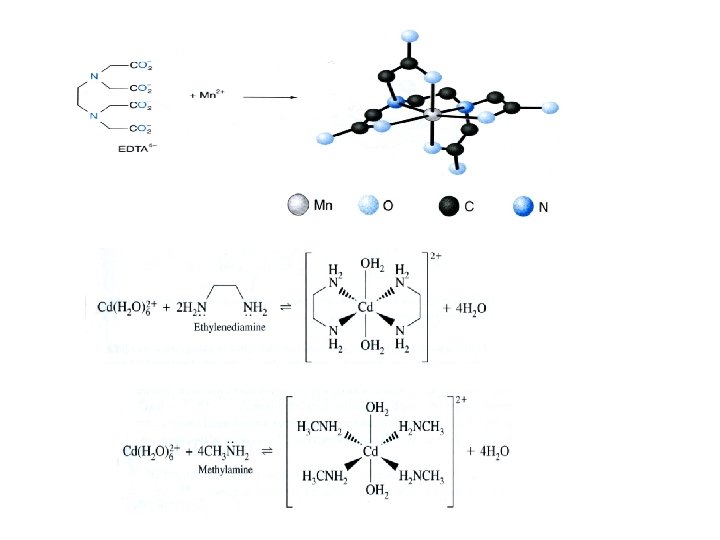
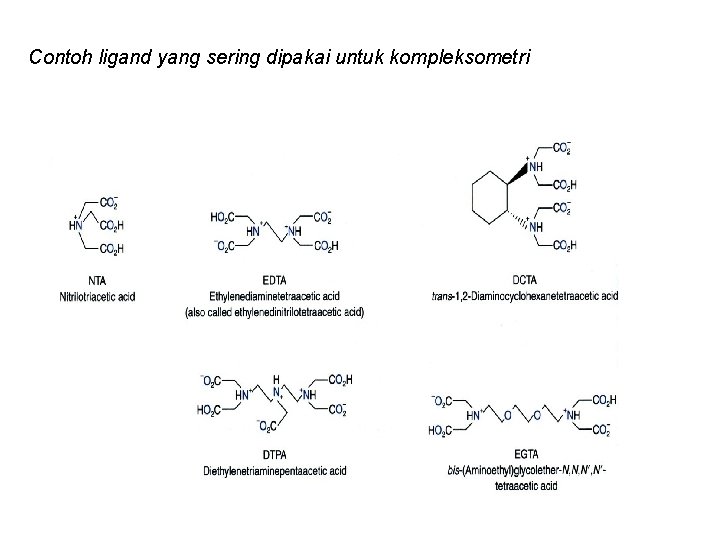
Contoh ligand yang sering dipakai untuk kompleksometri
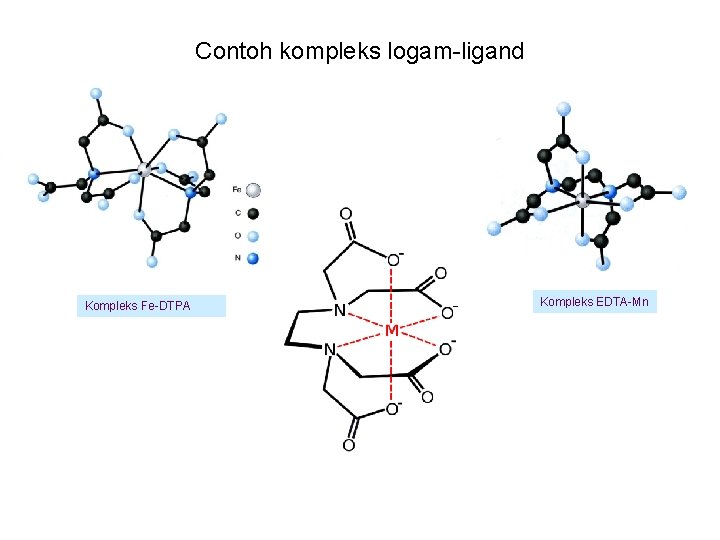
Contoh kompleks logam-ligand Kompleks Fe-DTPA Kompleks EDTA-Mn
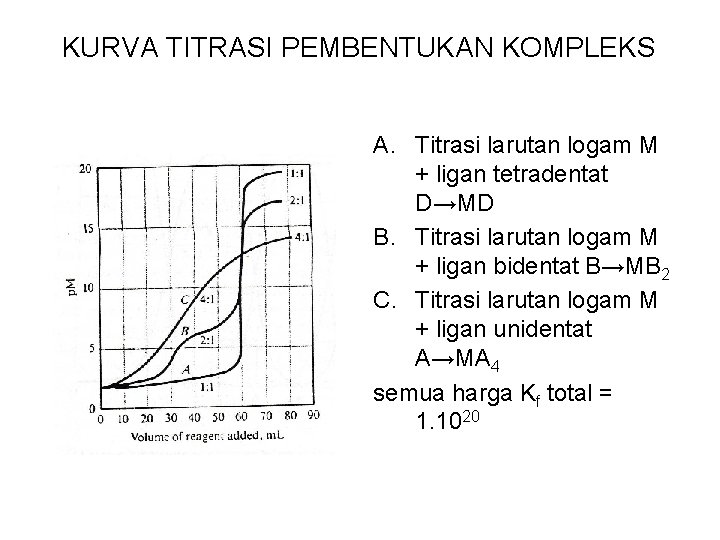
KURVA TITRASI PEMBENTUKAN KOMPLEKS A. Titrasi larutan logam M + ligan tetradentat D→MD B. Titrasi larutan logam M + ligan bidentat B→MB 2 C. Titrasi larutan logam M + ligan unidentat A→MA 4 semua harga Kf total = 1. 1020

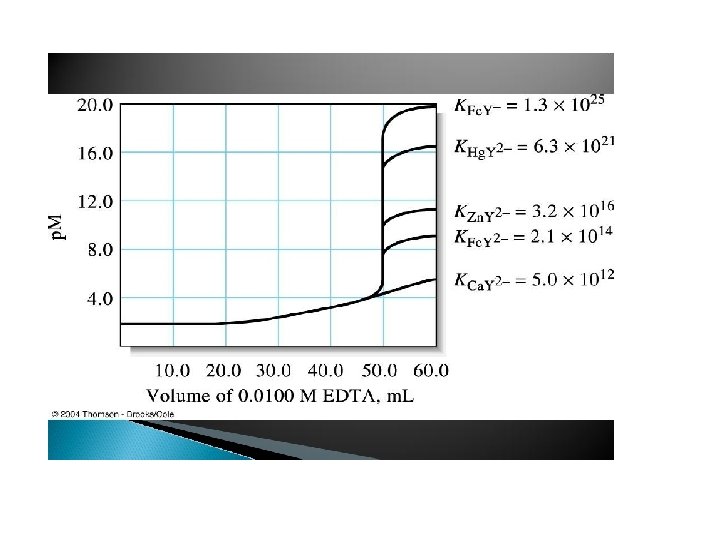

Konstanta Pembentukan , Kf v v Konstanta kesetimbangan dari reaksi antara ion logam (M+n) dan senyawa pengkelat (L-P) dikenal dengan konstanta pembentukan atau konstanta stabilitas. Umumnya senyawa pengkhelat dengan lebih dari satu pasang elektron untuk didonorkan akan membentuk senyawa kompleks yang lebih kuat dibanding yang memiliki satu pasang elektron - Biasanya lebih dari satu O atau N Harga Kf lebig besar Kf = [M: L](+n-p) [M(+n)] [: L(-p)]

Contoh titrasi kompleks Titrasi sianida – ion perak (metode Leibig) Larutan standart : ion perak (Ag. NO 3) Reaksi : TE : Ag+ + CN- ↔ Ag(CN)2 TA : Ag+ +Ag(CN)2 - ↔ Ag[Ag(CN)2]s putih

Modifikasi metode Leibig – Deniges Larutan standart : Ag. NO 3, KCN (titran) Suasana : basa (NH 3) Indikator : (KI) Penentuan : ion logam (mis : Ni 2+) dalam suasana basa (NH 3) dan KI Reaksi : 1. Ni(NH 3)42+ + Ag+ ↔ Ag(NH 3)4+ + Ni 2+ 2. Ag+ (lebih) + I- ↔ Ag. I(s) 3. Ag. I + 2 CN- ↔ Ag(CN)2 - + I 4. Ni(NH 3)42+ + 4 CN- ↔ Ni(CN)42 - + 4 NH 3 5. Ag+ + I- ↔ Ag. I

Titrasi ion klorida dengan ion merkuri Dasar : komplek antara ion halogen, sianida, dan tiosianat dengan ion merkuri(II) Ex : reaksi antara ion klorida – Hg(II) Cl- + Hg 2+ ↔ Hg. Cl+ Cl- + Hg. Cl+ ↔ Hg. Cl 2 Cl- + Hg. Cl 2 ↔ Hg. Cl 3 Cl- + Hg. Cl 3 - Hg. Cl 4 Kelebihan ion Hg lewat TE akan bereaksi dengan indikator natrium nitro prusida (Na 2 Fe(CN)5 NO TA : terbentuk endapan garam merkri (II) nitroprusida Hg 2+ + Fe(CN)5 NO 2 - ↔ Hg. Fe(CN)5 NO(s)

Titrasi dengan EDTA (khelatometri) EDTA : Ethylene diamine tetra acetic acid • paling banyak dipakai dalam titrasi kompleksometri • memiliki 6 pasang elektron bebas pada 4 atom O dan 2 atom N, yang dapat terikat pada ion logam harga Kf yang tinggi & punya 6 struktur asam-basa. Senyawa tersebut tidak larut dalam air, sedang bentuk garamnya larut baik dalam air. EDTA H 4 Y EDTA dijual dalam bentuk Na 2 H 2 Y. 2 H 2 O dengan nama komplekson III atau tritriplex trilon B
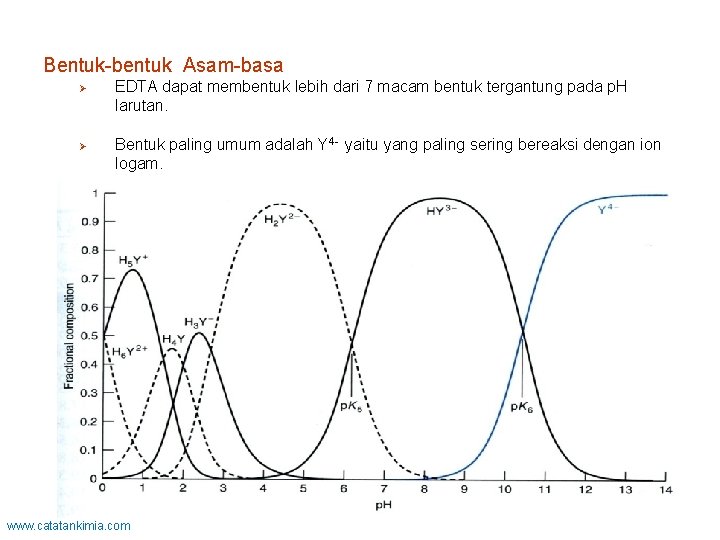
Bentuk-bentuk Asam-basa Ø Ø EDTA dapat membentuk lebih dari 7 macam bentuk tergantung pada p. H larutan. Bentuk paling umum adalah Y 4 - yaitu yang paling sering bereaksi dengan ion logam. www. catatankimia. com
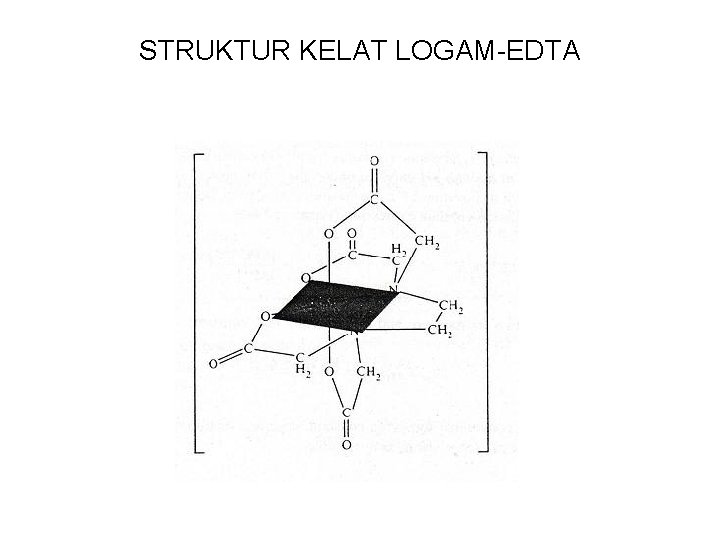
STRUKTUR KELAT LOGAM-EDTA
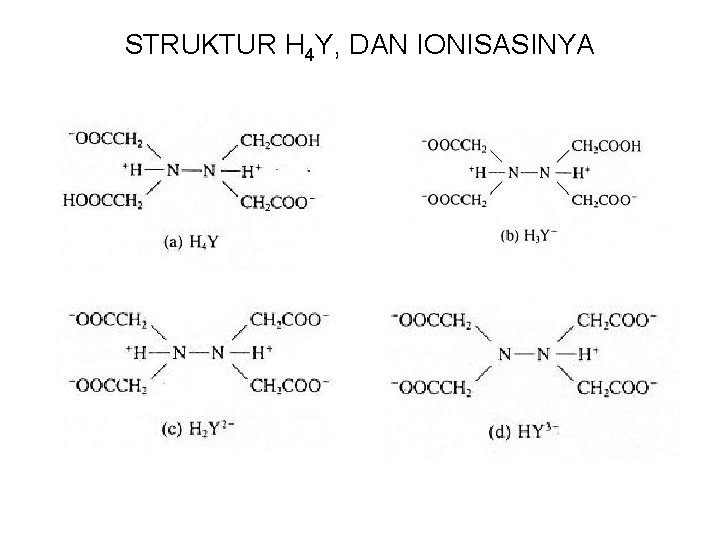
STRUKTUR H 4 Y, DAN IONISASINYA
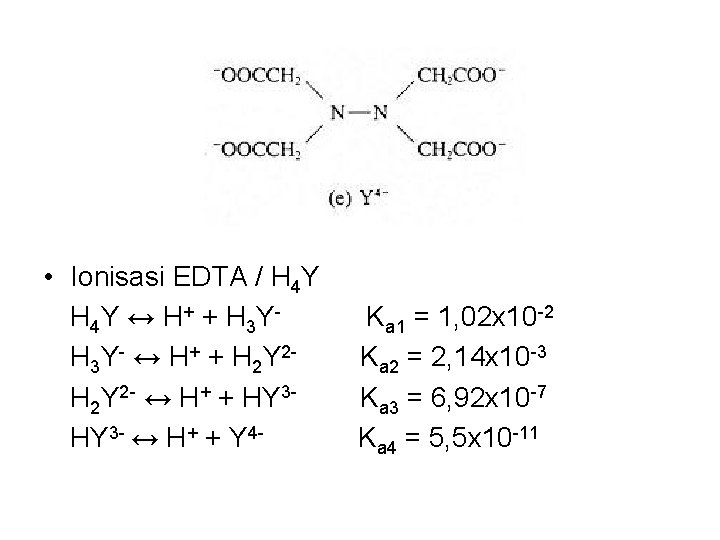
• Ionisasi EDTA / H 4 Y ↔ H + + H 3 Y- ↔ H+ + H 2 Y 2 - ↔ H+ + HY 3 - ↔ H+ + Y 4 - Ka 1 = 1, 02 x 10 -2 Ka 2 = 2, 14 x 10 -3 Ka 3 = 6, 92 x 10 -7 Ka 4 = 5, 5 x 10 -11
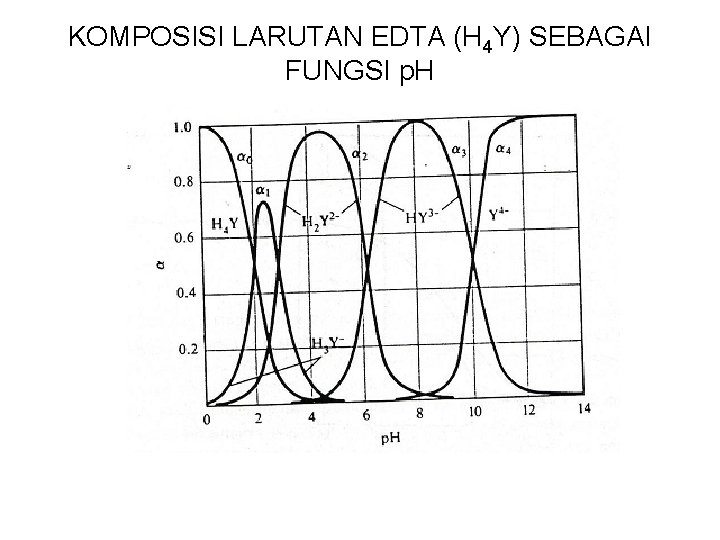
KOMPOSISI LARUTAN EDTA (H 4 Y) SEBAGAI FUNGSI p. H
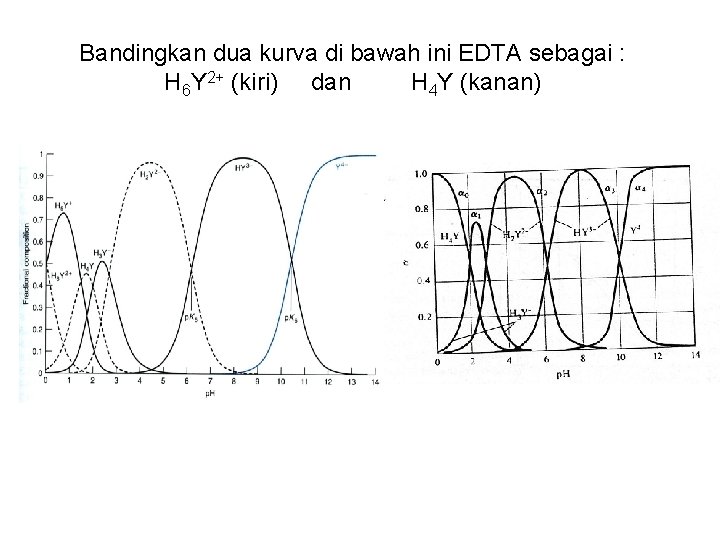
Bandingkan dua kurva di bawah ini EDTA sebagai : H 6 Y 2+ (kiri) dan H 4 Y (kanan)

KONSTANTA PEMBENTUKAN UNTUK KOMPLEKS EDTA

Indikator untuk titrasi EDTA • eriochrome Black T (EBT) dengan beberapa logam H 2 O + H 2 In- ↔ HIn 2 - + H 3 O+ K 1 = 5 x 10 -7 H 2 O + HIn 2 - ↔ In 3 - + H 3 O+ K 2 = 2, 8 x 10 -12 merah biru merah • kompleks logam (M) dengan EBT berwarna merah yaitu sebagai H 2 In • kelebihan EDTA larutan jadi biru MIn- + HY 3 - ↔ HIn 2 - + MY 2 • Kf Mg. In (1 x 107) lebih stabil dari pada Ca. In (2, 5 x 105), shg saat Ca. In HIn 2 - terjadi sebelum equivalen
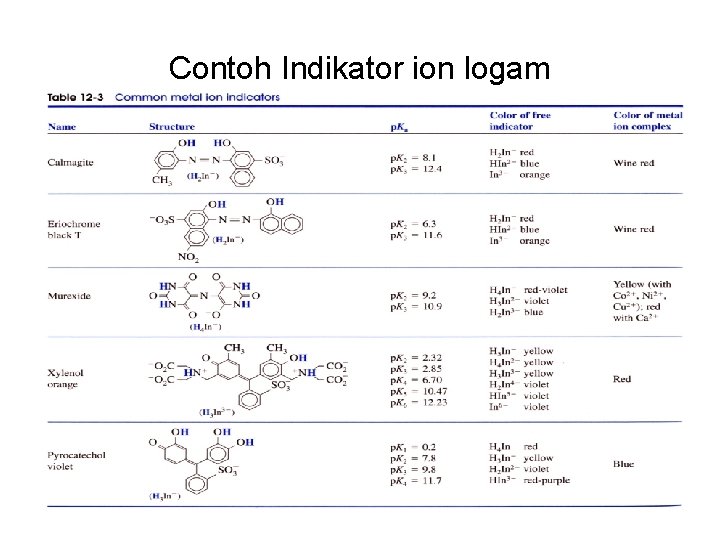
Contoh Indikator ion logam
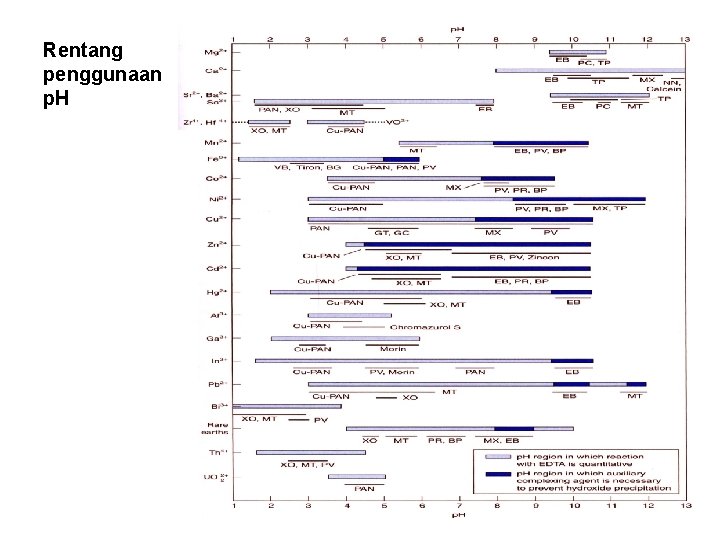
Rentang penggunaan p. H
- Slides: 24