KOMPLEKSOMETRI lanjutan Beberapa metode titrasi dengan EDTA 1

KOMPLEKSOMETRI lanjutan

Beberapa metode titrasi dengan EDTA 1. Titrasi langsung - didasarkan pada indikator untuk ion logam tertentu - penambahan ion logam lain - menambah sedikit ion logam lain ke dalam EDTA terbentuk kompleks – EDTA yg kurang stabil dari pada kompleks – analat ex : Ca 2+ + EBT kurang memuaskan, maka : a. di+ Mg. Cl 2 ke larutan EDTA b. awal titrasi : Mg 2+ + EDTA Mg – EDTA Ca 2+ + Mg – EDTA Ca – EDTA + Mg 2+ + EBT Mg – EBT , merah Mg – EBT + EDTA Mg – EDTA + EBT, biru Ca sudah terkompleks semua

Erio - T indicator or Eriochrome Black-T indicator is used in this titration. When it is chealted or acidifies, it produces a PINK RED solution. When it is not chelated and under basic conditions it is BLUE. The picture on the left shows the color of the indicator before titration. The three pictures to the right show the end point in this titration. There is a 1 drop difference of 0. 01 M EDTA between the first and second pictures and between the second and third pictures. Two or three seconds were allowed for colors in the second and third pictures to develop after adding the additional drop. In each case the solution was thoroughly mixed. This color change from wine red to violet to blue is due to the compact nature of the complex. The statement "the compact nature of the complex" means when the indicator is added to the hard water, the indicator Erio-T forms a complex with the Ca+2 ions that is pink in color. As EDTA is added to the solution, the EDTA forms a complex with the Ca+2 leaving the indicator Erio-T uncomplexed, which is blue in color.
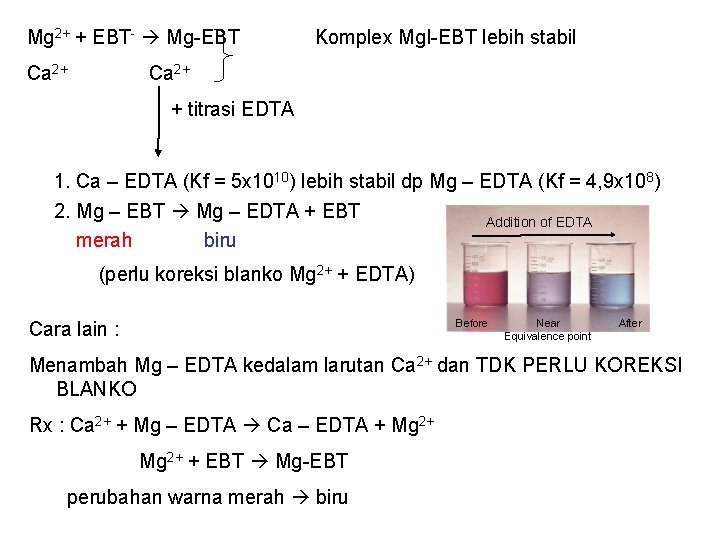
Mg 2+ + EBT- Mg-EBT Ca 2+ Komplex Mg. I-EBT lebih stabil Ca 2+ + titrasi EDTA 1. Ca – EDTA (Kf = 5 x 1010) lebih stabil dp Mg – EDTA (Kf = 4, 9 x 108) 2. Mg – EBT Mg – EDTA + EBT merah biru Addition of EDTA (perlu koreksi blanko Mg 2+ + EDTA) Cara lain : Before Near After Equivalence point Menambah Mg – EDTA kedalam larutan Ca 2+ dan TDK PERLU KOREKSI BLANKO Rx : Ca 2+ + Mg – EDTA Ca – EDTA + Mg 2+ + EBT Mg-EBT perubahan warna merah biru

2. Titrasi Balik - untuk menentukan kation yang bila dg EDTA terbentuk kompleks stabil. Tapi tidak ada indikator yg cocok - untuk penentuan kation yg bereaksi lambat dg EDTA - bila analat mengendap pada p. H yg diperlukan untuk titrasi M 1 n+ + EDTA berlebih M 1 - EDTA + EDTA sisa + M 2 n+ (standart) + EBT M 2 - EDTA (syarat M 1 - EDTA harus lebih stabil dp M 2 - EDTA
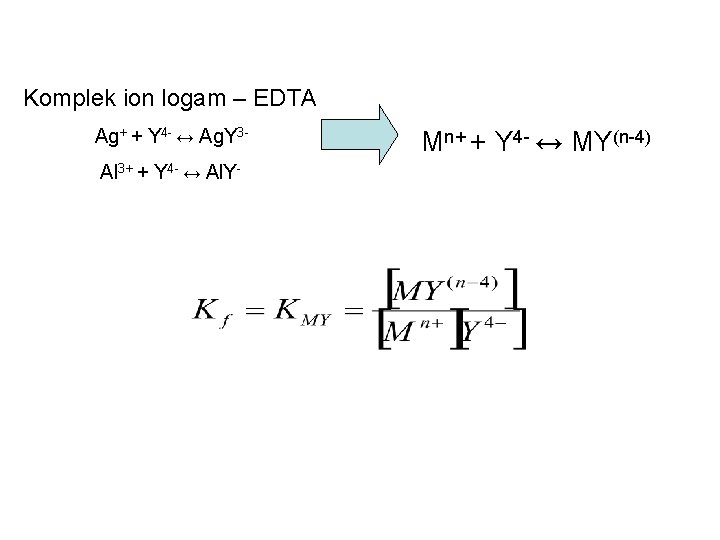
Komplek ion logam – EDTA Ag+ + Y 4 - ↔ Ag. Y 3 Al 3+ + Y 4 - ↔ Al. Y- Mn+ + Y 4 - ↔ MY(n-4)
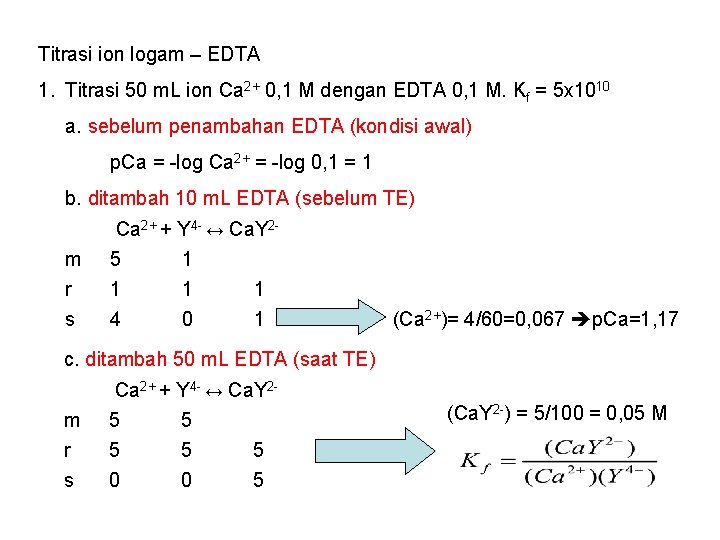
Titrasi ion logam – EDTA 1. Titrasi 50 m. L ion Ca 2+ 0, 1 M dengan EDTA 0, 1 M. Kf = 5 x 1010 a. sebelum penambahan EDTA (kondisi awal) p. Ca = -log Ca 2+ = -log 0, 1 = 1 b. ditambah 10 m. L EDTA (sebelum TE) m r s Ca 2+ + Y 4 - ↔ Ca. Y 25 1 1 4 0 1 (Ca 2+)= 4/60=0, 067 p. Ca=1, 17 c. ditambah 50 m. L EDTA (saat TE) m r s Ca 2+ + Y 4 - ↔ Ca. Y 25 5 5 0 0 5 (Ca. Y 2 -) = 5/100 = 0, 05 M
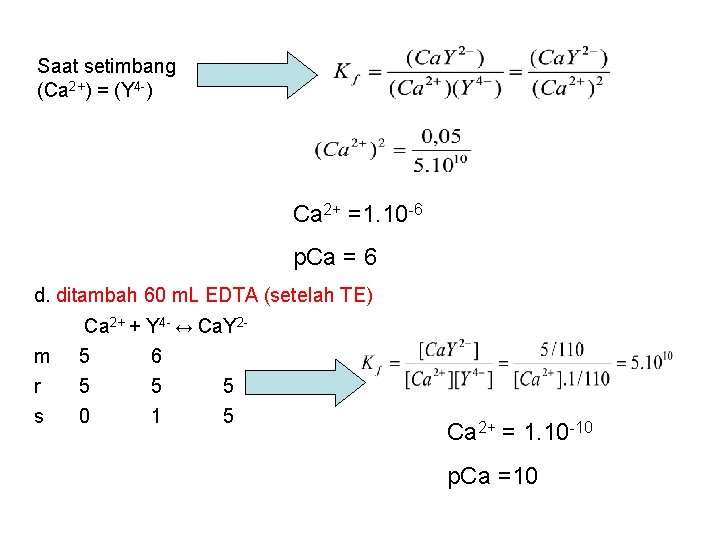
Saat setimbang (Ca 2+) = (Y 4 -) Ca 2+ =1. 10 -6 p. Ca = 6 d. ditambah 60 m. L EDTA (setelah TE) m r s Ca 2+ + Y 4 - ↔ Ca. Y 25 6 5 5 5 0 1 5 Ca 2+ = 1. 10 -10 p. Ca =10

Pengaruh p. H pada titrasi EDTA. Fraksi EDTA dalam bentuk Y 4 - dinyatakan sebagai : Dimana CT = konsentrasi total EDTA yang tidak membentuk komplek. CT = [Y 4 -] + [HY 3 -] + [H 2 Y 2 -] + [H 3 Y-] + [H 4 Y] [Y 4 -] tergantung α 4 dan α 4 merupakan fungsi [H+], makin besar [H+] makin sedikit Y 4 - yang tersedia.

Harga α 4 untuk EDTA pada berbagai p. H 2 α 4 = 3, 7 x 10 -14 p. H 3 α 4 = 2, 5 x 10 -11 p. H 4 α 4 = 3, 6 x 10 -9 p. H 5 α 4 = 3, 5 x 10 -7 p. H 6 α 4 = 2, 2 x 10 -5 p. H 7 α 4 = 4, 8 x 10 -4 p. H 8 α 4 = 5, 4 x 10 -3 p. H 9 α 4 = 5, 2 x 10 -2 p. H 10 α 4 = 3, 5 x 10 -1 p. H 11 α 4 = 8, 5 x 10 -1 p. H 12 α 4 = 9, 8 x 10 -1
![Jika : Dan [Y 4 -] = α 4 CT Tetapan kondisional yang tergantung Jika : Dan [Y 4 -] = α 4 CT Tetapan kondisional yang tergantung](http://slidetodoc.com/presentation_image/38f2560ba85e04cb4227ad227ef519ee/image-11.jpg)
Jika : Dan [Y 4 -] = α 4 CT Tetapan kondisional yang tergantung p. H

Kurva titrasi EDTA (Pengaruh p. H) 1. Hitung K’f 2. sebelum titrasi : p. M = -log [Mn+] 3. Sebelum TE sisa [Mn+] total = [Mn+] sisa + CT CT << [M] sisa p. M = -log [Mn+] sisa = CM sisa 4. Saat TE [Mn+] = CT dimana : [MY(n-4)] ≈ C MY(n-4) [Mn+] dihitung dari K’f 5. Setelah TE CT ~ [EDTA] sisa. sehingga [Mn+] dihitung dari K’f

Contoh : 50 m. L 0, 005 M Ca 2+ dititrasi dengan 0, 01 M EDTA pada p. H 10, Kurva titrasi ? 1. α 4 (p. H = 10 ) = 0, 35 K’Ca. Y = α 4. K Ca. Y = 0, 35 x (5. 1010) = 1, 75. 1010 2. Sebelum titrasi p. Ca = -log [Ca 2+] = -log 5. 10 -3 = 2, 30 3. Sebelum TE (mis. + 10 m. L EDTA) [Ca 2+] sisa = 50 x 0, 005 – 10 x 0, 01 + CT 60 ≈ 2, 5. 10 -3 p. Ca = 2, 6

4. Saat TE (mis. + 25 m. L EDTA) Ca 2+ + Y 4 - ↔ Ca. Y 2 -

5. Setelah TE (mis. + 35 m. L EDTA)

• Titrasi EDTA sering di pakai untuk penentuan kesadahan air penentuan ion Ca 2+ dan Mg 2+ yang sering ada secara bersamaan • Pengaruh p. H pada titrasi EDTA : p. H < TA kurang tajam [Y 4 -] berkurang dengan penurunan p. H • pada p. H yang sama (asam), maka Kf > akan memberikan ketajaman TA • p. H minim untuk titrasi logam – EDTA adalah 0 -1 (untuk Fe (III) & I (III)

Kurva titrasi Ca 2+ - EDTA & Mg 2+ - EDTA (HAL 247) • Kf untuk Mg – EDTA (4, 9 x 108) < Ca – EDTA (5, 0 x 1010) • Sehingga reaksi Ca – EDTA lebih sempurna (P Ca lebih tajam dan range lebih lebar)

• Makin rendah p. H (<6) maka TA makin kurang tajam, karena Y 4 - berkurang dengan penurunan p. H • Titrasi Ca - EDTA dilakukan minimum p. H = 8. • Makin besar Kf, maka TA makin tajam

• Hal 249 • p. H minimum untuk beberapa logam – EDTA. • Bila pada p. H tsb. Kation logam dapat membentuk endapan hidroksida, maka perlu di+ zat pengomplek lain seperti buffer • Ex. : Zn 2+ pada p. H ± 4 membentuk Zn(OH)2, perlu di+ buffer NH 3 – NH 4 Cl pada konsentrasi tinggi. Shg terbentuk komplek Zn-NH 3 (lihat Kf Zn – EDTA & Zn – NH 3

PENGARUH ZAT PENGOMPLEKS LAIN PADA KURVA TITRASI EDTA • Beberapa kation akan membentuk endapan hidrous oksida pada p. H yang diperlukan untuk titrasi dengan EDTA. • Maka diperlukan zat pengompleks lain agar dapat membentuk kompleks dengan logam yang bersangkutan. • Zat pengompleks lain biasanya dalam bentuk buffer. • Harga Kf untuk kedua bentuk kompleks harus diperhatikan. • Sehingga tetapan kondisionalnya harus dikalikan dengan alpha-value dari logam (αM = [Mn+]/CM)

• CM = jumlah konsentrasi spesi yang mengandung ion logam eksklusif yang bergabung dengan EDTA. untuk larutan yang mengandung ion logam Zn dengan buffer amonia, maka : CM = CZn= [Zn 2+]+ [Zn(NH 3)22+]+ [Zn(NH 3)32+]+ [Zn(NH 3)42+] • Tentukan harga Kf untuk logam-buffer • Misal titrasi ion logam Zn 2+ dengan EDTA yang dibuffer dengan amonia (NH 3). [Zn(NH 3)2+]=k 1. [Zn 2+][NH 3] Dengan cara yang sama , maka : [Zn(NH 3)22+]=k 1. k 2. [Zn 2+][NH 3]2 [Zn(NH 3)32+]=k 1. k 2. k 3. [Zn 2+][NH 3]3 [Zn(NH 3)42+]=k 1. k 2. k 3. k 4. [Zn 2+][NH 3]4 substitusikan pernyataan tersebut ke dalam persamaan CZn. CM=[Zn 2+]{1+ k 1. [Zn 2+][NH 3]+k 1. k 2. [Zn 2+][NH 3]2+ k 1. k 2. k 3. [Zn 2+][NH 3]3+ k 1. k 2. k 3. k 4. [Zn 2+][NH 3]4}

• Masukkan harga CM kedalam persamaan αM ( dengan mengganti M dengan Zn) • Harga konstanta kondisional untuk ion Zn 2+ dengan EDTA dalam buffer amonia adalah: • Dimana k”Zn. Y adalah tetapan kondisional yang baru titrasi kompleks yang dipengaruhi p. H dan di bufffer ( adanya zat pengompleks lain).

• 1. 2. Contoh: 50 m. L larutan Zn 2+ 0, 005 M dititrasi dengan larutan EDTA 0, 01 M, yang dibuffer dengan 0, 1 M NH 3 + 0, 176 M NH 4 Cl untuk menjaga p. H hingga 9. volume EDTA masing : 20, 25 dan 30 m. L. Tentukan Kf untuk logam-NH 3 Zn-NH 3. (lihat tabel) k 1 = antilog 2, 4= 2, 51. 102 k 1. k 2= antilog (2, 4 + 2, 4) = 6, 31. 104 k 1. k 2. k 3 = antilog(2, 4+2, 5)= 2, 00. 107 k 1. k 2. k 3. k 4 = antilog(2, 4+2, 5+2, 1)= 2, 51. 109 Hitung konstanta kondisional: hitung αM :

K”Zn. Y= α 4. αZn. k. Zn. Y = (5, 2. 10 -2)(3, 68. 10 -6)(3. 2. 1016)=6, 1. 109. 3. Hitung p. Zn setelah penambahan 20 m. L EDTA. pada titik ini hanya sebagian Zn yang dikomplekskan dengan EDTA. yang tertinggal adalah sebagai zn 2+ dan keempat kompleks amina. dari definisi jumlah konsentrasi 5 spesi tsb adalah harga CM. Zn 2+ + Y 4 - → Zn. Y 2 - (CM) (CT) M: 0, 25 0, 2 R; 0, 2 S: 0, 05 0, 0 0, 2 konsentrasi Zn 2+ = 0, 05/70 = 7, 14. 10 -4. Substitusi ke harga αM = [Mn+]/CM) αZn = [Zn 2+]/CZn [Zn 2+]= (3, 68. 10 -6)(7, 14. 10 -4)=2, 63. 10 -9 M p. Zn = 8, 58

• Hitung p. Zn setelah penambahan 25 m. L EDTA’ kondisi ini adalah titik ekivalen. Zn 2+ + Y 4 - → Zn. Y 2 - (CM) (CT) M: 0, 25 R; 0, 25 S: 0, 00 0, 25 konsentrasi Zn. Y 2 - = 0, 25/75 = 3, 33. 10 -3 M. Jumlah konsentrasi semua spesi Zn yang tidak bergabung dengan EDTA = jumlah konsentrasi EDTA yang tidak terkomplekskan. CM = CT Dan [Zn. Y 2 -]= 3, 33. 10 -3 M, substitusi ke harga k”Zn. Y. CM = 7, 38. 10 -7 M [Zn 2+]= (3, 68. 10 -6)(7, 38. 10 -7)=2, 72. 10 -12 M p. Zn = 11, 57

4. Hitung p. Zn setelah penambahan 30 m. L EDTA. (kondisi ini adalah setelah titik ekivalen). Zn 2+ + Y 4 - → Zn. Y 2 - (CM) (CT) M: 0, 25 0, 30 R; 0, 25 S: 0, 00 0, 05 0, 25 konsentrasi Y 4 -≈CT = 0, 05/80 = 6, 25. 10 -4 M. semua Zn terkomplekskan. Dan [Zn. Y 2 -]= 0, 25/ 80 = 3, 12. 10 -3 M, substitusi ke harga k”Zn. Y. [Zn 2+]= (3, 68. 10 -6)(8, 16. 10 -10)=3, 00. 10 -15 M p. Zn = 14, 52
- Slides: 26